无创正压通气联合肺表面活性物质治疗新生儿呼吸窘迫综合征的效果分析
2023-09-15谢雯鲍莉
谢雯,鲍莉
宜兴市人民医院儿科,江苏宜兴 214200
新生儿呼吸窘迫综合征是新生儿尤其是早产儿多发性危重症之一,是指在母体内新生儿肺脏发育不完全,导致肺表面先天缺乏肺表面活性物质,进而导致肺泡塌陷,严重者出现低氧血症[1]。早产儿因肺部发育不成熟,肺表面活性物质分泌不足,是新生儿呼吸窘迫综合征的主要发病群体[2]。新生儿呼吸窘迫综合征临床表现为呼吸困难、皮肤青紫、呻吟等症状,若治疗不及时,则会诱发肺动脉高压、呼吸衰竭等并发症,对新生儿健康安全造成极大威胁。无创正压通气是新生儿呼吸窘迫综合征首选的治疗手段,主要是通过改善肺泡塌陷,增强换气、通气功能,从而提升患儿肺部功能[3]。肺表面活性物质是一种复杂的脂蛋白,可以控制炎症因子,预防肺部感染,能减少肺部表面张力,对改善肺功能具有重要的价值。本研究随机选取2019年4月—2023年4月宜兴市人民医院儿科收治的新生儿呼吸窘迫综合征患儿50例分组治疗,探究无创正压通气+肺表面活性物质治疗的临床价值,现报道如下。
1 资料与方法
1.1 一般资料
随机选取本院儿科收治的新生儿呼吸窘迫综合征患儿50例,采取随机数表法分组。对照组25例,男14例,女11例;胎龄:28~34周,平均(32.15±1.16)周;出生体质量:842~2 367 g,平均(1 876.96±214.36)g。研究组25例,男15例,女10例;胎龄:28~35周,平均(32.16±1.14)周;出生体质量:853~2 371 g,平均(1 882.21±214.41)g。本研究经伦理委员会批准,两组一般资料对比,差异无统计学意义(P>0.05),具有可比性。
1.2 纳入与排除标准
纳入标准:经过临床诊断确诊为新生儿呼吸窘迫综合征;患儿胎儿≥28周;患儿家属对本研究目的知情,同意配合研究开展。排除标准:伴有先天性疾病患儿;合并呼吸系统疾病患儿;合并肝肾功能严重障碍患儿[4]。
1.3 方法
对照组:应用无创呼吸机(科曼,COMEN NV8)治疗,即予以患儿经鼻塞式持续正压无创通气治疗,设置通气模式为CPAP模式,PEEP:5~8 cmH2O,FiO230%~50%,氧流量参数为:4~6 L/min。
研究组:应用无创正压通气+肺表面活性物质治疗,即在对照组基础上应用肺表面活性物质(牛肺表面活性物质,国药准字H20052128;规格:70 mg/支),在使用无创呼吸机辅助通气同时,将70 mg/kg肺表面活性物质从气管内滴入,滴入前充分吸净气管内分泌物,药液温度在37℃,无菌注射器抽取药物,使用LISA(经微管气管内注入肺表面活性物质)技术滴入,滴入过程约2~3 min,同时使用心电监护仪密切监测患儿心率、脉氧。在药物注射后6 h内,不要对患者实施吸痰处理。
两组患者疗程均为3周。
1.4 观察指标
(1)临床疗效:①显效:治疗后患儿缺氧、呼吸困难等症状基本完全消失,X线检查肺部纹理清晰;②有效:治疗后患儿症状有显著好转,X线检查肺部阴影面积明显变小;③无效:不符合上述标准,临床总有效率=显效率+有效率[5]。
(2)机械通气时间、平均住院时间:记录患儿机械通气时间、平均住院时间。
(3)血气指标:应用血气分析仪对患儿动脉氧分压、血氧饱和度、动脉二氧化碳分压指标测定并记录[6]。
(4)炎性指标:治疗前后抽取患儿空腹静脉血2~3 mL,对患儿白介素-6、肿瘤坏死因子-α水平测定记录[7]。
(5)并发症:统计记录患儿气胸、肺炎、脑室内出血发生情况
1.5 统计方法
采用SPSS 27.0统计学软件分析数据,符合正态分布的计量资料以()表示,行t检验,计数资料用例(n)和率表示,行χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患儿临床疗效比较
研究组患儿临床总有效率明显高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组患儿临床总有效率对比
2.2 两组患儿机械通气时间及平均住院时间比较
研究组机械通气时间、平均住院时间均低于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患儿机械通气时间及平均住院时间比较()
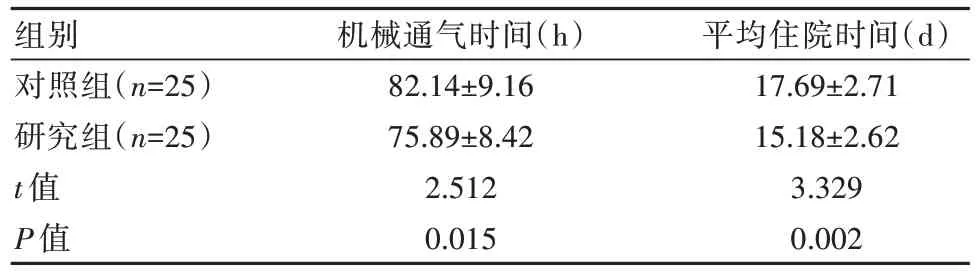
表2 两组患儿机械通气时间及平均住院时间比较()
组别对照组(n=25)研究组(n=25)t值P值机械通气时间(h)82.14±9.16 75.89±8.42 2.512 0.015平均住院时间(d)17.69±2.71 15.18±2.62 3.329 0.002
2.3 两组患儿血气指标比较
治疗前两组患儿动脉氧分压、血氧饱和度、动脉二氧化碳分压水平数据对比,差异无统计学意义(P>0.05),治疗后研究组动脉氧分压、血氧饱和度大于对照组,动脉二氧化碳分压水平小于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组患儿血气指标数据比较()
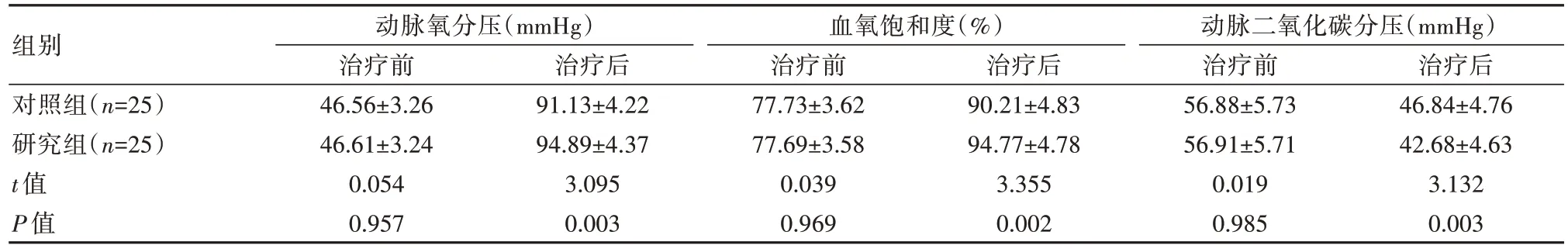
表3 两组患儿血气指标数据比较()
组别对照组(n=25)研究组(n=25)t值P值动脉氧分压(mmHg)治疗前46.56±3.26 46.61±3.24 0.054 0.957治疗后91.13±4.22 94.89±4.37 3.095 0.003血氧饱和度(%)治疗前77.73±3.62 77.69±3.58 0.039 0.969治疗后90.21±4.83 94.77±4.78 3.355 0.002动脉二氧化碳分压(mmHg)治疗前56.88±5.73 56.91±5.71 0.019 0.985治疗后46.84±4.76 42.68±4.63 3.132 0.003
2.4 两组患儿炎性指标水平比较
治疗前两组患儿炎性指标水平比较,差异无统计学意义(P>0.05),治疗后研究组各炎性指标水平均低于对照组,差异有统计学意义(P<0.05),见表4。
表4 两组患儿炎性指标水平比较()
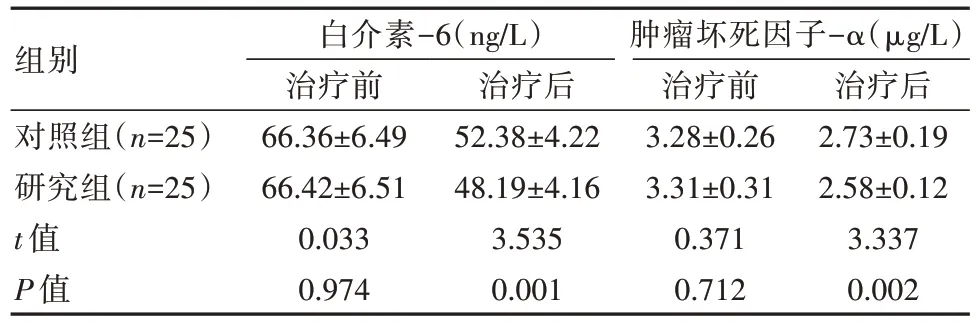
表4 两组患儿炎性指标水平比较()
组别对照组(n=25)研究组(n=25)t值P值白介素-6(ng/L)治疗前66.36±6.49 66.42±6.51 0.033 0.974治疗后52.38±4.22 48.19±4.16 3.535 0.001肿瘤坏死因子-α(μg/L)治疗前3.28±0.26 3.31±0.31 0.371 0.712治疗后2.73±0.19 2.58±0.12 3.337 0.002
2.5 两组患儿并发症发生率比较
研究组并发症发生率低于对照组,差异有统计学意义(P<0.05),见表5。

表5 两组患儿并发症发生率组间比较
3 讨论
新生儿是呼吸窘迫综合征常见发病群体,新生儿呼吸窘迫综合征的发生,致使通气功能、换气功能发生障碍,不能自主摄入足够氧气、排出二氧化碳[8-9]。新生儿呼吸窘迫综合征发生的主要原因是肺表面缺乏活性物质,此外,早产、母体患有糖尿病、胎儿在母体内血液循环量不足等也会诱发新生儿呼吸窘迫综合征发生[10-11]。清理呼吸道、保持水电解质平衡、营养支持、呼吸机辅助通气是新生儿呼吸窘迫综合征的主要治疗原则[12-13]。基于此,选择科学、优质的治疗方案成为临床研究的焦点问题。
无创正压通气用于新生儿呼吸窘迫综合征治疗,可增加肺部通气量,能促进药物的有效分布,增强其吸收效果,从而达到治疗目的[14]。大量研究指出,单一应用无创正压通气治疗,起效慢,且容易诱发新生儿气压伤, 并发症发生率高,若应用时间过长,还容易诱发感染,影响预后效果[15-16]。肺表面活性物质可以使新生儿肺部表面积扩张,能稳定肺泡内气体交换,是一种磷脂蛋白复合物,可以增强对肺泡上皮细胞的保护功能,降低肺毛细血管表面张力,延缓肺泡塌陷,增强肺纤毛顺应性,增强肺通气量,从而改善新生儿呼吸困难症状[17-18]。吴雷等[19]研究中指出,新生儿呼吸窘迫综合征在应用无创正压通气治疗的基础上,联合应用肺表面活性物质治疗,可降低炎性因子水平,并发症发生率仅为15.38%,明显低于单一应用无创正压通气治疗患儿,疗效显著、安全性高,证实了该治疗方案的有效性。对本研究结果分析,相比对照组,研究组患儿炎性因子水平降低,研究组并发症发生率为4.00%低于对照组的28.00%(P<0.05),这一研究结果与上述报道对比,存在一致性,说明新生儿呼吸窘迫综合征治疗中,应用无创正压通气+肺表面活性物质,可控制炎性因子水平,降低了并发症发生率,证实了该治疗方案的高效性、安全性。临床总有效率比较,研究组高于对照组(P<0.05),对其原因分析,无创正压通气能改善患儿通气、换气功能,辅助肺表面活性物质,可防止肺泡塌陷,能促进气体交换,两者起到协调作用,对肺泡上皮细胞具有保护作用,可维持其稳定性,从而改善缺氧症状,提高了整体疗效。血气指标(动脉氧分压、血氧饱和度、动脉二氧化碳分压)对比,研究组优于对照组,机械通气时间、平均住院时间比较,研究组低于对照组(P<0.05),说明联合应用无创正压通气、肺表面活性物质,可改善患者血气指标,缩短了无创通气时间,可加快患者病情转归。
综上所述,新生儿呼吸窘迫综合征应用无创正压通气+肺表面活性物质治疗,疗效确切,可作为重要治疗方案,临床推广应用价值大。
