ERAS对老年腹腔镜胃癌根治术患者的疗效及炎症因子的影响
2023-09-05唐芝翔
唐芝翔
(上饶市立医院预防保健科,江西 上饶 334000)
胃癌是极为严重的肿瘤病变之一,以胃黏膜上皮细胞起源,地域差异性明显,好发于东亚地区且病死率较高[1]。据统计,男性每10万病例中24例死亡,女性每10万病例中9.8例死亡[2]。目前临床治疗主要以腹腔镜手术为主,但老年人由于体质逐渐减弱、免疫功能降低等,手术治疗后并发症的发生率较高。临床分析发现,行手术治疗的胃癌患者多数会在术后出现程度不一的并发症及围术期创伤,不仅对患者的免疫功能造成损害,还从生理、心理等方面对患者产生不利影响,阻碍机体康复。尽管胃癌患者整个术中存在很多不可控的因素,但结合快速康复护理方式能够有效降低风险的发生,提升患者的疾病康复。加速康复外科(ERAS)理论于2001年由Wilemore和Kehlet提出,该理论主张采用一系列有循证医学证据的围术期处理优化措施,以促进患者快速康复[3],目前该理论已在胃肠外科中应用较为广泛[4]。本研究将ERAS应用于老年腹腔镜胃癌根治术患者中,旨在探究其应用效果及其炎症因子的影响。
1 资料与方法
1.1 一般资料
经医院伦委会审批,选取2019年3月至2021年3月本院收治的老年胃癌患者72例。(1)纳入标准:①均经病理确诊;②>60岁;③预期可行腹腔镜胃癌根治术;④均知情同意。(2)排除标准:①合并其他部位恶性病变;②行姑息性手术切除;③有炎症性或自身免疫性疾患;④合并幽门梗阻。随机分为对照组和观察组,各36例。两组一般资料均衡可比(P>0.05),见表1。
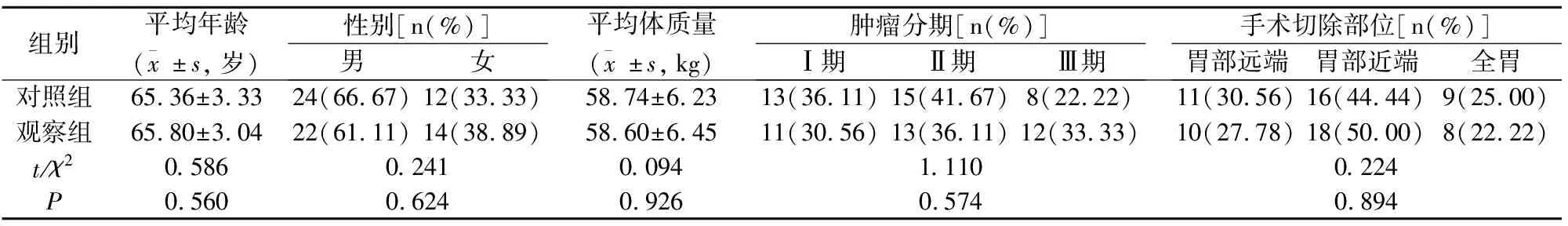
表1 两组一般资料比较(n=36)
1.2 方法
两组均由同一外科组医师完成腹腔镜胃癌根治术。对照组:按常规围术期方案予以术前、麻醉以及术后的指导,术后2~3d待首次肛门排气后拔除胃管,术后5d内予以流食,术后6d过渡至正常饮食。观察组:行ERAS管理。
1.2.1 术前:①心理及健康宣教:入院后即告知患者ERAS的主要内容,了解其心理需求,采用《华西心情指数评估量表》进行心情指数评分,对低度情绪不良患者行一对一心理护理,重度情绪不良患者填写《自杀风险评估表》并请院内心理专家进行疏导。②营养筛查:对患者行营养风险评估(NRS),NRS≥3分者给予其营养干预,医师与营养科交流后为患者制定个体化营养方案,NRS<3分者于7d后再次评估。术前责任护士应向患者宣教肠内营养制剂的功效、意义以及正确服用方法。③术前指导:控制患者的血糖及血压,对有长期吸烟史的患者需进行2周的戒烟训练,指导其学会正确咳痰及胸式呼吸,适应床上大小便。④肠道准备:术前6h内禁食,术前2h饮用≤400mL碳水化合物,合并有糖尿病者口服500mL果糖溶液。
1.2.2 术中:①保温:借助保温毯或暖风机等维持体温≥36℃。②麻醉:全身麻醉联合硬膜外麻醉。③液体治疗:6~8mL/kg·h,尽量减少患者的水钠潴留。④引流管放置:放置1根腹腔引流管至吻合口。⑤术中操作:术中操作轻柔,避免过度牵拉、钳夹,注意控制损伤,尽量减少术中出血。
1.2.3 术后:①引流管:术后1d拔除导尿管,术后2d拔除引流管。②早期活动:术后第1d床边站立及慢走1~2h,术后第2d床下活动2~4h,每天活动4~6h。③进食:利用“假饲”原理刺激肠蠕动,术后第1d无渣流质饮食,术后第2d流质饮食1000~1500mL,术后第3d流质饮食2000~2200mL。④输液:保持每日总入量2000~2500mL,当口服入量≥2000mL时,停止输液。
1.3 观察指标
①术后疗效。②炎症因子:分别于术前、术后1d、3d抽取患者空腹外周静脉血5mL,ELISA法测定白介素-6/8/10(IL-6/8/10)。③应激激素:分别于术前、术后1d抽取患者空腹外周静脉血5mL,采用化学发光法测定皮质醇(COR)、促肾上腺皮质激素(ACTH)、肾上腺素(EPI)水平。
1.4 统计学方法
2 结果
2.1 术后临床参数
观察组术后下床活动、首次肛门排气、术后住院时间均短于对照组(P<0.05),见表2。
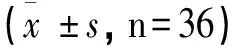
表2 两组患者术后各临床参数情况比较
2.2 炎症因子
观察组术后1d、3d的1L-6、IL-8水平均低于对照组,其IL-10水平高于对照组(P<0.05),见表3。
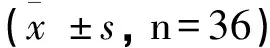
表3 两组患者不同时段炎症因子水平比较
2.3 应激激素
术后1d,观察组患者的COR、ACTH以及EPI水平均较对照组更低(P<0.05),见表4。
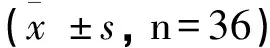
表4 两组应激激素水平对比
3 讨论
胃癌为消化系统常见疾患,治疗该疾患的首选措施为腹腔镜胃癌根治术,但由于解剖结构复杂、周围毗邻血管及胃周淋巴丰富,胃癌手术创伤性较大,加之大部分胃癌患者为高龄人群,手术的耐受力较差,易在术中及术后出现诸多的并发症,因此围术期的干预工作尤为重要[5]。目前外科已进入微创时代,其中腹腔镜手术与ERAS为主要的发展方向,前者具有创伤小、疼痛轻及恢复快的优势,后者则是通过围术期的诸多干预手段来减少手术应激反应,加快术后康复速度[6]。有研究指出,腹腔镜胃癌根治术患者围术期行ERAS理念干预,可有效缩短住院时间,加快患者康复[7]。
本研究中,观察组术后下床活动、首次肛门排气、术后住院均短于对照组(P<0.05),说明ERAS能够显著促进老年腹腔镜胃癌根治术患者的肠道恢复,缩短其住院周期,改善预后,这可能与术前胃肠道准备、术后肠内营养以及早期活动干预等有关,尤其是术后早期恢复饮食,有益于缓解机体的高分解状态,促进胃肠功能的恢复。胃癌患者的免疫功能处于抑制中,手术的创伤则会加重机体内环境的紊乱,降低机体免疫力[8];而炎性因子则能够调节介导免疫应答与炎性反应,进而引起组织以及器官的损害[9]。同时,手术应激以及炎性因子能够抑制机体的免疫功能,同时手术应激也可激活应激激素,造成切口、肺部感染以及尿潴留和尿失禁等不良并发症的出现[10]。在本研究中,观察组术后1d、3d的1L-6、IL-8水平均低于对照组,其IL-10水平高于对照组(P<0.05),同时术后1d,观察组患者的COR、ACTH以及EPI水平均较对照组更低(P<0.05),提示ERAS可减轻老年腹腔镜胃癌根治术患者炎症与应激反应。究其原因,ERAS理念注意术中患者的保温,可减少因温差诱发的应激反应,加之硬膜外麻醉的使用,可有效阻断伤害性感受传导,抑制手术应激,进而患者的炎症因子及应激激素等水平得以改善。
综上所述,ERAS可促进老年腹腔镜胃癌根治术患者术后胃肠功能的恢复,缩短住院周期,减轻机体的炎症及应激反应,具有较高的实用性及可行性。
