基于 NF-κB 信号通路探讨宣肺解痉方对支气管哮喘免疫失衡和炎症反应的影响
2023-08-12李玉杰罗春梅王峻游达田雪娇彭飞飞
李玉杰,罗春梅,王 玉,王峻游达,田雪娇,彭飞飞,武 蕾
(1. 河北中医学院研究生学院,河北 石家庄 050091;2. 河北省中医院,河北 石家庄 050013)
支气管哮喘(简称哮喘)是一种以气道高反应为特征的慢性炎症性疾病,以反复发作的喘息、气促为主要症状,多在夜间、清晨发作。据调查,中国成年人患病率约为4.2%,且患病率呈逐年上升趋势[1-2]。现代医学认为气道高反应性的病理机制可能与免疫失衡、炎症反应相关,以Th1/Th2免疫失衡、嗜酸性粒细胞(EOS)浸润性炎症为主[3-4], 形成气道高反应性,导致哮喘症状反复发作。随着哮喘机制的深入研究,上游核转录因子-κB(NF-κB)信号通路影响哮喘患者体内的免疫平衡和炎症微环境的研究日益增多[5-6],通过抑制该通路改善哮喘病理进程成为热点。当前西医治疗哮喘常选取布地奈德福莫特罗等吸入性糖皮质激素复合制剂,其可抑制NF-κB信号通路的表达,改善气道炎症反应,调节免疫,控制哮喘发作[7],但仍有患者激素不耐受,未能规律吸入药物或自行加减药量,难以有效控制哮喘症状。中医治疗哮喘有着丰富的经验,已成为哮喘患者易于接受的治疗方法。宣肺解痉方为自拟方剂, 前期研究表明,宣肺解痉方治疗哮喘患者疗效显著,并能够降低体内炎症因子、免疫因子的水平[8-9],但其上游作用机制尚不明确。本研究基于NF-κB信号通路,进一步探讨了宣肺解痉方纠正免疫失衡、抑制炎症反应的作用机制,以期为宣肺解痉方的临床应用提供客观依据。现报道如下。
1 资料与方法
1.1诊断标准 西医诊断标准符合《支气管哮喘防治指南(2020年版)》[7]中哮喘慢性持续期的诊断标准。中医诊断标准参照《支气管哮喘中医证候诊断标准(2016版)》[10]中哮病的诊断标准。
1.2纳入标准 ①年龄20~70岁;②符合哮喘慢性持续期西医诊断标准;③符合中医哮病诊断标准;④患者自愿签署知情同意书并接受治疗。
1.3排除标准 ①哮喘急性发作期、临床控制期者;②合并严重心脑血管疾病、肝肾功能异常、肿瘤者;③合并其他呼吸系统疾病(支气管扩张症、肺纤维化、慢性阻塞性肺疾病、慢性呼吸衰竭及其他严重呼吸疾病)者;④处于妊娠或哺乳期妇女;⑤合并严重认知及精神障碍者;⑥入选前1个月内参加其他临床试验者;⑦对本项目药物不耐受或过敏者。
1.4一般资料 选择2021年3月—2022年3月河北省中医院诊治的80例哮喘患者,按照随机数字表法分为对照组和观察组各40例。对照组男16例,女24例;年龄20~66(39.3±10.9)岁。观察组男18例,女22例;年龄21~67(42.6±12.2)岁。2组研究对象性别、年龄等基线资料相比差异均无统计学意义(P均>0.05),具有可比性。本研究经河北省中医院伦理委员会审查批准。
1.5治疗方法 对照组患者吸入布地奈德福莫特罗粉吸入剂(AstraZeneca AB,国药准字H20140458,规格:160 μg/4.5 μg,60吸/支),1吸/次,2次/d。观察组在对照组治疗基础上给予宣肺解痉方汤剂口服,方药组成:防风10 g、荆芥10 g、蝉蜕10 g、僵蚕12 g、地龙10 g、厚朴10 g、炙麻黄6 g、苦杏仁10 g、炙甘草6 g、陈皮10 g、清半夏9 g、桑白皮10 g、化橘红10 g、茯苓12 g。随症加减:怕风怕冷,痰白、质稀者加细辛、干姜、五味子;咳吐黄痰、便干尿赤者加浙贝母、知母、桑白皮;咽痒、眼痒、打喷嚏、流鼻涕者加乌梅、柴胡、五味子;气短、频繁感冒者加黄芪、白术;腰痛、头晕耳鸣者加熟地黄、补骨脂。由河北省中医院中药房提供饮片,同时采用常规煎煮法取汁400 mL,分早晚2次温服。2组治疗周期均为28 d。
1.6观察指标
1.6.1临床症状体征积分 参照《中药新药临床研究指导原则(试行)》[11]评估患者治疗前后症状、体征的严重程度,共有一天中咳嗽次数,痰量,喘息持续时间,胸闷、气短与活动关系,每周夜间憋醒次数,哮鸣音、痰鸣音、湿啰音肺部分布情况9个条目,分为无、轻、中、重4级,分别记录为0~3分。积分总和的高低代表症状严重程度。
1.6.2哮喘控制水平 记录患者治疗前后哮喘控制情况,从日常活动影响情况、夜间醒来次数、呼吸困难次数、急救药物使用次数以及自我评价5个维度量化。每个条目分别有1~5分,总和为ACT得分。得分25分为完全控制,20~24分为部分控制,小于20分为控制较差。
1.6.3肺功能指标 通过肺功能仪检测2组患者治疗前后肺功能,记录第一秒用力呼气容积占预计值百分比(FEV1%)、呼气峰值流速(PEF),以评价患者气道阻塞情况。
1.6.4呼气一氧化氮(FeNO)水平 治疗前后使用呼出一氧化氮分析仪检测2组患者FeNO水平,<25 ppb考虑非嗜酸性气道炎症,25~50 ppb考虑混合型气道炎症,>50 ppb提示嗜酸性气道炎症。
1.6.5血清指标 采集2组患者治疗前后空腹静脉血液,静置1 h后以转速3 000 r/min离心10 min,常规分离血清,-80 ℃冰柜储存。统一采用酶联免疫吸附试验(ELISA)检测EOS计数和总免疫球蛋白 E(IgE)水平、白细胞介素-4(IL-4)、γ干扰素(IFN-γ)、核转录因子-κB p65(NF-κB p65)、核转录因子κB抑制蛋白α(IκBα)水平。
1.6.6临床疗效 治疗28 d后按照《中药新药临床研究指导原则(试行)》[11]中的疗效评判标准评估2组临床疗效。临床控制:治疗后患者哮喘症状消失,肺部听诊未见异常,临床症状体征积分改善率≥95%;显效:治疗后患者哮喘症状、肺部听诊大幅度改善,临床症状体征积分改善率≥70%,但<95%;有效:治疗后患者哮喘症状、肺部听诊稍有改善,临床症状体征积分改善率≥30%,但<70%;无效:治疗后患者哮喘症状及体征未见好转,或反加重,临床症状体征积分改善率<30%。临床症状体征积分改善率=(治疗前临床症状体征积分-治疗后临床症状体征积分)/治疗前临床症状体征积分×100%。
2 结 果
2.12组患者治疗前后临床症状体征积分、ACT评分比较 2组患者治疗后临床症状体征积分均明显低于本组治疗前,ACT评分均明显高于本组治疗前,且观察组治疗后临床症状体征积分、ACT评分改善情况明显优于对照组,差异均有统计学意义(P均<0.05)。见表1。

表1 2组支气管哮喘患者治疗前后临床症状体征积分、ACT评分比较分)
2.22组患者治疗前后FEV1%、PEF比较 2组患者治疗后FEV1%、PEF均明显高于本组治疗前,且观察组均明显高于对照组,差异均有统计学意义(P均<0.05)。见表2。
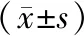
表2 2组支气管哮喘患者治疗前后FEV1%、PEF比较
2.32组患者治疗前后FeNO水平及血清EOS计数、IgE比较 与治疗前比较,治疗后2组患者FeNO水平及血清EOS计数、IgE水平均明显降低,且观察组均明显低于对照组,差异均有统计学意义(P均<0.05)。见表3。
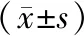
表3 2组支气管哮喘患者治疗前后FeNO水平及血清EOS计数、IgE水平比较
2.42组患者治疗前后血清IL-4、IFN-γ水平比较 与治疗前比较,治疗后2组患者血清IL-4水平均明显降低,IFN-γ水平均明显升高,且观察组各指标改善情况均显著优于对照组,差异均有统计学意义(P均<0.05)。见表4。

表4 2组支气管哮喘患者治疗前后血清IL-4、IFN-γ水平比较
2.52组患者治疗前后血清NF-κBp65、IκBα水平比较 与治疗前比较,治疗后2组患者血清NF-κBp65水平均明显降低,IκBα水平均明显升高,且观察组各指标改善情况均显著优于对照组,差异均有统计学意义(P均<0.05)。见表5。

表5 2组支气管哮喘患者治疗前血清NF-κBp65、IκBα水平比较
2.62组患者临床疗效比较 治疗后观察组总有效率为90.0%,明显高于对照组的77.5%,差异有统计学意义(P<0.05)。见表6。

表6 2组支气管哮喘患者治疗28 d后临床疗效比较 例(%)
3 讨 论
哮喘是呼吸系统的常见疾病,患者表现为可逆性的气流受限,出现喘息、胸闷、气短、咳嗽等症状,可自行缓解或治疗后缓解。西医治疗哮喘一般以抗感染、扩张支气管等为主要手段,常采用吸入性糖皮质激素联合长效β2受体激动剂治疗,如布地奈德福莫特罗粉吸入剂,但其长期使用会产生耐药性,影响疗效[7]。中医药治疗此类疾病疗效可靠,已广泛应用于临床中。
哮喘属于中医“哮病”的范畴。《素问·阴阳别论》记载“阴争于内,阳扰于外,魄汗未藏,四逆而起,起则熏肺,使人喘鸣”,并提出了脏腑功能失调于内、外邪侵袭于外、气机逆乱的病机特点。笔者认为,“夙根伏痰”是哮喘发病的核心病理因素,风邪夹杂其他病邪或病理因素是发病的重要诱因,肺失宣降、气道挛急是贯穿哮喘整个病程和各个证型的基本病机。在治疗过程中要重视“风邪”“伏痰”。贼风夹邪袭肺,引动伏痰,风痰阻滞,气道挛急,肺失肃降是哮喘发生发展的病理过程。正如《黄帝内经》中记载:“犯贼风虚邪者……上为喘呼。”《活幼心书·咳嗽》中提到:“有风生痰,痰实不化,因循日久……遂成痰母,故痰母发动,而风随之,风痰渐紧,气促而喘,乃成痼疾。”基于这一基本病机提出“宣肺解痉”为总的治疗原则。武蕾教授自拟宣肺解痉方,该方由三拗汤、华盖散、二陈汤三方化裁而来,共计13味中药。方中君药为麻黄、杏仁,一宣一降,二者相须为用,发挥宣肺平喘之功;臣药清半夏、陈皮、茯苓、橘红四药味辛温,应“病痰饮者当以温药合之”之理,协同理气健脾、燥湿化痰,以杜生痰之源;佐药以防风、荆芥辛散之品,助麻黄祛风散邪。蝉蜕、僵蚕、地龙属动物类药,具有搜风通络之力,可引贼风外出,三药均有缓解支气管痉挛的作用[12]。桑白皮为化痰良药,且其性寒,可缓和方中麻黄、荆防等温燥之性;甘草调和诸药为使药。全方共奏疏风宣肺、理气化痰、解痉平喘之效。在此基础上,根据不同的证型酌情加减。怕风怕冷、痰白、质稀者加细辛、干姜、五味子以温肺散寒;咳吐黄痰、便干尿赤者加浙贝母、知母以清热化痰;咽痒、眼痒、打喷嚏、流鼻涕者加乌梅、柴胡、五味子以祛风止痒;气短、频繁感冒者加黄芪、白术以补肺益气;腰痛、头晕耳鸣者加熟地黄、补骨脂以补肾助阳。陈旭[13]实验研究证实麻黄、杏仁、甘草三者不可分割,整体发挥抗炎平喘的作用。刘新桥等[14]报道华盖散联合二陈汤可提高哮喘患者FEV1,降低PEF变异率。本研究结果表明,观察组干预后有效率提高至90.0%,且患者临床症状体征积分降低和ACT评分升高更显著,证实联合宣肺解痉方治疗更有利于控制哮喘症状。同时治疗后观察组FEV1%、PEF明显升高且均高于对照组,进一步客观地证实宣肺解痉方治疗哮喘疗效确切。
长期存在的免疫失衡和气道炎症反应是哮喘发作的关键,有多种细胞(EOS、肥大细胞、淋巴细胞等)及细胞组分(细胞因子、炎症介质等)参与该过程。哮喘表型研究显示,在众多表型中以Th2相关性哮喘、嗜酸性粒细胞型炎症居多[13]。Th2相关性哮喘表型以Th1/Th2失衡为基础。Th1和Th2是辅助T淋巴细胞的两个亚群,处于动态平衡状态。若受到外界刺激导致Th2优势应答,Th1活性受到抑制,表现为Th2细胞分泌大量的炎症因子IL-4,Th1细胞分泌的炎症因子IFN-γ减少。IL-4可作用于B淋巴细胞,诱导其释放IgE,IgE交联引起肥大细胞脱颗粒,释放白三烯、组胺等炎症介质,造成气道痉挛;IL-4或可直接诱导以EOS为代表的炎性细胞聚集、活化、脱颗粒,损伤气道黏膜上皮,引发气道高反应性。IFN-γ虽然可以抑制B细胞产生IgE,但其表达下降,使其抑制哮喘气道炎症反应的作用减弱。由此可见,维持IFN-γ/IL-4平衡在治疗哮喘中尤为重要。另一种常见的嗜酸性粒细胞型炎症表型,以EOS炎性浸润为突出特点[15]。在Th2细胞分泌的细胞因子和IgE的刺激下,诱导大量EOS向病灶处迁移,继而脱颗粒,产生碱性蛋白、嗜酸性粒细胞阳离子蛋白等,这类蛋白可增强气道对外界刺激的反应性[16]。与此同时Th2型细胞因子刺激一氧化氮合成酶高表达,形成大量NO,FeNO升高[17]。林敏仪等[18]认为FeNO水平与痰EOS计数呈正相关,能够间接反映嗜酸性粒细胞性炎症程度。临床利用IgE、EOS、FeNO三者联合诊断嗜酸性粒细胞型炎症表型准确程度更高[19]。因此,以Th1/Th2失衡为主的免疫紊乱导致IgE、EOS、FeNO升高,产生炎症的级联反应,是哮喘反复发作的重要病理机制。顾莅冰等[20]证实三拗汤中两两组合或全方运用,均能降低哮喘小鼠血清IgE水平和肺泡灌洗液中IL-4、IL-5、IL-6水平,抑制哮喘发作。左志通等[21]报道三子二陈汤治疗哮喘患者可上调Th1细胞因子水平,下调Th2细胞因子水平,调节Th1/Th2平衡。黄泽清等[22]发现僵蚕可降低血清IL-4水平,提高IFN-γ水平,恢复Th1/Th2平衡。本研究结果也显示:治疗后2组FeNO水平、EOS计数及血清IL-4、IgE水平均较治疗前下降,IFN-γ水平较治疗前上升,且观察组改善情况优于对照组。说明宣肺解痉方可调节Th1/Th2免疫失衡,降低炎症因子水平,减少EOS浸润。
宣肺解痉方具备调节免疫失衡的作用,但其上游分子机制尚不明确。有文献报道,NF-κB以IκBα-NF-κB p50/65的异二聚体形式广泛存在于全身淋巴细胞、EOS等导致哮喘发作的细胞中,是哮喘重要的免疫和炎症反应的核心介质[23]。IκBα可抑制NF-κB p50/65活化进入细胞核,阻止后续基因表达,NF-κB p50负责核转移,NF-κB p65负责下游基因转录,通过调控多种复杂的细胞因子的基因转录,参与哮喘免疫和炎症信号的传递[23]。当细胞受到刺激时,IκBα被降解,NF-κB p50/p65活化,由细胞质转移至细胞核[24],NF-κB p65与相应的靶基因位点结合,启动基因转录,调控下游IgE、IL-4、IFN-γ等因子的表达[25-26],不断反复的刺激形成炎症级联放大效应,加剧哮喘发生。故而IκBα、NF-κB p65常作为通路关键蛋白,用于评价NF-κB信号通路是否被激活。Gregorczky等[27]设计实验阻断NF-κB易位,通过流式分析检测,发现释放IL-4的小鼠Th2细胞百分比下降。Zhi等[28]发现右美托咪定可通过TLR4/NF-κB信号通路的下调减少IL-4和IgE的产生,从而减轻哮喘小鼠肺部炎症和气道高反应性。Pang等[29]报道中药及其提取物可以通过抑制NF-κB信号通路的激活调控免疫反应,抑制气道炎症。刘永生等[30]动物实验表明,麻黄-杏仁对药可通过下调NF-κBp65蛋白表达,降低IL-4水平,升高IFN-γ水平,减轻哮喘大鼠气道炎性反应和气道高反应性。尚立芝等[31]研究显示,二陈汤加味治疗可降低慢性阻塞性肺疾病大鼠肺中NF-κB p65 mRNA以及蛋白表达。橘红成分中的柚皮苷以及甘草中的甘草酸有抑制NF-κB信号通路激活的作用,从而发挥抗炎作用[32]。本研究结果显示,治疗后2组NF-κB p65水平均降低,IκBα水平均升高,观察组各指标变化更显著。结合观察组IgE、IL-4、IFN-γ的变化,提示宣肺解痉方可能通过抑制NF-κB信号通路,降低IgE、IL-4水平,升高IFN-γ水平,减轻炎症反应,调节免疫紊乱,有效控制哮喘症状。
综上所述,宣肺解痉方可有效改善哮喘患者症状,提高肺功能,其作用可能是通过抑制NF-κB信号通路的激活,纠正Th1/Th2失衡,改善免疫功能,降低炎症反应而实现的。但本次研究选取样本量较少,结论证据较为薄弱,后期可以扩大样本量进行深入研究。
利益冲突:所有作者均声明不存在利益冲突。
