肝硬化肝性脑病患者合并自发性门体分流的临床特征分析
2023-08-02王智勇郭武华
王智勇 郭武华
(福建医科大学孟超肝胆医院介入科,福建 福州 350025)
肝硬化是慢性肝病发展的晚期阶段,近年来其发病率及致死率逐渐升高。据2015年全球肝病相关致死率报告,肝硬化每年约致116万人死亡,位居全球常见疾病死因第11位[1]。肝性脑病(hepatic encephalopathy,HE)是导致肝硬化患者死亡的重要因素。据既往1项对111例肝硬化患者的研究发现,3级和4级HE患者的1年和3年生存率分别为42%、23%[2]。自发性门体分流(spontaneous portosystemic shunts,SPSS)的定义为门静脉系统或内脏静脉系统与全身静脉系统之间的任何血管的连接[3]。早期研究认为,SPSS在一定程度上减轻门静脉系统压力。然而最近的研究认为,这种代偿机制是不充分的,且SPSS会减少肝脏的血流灌注,导致各种肝硬化失代偿事件发生,其中就包括HE[4-7]。在肝硬化患者中,SPSS对门静脉高压的减压能力以及对HE分级、肝功能、门静脉血栓与腹水形成的影响,目前尚存争议。本研究以肝硬化HE伴自发性门体分流为研究的切入点,旨在探讨SPSS对此类患者的临床影响,为合并SPSS的HE患者的治疗提供更多理论依据。
1 资料与方法
1.1 一般资料 选取我院2016年1月至2021年11月临床资料完整的肝硬化HE患者367例作为研究对象。通过腹部增强CT或MRI诊断合并SPSS的HE患者227例,未合并SPSS的HE患者140例。纳入标准:经临床明确诊断肝硬化合并慢性HE;年龄>18岁;预期寿命>6个月;具有完整的临床资料者。排除标准:A或B型HE患者;肝切除、肝移植及肝脏介入治疗后;脾切除及脾动脉栓后;存在超过米兰标准的肝细胞癌或合并肝外恶性肿瘤;有外科分流道手术史;存在精神或神经性疾病。
1.2 扫描仪器与方法 采用荷兰飞利浦256层ICT扫描仪或使用德国西门子Verio Dot 3.0T磁共振成像仪对患者进行上腹部三期增强扫描;采用美国GE LOGIQ E9彩色多普勒超声仪测量患者门静脉血流方向。
1.3 影像图像分析 由2位放射科中级医师共同进行CT或MRI图像分析,当意见遇到分歧时,引入1名高年资主任医师协调、讨论得出最终意见。
1.5 数据收集和分析 收集所有研究对象的临床资料,观察两组是否存在差异;并分析SPSS与肝脏储备功能的关系;收集患者的门静脉及属支内径、脾静脉、肠系膜上静脉及自发性门体分流内径,观察SPSS与这三者是否相关;观察SPSS对两组患者肝硬化失代偿事件是否存在影响。
1.7 统计学方法 采用统计软件包SPSS 22.0进行分析。计量资料集中趋势描述符合正态分布且方差齐者采用(±s)表示,呈偏态分布的定量资料用中位数(四分位数间距)M(P25,P75)表示;符合正态分布的计量资料,两组数据之间比较采用t检验;不符合正态分布的计量资料,两组数据之间比较采用Mann-WhitneyU检验;定性资料的统计推断使用χ2检验或Fisher确切概率法。P<0.05表示差异有统计学意义。
2 结果
2.1 研究组与对照组的基本特征比较 两组患者在性别构成比上差异无统计学意义,但研究组的平均年龄较对照组大,研究组乙型肝炎病例占比更少,酒精性肝病占比更多。见表1。

表1 研究组与对照组基本特征比较
2.2 研究组与对照组实验室检验指标比较 研究组白蛋白更低,球蛋白、总胆红素、血浆氨水平较对照组更高(P<0.05)。见表2。

表2 研究组与对照组实验室检验指标比较
2.3 研究组与对照组肝脏储备功能比较 两组在Child-Pugh肝功能分级上差异无统计学意义;但研究组MELD评分更高,差异有统计学意义(P<0.05)。见表3。
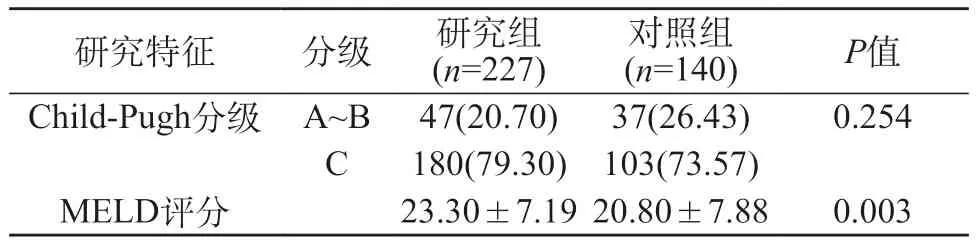
表3 研究组与对照组肝脏储备功能比较
2.4 研究组与对照组影像学指标比较 研究组门静脉右支更细、脾静脉及肠系膜上静脉直径更粗,门静脉主干离肝血流的比例更高(P<0.05)。见表4。

表4 研究组对照组影像学指标比较
2.5 研究组与对照组肝硬化失代偿事件比较 研究组门静脉血栓、腹水及消化道出血等肝硬化失代偿事件发生率更高(P<0.05)。见表5。
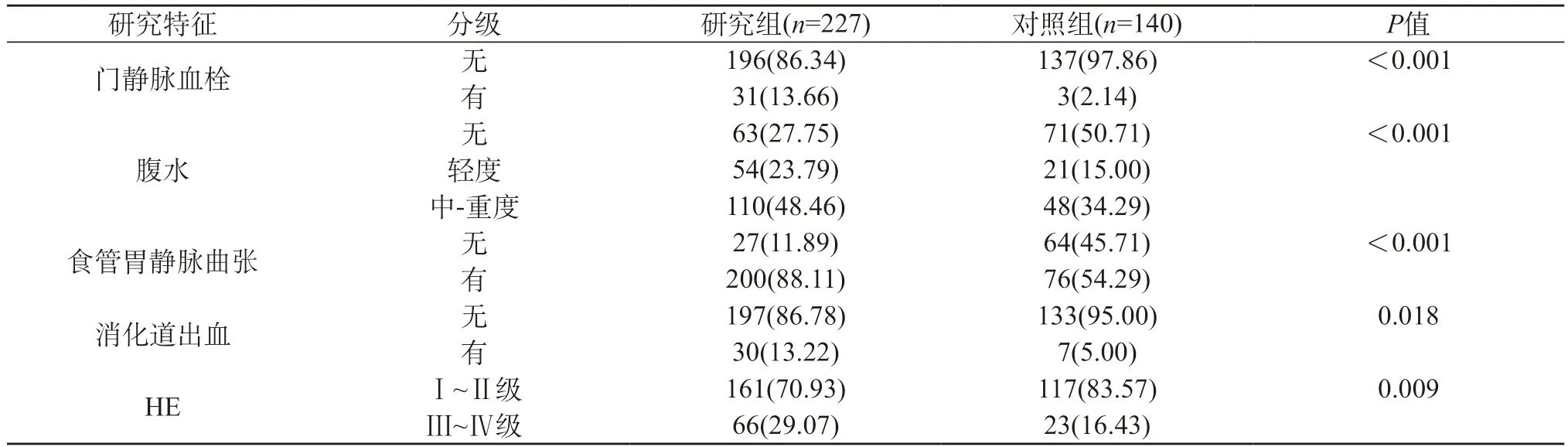
表5 研究组与对照组肝硬化失代偿事件比较[n(%)]
3 讨论
HE是导致肝硬化患者死亡的重要因素。SPSS引流未经肝脏解毒的肠源性血液进入体循环,既增加了血液中有毒物质的含量,又减少肝脏的血流灌注,对肝功能及肝硬化失代偿事件的发生有着重要影响。本研究中肝硬化HE患者SPSS的发生率较高(61.85%),同时,SPSS的存在加重了患者肝功能损害,导致腹水、门静脉血栓、消化道出血等门静脉高压并发症发生率增高。
本研究中研究组中乙型肝炎病例占比更少,酒精性肝病占比更多;在发病年龄上,研究组的平均年龄较对照组大。分析造成这一差异的原因可能是,病毒性肝炎患者很可能在无临床症状的早期常规体检中被诊断,而酒精性肝硬化患者在诊断时多已临床症状比较显著;其次在肝硬化患者中,门静脉高压是导致SPSS形成的重要驱动因素,随着肝功能的恶化,SPSS的发病率明显增加,这可能是研究组患者年龄偏大的原因[3,8-10]。
最近的研究证实,合并SPSS的肝硬化患者具有更差的Child-Pugh分级和更高的MELD评分[3,11-12]。本研究中Child-Pugh C等级的患者SPSS发病率最高(77.11%),在研究组Child-Pugh C等级的患者占比(79.30%)高于对照组(73.57%),但两组患者在Child-Pugh不同分级间差异无统计学意义。该结果与其他文献可能存在差异,原因可能是本研究中所有患者均为肝硬化合并HE患者,其基础肝功能情况较差。虽然本研究中两组在Child-Pugh肝功能分级上无显著差异,但研究组MELD评分更高,与多篇文献结果一致[6,11-12]。
HE合并SPSS的患者食道静脉曲张及急性静脉曲张出血的发生率低[4],这支持SPSS是一种代偿机制[5]。SPSS患者更易出现HE、腹水、静脉曲张出血、感染和急性肾损伤[13]。本研究结果也显示,研究组较对照组患者腹水、食管胃静脉曲张、消化道出血、Ⅲ~Ⅳ级HE的发生率更高,与既往研究结果基本一致。此外,研究组门静脉右支更细、脾静脉及肠系膜上静脉直径更粗,门静脉血栓发生率及门静脉主干离肝血流的比例更高。这些不同的研究结果,可解释为肝硬化是一个动态发展的过程,在不同的阶段,受到不同的代偿机制影响,在SPSS形成的早期阶段,SPSS可代表一种低效的代偿机制,能在一定程度上降低门静脉压力及相关并发症,但随着门静脉压力增高,SPSS不断进展,当分流道足够大、分流血流足够多时可以完全引流内脏血流,并与肝脏竞争门静脉的血流。这相当于肝损害、门静脉高压及SPSS形成了一个相互作用的恶性循环[14]。
4 结论
综上所述,肝硬化HE患者中SPSS的发生率较高,SPSS对降低门静脉高压的代偿能力是不充分的,反而导致大量血液绕过肝脏解毒,减少肝脏血流灌注、加重肝功能损害,从而导致腹水、门静脉血栓、消化道出血及严重HE等门静脉高压并发症的发生率增高。鉴于SPSS对肝硬化HE患者带来的巨大危害,临床上应重视此类患者的诊断及治疗工作,以期改善肝硬化相关症状,延缓肝硬化进展。
