胰腺去分化脂肪肉瘤一例并文献分析
2023-07-30王泽康吴仁毅陈峰陈雷
王泽康,吴仁毅,陈峰,陈雷
温州市中心医院 急诊外科,浙江 温州 325000
脂肪肉瘤(liposarcoma,LPS)是一种起源于间充质细胞有向脂肪组织分化倾向的恶性肿瘤,约占所有软组织肉瘤的15%~20%[1-2]。去分化脂肪肉瘤(dedifferentiated liposarcoma,DDLPS)作为一种特殊的亚型,最常发生于四肢和腹膜后,发生在胰腺非常罕见[1]。现报道温州市中心医院收治的1例胰腺DDLPS患者并复习相关文献,探讨其临床表现、诊断及治疗方法。
1 临床资料
1.1 本院病例的临床资料
患者男性,49岁,因“腹痛2个月余,加重16 h”至我院急诊科就诊,无恶心呕吐,无发热寒战,于2022年9月21日收住入院。查体:皮肤巩膜无黄染,腹平软,上腹部轻压痛、无反跳痛,Murphy征(-)。辅助检查:血葡萄糖15 mmol/L,糖化血红蛋白14.9%,尿葡萄糖2+,糖类抗原199(CA199)38.5 kU/L,凝血、肝功能等未见明显异常。急诊CT血管成像(CTA):胰腺体尾区见软组织团块影,大小约7.0 cm×8.5 cm,呈分叶状,增强扫描不均匀强化,动脉期内见多发肿瘤血管影,脾动脉部分被包埋,胰腺体颈交界处见一囊性无强化团块影,大小约3.8 cm×5.2 cm,边界清(图1)。增强MRI:胰腺体颈部见不规则囊实性团块状异常信号影,大小约8.5 cm×6.9 cm×9.8 cm,边界尚清,增强后实性部分不均匀强化,囊性部分未见明显强化(图2)。术前诊断考虑“胰腺肿瘤:实性假乳头状瘤?乏血供型神经内分泌瘤?”。完善术前相关检查,排除手术禁忌证后于2022年9月27日行剖腹探查术。术中见胰颈体交界处一肿块(肿块1),大小约3.0 cm×4.0 cm,质软,边界尚清,胰体尾部一肿块(肿块2),大小约8.0 cm×5.0 cm,质硬,活动性差,边界不清,与脾动脉致密粘连,胰颈体交界处肿块能够顺利从颈部剥离,遂决定行胰体尾及脾脏切除术,完整切除胰体尾及脾脏后送病理检查。由于手术创面较大,渗血较多,术中输自体血2 U。术后病理:胰“颈体”部肿块(肿块1)切面灰红质,胰“体尾”部肿块(肿块2)切面灰白质,肿块内未见胰腺组织(图3)。免疫组化:CD34部分(+)、CD117(-)、DOG-1(-)、Desmin(-)、H-caldesmon(-)、SOX10(-)、S-100(-)、SDHB核旁点状(+)、CK(-)、P53 部分(+)、SMA(-)、STAT6(-)、CD99(-)、EMA(-)、β-catenin弱(+)、INI-1弱(+)、HMB45(-)、MelanA(-)、CDK4(-)、P16少数(+)、Vimentin(+)、Bc1-2(-)、Ki-67(约30%+)。结合形态学特点及免疫标记结果,首先考虑DDLPS(去分化成分为纤维肉瘤)。术后患者出现胰漏,经保守治疗后有所好转,后因经济原因自动出院,随访1个月,未见肿瘤复发转移。

图1 本例胰腺DLPS患者腹部CTA

图2 本例胰腺DLPS患者增强MRI
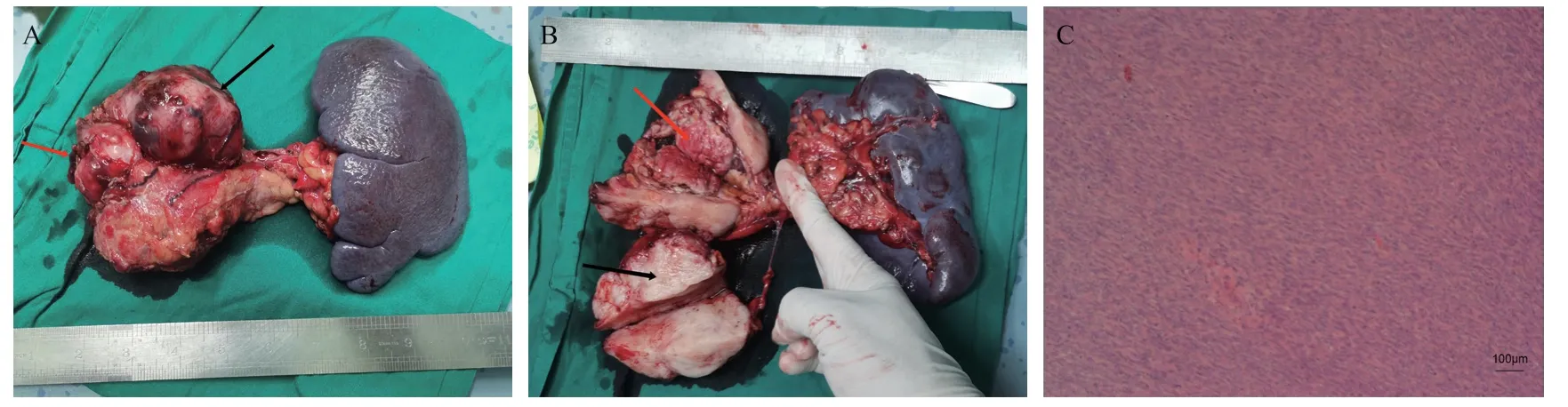
图3 本例胰腺DLPS患者手术大体标本及术后病理
1.2 文献查阅的临床资料
以“胰腺”“胰腺肿瘤”“脂肪肉瘤”“去分化脂肪肉瘤”“pancreatic dedifferentiated liposarcoma”“pancreatic liposarcoma”等为关键词在万方数据、中国知网、PubMed等文献数据库中检索近20年(2002年9月至2022年9月)相关文献报道,选择其中临床资料完整的病例进行报道,经过筛选,最终纳入9例患者(见表1),加上本院病例患者,10例中女6例,男4例,平均年龄为(59.3±20.7)岁。5例临床表现以消化道症状为主,包括腹痛、腹胀、腹泻等,可伴有乏力、体重减轻等,另5例因体检时发现。肿瘤位置:胰头体1例,胰体1例,胰颈体尾1例,胰尾7例。10例患者均行手术治疗,根据肿瘤位置行不同手术方式,胰头体肿瘤因肿瘤靠近胰头体交界行胰体尾及脾切除术,其余患者术式详见表1。7 例获得1~60个月随访,均未见复发。

表1 10例胰腺DDLPS患者的临床资料
2 讨论
脂肪肉瘤是最常见的恶性软组织肉瘤之一,其根据临床病理和分子特征可分为高分化脂肪肉瘤、去分化脂肪肉瘤、黏液/圆细胞脂肪肉瘤及多形性脂肪肉瘤四种亚型[1]。其中高分化脂肪肉瘤是最常见的脂肪肉瘤亚型,其具有恶性程度较低、低转移潜能等特点;去分化脂肪肉瘤相较于前者更具侵袭性,其局部侵袭性和复发转移风险更高;黏液/圆细胞脂肪肉瘤具有较高的远处转移风险,其预后与圆细胞占比相关;多形性脂肪肉瘤是临床上较少见的亚型,占比少于5%,但其恶性程度较高,有更高的远处转移频率(约30%~50%),可转移至肺、骨和肝等部位,预后最差[1,11-12]。去分化脂肪肉瘤约占脂肪肉瘤的15%~20%,好发年龄为50~60 岁,常发生于四肢和腹膜后[1],而胰腺脂肪去分化肉瘤在国内外相关报道中较罕见,本文检索近20年国内外文献共筛选出9例,加上笔者单位1例,共10例。
2.1 胰腺DDLPS的诊断
胰腺DDLPS患者通常无明显临床症状,常在体检时发现,部分患者因肿瘤体积巨大而压迫邻近脏器出现腹部症状,如腹痛、腹胀等。本例患者就诊时自诉腹痛剧烈,于外院就诊考虑“泌尿系结石”,对症处理后症状未见明显缓解,查体时表现为上腹部轻压痛,为排除血管性疾病遂行急诊CTA检查,结合检查结果,考虑腹痛剧烈原因与肿瘤较大压迫临近脏器以及压迫血管引起脏器缺血有关。本文统计的10 例患者中5 例出现消化道症状,有症状组平均肿瘤最大径为(12.8±7.2)cm,无症状组平均肿瘤最大径为(8.3±7.1)cm,有症状患者肿瘤直径往往较大。其以中老年人多见,病变多位于胰尾。实验室检查肿瘤标志物往往都显示正常,有CA199轻微升高的病例报道[2],考虑可能与肿瘤压迫导致主胰管梗阻有关,本例患者CA199轻微升高也考虑与此相关。因其临床及影像学表现的非特异性,术前准确诊断往往较困难。DDLPS在CT上表现以实性软组织团块为主,含有部分脂肪瘤样成分,增强扫描时去分化成分可表现为软组织密度、混合密度、液性密度。本例患者的肿瘤在CTA表现出液性密度(肿块1)以及软组织密度(肿块2),术后病理均提示DDLPS。在MRI上其可见脂肪性成分和非脂肪性成分组成,去分化成分在T1WI上呈现等或稍低信号,在T2WI上呈混杂高低或中高信号,病变内可以出现钙化或骨化区域。CT、MRI增强扫描后去分化成分大多呈现不均匀强化,即强化程度高于同层肌肉,且中央多伴有囊变、坏死。鉴于术前影像学检查均较难进行明确诊断,超声内镜下细针穿刺活组织检查有助于提高诊断的准确性[13-15]。病理学检查仍是确诊胰腺DDLPS的金标准,双微体同源基因2(MDM2)的扩增和过表达是DDLPS的特征,荧光原位杂交(FISH)和免疫组化已经成为脂肪肉瘤类型诊断的常用的检测方法。周期蛋白依赖性激酶4(CDK4)、MDM2和p16基因检测联合使用有助于区分高分化、去分化脂肪肉瘤和其他脂肪肉瘤,93%的去分化脂肪肉瘤表达至少两种标志物抗原。MDM2扩增虽然是DDLPS非常重要的生物标志物,但它不能成为诊断的绝对标准[2,16]。Liu等[5]提出建议以下几个方面对胰腺DDLPS做出诊断:(1)术前的CT检查显示胰腺肿块与腹膜后、胃、结肠、小肠之间存在清晰的“间隙”;(2)术中探查发现胰腺肿块经过钝、锐分离后可以完全切除;(3)术后显微镜下发现胰管共存区域、高分化脂肪肉瘤、未分化脂肪肉瘤;(4)通过荧光原位杂交检查MDM2基因扩增,证实胰腺肿块组织扩增为阳性,腹膜后或其他对照组织扩增阴性;(5)在其他部位未发现脂肪肉瘤的证据。结合术前影像学表现、术中探查所见以及术后病理学检查、免疫组化、基因检测等有助于对胰腺DDLPS做出准确诊断。
2.2 胰腺DDLPS的治疗
手术切除原发肿瘤目前是唯一有效的治疗方法,必要时可行多脏器联合切除。根据肿瘤的不同位置以及肿瘤侵犯的脏器可采取不同的手术方式,本文统计的10 例患者均联合脾脏切除,我院该例患者术中发现胰颈体交界处肿瘤能够顺利从颈部剥离,胰体尾部肿瘤滋养血管较多,且与脾动脉致密粘连,考虑已侵犯脾动脉,遂行胰体尾联合脾脏切除。获得随访的7 例胰腺去分化脂肪患者在随访过程中均未见复发,可能与样本量较少有关,但结合既往研究,DDLPS侵袭性较高,在行根治性切除术后其局部复发率仍高达40%,预后较差[17]。对于有转移或复发的患者来讲,化疗可能是改善其预后或延生存期的必要选择,虽然DDLPS的化学敏感性往往较差,但研究表明在化疗后,部分患者可改善结局[18]。相关研究表示,对于不可切除或者已发生转移的DDLPS患者,推荐的一线治疗仍然是基于蒽环类药物的化疗方案[19]。近来,新型的抗肿瘤药物如艾瑞布林、曲贝替定、酪氨酸激酶抑制剂、MDM2抑制剂、CDK4抑制剂等在脂肪肉瘤治疗中也起着越来越大的作用[17],但其在胰腺DDLPS的治疗中疗效尚不明确。Han等[7]报道了一例酪氨酸激酶抑制剂阿帕替尼对晚期胰腺DDLPS有显著疗效,这为临床相关病例的治疗提供了思路,阿帕替尼的抗血管生成作用可能是治疗晚期胰腺DDLPS的一种新的有效方案。
3 小结
胰腺DDLPS临床上比较罕见,我们对其认识还不全面。患者早期并无特异性临床表现,直至肿块增大压迫临近脏器后才出现消化道症状。影像学上也多无特异性表现,CT表现实性软组织团块为主,增强CT动脉期可有软组织密度、混合密度、液性密度等多种表现,在MRI上信号不均匀,由脂肪性和非脂肪性成分组成,两者之间分界清楚。结合术中探查所见、术后病理学检查、免疫组化、基因检测等有助于对胰腺DDLPS做出准确诊断。若高度怀疑此病,应尽早行手术治疗(R0切除);晚期患者可行个体化的化疗、靶向治疗等治疗方案,以延长患者生存期。随着对脂肪肉瘤的生物学及细胞遗传学进一步认识,越来越多的脂肪肉瘤致病机制、新靶点、靶向药物等被发现,患者预后得到显著改善,但对胰腺DDLPS是否具有同样效果尚需我们进一步验证。尽管本研究获得随访的7 例胰腺去分化脂肪患者在随访过程中均未见复发,但考虑其在其他部位的复发率较高,患者的定期复查、随访十分重要。