肺炎克雷伯菌性眼内炎在糖尿病人群中的特点及预后分析
2023-07-12张小燕李姣李从心原越温莹
张小燕,李姣,李从心,原越,温莹
(山东中医药大学附属眼科医院,济南 250002)
内源性眼内炎也称转移性眼内炎,是全身其他部位的感染灶经过血行途径播散致眼内感染,是一种少见的败血症并发症,约占所有眼内炎的2%~8%,严重威胁人类的视力。内源性眼内炎在东亚和西方国家有不同的致病性微生物[1-2]。西方国家主要以G+菌和念珠菌为主,东亚国家常见G-菌[3-5],目前发现肺炎克雷伯菌为主要病原菌,其发病率近年来呈上升趋势[6]。亚洲国家中全身感染肺炎克雷伯菌后约3.8%~11%发生内源性眼内炎。肝脓肿是最常见的感染灶来源[7]。文献报道肝脓肿伴糖尿病患者中,肺炎克雷伯菌肝脓肿患病率约为39.9%~75.0%,约68.3%发生内源性眼内炎,血糖控制不佳是主要危险因素[8-10]。肺炎克雷伯菌性眼内炎主要由经典肺炎莫尼亚株和高毒力亚株(K1血清型)引起。K1型与糖尿病的关联性约是普通型的20倍,且K1与肝脓肿高度相关,是导致肝外转移感染的重要因素[11]。由于肺炎克雷伯菌毒力强、发病迅速,严重威胁患者视力,而临床工作中对肺炎克雷伯菌性眼内炎的早期诊断缺乏经验,常由于误诊和治疗不及时导致视力严重受损,甚至失明、眼球摘除。因此本文总结分析肺炎克雷伯菌内源性眼内炎在糖尿病患者中的临床表现、影像学特征及治疗,为临床提供一些经验。
1 对象与方法
1.1 研究对象
回顾性分析2019年1月至2022年3月就诊于山东中医药大学附属眼科医院的肺炎克雷伯菌内源性眼内炎7例8眼。所有患者均排除外伤导致的眼内炎。
1.2 研究方法
分析患者视力、眼压、裂隙灯检查、眼底检查、眼科B超、胸腹部颅脑CT,血细胞分析、C反应蛋白、肝肾功能、凝血功能、病毒系列、糖化血红蛋白、心电图检查、治疗经过及复查等病例资料。随访观察0.3~2.0 年。本研究通过医院伦理委员会同意,并遵守赫尔辛斯基宣言。
1.3 统计学方法
2 结果
2.1 一般情况
本组7例8眼,男性5 例(5/7),女性2 例(2/7)。年龄24~75岁,平均(63±17.6)岁。单眼6例(85.7%),双眼1例(14.3%)。左眼6眼(75%),右眼2眼(25%)。糖尿病史0.5~20年,中位数11年。糖尿病是导致患者身体免疫力下降引发感染的一个诱发因素。6例患者到眼科就诊前有发热症状,发热后出现眼部视力下降,就诊时间为3~35 d,平均(16.4±13.2)d。2例患者胸部CT显示肺部感染、1例CT显示肝脓肿,1例为尿路感染;发热与肝脓肿、肺部感染、尿路感染有关。发热引起血流加速,细菌栓子转移导致内源性眼内炎。见表1。
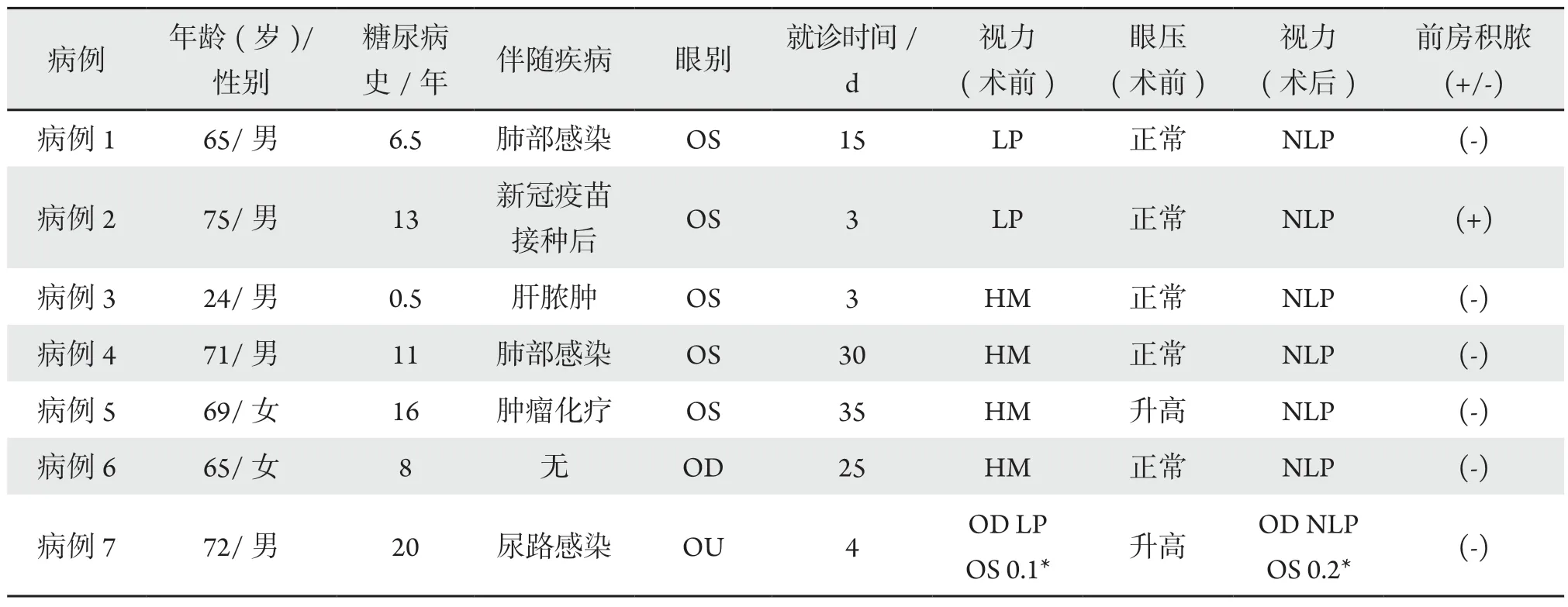
表1 肺炎克雷伯菌眼内炎临床资料Table1 Clinical data of Klebsiella pneumoniae endophthalmitis
2.2 辅助检查
2.2.1 实验室检查
血细胞分析6 例患者的白细胞升高(11.1~27.1)×109/L,中位数15.3×109/L 。7例患者C反应蛋白检测47~161 mg/L,中位数84 mg/L。空腹血糖6.3~14.3 mmol/L,中位数8.1 mmol/L。糖化血红蛋白(7.3~9.4)%,中位数8.2%。1例(16.7%)患者尿常规白细胞升高。所有患者肝肾功能和凝血功能正常。
2.2.2 临床表现及病原学检查
8眼(100%)结膜混合充血;2眼(25%)眼压升高;1眼(12.5%)前房积脓;眼前部临床表现前房积脓少见。8眼(100%)眼底检查玻璃体灰白色浑浊,7眼(87.5%)B超显示脓肿灶来源于脉络膜(图1),表明患者眼内感染来源于血液循环。所有患者术中均取玻璃体液涂片、培养,培养结果显示肺炎克雷伯菌,确诊内源性眼内炎为肺炎克雷伯菌所致。
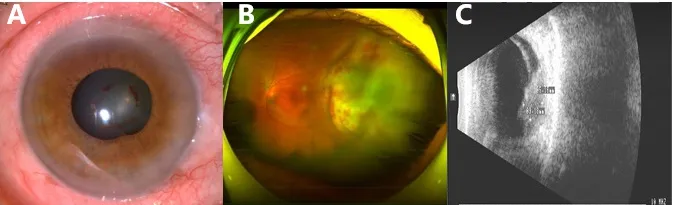
图1 肺炎克雷伯菌眼内炎临床表现Figure 1 Clinical manifestations of Klebsiella pneumoniae endophthalmitis
2.3 治疗结果
所有患者感染均控制,无一例眼球摘除。头孢他啶例6例(85.7%),头孢曲松钠1例(14.3%);培养结果出来后根据病情5例改为美罗培南;7眼(87.5%)行玻璃体切除+玻璃体腔注药术,术中玻璃体腔注射万古霉素联合头孢他啶。1眼单纯美罗培南玻璃体腔注药术。平均注药次数1~3次,中位数2次。4眼(50%)在术后1周内眼压升高,使用降眼压药物及感染控制后眼压正常。治疗后所有患者感染无复发。
3 讨论
肺炎克雷伯菌是一种常见的条件致病菌,常定植于人体呼吸道和肠道。感染时易发生败血症及其他部位迁移性脓肿,引起“侵袭综合征”。常见表现为肝脓肿、尿路感染、脓胸、腹膜炎、脾脓肿、脑膜炎、肌肉骨骼和软组织感染等。肺炎克雷伯菌致内源性眼内炎约9%[3-5],主要发生在糖尿病、恶性肿瘤、肾脏和泌尿生殖系统感染、滥用毒品等免疫力低下人群中。可能与肺炎克雷伯菌比其他微生物的转移扩散率高100倍有关[10]。K1菌株毒力最强,转移感染率高,不仅可以抵抗中性粒细胞的吞噬还可产生一种超黏稠的胞外多糖基质来增强其毒力[11]。研究表明,高毒力致病菌在亚洲人群中高发可能与亚洲人群的基因易感性有关。Chung 等[12]研究发现90%以上的克雷伯菌眼内炎以肝脓肿为主要感染灶。Wong等[13]的病例系列中,发现肝脓肿中约48%的人可能发生内源性眼内炎。Lin等[14]研究发现糖尿病是肺炎克雷伯菌感染的一个主要危险因素,主要为男性患者,平均年龄为58岁。本组6例均为糖尿病患者,糖化血红蛋白在8%以上,有反复发热病史,且均在发热后出现视力下降,表明发热是肺炎克雷伯菌性眼内炎的危险因素,也是其临床特征之一。目前关于糖尿病患者易发生肺炎克雷伯菌感染的机制尚不清楚。这可能是由于长期的高血糖导致身体抵抗力下降,肺炎克雷伯菌和宿主防御机制之间的不平衡促进其通过胃肠道进入血流。血糖控制不稳定导致血管通透性升高,血液屏障被破坏,细菌栓子经血源播散并滞留于脉络膜和视网膜末梢小血管内。糖尿病患者机体免疫力下降,白细胞的趋化、黏附和吞噬功能受到抑制,清除病原菌能力下降导致细菌转移定植引起眼内炎[10]。因此临床中对于血糖控制差的糖尿病患者,反复发热后出现视力下降需警惕内源性眼内炎的发生。一旦发生,建议行胸腹部CT检查寻找感染灶。本组病例中发现1例肺、肝多处小脓肿灶,1例泌尿系统感染,2例肺部感染。合并肝脓肿仅为1例,可能与样本量少有关。但也有研究表明,克雷伯菌性眼内炎患者也可不伴全身感染。同时,肺炎克雷伯菌引起的内源性眼内炎多见于中老年男性,常单眼受累,这和本研究结果类似。
肺炎克雷伯菌眼内炎眼部表现早期不典型,仅出现轻微的眼红、视力模糊、飞蚊症等症状,被误诊为青光眼和葡萄膜炎进行治疗。后期表现可出现多样性、局灶性或弥漫性炎症、全眼球炎等[15]。本组患者中,早期症状均以眼红为主,裂隙灯检查表现为结膜充血,房闪(+++),虹膜后粘连,早期易被误诊。其中2例患者误诊为青光眼,行YAG激光联合降眼压药物治疗。4例被误诊为葡萄膜炎。早期误诊不仅延误治疗同时严重损伤视力,本组6例患者就诊时间为(15.71±12.62)d,术后视力预后差。眼科B超可帮助早期诊断,Chung等[12]研究发现87.5%的患者眼科B超表现为弥漫性的玻璃体浑浊,可能与病原微生物随着血液循环定植于脉络膜内,宿主防御被突破后,通过视网膜扩散到玻璃体腔内。本研究中眼科B超早期可表现为均匀致密的玻璃体浑浊,伴有视网膜及球壁的水肿,部分在早期即可出现来源于脉络膜的局灶性的隆起,随着病程的延长隆起逐渐增大。因此,对于可疑肺炎克雷伯菌性眼内炎的患者,应密切观察其眼科B超检查结果,以进行初步诊断。其次,前房积脓是诊断眼内炎的一项重要指标,当炎症反应到一定程度后,炎症细胞或组织碎屑通过小梁网或悬韧带进入前房形成。文献报道患者从出现症状到就诊平均在7 d左右,80.5%患者出现房闪(++),60.1%的患者出现前房积脓[10]。Ranjan等[16]发现肺炎克雷伯菌性眼内炎者前房积脓出现较晚或不出现。本研究中仅有1例患者出现前房积脓,且发生在眼内炎的晚期,可能与内源性眼内炎多从后部脉络膜血行途径转移、血-眼屏障的存在有关,多集中表现在脉络膜炎症和玻璃体腔炎症,前房积脓少见。因此,在临床中对于糖尿病患者在发热后出现视力下降且伴有前部葡萄膜炎、玻璃体灰白色混浊的情况下,需警惕内源性眼内炎的发生。同时,我们还发现患者白细胞计数和C反应蛋白均高于正常值,尤其中性粒细胞,可作为一个重要辅助诊断指标。虽然可根据病史、临床表现、眼科B超早期做出初步诊断,但血液或组织液微生物培养仍是诊断和治疗的金标准,但血培养阴性不能排除诊断。若伴有肝脓肿或全身其他部位感染需穿刺脓肿培养或血培养,脓肿培养阳性率高于血培养[3-5]。目前,眼内液培养不同文献报道的阳性率不一样,约为30%~50%,宏基因检测阳性率约70%。低的培养阳性率可能取材和接种时机和方法有关。本研究在不建立灌注的情况下直接切取玻璃体液,取出后直接涂片查菌和接种培养皿,培养率可达75%。玻璃体切割术中,我们发现肺炎克雷伯菌性眼内炎玻璃体呈灰白色浑浊并夹杂一些红色色素颗粒,视网膜血管闭锁阻塞呈白线状,管壁黄白色渗出,出血少见;视网膜均匀弥漫灰色浑浊水肿,严重者视网膜出现白色碎片状坏死;脉络膜散在多灶性、灰白色地图状改变。这也可作为肺炎克雷伯菌性眼内炎的一个表现,可根据术中所见经验性选择玻璃体腔注射药物。
针对肺炎克雷伯菌性眼内炎治疗还没有一致的专家共识。目前治疗包括全身治疗和局部治疗。肺炎克雷柏杆菌性眼内炎合并肝脓肿死亡率约6%~21%,不同文献报道不一致[17],易发生弥散性血管内凝血或感染性休克。由于内源性眼内炎可能存在原发感染灶和脓毒血症,需要多手段联合治疗,包括全身使用抗菌药物、脓肿穿刺引流、控制血糖、全身营养支持等。针对肺炎克雷伯菌感染,国内首选的抗菌药物为碳青霉烯类,具有广谱、强细菌耐药发生率低等特点,对肺炎克雷伯菌的敏感性强。常用亚胺培南、美罗培南、比阿培南等。目前亚洲出现耐第三代头孢菌素和氟喹诺酮类药物的肺炎克雷伯菌(CnSKP)。Rossi等[18]报道注射亚胺培南/西司他丁钠治疗多重耐药的肺炎克雷伯菌取得满意效果。局部治疗包括眼内液涂片、培养和药物敏感试验,以及玻璃体腔内注射广谱抗菌药物、玻璃体切除等。目前大多数研究建议进行早期积极的干预,尤其当玻璃体腔药物注射效果差或玻璃体浑浊加重时,建议尽早行玻璃体切割术。Modjtahedi等[19]发现尽早行玻璃体切割术治疗优于玻璃体腔药物注射的患者,前者感染控制和视力恢复更好。玻璃体切割术不仅可以清除细菌和炎症物质,还可增加抗菌药物的眼内渗透性。研究表明53.9%的内源性眼内炎患者需行玻璃体切除联合全身静脉使用抗菌药物,39.8%的患者需要玻璃体腔注药联合静脉用药,只有6.3%的患者仅单纯玻璃体腔注射抗菌药物[20]。Sadiq等[21]研究玻璃体切割术的患者,与单纯玻璃体内注药患者相比较,后者约50%最终需要进行眼内容手术。我们的观点是患者视力下降明显,玻璃体浑浊即行玻璃体切割术。术中根据眼底表现经验性选择万古霉素1 mg/0.1 mL或头孢他啶2.25 mg/0.1 mL单独或联合玻璃体腔注射;视网膜坏死严重者选择美罗培南1 mg/0.1 mL眼内注射,因其对玻璃体腔和脑脊液有强的穿透性。眼内注药可根据病情36~72 h重复注射,治疗过程中监测全身系统症状及血细胞情况。肺炎克雷伯菌性眼内炎病程长短、就诊时间、血糖与预后密切相关。感染早期发现并积极治疗视力预后好;发病时间长、就诊时视力差预后往往较差。控制血糖联合治疗全身感染灶,眼球摘除率相对低,本组病例中无一例摘除眼球。所有患者入院后即接受全身抗菌药物和强化局部抗菌药物治疗,全身一般选择第三代或第四代头孢菌素,细菌培养及药敏结果出来后根据病情选择全身及局部美罗培南治疗。病情稳定后,根据血细胞检查结果改为口服喹诺酮类和三代头孢菌素,一般使用2~3个月停药。
综上所述,肺炎克雷伯菌性眼内炎是一种严重的疾病,对视力造成不可逆的损伤,需要多学科联合快速的诊断和治疗改善预后。正确使用抗菌药物之外,仍需引流和治疗原发部位脓肿。首诊在眼科的可疑内源性眼内炎患者,医生要进行排查全身疾病,尤其关注糖尿病患者,确诊后应积极进行多学科会诊治疗。鉴于转移性眼部感染的高趋势,建议克雷伯菌败血症患者常规进行眼科的筛查,尽早治疗可有效控制病情并保留视力。
利益冲突所有作者均声明不存在利益冲突
开放获取声明
本文适用于知识共享许可协议(Creative Commons),允许第三方用户按照署名(BY)-非商业性使用(NC)-禁止演绎(ND)(CC BY-NC-ND)的方式共享,即允许第三方对本刊发表的文章进行复制、发行、展览、表演、放映、广播或通过信息网络向公众传播,但在这些过程中必须保留作者署名、仅限于非商业性目的、不得进行演绎创作。详情请访问:https://creativecommons.org/licenses/by-ncnd/4.0/。