心脏外科术后病人呼吸机相关性肺炎危险因素的Meta分析
2023-07-11吉双对张竹英郑栋莲郭淑萍刘风景米光丽
吉双对,张竹英,郑栋莲,郭淑萍,白 雪,刘风景,米光丽,*
1.宁夏医科大学护理学院,宁夏 750004;2.宁夏医科大学总医院
呼吸机相关性肺炎(ventilator-associated pneumonia,VAP)是指病人在建立人工气道及机械通气48 h后或停止机械通气48 h以内新发生的医院获得性肺炎[1]。VAP的发生可导致病人机械通气时间延长、医疗费用增加和住院时间延长,甚至增加病人的死亡率[2-3]。研究表明,在接受机械通气48 h以上的病人中,10%~20%的病人会发生VAP[4]。8%~15%的心脏外科术后病人机械通气时间超过48 h[5],导致VAP的发生率进一步增加。有研究表明,VAP是心脏术后病人最常见、最严重的感染,且已被确定为心脏手术后病人死亡的独立危险因素[6]。目前,国内外对心脏术后VAP危险因素的研究结果差异较大,纳入相同危险因素的结果也存在差异。因此,本研究旨在对国内外关于心脏术后病人发生VAP的危险因素研究进行Meta分析,探讨心脏术后发生VAP的危险因素,为临床识别潜在高危人群和预防VAP提供科学依据。
1 资料与方法
1.1 资料来源与检索策略
计算机检索中国知网、中国生物医学文献数据库、万方数据库、维普数据库、PubMed、EMbase、Web of Science等数据库,收集有关心脏外科术后病人发生VAP危险因素的文献,检索时限为建库至2022年8月30日。采用主题词与自由词相结合方式,中文检索式:(心脏术后 OR 心脏手术 OR 冠状动脉搭桥术 OR 冠状动脉旁路移植术 OR 瓣膜置换术 OR 瓣膜手术 OR 体外循环)AND(呼吸机相关性肺炎OR 呼吸机相关肺炎 OR 机械通气相关性肺炎 OR 机械通气相关肺炎) AND (危险因素 OR 影响因素 OR 相关因素 OR 病因);英文检索式:(cardiac surgery OR heart surgery OR coronary artery bypass OR aortocoronary bypasses OR extracorporeal circulation) AND (VAP OR ventilator-associated pneumonia) AND (risk factor OR relevant factors OR influencing factor)。
1.2 文献纳入标准
1)文献类型:国内外公开发表的关于心脏外科术后VAP危险因素的病例对照研究、队列研究,文献语言为中文、英文,发表时间为2000年1月—2022年6月;2)VAP有明确的诊断标准或指南;3)研究对象:心脏外科术后病人机械通气时间≥48 h,以是否发生VAP为标准分为病例组(VAP组)和对照组(非VAP组),年龄≥18岁;4)结局指标:原始文献采用多因素Logistic回归分析,文献提供VAP危险因素的比值比(OR)值及其95%的置信区间(CI)。
1.3 文献排除标准
1)非病例对照研究、非队列研究;2)对VAP没有明确的诊断标准,或对危险因素的定义与纳入的大部分研究不一致;3)未对影响因素进行统计学分析或统计方法不当;4)无法获取全文或数据不完整的研究;5)会议摘要、文献综述、案例报告等。
1.4 资料提取
资料提取由2名研究者独立完成并交叉核对,不一致时及时核查原始资料。主要提取内容包括作者、发表年份、研究类型、样本量(病例组/对照组)、心脏手术类型、危险因素、危险因素的OR值及其95%CI等。
1.5 文献质量评价
参考观察性研究的文献质量评价量表——纽卡斯尔-渥太华量表(NOS)[7],对纳入文献研究的人群选择、组间可比性、暴露因素等3个方面进行质量评价,满分为9分,评分≥5分为高质量文献[6]。2名研究者分别按照相应的标准对纳入文献独立进行评价。若意见出现分歧,则经讨论决定,难以达成一致时咨询第3方。
1.6 统计学方法
采用RevMan 5.3软件,首先对符合纳入标准的文献进行异质性检验,如果P>0.1、I2<50%认为各研究间具有同质性,选用固定效应模型进行分析;如果P<0.1、I2≥50%,采用随机效应模型进行分析。结果采用OR和95%CI表示,用敏感性分析寻找异质性来源,无法判断来源者,则采用描述性分析,同时绘制漏斗图进行发表偏倚评价。
2 结果
2.1 文献检索结果
初步检索获得相关文献706篇,通过阅读题目、摘要、关键词及全文最终纳入11篇文献,其中中文文献8篇,英文文献3篇。见图1。
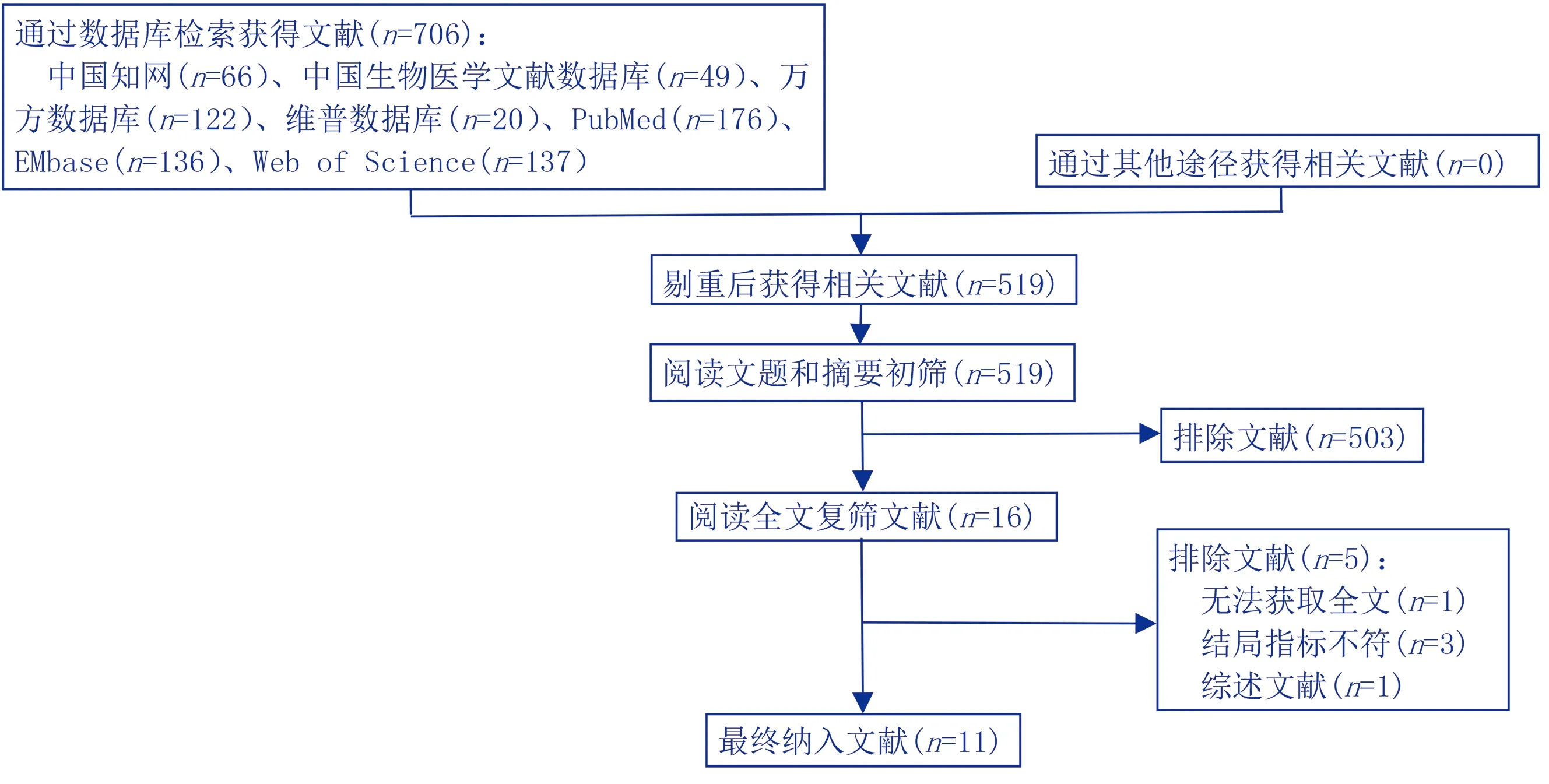
图1 文献筛选流程图
2.2 纳入文献研究的基本特征
纳入的11篇文献发表时间为2009年—2020年,其中10篇为病例对照研究,1篇为队列研究,样本量为77~1 688例,累计4 561例,术后发生VAP 697例,发生率为15.28%。纳入研究的基本特征见表1。
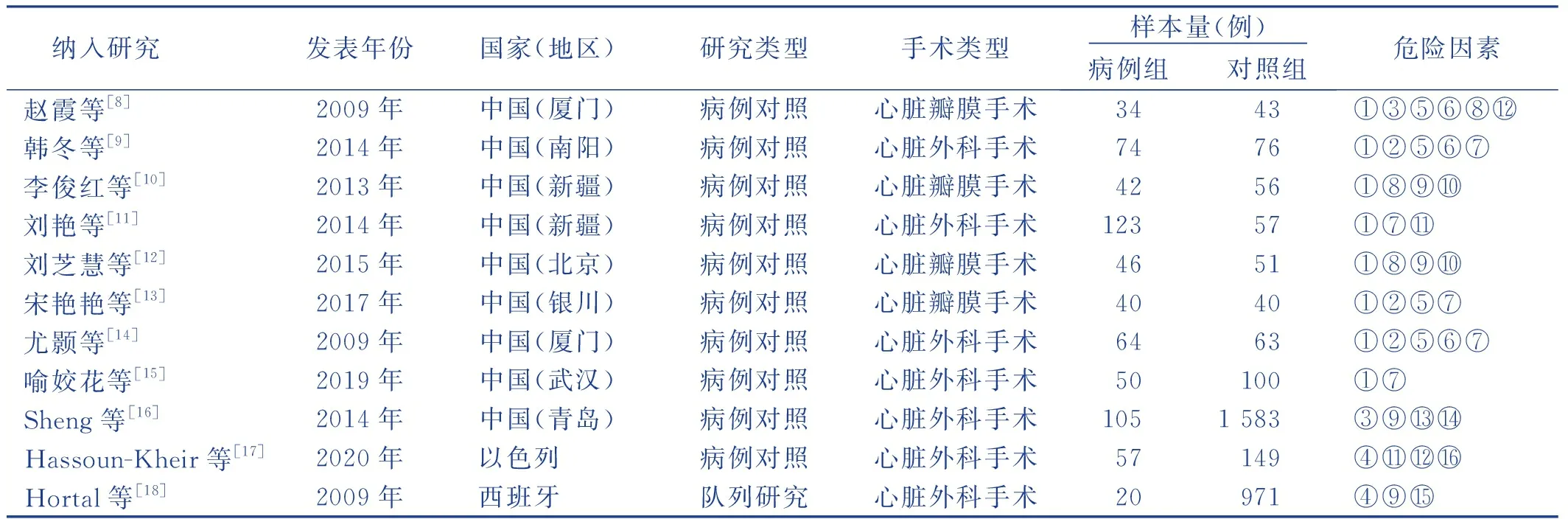
表1 纳入文献基本特征
2.3 纳入研究质量评价
所有纳入研究均严格按照NOS标准进行评分,得分在6~8分,总体质量在中等以上。见表2。

表2 纳入文献质量评价 单位:分
2.4 Meta分析结果
Meta分析结果显示:体外循环时间≥120 min,输血量>1 200 mL、术后氧合指数≤300 mmHg、气管切开、机械通气时间≥5 d、再次插管、应用抑酸剂、二次开胸、肺动脉高压是心脏外科术后发生VAP的危险因素,差异均具有统计学意义(P<0.05),见表3。有研究报道,年龄>70岁、急诊手术、升主动脉手术、充血性心力衰竭等因素也与心脏外科术后VAP有关,但文献大多数仅为1篇,故未对此进行Meta分析。

表3 心脏外科手术后发生VAP危险因素的Meta分析结果
2.5 敏感性分析
为检验分析结果的稳定性和可靠性,对纳入的11项指标分别采用随机效应模型和固定效应模型计算OR值和95%CI,讨论其结果的稳定性。结果表明各危险因素在两种模型下的合并效应接近,结果较为稳定。见表4。
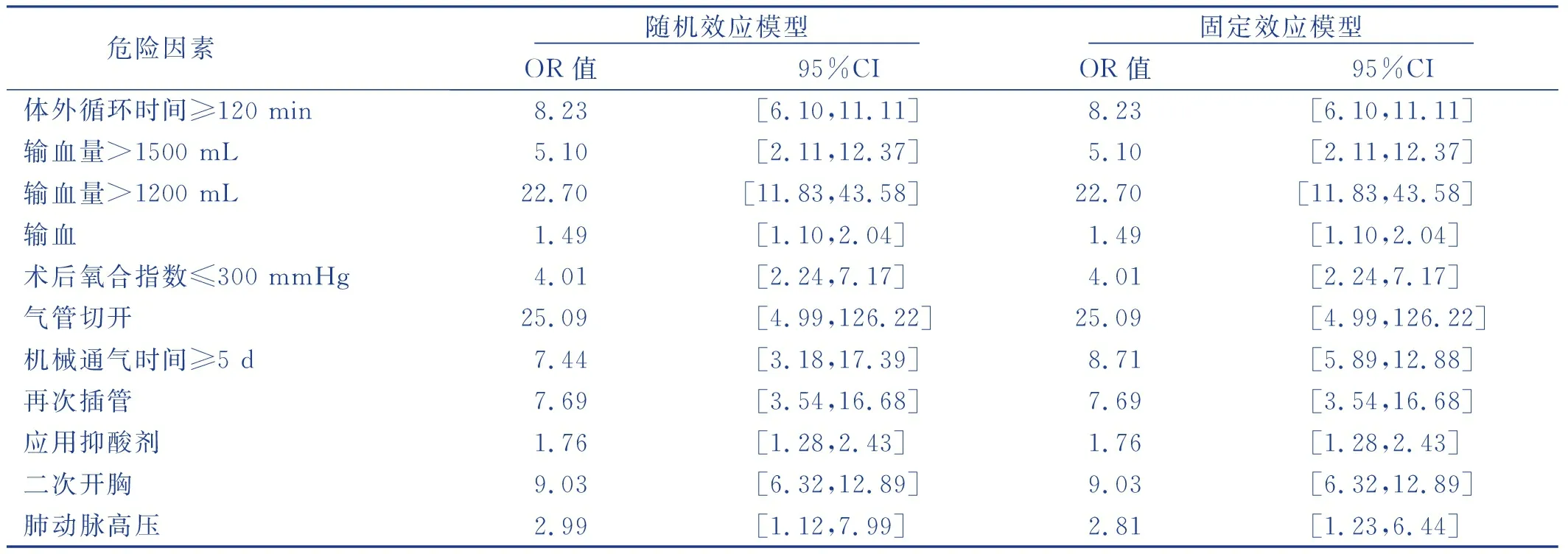
表4 随机和固定效应模型的效应量合并结果
2.6 发表偏倚
采用Egger′s检验对发表偏倚进行判断,结果显示,术后氧合指数≤300 mmHg(P<0.05)存在一定的发表偏倚,其余危险因素未见明显偏倚。漏斗图以术后氧合指数≤300 mmHg为例,见图2。
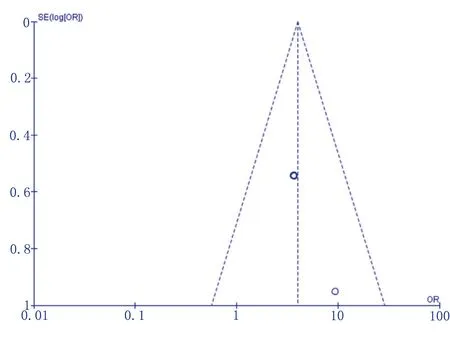
图2 术后氧合指数≤300 mmHg发表偏倚评价
3 讨论
3.1 纳入文献的特征分析
本研究共纳入11篇文献,以病例对照研究为主,研究对象共4 561例,其中9篇来自国内,2篇来自国外。依据NOS质量评分均在6~8分,说明文献质量在中等以上。所有研究对象均为成年人,避免了因年龄造成的偏倚。所有研究均明确了研究对象的来源、结果的诊断标准,但是未区分心脏手术类型,可能会对结果造成一定的影响。
3.2 心脏外科术后VAP的危险因素分析
3.2.1 体外循环时间≥120 min
本研究表明,体外循环时间≥120 min与病人术后VAP发生密切相关。体外循环时间是术中唯一被证实可影响术后呼吸衰竭的危险因素,且体外循环时间越长,肺部损伤越严重[19],主要因为系统性炎症反应导致白细胞在肺内黏附和聚集、多形核白细胞的激活等造成肺组织损伤和肺脏缺血/再灌注损伤;体外循环时血液稀释造成低蛋白血症,血浆胶体渗透压下降、左心引流不畅等造成的肺功能受损;体外循环机造成血液成分的破坏,释放组胺、激肽等物质使肺毛细血管通透性增加,出现水肿和出血,在肺内形成透明膜等[11]。体外循环时间延长可并发急性呼吸功能不全、引起机械通气时间延长,从而导致VAP发生。因此,外科医师需提高手术水平,加强与麻醉师、体外循环师及器械护士的配合,尽可能缩短体外循环时间,以减轻肺脏损伤。
3.2.2 术后氧合指数≤300 mmHg或机械通气时间≥5 d
本研究表明,术后氧合指数≤300 mmHg或机械通气时间≥5 d均为心脏手术后病人发生VAP的危险因素。有研究表明,呼吸机使用时间每延长1 d,VAP发病率增加2.0%~3.8%[20]。主要原因为心脏手术体外循环时间越长,肺组织损伤越严重,从而导致氧合指数越低[13];术后机械通气支持过程中气管插管可能导致咽喉部损伤,破坏气道的防御功能;手术本身作为应激源,也可引起局部气道防御功能减退,细菌易在气道上皮细胞附着[9],从而增加肺部感染的机会,延长机械通气辅助时间,增加VAP发生的风险。本研究对纳入机械通气时间≥4 d的3篇文献[8,10,12]和机械通气时间≥5 d的5篇文献[9,11,13-15]进行亚组分析,结果显示,机械通气时间≥5 d,VAP的发生风险进一步增加。因此,心脏术后应积极控制原发疾病,早期使用抗生素[21-22],严格呼吸道管理,增强病人免疫力,尽快控制病情,在条件允许情况下尽早撤机以降低并发症发生风险。
3.2.3 输血量
本研究对输血量>1 500 mL的3篇文献[9,13-14]、>1 200 mL的2篇文献[8,16]、未明确定义输血量的2篇文献[17-18]进行亚组分析,输血量>1 500 mL时,合并OR值及95%CI为[5.10(2.11,12.37)];输血量>1 200 mL时,合并OR值及95%CI为[22.70(11.83,43.58)],2篇文献未明确定义输血量,合并OR值及95%CI为[1.49(1.10,2.04)]。结果显示,随着输血量的增加,VAP的发生风险随之增加。心脏外科手术长时间的体外循环需消耗大量的血液制品,输入的血液中常含有与受血者白细胞抗原相应的人类组织相容性抗原或抗粒细胞抗体,进而发生抗原抗体反应[23],引起肺损伤或病人免疫功能抑制,从而延长机械通气时间,导致VAP发生风险增加。
3.2.4 气管切开
气管切开病人气道正常组织结构和保护屏障遭到破坏,吞咽、咳嗽反射减弱或消失,也导致气管内部暴露在空气中[14],从而增加了病原菌侵入气管的风险,加上病人免疫功能低下,从而增加了病人病原菌感染风险,最终导致机械辅助通气时间延长,增加病人术后VAP的发生风险。
3.2.5 再次插管
再次插管主要是由于病人拔管后病情恶化、气管套管脱出等原因引起,不仅延长了机械通气时间,还增加了感染的风险[14];同时侵入性操作导致病人机体再次受到损伤,产生应激反应,导致免疫力下降,增加感染风险[9];再次插管时还会使口咽部潜在的致病菌被吸入[24]。因此,再次插管不仅可增加VAP的发生风险,还会增加死亡的风险[25]。
3.2.6 应用抑酸剂
本研究表明,应用抑酸药可增加VAP发生的风险。抑酸药是心脏外科术后通过降低胃液酸度预防应激性溃疡的常用药物,但胃酸降低可使胃内细菌大量繁殖,而胃食管反流过程中大量细菌随反流液进入肺内引起肺部感染,进而发生VAP[12]。因此,在心脏术后应用抑酸剂时应将病人床头抬高30°~45°或取半卧位,以减少胃内容物反流,或使用胃黏膜保护剂,如硫糖铝等代替抑酸剂治疗[10,26]。
3.2.7 二次开胸
心脏手术病人本身承受巨大的手术创伤,二次开胸术使病人再次经历创伤,创伤导致机体免疫功能减弱[27],手术镇静时间延长、呼吸机使用时间延长等,进而发生VAP的风险增加。术中应严格止血并观察各项指标,术后应密切观察病人病情变化,及时检测凝血功能,严格掌握输血适应证等以减少二次开胸的机会。
3.2.8 肺动脉高压
肺动脉高压是一类以肺动脉内压力异常升高,伴或不伴有小肺动脉病变为特征的疾病或病理生理综合征,存在肺循环障碍和右心高负荷,可导致病人心力衰竭甚至死亡[28]。肺动脉高压时由于肺血管扩张、血管平滑肌张力增加或增殖均可影响小气道的功能[29],导致肺泡换气功能受损,氧合指数降低,延长机械通气辅助时间,从而增加VAP的发生风险。
3.3 研究的局限性及展望
1)本研究纳入的文献数量有限,样本量较小,可能会导致结果在一定程度上出现偏差;2)由于国内外对心脏术后VAP发生的危险因素研究有限,且大多数为回顾性研究,文献质量参差不齐,可能存在一定的发表偏倚;3)部分危险因素涉及的文献数量较少无法进行数据的整合,也会对结果产生不同程度的影响。因此,未来还需开展更多设计严谨、大样本、多中心的前瞻性研究,进一步明确心脏术后病人发生VAP的危险因素。
4 小结
本研究结果显示:心脏外科术后VAP的危险因素共计9项,即体外循环时间≥120 min、输血量>1 200 mL、术后氧合指数≤300 mmHg、气管切开、机械通气时间≥5 d、再次插管、应用抑酸剂、二次开胸、肺动脉高压等。医护人员应关注这些危险因素,早期识别心脏术后VAP高发人群,采取科学、有效的预防措施,减少心脏手术后VAP的发生。
