基于“辨状论质”结合指纹图谱的杜仲药材质量等级标准研究
2023-07-11周正宗吕尚金浩鑫杨华杰吴柳瑾吴海信饶毅江西中医药大学江西南昌330004中药固体制剂制造技术国家工程研究中心江西南昌330006
周正宗,吕尚,,金浩鑫,杨华杰,,吴柳瑾,吴海信,饶毅, (. 江西中医药大学,江西 南昌 330004;. 中药固体制剂制造技术国家工程研究中心,江西 南昌 330006)
杜仲是杜仲科植物杜仲EucommiaulmoidesOliv.的干燥树皮,富含木脂素类、环烯醚萜类、酚类、多糖、杜仲胶等多种成分[1-2],其中松脂醇二葡萄糖苷等木脂素类成分具有降压、预防骨质疏松的作用[3],京尼平苷酸、京尼平苷和京尼平等环烯醚萜类成分具有保护肝脏的作用[4]。杜仲分布范围广,在四川、湖南、江苏、江西等10 余个省份均有产出[5],加之采收时间、产地、加工方法及药材贮藏条件等影响,导致市场上杜仲药材质量有很大区别[6-7]。现行的杜仲商品规格等级以厚度为主要参考指标,具有很强的实用性,但对杜仲药材的内在质量表征不够全面,在进行内在指标检测时常存在不合格情况[8-9]。传统的“辨状论质”观点认为杜仲以皮厚、内表面黑色、折断白丝多为佳。本研究将传统指标进行量化,运用多元统计分析方法,建立杜仲药材质量等级标准。为了进一步验证所建立的等级标准对杜仲药材内在质量的表征情况,建立杜仲药材高效液相色谱(HPLC)指纹图谱,以共有峰面积进行系统聚类分析,用以评价不同等级杜仲药材的质量,以期建立科学合理的杜仲药材质量等级标准。
1 仪器与材料
1.1 仪器 LC-20AT 高效液相色谱仪(日本岛津公司);KDW 控温电热套(山东鄄城华鲁仪器公司);CS101-2EB 电热鼓风干燥箱(重庆万达仪器有限公司);Ci7800 型台式色差仪(上海爱色丽色彩科技有限公司);AB-104N 万分之一天平(瑞士梅特勒-托利多公司);Milli-Q 超纯水仪(美国Millipore 公司);MNT-150T 游标卡尺(德国美耐特公司)。
1.2 材料 本研究共收集了江西、四川、湖南、陕西、湖北、河南、安徽、甘肃共8 产地28 批次的杜仲药材。样品信息见表1。甲醇(分析纯,国药集团化学试剂有限公司);甲醇(色谱纯,AQA 公司);磷酸(色谱纯,上海阿拉丁生化科技股份有限公司);松脂醇二葡萄糖苷对照品(批号:YRS003-210302)、京尼平苷(批号:YRL2005-210101),成都仪睿生物科技有限公司;京尼平苷酸对照品(批号:111530-201713)、绿原酸对照品(批号:110753-201817),中国食品药品检定研究院;京尼平(中药固体制剂制造技术国家工程研究中心自制,纯度>98%)。
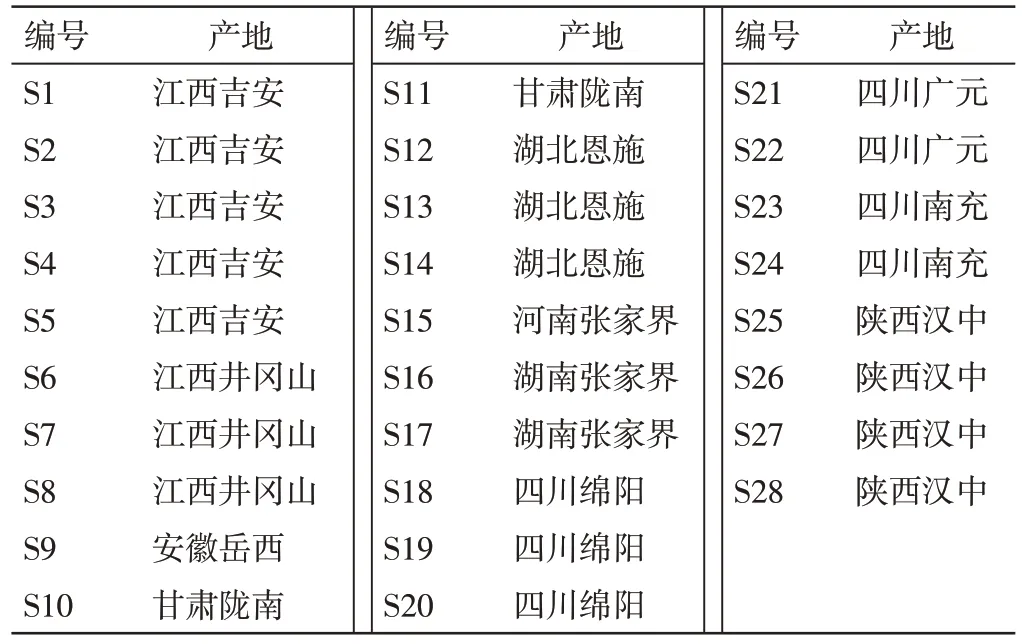
表1 28 批杜仲药材样品信息Table 1 Sample information of Eucommiae Cortex
2 方法
2.1 杜仲药材指标成分HPLC 含量测定
2.1.1 色谱条件 以Agilent-C18(4.6 mm×250 mm,5 μm)为色谱柱,甲醇(A)-0.1%磷酸水溶液(B)为流动相,梯度洗脱(0~10 min,5%~10% A;10~15 min,10% A;15~20 min,15%~22% A;20~35 min,22%;35~45 min,22%~25% A;45~60 min,25%~30% A);检测波长为240 nm(京尼平苷酸、京尼平苷、京尼平)、277 nm(松脂醇二葡萄糖苷);柱温为30 ℃;流速为1 mL·min-1;进样量为10 μL。杜仲药材的HPLC 色谱图见图1。
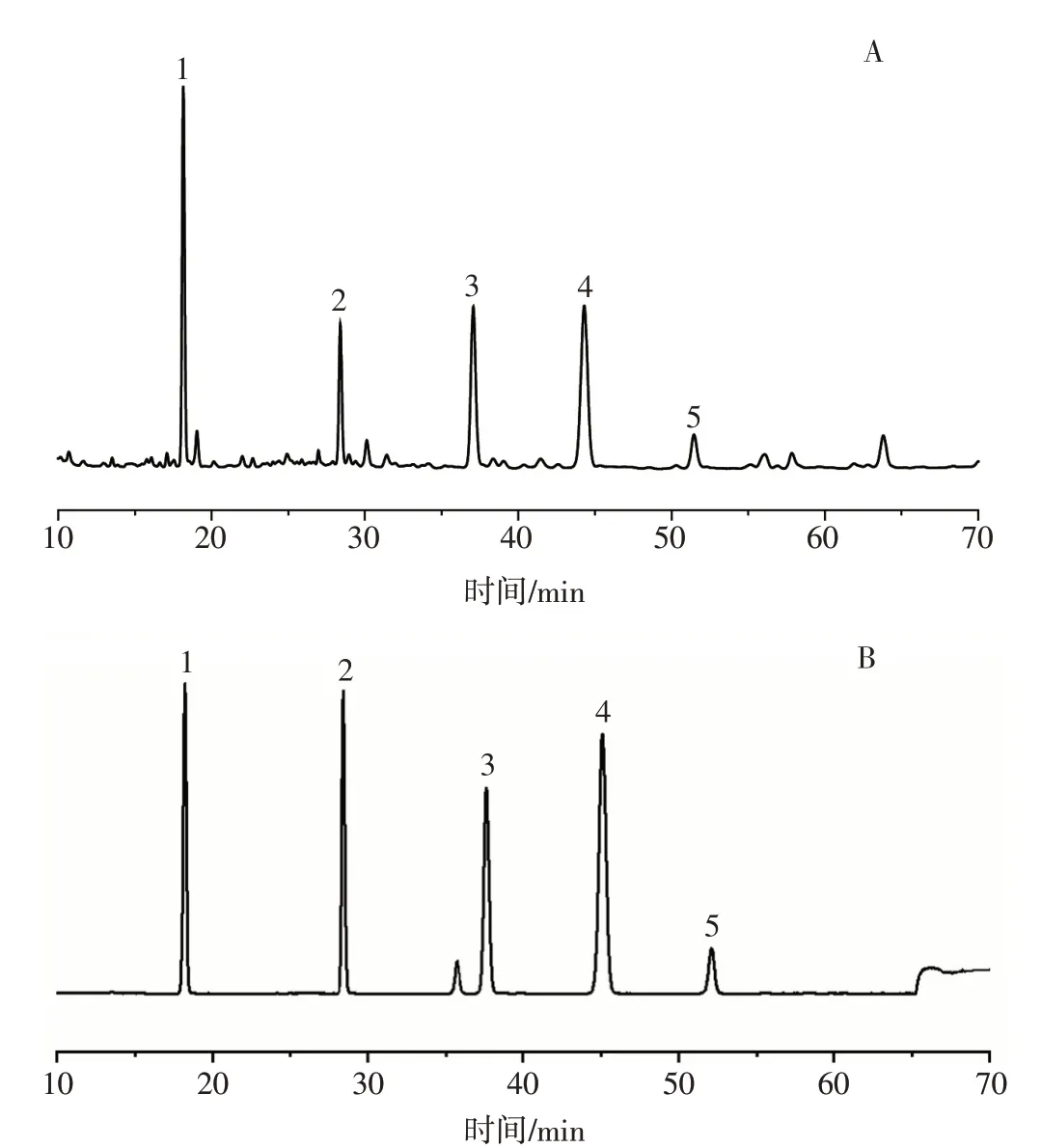
图1 杜仲药材(A)和对照品(B)的高效液相色谱图Figure 1 HPLC chromatogram of Eucommiae Cortex(A)and samples(B)
2.1.2 供试品制备 精密称取杜仲粉末(过3 号筛)约1.5 g,加70%甲醇25 mL,称定质量,加热回流1 h,放冷;再称质量,用70%甲醇补足减失的质量;摇匀,滤过,取续滤液,作供试品溶液。
2.1.3 对照品溶液的制备 取京尼平苷酸、京尼平苷、京尼平和松脂醇二葡萄糖苷对照品适量,精密称定,加甲醇制成每毫升含0.2 mg 京尼平苷酸、0.1 mg 京尼平苷、0.1 mg 京尼平和0.2 mg 松脂醇二葡萄糖苷的混合溶液,即得。
2.1.4 方法学验证 对京尼平苷酸、京尼平苷、京尼平和松脂醇二葡萄糖苷进行方法学考察(线性关系、精密度试验、重复性试验、稳定性试验、加样回收率试验),计算相关系数(r)、平均加样回收率和其及RSD,结果表明此方法的线性关系(r>0.999)、回收率、重复性、稳定性和仪器精密度(RSD 均小于3%)均良好。
2.2 厚度、皮长、皮宽测定 从每批杜仲药材中选取3 片,用游标卡尺测定杜仲两端的厚度,用皮尺测定杜仲药材的皮长和皮宽,每片测量3 次,计算平均值,记录数据。
2.3 颜色测定 使用台式色差仪,光源:D65/10°;测定孔径25 mm;仪器经过黑、白板背景校正后开始进行样品测定,得到L*、a*、b* 3 个数值,每份样品测定6 次,以均值为该样品的色差值。其中L*值为明暗度指标,L*值越大代表样品色泽越明亮,反之代表样品越暗;a*值为红绿色度的指标,a*值越大,代表样品颜色越红,反之代表样品越绿;b*值为黄蓝色度的指标,b*值越大代表样品颜色越黄,反之越蓝。结果见表2。
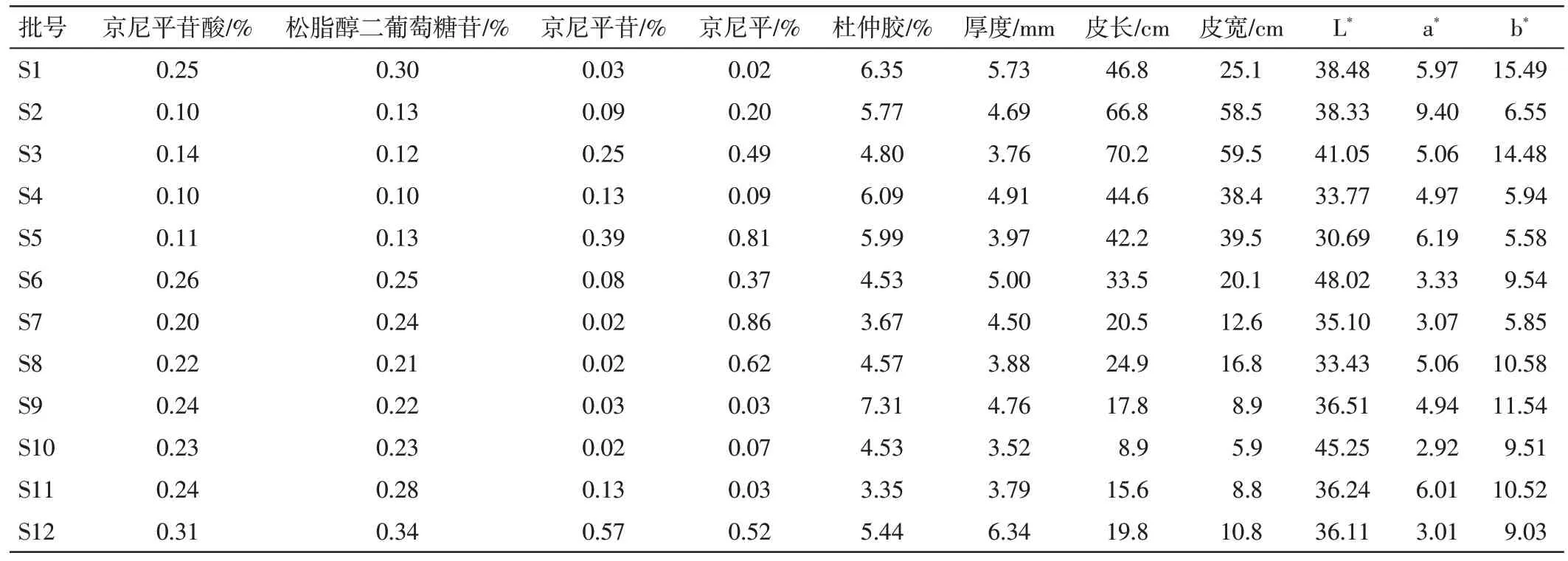
表2 28 批杜仲药材内在质量和外形性状指标的测定结果Table 2 The internal quality and external properties of 28 batches of Eucommiae Cortex
2.4 杜仲胶测定 取杜仲约3 g,剪碎,揉成絮状,取约2 g,精密称定。将样品置于索式提取器中,加入乙醇100 mL,加热回流3 h。弃去乙醇,加入氯仿100 mL,索氏回流提取6 h。再用30 mL 氯仿分3 次润洗后合并氯仿,利用旋转蒸发器进行回收,蒸干后用适量三氯甲烷润洗,置于恒重蒸发皿上蒸干。之后转入真空干燥箱,温度设置为40 ℃。真空干燥10 h 后放入干燥器中,放冷后称质量。通过对提取溶剂(氯仿、石油醚、乙醚)、提取时间(4、6、8 h)考察,得出以氯仿索氏提取6 h 最佳,且方法重现性良好(RSD<2.6%,n= 6),可用于杜仲内杜仲胶的含量测定。
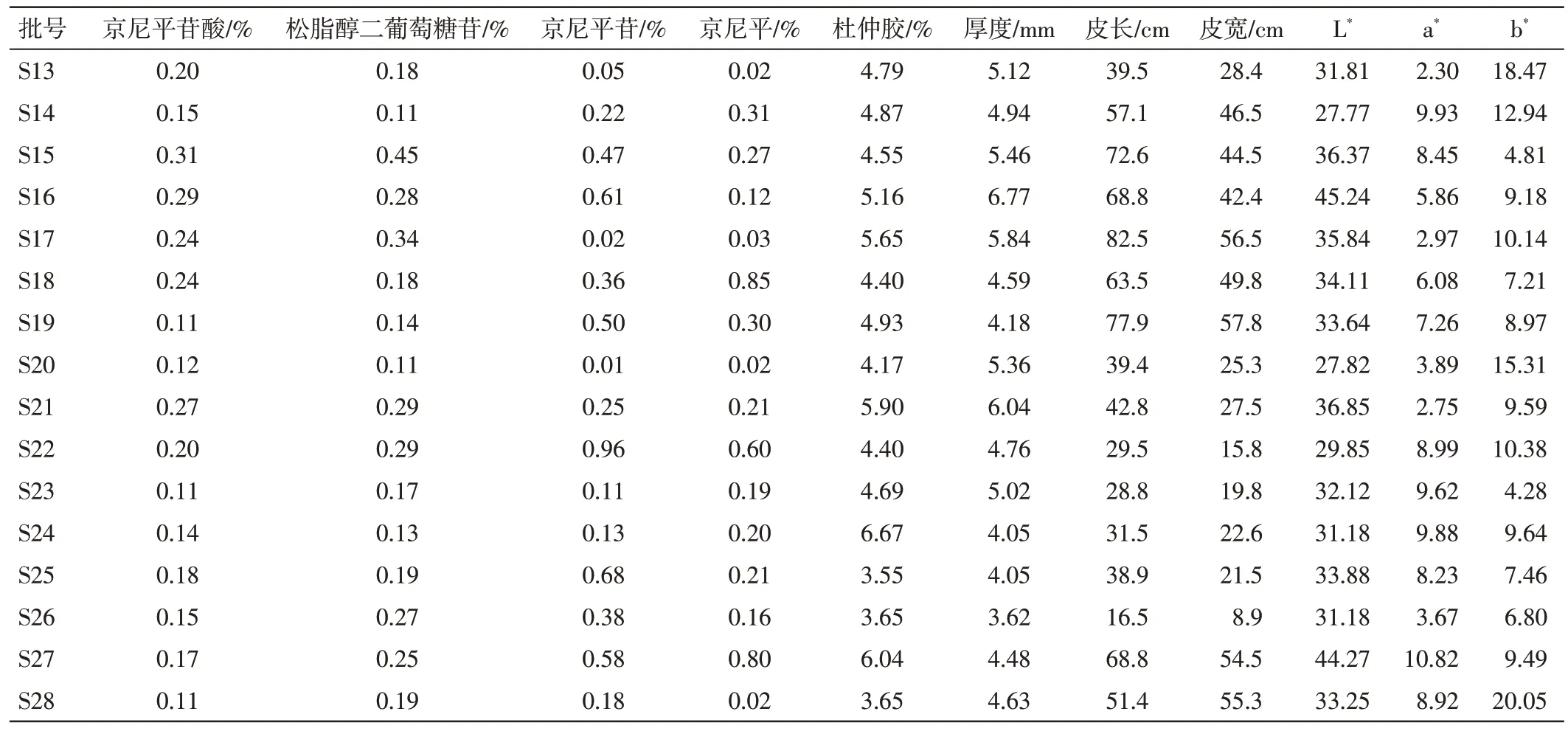
(续表2)
3 结果与分析
28 批杜仲药材内在质量和外形性状指标测定结果见表2。
3.1 杜仲外观性状与内在质量的相关性分析 将S1~S28 批样品的京尼平苷酸、松脂醇二葡萄糖苷、京尼平苷、京尼平、杜仲胶含量,以及厚度、皮长、皮宽、内表皮颜色(L*、a*、b*值)11 个指标数据导入Origin 2022 进行Pearson 相关性分析。结果见图2。其中红色代表正相关,蓝色代表负相关,相关性越显著,其颜色越亮,面积也越大。厚度与京尼平苷酸、松脂醇二葡萄糖苷含量呈显著性正相关(P<0.05),说明厚度越大,京尼平苷酸、松脂醇二葡萄糖苷含量含量越高;内表皮颜色L*值越大,京尼平苷酸含量越高(P<0.05);内表皮颜色a*值越大,京尼平苷含量越大(P<0.05),而京尼平苷酸含量越低(P<0.05);内表皮颜色b*值越大,京尼平含量就越低(P<0.05);皮长、皮宽和杜仲胶含量与内在质量无显著性关系。提示厚度、L*值、a*值、b*值和京尼平苷酸、松脂醇二葡萄糖苷、京尼平苷、京尼平可作为质量等级划分的指标进一步研究。
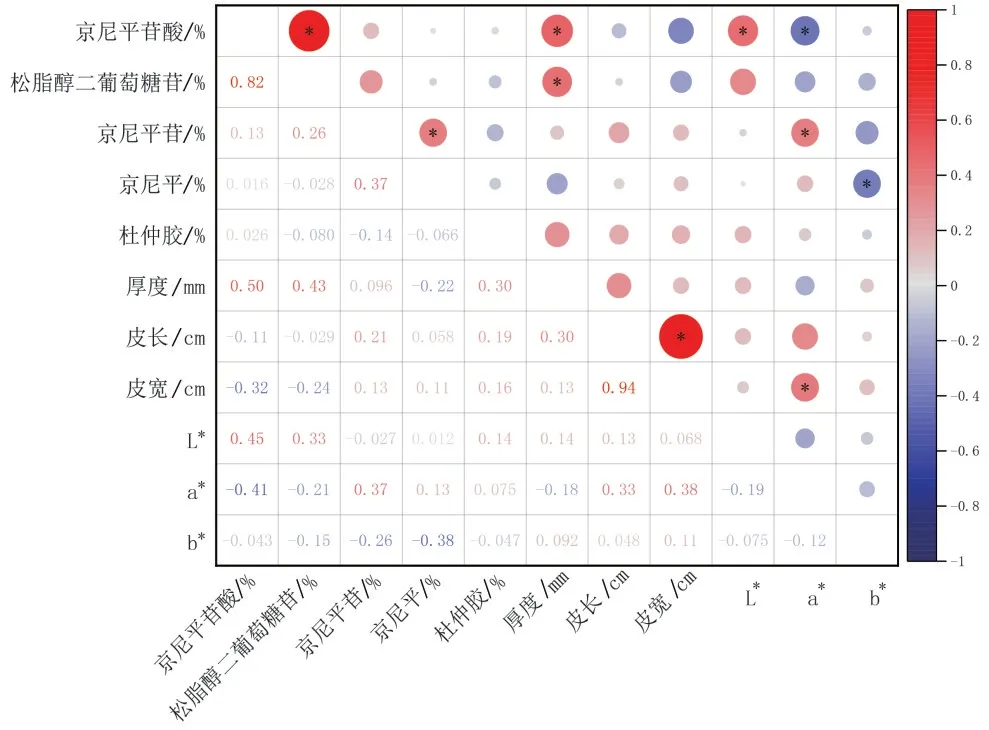
图2 杜仲各指标相关性分析Figure 2 Correlation analysis of various indicators of Eucommiae Cortex
3.2 主成分分析(PCA)和正交偏最小二乘判别分析(OPLS-DA)结果 在对多指标进行综合评定时,指标之间往往存在信息重复或不统一等问题,难以建立可行的等级标准。主成分分析是一种无监督模式的分析方法,在尽可能地保留原始数据信息的基础上,用少数几个或者新的变量指标来描述原始数据特征,达到降维目的[11]。将“3.1”项下筛选的8 个指标导入SIMCA 14.1 进行主成分分析。模型结果见图3-A。第一个主成分特征值为2.588,第二个主成分特征值为1.862,第三个主成分特征值为1.111,3 个主成分累积贡献率达到69.153%,表明可以较好地反映大部分的初始药材信息。28 批药材可较为明显地分为3 类,样品S1、S6、S12、S15、S16、S17、S21 为一类,样品S7、S8、S9、S10、S11、S13、S18、S22、S26、S27 为一类,其他样品归为一类。
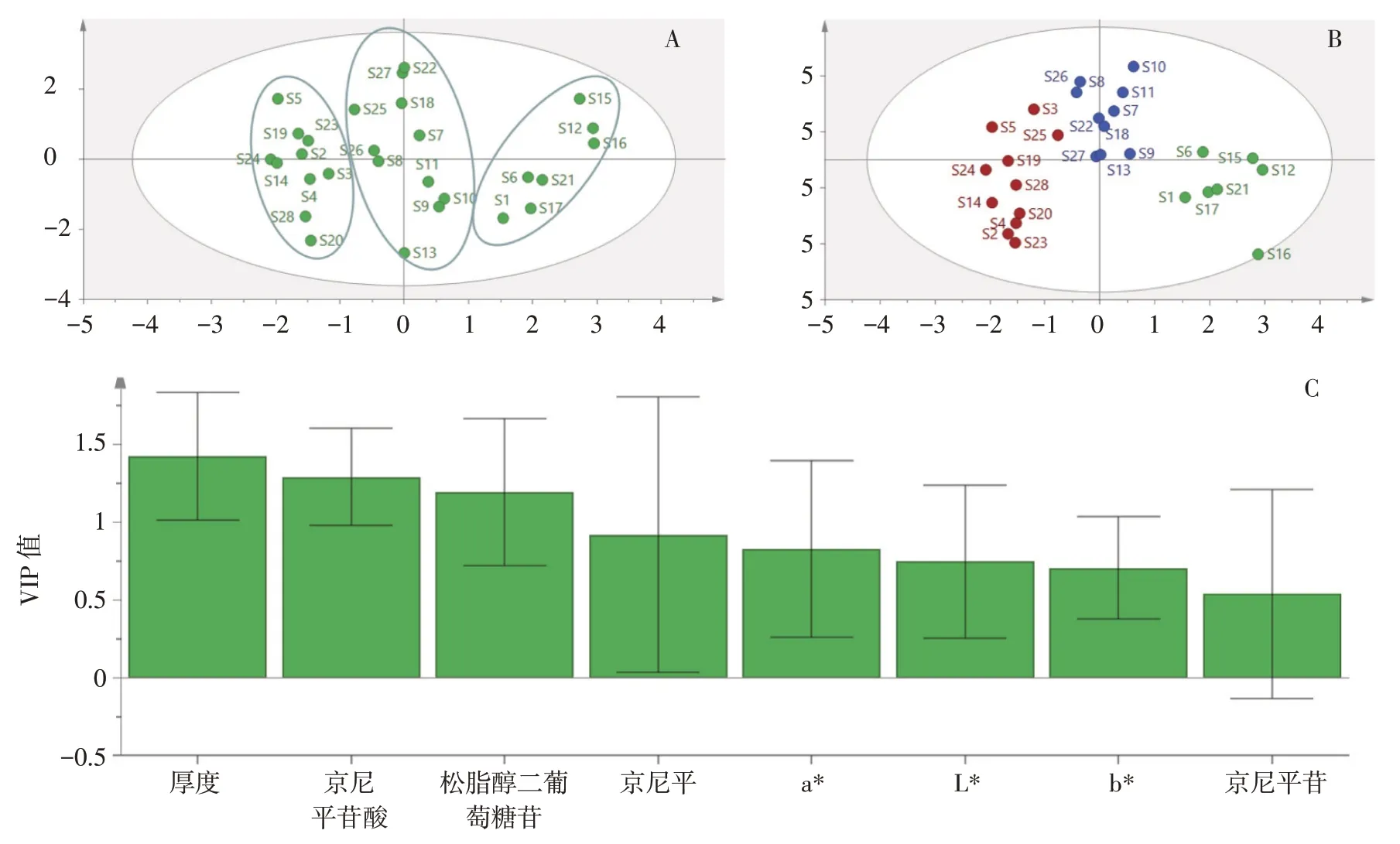
图3 杜仲药材等级划分PCA 得分图(A)、OPLS-DA 得分图(B)和VIP 得分图(C)Figure 3 PCA score chart(A)、OPLS-DA score chart(B)and VIP score chart(C)of grade differentiation of Eucommiae Cortex
利用SIMCA14.1 对28 批杜仲药材进行有监督的OPLS-DA 分析,结果可将样品分为3 类,见图3-B。为了分析变量对药材等级划分的影响,进一步绘制变量投影重要性分析(VIP)得分图,见图3-C。从图中可以看出,VIP 值的顺序为厚度>京尼平苷酸>松脂醇二葡萄糖苷含量>京尼平>a*>L*>b*>京尼平苷,其中厚度、京尼平苷酸含量和松脂醇二葡萄糖苷含量这3 个指标的VIP 值>1,表明这3 个指标在等级划分中起到重要作用。
3.3.2 K-均值聚类的等级划分标准 通过多元统计分析得知,厚度和内在质量有显著的相关性,同时京尼平苷酸和松脂醇二葡萄糖苷含量也是评价杜仲品质的重要指标,故将这3 个指标列为最终杜仲药材的等级划分指标。利用SPSS 26.0 软件对分级指标——厚度、松脂醇二葡萄糖苷和京尼平苷酸含量进行K均值聚类,将杜仲分为3 类。杜仲药材规格等级的K均值聚类法的最终聚类中心值见表3。
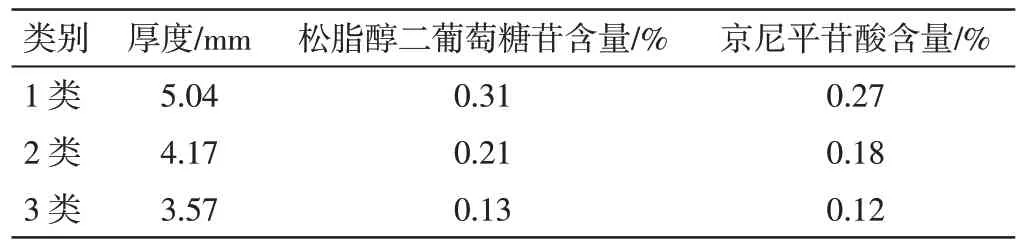
表3 杜仲分级指标的最终聚类中心值Table 3 Final clustering center values of classification index of Eucommiae Cortex
根据以上分析结果,可以得出以下结论:杜仲厚度数值越大,其内在质量成分含量(京尼平苷酸、松脂醇二葡萄糖苷含量)越高,成正比关系。根据K均值聚类最终中心值,并结合行业内药材分级情况和实际可操作性,建立杜仲药材质量等级划分标准。见表4。
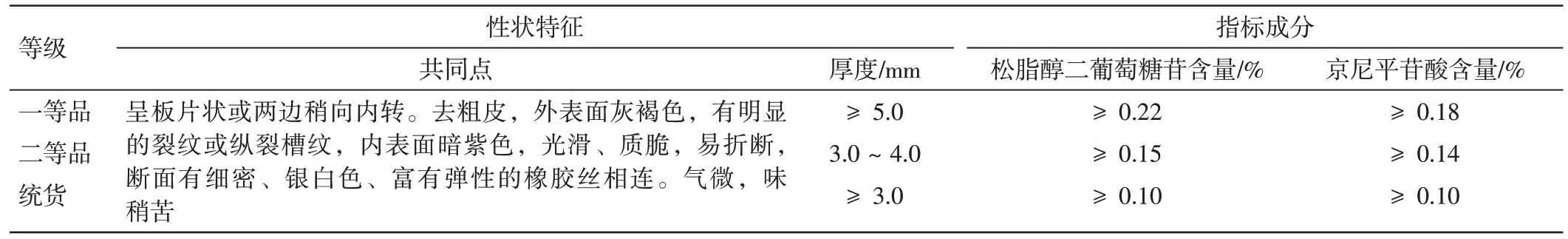
表4 杜仲药材质量等级划分Table 4 Quality classification of Eucommiae Cortex
4 基于HPLC 指纹图谱的杜仲药材聚类分析
指纹图谱常用于药材整体质量的控制,并广泛应用于不同产地、不同质量药材的评价[12]。本研究以杜仲药材HPLC 指纹图谱共有峰面积对28 批杜仲药材进行聚类分析,用以评价不同等级杜仲药材质量。
4.1 色谱条件 除洗脱梯度增加(60~70 min,30%~35% A)外,其余色谱条件同“2.1.1”项下。
4.2 方法学考察 依据2020 年版《中国药典》(四部)分析方法验证指导原则进行方法学考察。以4 号峰(绿原酸)为参照峰(S)计算各共有峰的相对保留时间和相对峰面积。结果显示,精密度试验、重复性试验、稳定性试验中各共有峰相对保留时间和相对峰面积的RSD 分别均小于5.26%,表明该方法学考察各指标符合要求,方法可行。
4.3 杜仲药材的HPLC 指纹图谱的建立 供试品制备同“2.1.2”项下,按“4.1.1”项下色谱条件,波长为240 nm,记录28 批药材数据。在28 批杜仲药材中共标定出10 个共有峰。通过与对照品溶液比对,指认出了其中的5 个成分,分别为峰1(京尼平苷酸)、峰4(绿原酸)、峰6(京尼平苷)、峰7(京尼平)和峰8(松脂醇二葡萄糖苷),28 批杜仲药材高效液相色谱叠加指纹图谱及对照指纹图谱(R)见图4。
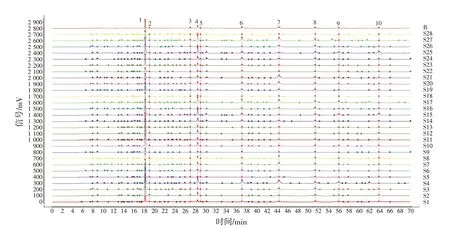
图4 28 批杜仲药材的HPLC 指纹图谱叠加图及其对照指纹图谱(R)Figure 4 HPLC fingerprint overlay of 28 batches of Eucommiae Cortex and its reference fingerprint(R)
4.4 聚类分析 以28 批杜仲药材中10 个共有峰的相对峰面积为变量,利用SPSS 23.0 软件进行系统聚类分析。结果见图5。28 批杜仲药材被分为3 类:一等杜仲药材(S1、S6、S12、S15、S16、S17、S21)为第1 类;二等杜仲药材(S7、S8、S9、S10、S11、S13、S18、S22、S26、S27)为第2 类;统货杜仲药材(S2、S3、S4、S5、S14、S19、S20、S23、S24、S25、S28)为第3 类。聚类分析结果与上述建立的杜仲药材质量级划分结果一致,提示本研究建立的等级标准可很好地表征杜仲药材的内在质量。
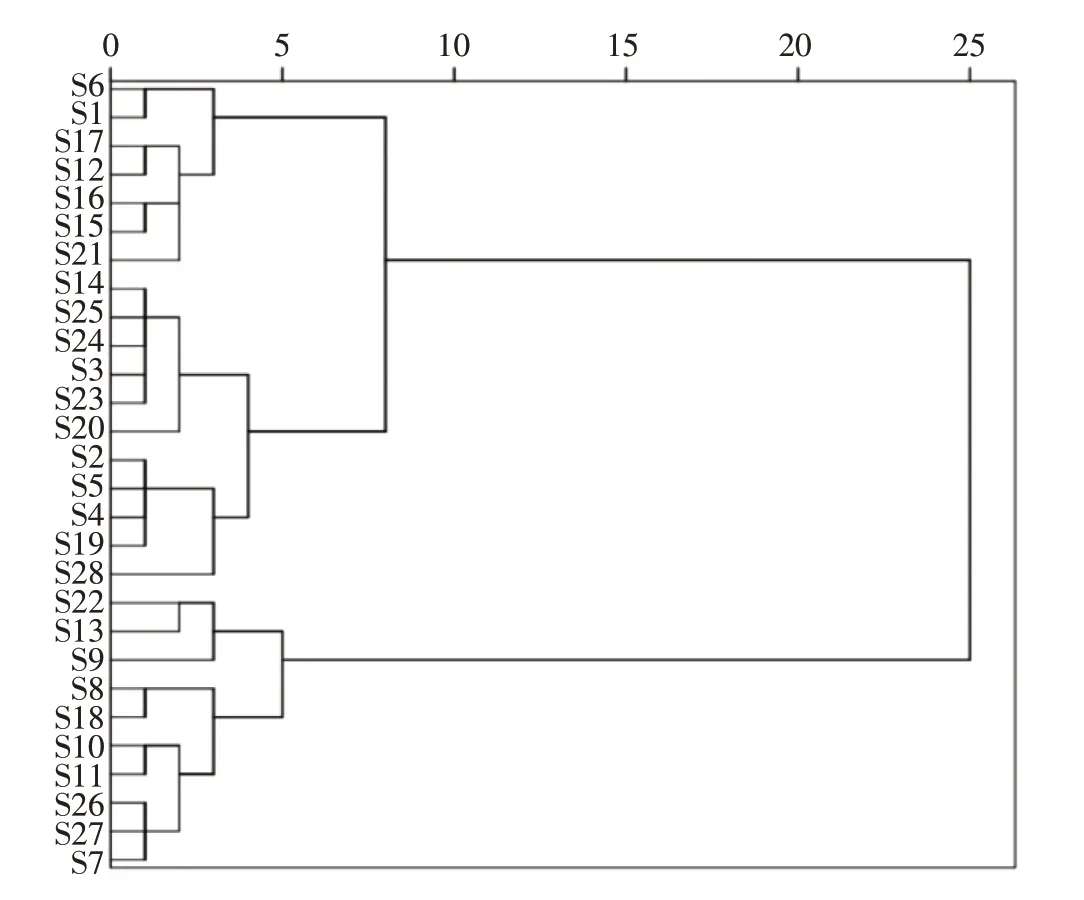
图5 28 批杜仲药材的聚类分析树状图Figure 5 Tree diagram of cluster analysis tree view of 28 batches of Eucommiae Cortex
5 讨论
5.1 样品前处理考察 2020 年版《中国药典》杜仲含量测定成分为松脂醇二葡萄糖苷。为尽可能多地提取目标成分和成分种类,本研究在此基础上比较了甲醇、乙醇、30%乙醇、70%乙醇等提取溶剂,发现70%乙醇的色谱峰数量及丰度最佳。《中国药典》对松脂醇二葡萄糖苷的提取采用索氏提取,过程需使用大量氯仿。本研究比较了索氏提取、回流和超声3 种提取方式和不同提取时间,发现回流和索氏提取对各目标成分的提取效率影响不大,且回流1 h后峰面积无明显增加,最终选择回流1 h 为前处理方法。
5.2 分级指标的选择 杜仲因其断面独特的杜仲丝而备受历代学者关注,并以杜仲丝多、皮厚为优质杜仲的辨别要点,如唐代《新修本草》记载杜仲以“皮厚、内表面黑色、折之白丝多为佳”[13]。本实验对杜仲药材中杜仲胶含量进行测定以表征“丝多”,以色差仪测定内表皮颜色表征“内表面黑色”。通过Pearson 相关性分析发现杜仲胶含量与其他指标无显著性关系,原因可能是由于杜仲胶含量受多因素影响,其合成有多种途径,包括微生物在内的许多物种体内都存在合成杜仲胶的重要中间产物[14],并且杜仲胶含量与杜仲生长年限和杜仲不同变异皮的类别相关[15]。杜仲皮厚与杜仲多成分含量存在相关性,与传统杜仲分级规律相一致,体现了研究工作的合理性。杜仲内表面的L*值与京尼平苷酸、a*值与京尼平苷均为正显著相关,而a*值与京尼平苷酸、b*值与京尼平呈负显性相关,可见杜仲内表面的颜色指标与杜仲中某一成分存在一定关联。据报道[16],中药玄参、地黄、梓实等加工后引起颜色变黑是由于环烯醚萜类成分分解所致。而杜仲在产地初加工“发汗”过程中,桃叶珊瑚苷含量变少,而京尼平苷酸含量增加[17],表明杜仲内表皮颜色的变化可能牵涉到多种环烯醚萜类成分变化。环烯醚萜类成分与杜仲疗效具有很强的相关性,其具有促进成骨细胞增殖[16],减少成骨细胞的转化[18],可作为体现杜仲内在质量的重要指标。所以本研究在《中国药典》测定松脂醇二葡萄糖苷的基础上,增加京尼平苷酸、京尼平苷和京尼平含量作为等级划分的内在指标,体现了指标筛选的科学性。
5.3 等级划分的合理性 本研究以12 个分级指标进行Pearson 相关性分析,初步筛选可反映杜仲质量外在性状指标,再根据初筛结果进行PCA 和OPLS-DA分析,以VIP 值>1 指标作为等级划分关键指标,最终以杜仲厚度、松脂醇二葡萄糖苷和京尼平苷酸含量建立药材等级划分标准。系统多元统计分析的应用使筛选出的指标更能表征药材质量。为了进一步探究该标准对于药材内在质量的表征情况,本研究建立HPLC 指纹图谱并进行了共有峰面积的聚类分析,聚类结果与所建立的药材等级划分标准相一致。
综上所述,本研究建立的杜仲药材质量等级划分标准不仅可以从外观特性上对杜仲进行等级评价,同时也能对其内在质量进行很强的表征,可为杜仲药材的质量控制及等级划分提供一定的参考。
