阿达木单抗治疗成年活动性强直性脊柱炎患者对其生存质量的影响
2023-07-11曹双燕邵战琴古洁若
曹双燕?邵战琴 ?古洁若


【摘要】目的 探讨阿达木单抗治疗成年活动性强直性脊柱炎(AS)患者在改善生存质量方面的效果。方法 本研究为阿达木单抗与安慰剂随机双盲对照临床试验的事后分析,在临床研究中,AS患者按照2∶1的比例随机分配至阿达木单抗组或安慰剂组治疗12周,其中阿达木单抗组予阿达木单抗治疗,每次40 mg,每2周1次。在用药前和用药第12周发放健康调查简表(SF-36),让患者对其健康状况自行评分。结果 接受阿达木单抗治疗的AS患者,在生理机能、躯体疼痛和社会功能方面的改善均优于安慰剂组(P均< 0.05)。阿达木单抗组在生理机能、生理职能、躯体疼痛、总体健康、精力和社会功能评分中均较基线期有所提高(P均< 0.05)。结论 阿达木单抗可有效提高成年活动性AS患者的生存质量。
【关键词】活动性强直性脊柱炎;阿达木单抗;生存质量;成年;健康调查简表
Effect of adalimumab on quality of life in patients with active ankylosing spondylitis Cao Shuangyan, Shao Zhanqin, Gu Jieruo. Department of Rheumatology and Immunology, the Seventh Affiliated Hospital of Sun Yat-sen University, Shengzhen 517108, China
Corresponding author, Gu Jieruo, E-mail: gujieruo@163.com
【Abstract】Objective To evaluate the efficacy of adalimumab in improving the quality of life of adult patients with active ankylosing spondylitis (AS). Methods This was a post-hoc study of the randomized, double-blind controlled clinical trial of adalimumab and placebo in AS patients. In this clinical trial, AS patients were randomly divided into the 12-week adalimumab and placebo groups according to the proportion of 2∶1. In the adalimumab group, AS patients were treated with adalimumab at a single dose of 40 mg, once every two weeks. The SF-36 Quality of Life Questionnaire was distributed to patients to self-evaluate health status before and at the 12th week after medication, respectively. Results AS patients in the adalimumab group obtained significant improvement in the scores of physiological functioning, bodily pain and social functioning compared with their counterparts in the placebo group (all P < 0.05). In the adalimumab group, the scores of physical functioning, role-playing physical functioning, bodily pain, overall health, vitality and social functioning after 12-week medication therapy were improved compared with the baseline scores(all P < 0.05). ConclusionAdalimumab is beneficial to enhancing the quality of life of adult patients with active AS.
【Key words】Active ankylosing spondylitis; Adalimumab; Quality of life; Adult; SF-36 Quality of Life Questionnaire
強直性脊柱炎(AS)是一种慢性全身性炎性疾病,主要累及中轴骨骼。它以骶髂关节炎为主要特征,并可累及外周关节、肌腱端和其他器官。有报道指,AS的平均发病率在欧洲为23.8/万,在亚洲为16.7/万,在北美洲为31.9/万,在拉丁美洲为10.2/万,在非洲为7.4/万[1]。在中国汉族人群中,AS的患病率在0.20%~0.54%[2]。AS患者以男性更为常见,起病年龄早,致残性强,需要长达数十年甚至终身的治疗。研究显示,该病引起的残疾与类风湿关节炎(RA)相似,无论在直接费用还是间接费用方面均对患者和社会造成沉重负担[3]。在AS患者中,功能残疾是预测总治疗费用最重要的因素[4]。早期诊断、早期治疗及尽可能保全患者的躯体功能是减少疾病社会负担的关键点。随着近年来对AS致病机制的深入研究,研究者发现促炎细胞因子TNF-α与AS的发病及疾病活动度密切相关[5]。临床研究显示,TNF-α拮抗剂对包括RA和AS在内的多种自身免疫性疾病疗效良好[6]。阿达木单抗为TNF-α拮抗剂之一,是一种全人源化的单克隆抗体,国内外大规模的研究证实阿达木单抗治疗AS患者临床疗效显著[7]。近年来随着生物医学模式的转变,提高患者生存质量成为越来越多的学者所关注的重要指标,同时也是评价药物疗效的重要方面。本研究通过比较阿达木单抗或安慰剂治疗成年活动性AS患者的健康调查简表(SF-36)变化情况,分析其对提高AS患者生存质量的作用,现报道如下。
对象与方法
一、研究对象
本研究为多中心随机双盲对照临床试验事后分析,仅纳入2013-2015年在中山大学附属第三医院风湿免疫科参加临床试验的52例成年活动性AS患者。主要入组标准包括:①年龄18~65岁,配合度高;②根据1984年改良纽约标准诊断为AS;③活动性AS患者,即满足下列2项及以上条件者,a. BASDAI评分≥4 cm,b. 在视觉模拟评分表(VAS)中,总背痛VAS≥40 mm,c. 晨僵≥1 h;④女性受试者要求在整个研究期间和研究药物末次给药后150 d内采取避孕措施;⑤在筛选时,如受试者的结核菌素纯蛋白衍生物(PPD)试验和X线胸片(正位和侧位)均为阴性结果,可予入组,若PPD试验为阳性或曾经对PPD注射有溃疡性反应或X线胸片提示有既往结核病暴露史,受试者同意接受预防性TB治疗者可入组。本研究经中山大学附属第三医院伦理委员会审批通过(批件号:中大附三医伦[2009]1-35),所有患者均签署知情同意书。
排除标准:①脊椎完全僵直(竹节样脊柱);②在基线前2个月内脊柱或关节曾行相应手术治疗者;③在基线前28 d内接受过关节内、脊柱或脊柱旁注射过糖皮质激素(激素)者;④曾使用TNF抑制剂治疗者;⑤在基线访视之前30 d内曾行全身抗感染治疗或者在基线访视之前14 d内曾口服抗菌药、抗病毒药或抗真菌药治疗者;⑥有李斯特菌病史、网状内皮细胞真菌疾病史、慢性或活动性HBV感染、HIV感染、免疫缺陷综合征、慢性复发感染或活动性结核者;⑦中等或重度充血性心力衰竭或近期发生脑血管意外者。
二、试验分组与给药
入组患者按照2∶1的比例通过数字化随机系统分配到阿达木单抗或安慰剂组,每2周进行40 mg阿达木单抗或安慰剂皮下注射一次。受试者与研究者均不知道分配组别。所有患者均服用NSAID(本中心患者使用的NSAID包括塞来昔布、美洛昔康、美诺芬、布洛芬、双氯芬酸钠、洛索洛芬钠、萘丁美酮)作为基础治疗,参加临床试验期间的剂量保持不变。
三、评价方法
采用美国波士顿健康研究所研制的SF-36进行生存质量的评估[8]。该量表广泛应用于多个领域,如生存质量评估、评价临床试验效果及评估卫生政策等领域。SF-36对受试者的生理机能、生理职能、躯体疼痛、一般健康状况、精力、社会功能、情感职能及精神健康等8个领域进行评估,共36个条目。根据计分方法进行每一领域评分,每一领域的标准化得分为0~100分,分数越高,说明健康状况越好。在基线期和第12周随访时,由受试者本人完成该问卷,完成后交给研究护士。医护人员需要在受试患者离开医院前,仔细核查其调查问卷与评估回答情况,一人一份,避免遗漏。
四、不良事件统计
收集研究期间出现的不良事件及严重不良事件,并详细记录处理经过及结果,根据不良事件与药物相关性进行判定。
五、统计学处理
所有数据均采用STATA 16.0软件进行统计分析。对符合正态分布的计量资料以表示,组间比较采用独立样本t检验;治疗前后的生存質量比较采用配对t检验。计数资料以例(%)表示,组间比较采用χ2检验或Fisher确切概率法。P < 0.05为差异有统计学意义。
结果
一、阿达木单抗组与安慰剂组成年活动性AS患者的基线期一般情况比较
本研究共纳入52例成年活动性AS患者,年龄(27.62±6.90)岁,其中男45例、女7例,阿达木单抗组33例、安慰剂组19例。阿达木单抗组及安慰剂组患者的年龄、背痛时间、总背痛分数、CRP、Bath AS疾病活动性指数(BASDAI)和CRP相关疾病活动度评分(ASDAS-CRP)在基线期相对均衡(P均> 0.05),提示2组受试患者具有可比性。见表1。
二、阿达木单抗组与安慰剂组成年活动性AS患者的临床疗效比较
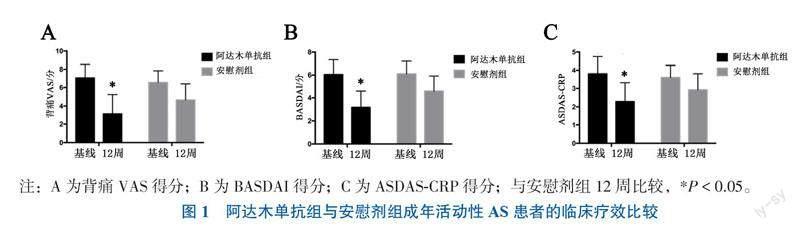
在第12周,阿达木单抗组患者的背痛VAS得分、BASDAI、ASDAS较安慰剂组患者均有所下降(P均< 0.05),见图1。在炎症指标方面,阿达木单抗组CRP为6.3(0.6, 15.9)mg/L,而安慰剂组为10.8(6.0, 25.0)mg/L,组间比较差异有统计学意义(P < 0.05)。
三、阿达木单抗组与安慰剂组成年活动性AS患者的生存质量评估
阿达木单抗组与安慰剂组患者在基线期的8个维度生存质量评分比较差异均无统计学意义(P均> 0.05),具有可比性。经过12周的治疗,阿达木单抗组患者在生理功能、生理职能、躯体疼痛、总体健康、精力和社会功能评分中均有所改善,治疗前后比较差异均有统计学意义(P均< 0.05),而安慰剂组患者在一般健康状况、精力和情感职能评分中均较治疗前提高(P均< 0.05)。治疗后,阿达木单抗组患者在生理机能、躯体疼痛、社会功能3个方面均优于安慰剂组(P均< 0.05)。见表2。
四、阿达木单抗组与安慰剂组成年活动性AS患者的不良事件比较
在治疗期间共发生不良事件39例,无严重不良事件。其中以上呼吸道感染最为常见,共20例,消化道不良事件如胃部不适或转氨酶升高8例,皮肤病变6例,结膜炎2例,其他共4例(包括白细胞减少1例、胸痛1例、头晕2例)。2组患者的不良事件发生率比较差异均无统计学意义(P均> 0.05)。见表3。
讨论
对一般健康人群生命质量评估方式中,以SF-36应用率最高,重复测量可靠性高[9]。国外学者认为,该问卷更适用于临床试验、患病人群群体之间的比较、对患者身体健康和功能的疗效评定,以及评估干预措施对健康的影响。在慢性风湿性疾病中,SF-36可评估疾病对患者躯体、精神健康及功能的影响,同时可帮助评价药物治疗前后对生存质量的影响。在RA中,SF-36可同时评估身体因素和精神因素对患者生活质量的影响[10-11]。多项研究显示,SF-36能较好地反映AS患者的生存质量,为调整临床治疗方案提供依据[12]。
AS患者因起病早、致殘率高,需要长期的药物治疗。有研究显示,AS患者产生抑郁、焦虑等负面情绪的比例高于健康对照组,约35%的患者达到抑郁的诊断标准;与健康对照组相比,AS患者出现抑郁的相对风险为1.76[13]。AS导致患者持续的疼痛、关节畸形及身体活动度的下降,严重降低患者生活质量,同时患者的工作能力也受到损害,给个人和社会带来沉重的负担[14]。评估AS患者的健康相关生活质量,能更好地了解患者疾病相关的痛苦,也能帮助医生和卫生政策制定者优化医疗决策。近年研发的生物制剂能迅速缓解AS患者的躯体疼痛和改善身体活动度,但是高昂的费用限制了其应用范围。另外,生物制剂的使用能在短时间内减轻患者的症状和体征,提高患者的工作能力,或许能弥补昂贵的药费带来的社会负担。有研究显示,阿达木单抗可迅速改善患者的症状及体征,改善其生存质量和工作能力,从而减少患者的经济负担[15]。近年的系统综述评估了生物制剂对脊柱关节炎患者生存质量的影响,共纳入16项随机对照研究,涉及5种TNF抑制剂和2种IL-17A抑制剂,结果显示与安慰剂相比,生物制剂治疗与SF-36、欧洲五维健康量表(EQ-5D)和AS生活质量量表(ASQoL)评分明显改善相关[16]。
在本研究中,与基线相比较,经阿达木治疗第12周时,SF-36中6个维度评分均明显升高,包括生理机能、生理职能、躯体疼痛、总体健康、精力和社会功能。阿达木治疗组在生理机能、躯体疼痛、社会功能3个方面的改善优于安慰剂组,结合患者疼痛及疾病活动度改善情况,表明阿达木单抗治疗能迅速通过改善AS患者的背痛、疾病活动度,从而改善生存质量。这与国外研究结果相似,生物制剂在改善患者症状和体征的同时能提高生存质量。
本研究中未观察到与药物相关的严重不良事件,无患者因为出现不良事件而退出本研究。不良事件中以上呼吸道感染多见,程度较轻,其他多见的有消化道不良反应、皮肤病变等。阿达木单抗组和安慰剂组间的不良事件发生率比较差异无统计学意义,提示阿达木单抗在AS患者中的安全性及耐受性良好。
综上所述,活动性AS患者接受阿达木单抗治疗后其生存质量有明显的提高。尽管阿达木单抗价格昂贵,但相比其在迅速减轻患者疼痛、提升身体机能和提高生存质量方面的明显效果而言,仍然是AS患者治疗的一个较好的选择。
参 考 文 献
[1] Dean L E, Jones G T, MacDonald A G, et al. Global prevalence of ankylosing spondylitis. Rheumatology (Oxford), 2014, 53(4): 650-657.
[2] Zeng S Y, Gong Y, Zhang Y P, et al. Changes in the prevalence of rheumatic diseases in Shantou, China, in the past three decades: a COPCORD study. PLoS One, 2015, 10(9): e0138492.
[3] Zink A, Braun J, Listing J, et al. Disability and handicap in rheumatoid arthritis and ankylosing spondylitis—results from the German rheumatological database. German Collaborative Arthritis Centers. J Rheumatol, 2000, 27(3): 613-622.
[4] Ward M M. Functional disability predicts total costs in patients with ankylosing spondylitis. Arthritis Rheum, 2002, 46(1): 223-231.
[5] Du J, Sun J, Wen Z, et al. Serum IL-6 and TNF-α levels are correlated with disease severity in patients with ankylosing spondylitis. Lab Med, 2022, 53(2): 149-155.
[6] Ward M M, Deodhar A, Gensler L S, et al. 2019 Update of the American College of Rheumatology/Spondylitis Association of America/Spondyloarthritis Research and Treatment Network Recommendations for the treatment of ankylosing spondylitis and nonradiographic axial spondyloarthritis. Arthritis Care Res (Hoboken), 2019, 71(10): 1285-1299.
[7] van der Heijde D, Kivitz A, Schiff M H, et al. Efficacy and safety of adalimumab in patients with ankylosing spondylitis: results of a multicenter, randomized, double-blind, placebo-controlled trial. Arthritis Rheum, 2006, 54(7): 2136-2146.
[8] 李鲁, 王红妹, 沈毅. SF-36健康调查量表中文版的研制及其性能测试. 中华预防医学杂志, 2002, 36(2): 38-42.
[9] 万崇华. 常用生命质量测定量表简介. 中国行为医学科学, 2000, 9(1): 69-71.
[10] Matcham F, Scott I C, Rayner L, et al. The impact of rheumatoid arthritis on quality-of-life assessed using the SF-36: a systematic review and meta-analysis. Semin Arthritis Rheum, 2014, 44(2): 123-130.
[11] Rahman M M, Khasru M R, Rahman M A, et al. Quality of life assessment by SF-36 among the patients with rheumatoid arthritis. Mymensingh Med J, 2022, 31(3): 586-591.
[12] Yang X, Fan D, Xia Q, et al. The health-related quality of life of ankylosing spondylitis patients assessed by SF-36: a systematic review and meta-analysis. Qual Life Res, 2016, 25(11): 2711-2723.
[13] Zhang L, Wu Y, Liu S, et al. Prevalence of depression in ankylosing spondylitis: a systematic review and meta-analysis. Psychiatry Investig, 2019, 16(8): 565-574.
[14] Tu L, Rai J C, Cao S, et al. Costs and work limitation of patients with ankylosing spondylitis in China. Clin Exp Rheumatol, 2014, 32(5): 661-666.
[15] Tu L, Xie Y, Liao Z, et al. Cost of illness, quality of life, and work outcomes in active ankylosing spondylitis patients treated with adalimumab in China. Front Public Health, 2020, 8: 602334.
[16] Tański W, ?wi?toniowska-Lonc N, Dudek K, et al. Benefit of biological drugs for quality of life in patients with ankylosing spondylitis: a systematic review and meta-analysis of clinical trials. Adv Exp Med Biol, 2021, 1335: 63-78.
(收稿日期:2022-11-15)
(本文編辑:林燕薇)
