芪连降糖片的质量标准研究
2023-07-07杨春静黄明月
张 蕾 ,杨春静 ,黄明月
(1. 首都医科大学附属北京世纪坛医院药学部,北京 100038;2. 临床合理用药生物特征谱学评价北京市重点实验室,北京 100038)
芪连降糖片处方来源于清华大学医学院、清华大学玉泉医院全国百名杰出青年中医、首都中青年名中医冯兴中教授的临床经验方[1-2],具有益气补中,清热解饥之功效。方中黄芪味甘性微温,具有补益中气之功效,为君药;黄连味苦性寒,具有清热燥湿之功效,为臣药;两药合用,补气为主,清热为辅。用于中气虚弱,湿热内生所致的消渴病,症见短气懒言,疲劳乏力,口渴喜饮,消谷善饥,舌红苔腻,脉细数。轻、中型2型糖尿病见上述症状者。
芪连降糖片为薄膜衣片,是在上述临床经验方基础上开发的中药1.1类新药。为有效控制芪连降糖片的质量,保证临床用药安全稳定,本实验采用薄层色谱法对制剂中黄芪、黄连(味连)进行定性鉴别,采用高效液相色谱法测定了制剂中黄芪甲苷、表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱的含量,建立了稳定可靠、专属性强、重现性好的质量控制方法。
1 材料与仪器
1.1 仪器
Agilent 1260高效液相色谱仪(四元梯度洗脱泵,自动进样器,ELSD检测器,DAD检测器,安捷伦),Agilent OpenLAB CDS EZChrom色谱工作站(安捷伦);phenomenex Luna C18色谱柱(250 mm×4.6 mm,5 μm,广州菲罗门);十万分之一电子分析天平(BT125D,赛多利斯),万分之一电子分析天平(ME204E/02,梅特勒-托利多);Milli-Q Intergral 水纯化系统(Q-POD,默克);数控超声波清洗器(KQ-600DE,昆山市超声仪器);ZF-7紫外检测灯(上海硕光);硅胶G薄层板(烟台江友)。
1.2 药品与试剂
黄芪甲苷对照品(批号:110781-201717,含量96.9 %,中国食品药品检定研究院);表小檗碱对照品(批号:MUST-18072402,含量98.9 %,成都曼斯特);盐酸黄连碱对照品(批号:112026-201601,含量95.1 %,中国食品药品检定研究院);盐酸巴马汀对照品(批号:110732-201812,含量97.6 %,中国食品药品检定研究院);盐酸小檗碱对照品(批号:110713-201814,含量86.7 %,中国食品药品检定研究院);黄芪对照药材(批号:120974-201612,中国食品药品检定研究院);黄连对照药材(批号:121752-201801,中国食品药品检定研究院)。芪连降糖片(批号:20190401,20190402,20190403,每片重0.56 g,首都医科大学附属北京世纪坛医院);黄芪、黄连(味连)的阴性样品均为自制。乙腈(批号:191613,色谱纯,赛默飞世尔科技);十二烷基硫酸钠(批号:STBG9926,色谱纯,Sigma-Aldrich公司);磷酸二氢钾(批号:C9920060,色谱纯,上海安谱);其他试剂均为分析纯。
2 方法与结果
2.1 薄层色谱鉴别
2.1.1 黄芪的薄层色谱鉴别 取芪连降糖片样品5片,除去包衣后研细,置入圆底烧瓶。加甲醇20 ml,加热回流提取1 h,滤过,放冷后滤液在中性氧化铝柱(100~120目,5 g,内径为10~15 mm)上用100 ml 40 %甲醇洗脱。洗脱液蒸干后加水30 ml将残渣溶解,并用水饱和的正丁醇萃取2次(每次用量20 ml),将正丁醇萃取液混合后再分别用20 ml水洗涤2次,弃去水液后将正丁醇液在水浴上蒸干。加甲醇0.5 ml溶解所得残渣,作为供试品溶液;取黄芪阴性样品粉末0.6 g,采用同样方法制成黄芪阴性样品溶液;精确称量黄芪甲苷对照品0.62 mg,加l ml甲醇使其溶解,作为对照品溶液。参照2020年版《中国药典》第四部薄层色谱法(通则0502)[3]试验,吸取上述供试品溶液(批号:20190401,20190402,20190403)、阴性样品溶液和对照品溶液各2 μl,在同一硅胶G薄层板上分别点样,按照13:7:2的比例将三氯甲烷-甲醇-水的下层溶液为展开剂展开,取出晾干后喷以10 %体积分数的硫酸乙醇溶液,于105 ℃加热至各斑点显色清晰。结果显示在相应的位置上,供试品色谱与对照品色谱日光下显相同的棕褐色斑点;紫外光(波长365 nm)下显相同的橙黄色至棕褐色荧光斑点,而阴性样品则在相应位置处未见斑点。见图1-A,B。
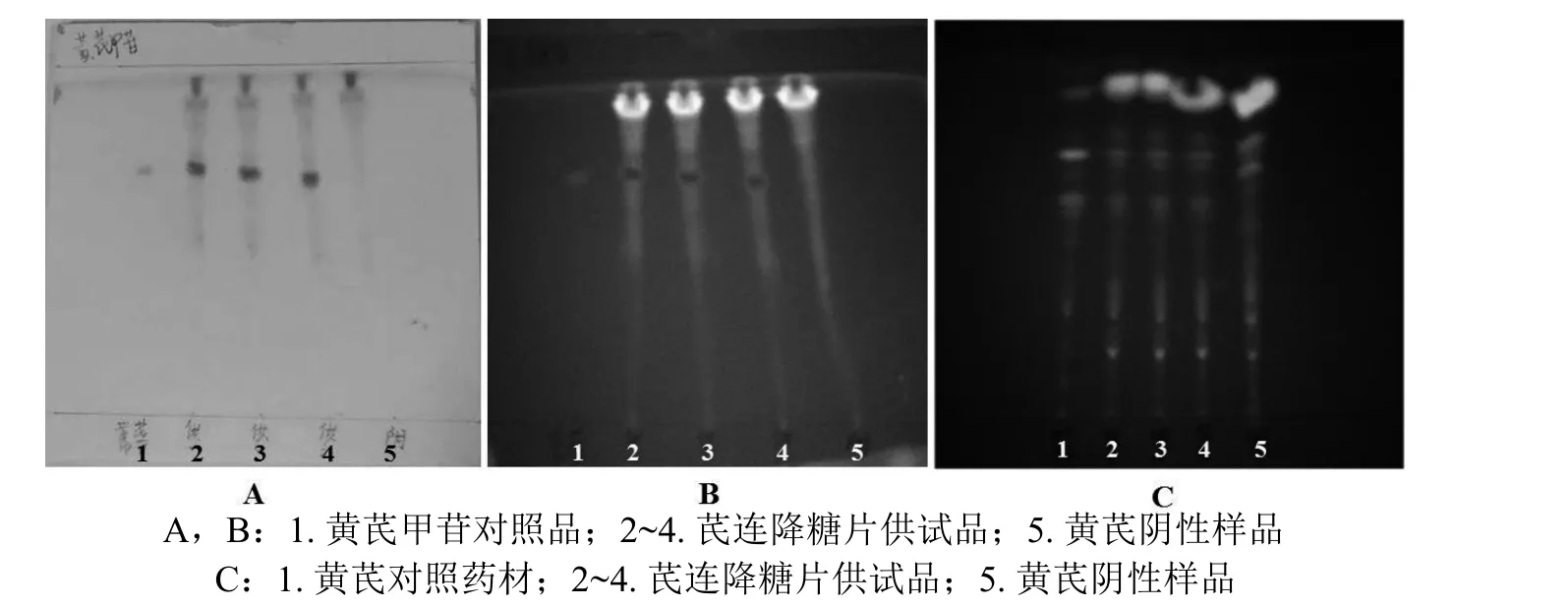
图1 芪连降糖片中黄芪的薄层色谱图
取芪连降糖片样品5片,除去包衣后研细,置圆底烧瓶中加乙醇30 ml,加热回流提取20 min,滤过,滤液置水浴上蒸干,残渣加0.3 % 氢氧化钠溶液15 ml溶解并滤过。使用稀盐酸将过滤液pH值调节至5~6,再取乙酸乙酯15 ml萃取。将乙酸乙酯萃取液用铺有无水硫酸钠的滤纸滤过,并浓缩干燥。所得残渣加入l ml乙酸乙酯使其完全溶解,作为供试品溶液;取黄芪阴性样品粉末0.4 g制得黄芪阴性样品溶液,制备方法同上;取黄芪对照药材1.5 g,按照上述方法制成对照药材溶液。参照2020年版《中国药典》第四部薄层色谱法(通则0502)[3]试验,吸取上述供试品溶液(批号:20190401,20190402,20190403)、阴性样品溶液和对照药材溶液各10 μl,在同一硅胶G薄层板上分别点样后利用展开剂(三氯甲烷-甲醇,10: 1)展开,取出室温晾干,采用氨蒸气熏蒸后,置紫外光(波长365 nm)下检视。结果表明,供试品色谱在与对照药材色谱相应的位置上,显相同颜色的荧光主斑点,而阴性样品则在相应位置处未见斑点。详见图1-C。
2.1.2 黄连的薄层色谱鉴别 取芪连降糖片样品2片,除去包衣后研细,置具塞锥形瓶中加甲醇25 ml,超声处理30 min,滤过,取滤液作为供试品溶液;另取黄连对照药材0.14 g,按照同样方法制成对照药材溶液;同法,取黄连阴性样品粉末0.45 g制得黄连阴性样品溶液;精确称取盐酸小檗碱对照品0.89 mg,加甲醇l ml使溶解,作为对照品溶液。参照2020年版《中国药典》第四部薄层色谱法(通则0502)[3]试验,吸取上述供试品溶液(批号:20190401,20190402,20190403)、对照药材溶液、阴性样品溶液和对照品溶液各2 μl,在同一硅胶G薄层板上分别点样,以环己烷-乙酸乙酯-异丙醇-甲醇-水-三乙胺(3:3.5:1:1.5:0.5:1)为展开剂,在浓氨试液预饱和20 min的展开缸内展开,取出室温晾干,置紫外光(波长365 nm)下观察。结果表明,供试品色谱在与对照药材色谱相应的位置上,显5个相同颜色的荧光斑点;在对照品色谱相应的位置上,显相同的黄色荧光斑点,而阴性样品则在相应位置处未见斑点。见图2。
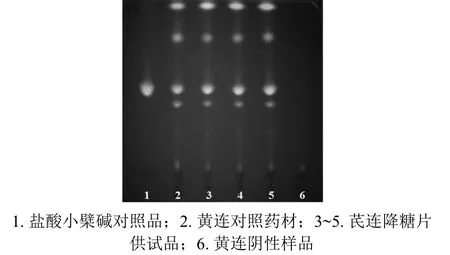
图2 芪连降糖片中黄连的薄层色谱图
2.2 含量测定
2.2.1 黄芪甲苷(黄芪)的含量测定
2.2.1.1 色谱条件 Phenomenex Luna C18色谱柱(250 mm×4.6 mm,5 μm);流动相为乙腈-水(33:67);Agilent 1260 Infinity蒸发光散射检测器(漂移管温度30 ℃,载气流速1.6 L/min);柱温:30 ℃;进样量10 μl;流速1.0 ml/min。理论塔板数按黄芪甲苷计算应不低于4000。
2.2.1.2 对照品溶液的制备 取黄芪甲苷对照品适量,精密称定后置入棕色量瓶,加甲醇制成质量浓度为1.0 mg/ml的对照品溶液。
2.2.1.3 供试品溶液的制备 取芪连降糖片20片,除去包衣后研细,取约3.1 g,精密称定,置入索氏提取器,加入甲醇40 ml,冷浸过夜,再加入适量甲醇,加热回流提取4 h。将提取液减压浓缩干燥后加去离子水10 ml,置温水上使其溶解后,用水饱和的正丁醇萃取4次,每次获得正丁醇萃取液40 ml。将所有正丁醇萃取液混匀后,再分别用40 ml氨试液充分洗涤2次,弃去氨液,正丁醇液减压浓缩干燥,所得残渣再次加入5 ml去离子水溶解,待冷却完全后上样于D101型大孔吸附树脂柱(内径为1 cm,柱高为16 cm),先用水50 ml洗脱除去水溶性杂质,再用30 ml浓度为40 %乙醇洗脱弃去中等极性洗脱液,最后用80 ml浓度为70 %的乙醇洗脱,收集洗脱液,浓缩干燥。利用甲醇将残渣溶解并转移至量瓶中,加甲醇定容至50 ml,摇匀后用0.45 μm微孔滤膜滤过,取续滤液,即得。
2.2.1.4 阴性对照溶液的制备 依据芪连降糖片处方中药味的比例,称定相应比例的黄连药材粉末,按其工艺制成空白制剂的药粉,再按2.2.1.3项方法制得相应阴性对照溶液。
2.2.1.5 专属性试验 依次吸取以上制备的黄芪甲苷对照品溶液、供试品溶液及阴性对照溶液各10 μl,按2.2.1.1项色谱条件进行测定。结果表明,在与对照品色谱峰相应的位置上,供试品溶液有对应的色谱峰,且阴性无干扰,按黄芪甲苷色谱峰计,理论塔板数为22 753,与前后峰的分离度均较好。表明本研究所建立的色谱条件专属性良好,适用于芪连降糖片中黄芪甲苷的含量测定。色谱图见图3。
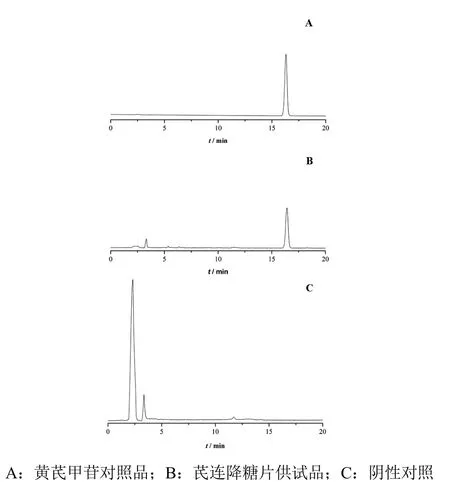
图3 芪连降糖片中黄芪的高效液相色谱图
2.2.1.6 线性关系考察 精密称取黄芪甲苷对照品适量,加甲醇逐级稀释配制成浓度30.28,60.56,121.13,242.25,484.50,969.00 μg/ml对照品溶液。按2.2.1.1项色谱条件,分别进样10 μl,记录色谱图。以峰面积的对数(lgA)为纵坐标,黄芪甲苷质量浓度对数(lgC)为横坐标进行线性回归分析,得标准曲线方程,lgA=1.6334 lgC+1.9910,相关系数r=0.9989。结果表明,黄芪甲苷在30.28~969.00 μg/ml浓度范围内线性关系良好。
2.2.1.7 精密度试验 精密吸取黄芪甲苷对照品溶液(黄芪甲苷含量242.25 μg/ml),按2.2.1.1项色谱条件连续进样6次,计算黄芪甲苷峰面积的RSD为1.35 %,表明仪器精密度良好。
2.2.1.8 稳定性试验 取同一供试品溶液(批号:20190401),分别于配制后0,2,4,6,12 h(低温避光保存)按2.2.1.1项色谱条件进样,记录黄芪甲苷峰面积,计算RSD为2.86 %,表明供试品在低温避光保存条件下12 h内稳定性良好。
2.2.1.9 重复性试验 取同一批次芪连降糖片样品(批号:20190401)共计6份,精密称定,按2.2.1.3项方法制备供试品溶液,再按2.2.1.1项色谱条件进行测定。结果黄芪甲苷的平均含量为3.89 mg/g,RSD为2.57 %,表明此法重复性良好。
2.2.1.10 加样回收率试验 取2.2.1.9项已测定含量的芪连降糖片样品(批号:20190401)适量,除去包衣后研细,精密称取6份,每份约1.5 g,分别精密加入黄芪甲苷对照品溶液(1.1 mg/ml)5 ml,按2.2.1.3项供试品溶液制备方法操作,再按2.2.1.1项色谱条件测定含量,计算得黄芪甲苷的平均回收率为98.8 %,RSD为2.25 %,回收率良好,结果见表1。
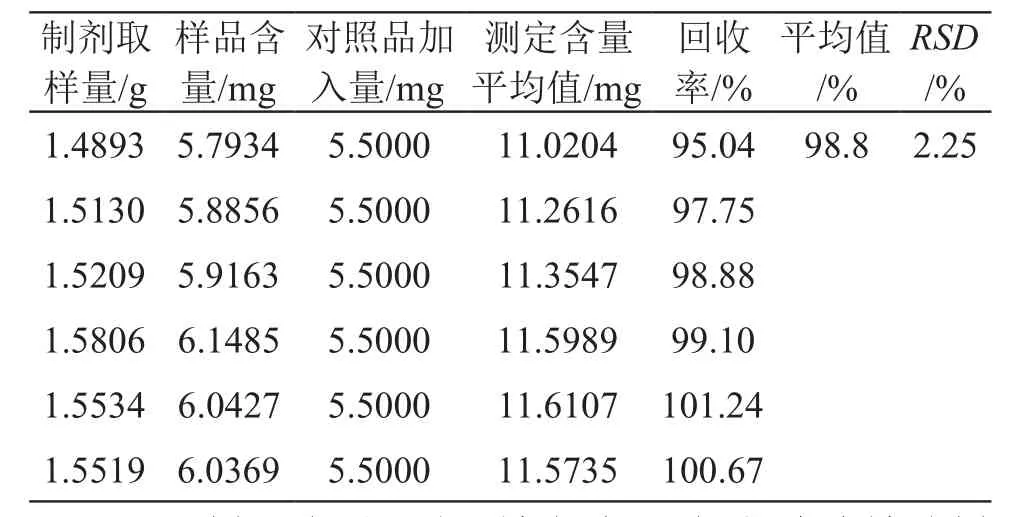
表1 黄芪甲苷加样回收率试验结果 (n=6)
2.2.1.11 样品含量测定 精密称取3批芪连降糖片样品,按2.2.1.3项方法制备供试品溶液,按2.2.1.1项色谱条件,测定样品中黄芪甲苷的含量,结果见表4。
2.2.2 生物碱类成分(黄连)的含量测定
2.2.2.1 色谱条件 Phenomenex Luna C18色谱柱(250 mm×4.6 mm,5 μm);流动相为乙腈-0.05 mol/L磷酸二氢钾溶液(48:52)(每100 ml中加十二烷基硫酸钠0.4 g,再以磷酸调节pH值为4.0);检测波长345 nm;柱温:30 ℃;进样量10 μl;流速1.0 ml/min。理论塔板数按盐酸小檗碱峰计算应不低于5000。
2.2.2.2 混合对照品溶液的制备 取表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱对照品适量,精密称定后置棕色量瓶中,加甲醇制成质量浓度分别为30.91,118.88,30.50,520.20 μg/ml的混合对照品溶液。
2.2.2.3 供试品溶液的制备 取芪连降糖片样品20片,除去包衣后研细,取约0.56 g,精密称定,置具塞锥形瓶中,精密加入甲醇-盐酸(100: 1)混合溶液50 ml,密闭后称定重量,超声处理(功率250 W,频率40 kHz)30 min,放冷,再称定重量,加入甲醇补足减失的重量,摇匀,滤过,精密量取续滤液2.0 ml,置入10 ml量瓶,加甲醇至刻度,摇匀,用0.45 μm微孔滤膜滤过,即得。
2.2.2.4 阴性对照溶液的制备 按芪连降糖片处方中药味的比例,称定相应比例的黄芪药材粉末,按其工艺制成空白制剂的药粉,再按2.2.2.3项方法制得相应阴性对照溶液。
2.2.2.5 专属性试验 分别吸取上述制备的表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱混合对照品溶液、供试品溶液及阴性对照溶液各10 μl,按2.2.2.1项色谱条件测定。结果表明,在与对照品色谱峰相应的位置上,供试品溶液有对应的色谱峰,且阴性无干扰,按表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱色谱峰计,理论塔板数分别为16 715,17 808,18 715和17 725,相邻色谱峰的分离度均大于1.5。表明建立的色谱条件专属性良好,适用于芪连降糖片中表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱的含量测定。色谱图见图4。
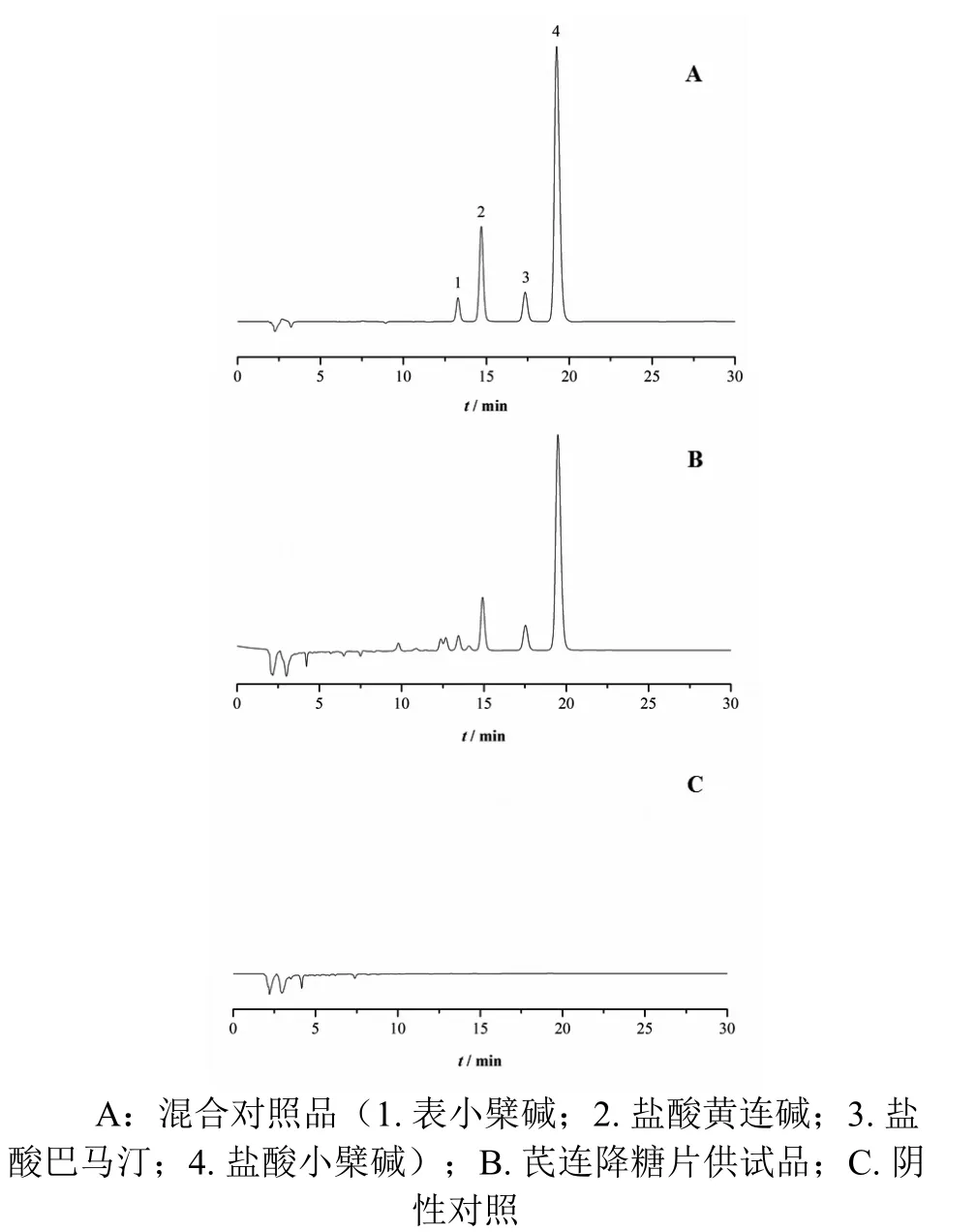
图4 芪连降糖片中黄连的高效液相色谱图
2.2.2.6 线性关系考察 分别精确吸取混合对照品溶液62.5,125,250,500,1000,2000 μl,置入2 ml量瓶,不足部分加甲醇定容至刻度,摇匀后即得系列质量浓度的混合对照品溶液。按2.2.2.1项色谱条件进样测定。以各对照品的峰面积(A)为纵坐标,质量浓度(C)为横坐标,绘制标准曲线,进行线性回归分析得到回归方程,结果见表2。
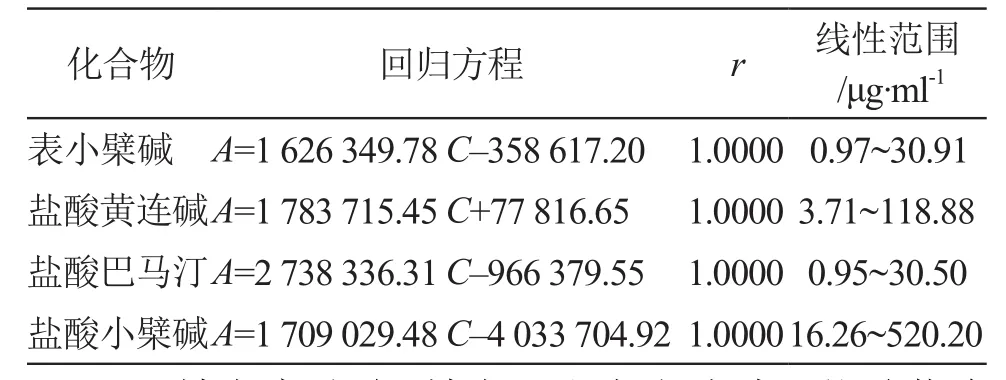
表2 表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱线性关系及其范围
2.2.2.7 精密度试验 精密吸取表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱混合对照品溶液,按2.2.2.1项色谱条件连续进样6次,计算表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱峰面积的RSD分别为0.99 %,2.53 %,0.52 %和0.36 %,表明仪器精密度良好。
2.2.2.8 稳定性试验 取同一供试品溶液(批号:20190401),分别于配制后0,3,4,6.5,14 h(低温避光保存)按2.2.2.1项色谱条件进样,记录表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱峰面积,计算RSD分别为2.85 %,1.93 %,2.16%和1.89 %,表明供试品溶液在低温避光保存条件下14 h内稳定性良好。
2.2.2.9 重复性试验 取同一批次芪连降糖片样品(批号:20190401)共计6份,精密称定,按2.2.2.3项方法制备供试品溶液,再按2.2.2.1项色谱条件进行测定。结果表明,表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的平均含量分别为4.83,15.20,6.17 ,94.69 mg/g;RSD分别为1.51 %,1.26 %,1.24 %,1.04 %。表明此法重复性良好。
2.2.2.10 加样回收率试验 取2.2.2.9项下已测定含量的芪连降糖片样品(批号:20190401)6份,每份取约0.26 g,精密称定,置入具塞锥形瓶,分别加入表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱含量分别为53,140,80,1000 μg/ml的混合对照品溶液25 ml,按2.2.2.3项方法制备供试品溶液,按2.2.2.1项色谱条件测定含量,计算各待测成分的加样回收率。结果表明,表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱的平均回收率为97.8 %,101.2 %,98.9 %,97.3 %;RSD为1.89 %,1.35 %,2.40 %,1.25 %,见表3。
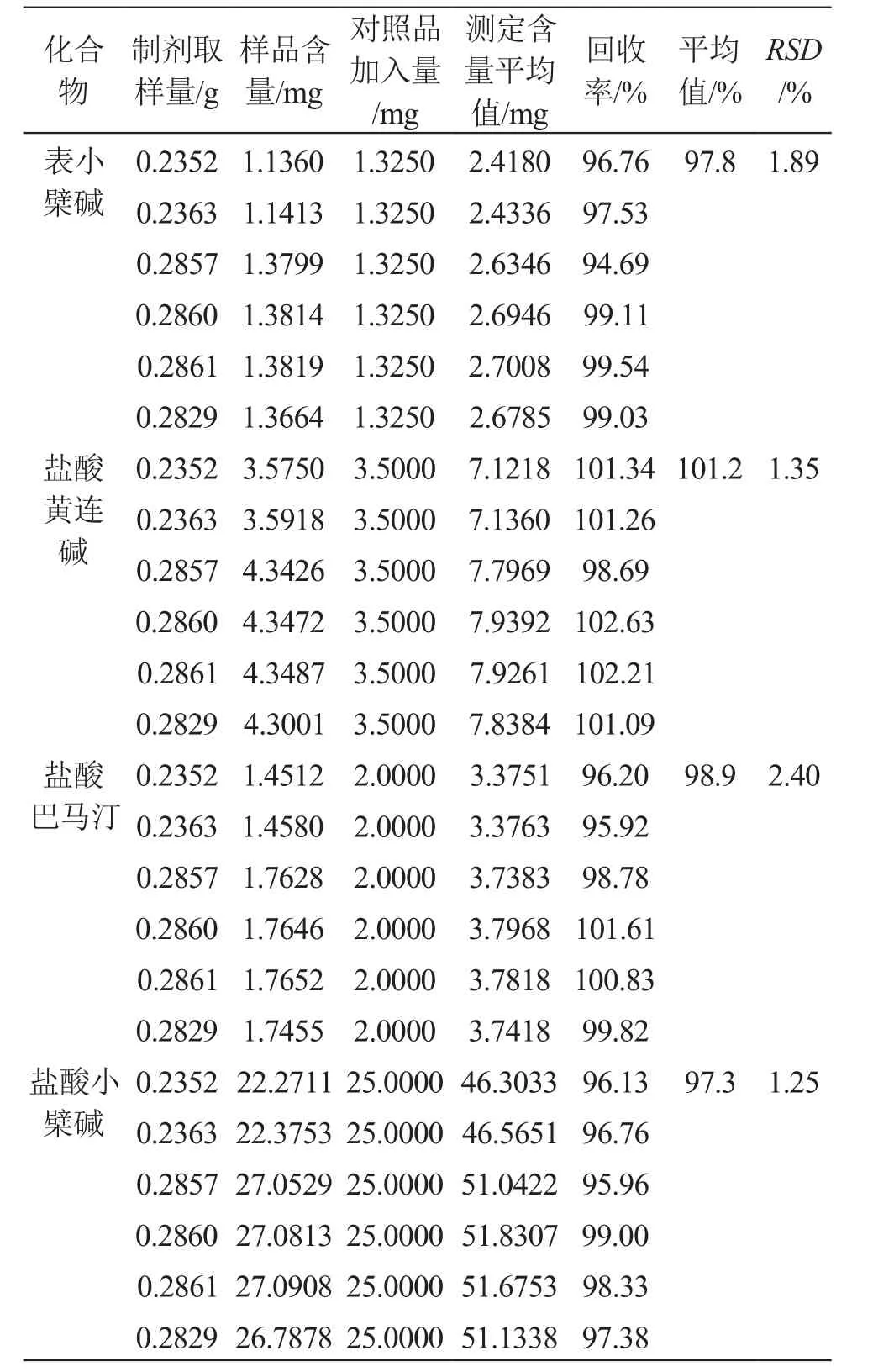
表3 表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱加样回收率试验结果(n=6)
2.2.2.11 样品含量测定 精密称取3批芪连降糖片样品,按2.2.2.3项方法制备供试品溶液,按2.2.2.1项色谱条件,测定样品中表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱的含量,结果见表4。
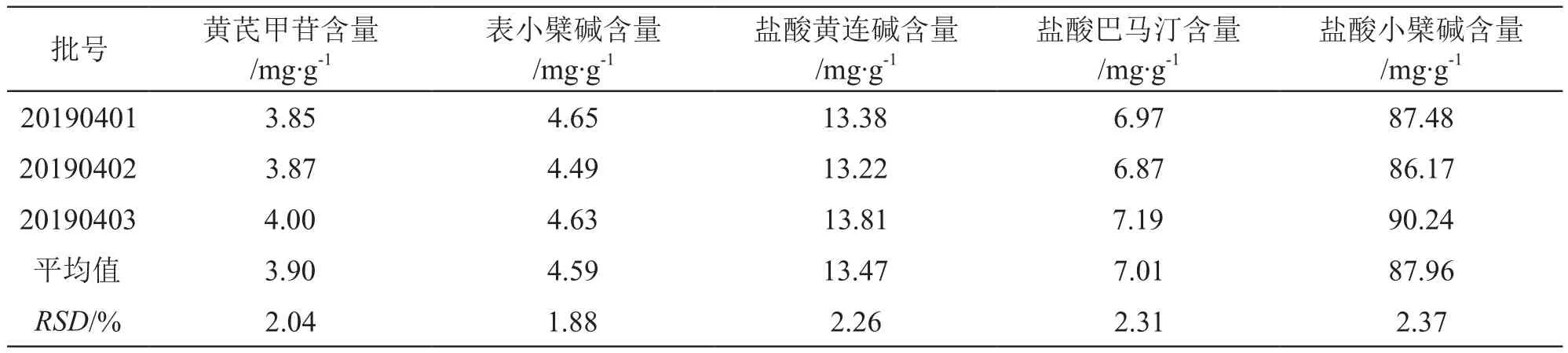
表4 3批芪连降糖片含量测定结果(n=3)
3 讨论
3.1 薄层色谱鉴别
芪连降糖片由黄芪、黄连(味连)两味药组成,均被《中国药典》收载并明确了相应鉴别方法。为了建立较完善的质量标准,本品参照《中国药典》2020年版(一部)和《中国药典》2015年版(一部)中黄芪、黄连项下的薄层色谱鉴别方法[4-5],对成品中黄芪和黄连(味连)两味药材均建立了薄层色谱鉴别方法。结果表明,在本实验选择的薄层色谱条件下,黄芪和黄连的供试品色谱在与对照品色谱、对照药材色谱相应的位置上,均显相同颜色的清晰斑点,分离度和重现性良好,阴性样品无干扰。
3.2 含量测定研究
黄芪甲苷为君药黄芪主要有效成分,具有抗炎、调节糖脂代谢、抗氧化应激、免疫调节、抗凋亡等多种药理作用[6-10];表小檗碱、黄连碱、巴马汀、小檗碱为臣药黄连主要有效成分,可协同调节与糖脂代谢紊乱、炎症反应、胰岛素抵抗、胰岛β细胞功能相关的靶点及通路,改善肠道菌群失调状态,综合发挥抗糖尿病作用[11-20]。本文根据药典方法[4-5],并结合所用蒸发光散射检测器特点,经过多次优化[21],确定黄芪甲苷的含量测定方法,结果表明,供试品和对照品均峰型良好无干扰,为最佳色谱条件。
为了全面控制芪连降糖片的质量,体现与临床疗效的关联性,本实验以黄芪甲苷和表小檗碱、盐酸黄连碱、盐酸巴马汀、盐酸小檗碱为指标建立了芪连降糖片的含量测定方法,经方法学验证表明该方法灵敏简便、稳定可行。在黄连生物碱类成分的含量测定中,流动相乙腈-0.05 mol/L磷酸二氢钾溶液的比例为50:50时,供试品中表小檗碱和盐酸黄连碱的出峰位置附近有杂质干扰且分离度差,因此需将流动相极性增大,延长各物质出峰时间保证待测成分分离度良好。本文优化后的色谱条件下,供试品和对照品中各待测成分均峰型对称,分离度良好,阴性对照无干扰。
3.3 关于含量限度的建议
芪连降糖片规格为每片重0.56 g,根据表4中3批样品含量测定结果,计算得芪连降糖片每片中黄芪甲苷、表小檗碱、盐酸黄连碱、盐酸巴马汀和盐酸小檗碱的平均含量分别为2.1,2.5,7.3,3.8和47.5 mg。考虑实际生产中投料量和工艺的影响,本文建议芪连降糖片含量限度为:本品每片含黄芪以黄芪甲苷(C31H68O14)计,不得少于1.7 mg;本品每片含黄连以表小檗碱(C20H18ClNO4)、盐酸黄连碱(C19H14ClNO4)、盐酸巴马汀(C21H22ClNO4)和盐酸小檗碱(C20H18ClNO4)计,分别不得少于2.0,5.8,3.0和38.0 mg。
综上,本实验建立了芪连降糖片的薄层色谱鉴别方法,同时采用高效液相色谱法建立了芪连降糖片中5种主要有效成分的含量测定方法,依法测定了3批中试样品中各成分的含量。方法简便可靠,结果准确,专属性强,重现性好,可用于该制剂的质量控制。
