注射用紫杉醇(白蛋白结合型)联合光动力疗法治疗晚期非小细胞肺癌致中心气道狭窄的临床效果▲
2023-06-25牛建明赵晨茜张旭宇许雪林李润浦
牛建明 赵晨茜 张旭宇 赵 薇 许雪林 李润浦
(保定市第二中心医院呼吸与危重症医学二科,河北省保定市 072750)
原发性肺癌(以下简称肺癌)是我国发病率和死亡率最高的恶性肿瘤[1]。早期肺癌多无明显症状,且缺乏有效的检查手段,多数肺癌患者发现时已为晚期。非小细胞肺癌(non-small cell lung cancer,NSCLC)是肺癌最常见的病理类型,占所有肺癌的85%。NSCLC肿瘤主要侵犯的部位为气管、隆突、主支气管及中间段支气管,晚期常合并中心气道狭窄,导致患者出现呼吸困难、呼吸衰竭和阻塞性肺炎,甚至窒息死亡[2],造成患者预后不良。
光动力疗法是一种药械联合技术治疗方案,具有靶向性强、侵入性小、疗效高、毒副作用轻等优势,对于晚期NSCLC致中心气道狭窄患者,该介入疗法能够重新开放气道,有效缓解患者呼吸困难症状,改善其生活质量[3],目前已经广泛应用于临床。注射用紫杉醇(白蛋白结合型)是一种新型的紫杉醇制剂,与传统的紫杉醇制剂相比,不仅增强了对肿瘤细胞的杀伤能力,同时减少了毒副反应且提高了安全性,现已广泛用于晚期肺癌等实体瘤的化疗[4]。研究发现,注射用紫杉醇(白蛋白结合型)治疗晚期NSCLC的效果较好,较普通的注射用紫杉醇能更好地延缓疾病进展,且安全性较高[5]。本研究采用注射用紫杉醇(白蛋白结合型)联合光动力疗法治疗晚期NSCLC致中心气道狭窄患者,观察其近期疗效、治疗安全性及预后,为NSCLC致中心气道狭窄的临床治疗提供更多的选择方案。现报告如下。
1 资料与方法
1.1 一般资料 选取2018年1月至2020年5月保定市第二中心医院收治的60例晚期NSCLC致中心气道狭窄患者作为研究对象。纳入标准:(1)满足晚期NSCLC[6]及中心气道狭窄[7]的诊断标准;(2)年龄35~75岁;(3)既往无放化疗等抗肿瘤治疗史;(4)美国东部肿瘤协作组体力状况评分[8]为0~2分;(5)预计生存时间>3个月;(6)无认知及意识障碍;(7)患者及家属知情同意。排除标准:(1)合并高血压、糖尿病等基础疾病者;(2)伴有无法控制的胸腔积液者;(3)依从性差,不愿接受定期随访者;(4)合并心肝肾等重要脏器功能不全者。按随机数字表法将其分为观察组与对照组,各30例。其中观察组男性19例,女性11例;年龄39~75(57.5±7.2)岁;病理类型:鳞癌17例,腺癌9例,大细胞癌4例;临床分期[9]:Ⅲ期8例,Ⅳ期22例;气道狭窄部位:中央气道Ⅰ~Ⅳ区7例,中央气道Ⅴ~Ⅷ区23例。对照组男性17例,女性13例;年龄40~75(58.3±6.7)岁;病理类型:鳞癌16例,腺癌11例,大细胞癌3例;临床分期:Ⅲ期7例,Ⅳ期23例;气道狭窄部位:中央气道Ⅰ~Ⅳ区9例,中央气道Ⅴ~Ⅷ区21例。两组上述基线资料比较,差异均无统计学意义(均P>0.05),具有可比性。本研究经保定市第二中心医院医学伦理委员会批准。
1.2 治疗方法 (1)对照组采用光动力疗法治疗。①术前准备。使用血卟啉注射液(喜泊分,重庆迈东生物制药有限公司,规格为5 mL ∶25 mg,产品批号:20171106、20181205、20200107)行过敏试验,即取喜泊分原液在前臂皮肤做皮肤划痕试验,若无红肿硬结,则按2~3 mg/kg剂量加入250 mL生理盐水中,均匀混合后避光静滴,给药时间约60 min。②激光照射方法。注射光敏剂(喜泊分)后48~72 h行纤维支气管镜(以下简称纤支镜,OLYMPUS公司,型号:BF-1T60)检查,确定光照部位,再于纤支镜引导下将半导体激光光动力治疗机(深圳市雷迈科技有限公司,型号:PDT630-A)的柱形激光治疗光纤(波长为630 nm)越过病变部位。激光照射参数:治疗区功率密度为100 mV/cm2,照射时间为15~20 min,总能量密度为150~200 J/cm2;照射时光纤尽量处于腔道正中,光纤中心照射范围覆盖在气道最狭窄段上下各2 cm内。术中经纤支镜吸痰、灌洗、钳夹坏死物,监测患者生命体征,术毕拔出光纤,退出纤支镜。③术后处理。术后观察患者生命体征,术后1周内给予止咳、祛痰等对症治疗,并适当使用抗生素、地塞米松预防感染和水肿,术后1~2周内根据患者病情,采用纤支镜吸痰、灌洗、钳夹坏死物。术后继续避光1个月,病房里用厚窗帘遮光,患者避免将眼和皮肤暴露于室内强聚焦光和日光下,戴黑色太阳眼镜。 (2)观察组在光动力疗法治疗后(方法同对照组)第3天采用注射用紫杉醇(白蛋白结合型)(石药集团欧意药业有限公司,规格为100 mg/瓶,产品批号:B04171103、B04181209、B04191203)化疗,每次用量为130 mg/m2,静脉滴注,分别于第1 天、第8 天给药,每次给药时间应>30 min,以21 d为1个化疗周期。对照组治疗后42 d、观察组治疗2个化疗周期后(均简称治疗后)评价两组抗肿瘤疗效及以下观察指标。
1.3 疗效判定 治疗后按照实体瘤疗效评价标准[10]评价两组近期疗效。完全缓解:治疗后所有目标病灶消失;部分缓解:治疗后基线病灶长径总和缩小≥30%;病变稳定:治疗后基线病灶长径总和缩小但未达部分缓解,或有增加但不及病变进展;病变进展:治疗后基线病灶长径总和增加≥20%,或出现新病灶。客观缓解率=(完全缓解+部分缓解)例数/总例数×100%,疾病控制率=(完全缓解+部分缓解+病变稳定)例数/总例数×100%。
1.4 观察指标 (1)气道狭窄情况:治疗前后采用纤支镜下标尺测量患者气道狭窄段最小直径,计算气道狭窄程度。气道狭窄程度=气道狭窄段最小直径/正常气道管径×100%。(2)生存质量:治疗前后采用欧洲癌症研究与治疗组织生命质量核心量表(European Organization for Research and Treatment of Cancer Quality of Life Questionnaire-30-Item Core Instrument,EORTC QLQ-C30)[11]评估两组生存质量状况,该调查问卷共有30个项目,包含躯体功能(5个项目)、认知功能(2个项目)、社会功能(2个项目)、角色功能(2个项目)和情感功能(4个项目)5个功能子量表,疼痛(2个项目)、疲乏(3个项目)和恶心呕吐(2个项目)3个症状子量表,呼吸困难、食欲丧失、腹泻、失眠、便秘和经济困难6个单项测量项目,以及1个整体生存质量量表(2个项目),所有子量表及单项测量项目总分范围均为0~100分。其中功能子量表得分越高则对应的功能越好,症状子量表及单项测量项目的分数越高则对应的症状越明显,整体生存质量量表评分越高则整体生存质量越好。(3)肺功能:治疗前后采用FGC-A+型肺功能测试仪(安徽电子科学研究所)检测每例患者的肺功能,包括用力肺活量、第1秒用力呼气容积、最大自主通气量。(4)安全性评价:记录两组光动力治疗的不良反应及观察组药物毒副反应发生情况,注射用紫杉醇(白蛋白结合型)化疗毒副反应按美国国立癌症研究所常见不良反应评价标准[12]进行评估,分为1~5级。1级为轻度,无症状或轻度症状,仅临床或诊断发现,无须治疗;2级为中度,有最小的、局部的或非侵入性治疗指征,年龄相关工具性日常生活活动受限;3级为重度或重要医学意义,但不会立即危及生命,住院治疗或延长住院时间指征,致残,自理性日常生活活动受限;4级为危及生命,需紧急治疗;5级为死亡。(5)远期生存情况:所有患者自治疗开始后,每个月以电话或门诊方式对其进行追踪随访,调查其生存情况,末次随访时间为2021年6月1日,记录每例患者的终点事件,包括无进展生存期和总生存期。无进展生存期为治疗开始至首次病变进展或任何原因死亡或末次随访的时间。总生存期为治疗开始至任何原因死亡或末次随访的时间。
1.5 统计学分析 采用SPSS 21.0软件进行统计学分析。计数资料以例数和百分比表示,比较采用χ2检验;符合正态分布的计量资料以(x±s)表示,组间比较采用两独立样本t检验,同组治疗前后比较采用配对t检验。生存情况的比较采用log-rank检验。以P<0.05为差异具有统计学意义。
2 结 果
2.1 两组临床疗效的比较 治疗后,观察组客观缓解率为40.0%,高于对照组的16.7%(χ2=4.022,P=0.045);观察组疾病控制率为76.6%,高于对照组的50.0%(χ2=4.593,P=0.032)。见表1。

表1 两组临床疗效的比较(n)
2.2 治疗前后两组患者气道狭窄情况的比较 治疗前,两组气道狭窄段最小直径、气道狭窄程度比较,差异均无统计学意义(均P>0.05)。治疗后,两组气道狭窄段最小直径均大于治疗前、气道狭窄程度均小于治疗前,且观察组上述指标均优于对照组(均P<0.05)。见表2。
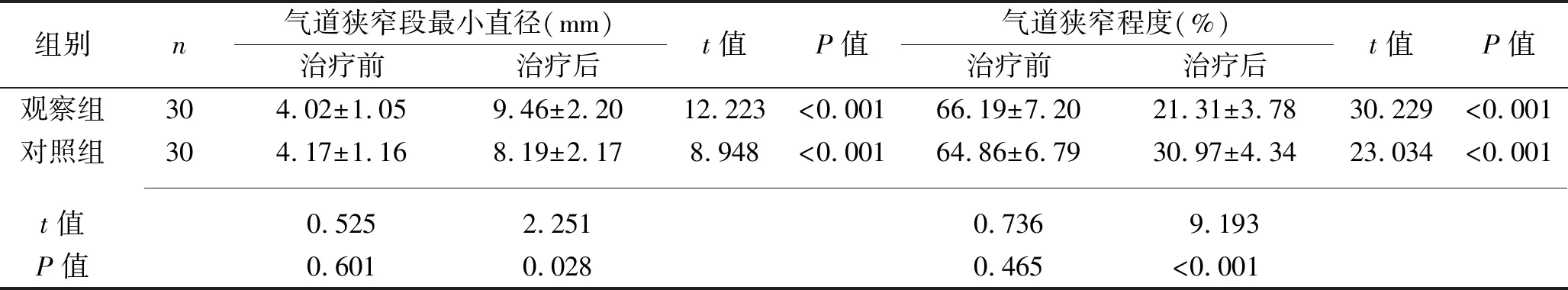
表2 治疗前后两组患者气道狭窄情况的比较(x±s)
2.3 治疗前后两组患者EORTC QLQ-C30评分的比较 治疗前,两组患者EORTC QLQ-C30中的各子量表和单项测量项目评分比较,差异均无统计学意义(均P>0.05)。治疗后,两组患者EORTC QLQ-C30中的躯体功能、整体生存质量评分均高于治疗前,疼痛、呼吸困难评分均低于治疗前,且观察组上述指标评分均优于对照组(均P<0.05)。两组治疗前后组内及同期组间其余子量表和单项测量项目的评分比较,差异均无统计学意义(均P>0.05)。见表3。

表3 治疗前后两组患者EORTC QLQ-C30评分的比较(x±s,分)
2.4 治疗前后两组患者肺功能的比较 治疗前,两组用力肺活量、第1秒用力呼气容积、最大自主通气量比较,差异均无统计学意义(均P>0.05)。治疗后,两组用力肺活量、第1秒用力呼气容积、最大自主通气量均较治疗前升高,且观察组上述指标均高于对照组(均P<0.05)。见表4。

表4 治疗前后两组患者肺功能的比较(x±s)
2.5 两组不良反应发生情况的比较
2.5.1 光动力疗法不良反应:所有患者治疗后48 h内均有不同程度的气管、支气管黏膜水肿。此外,观察组和对照组患者在光动力疗法治疗过程中分别有3例和2例患者出现咳嗽、咳痰症状,经纤支镜及时将坏死物清理后均缓解;光动力疗法治疗后72 h内,观察组和对照组分别有2例和1例患者出现低热,经退热、抗感染等对症治疗后体温均恢复正常;光动力疗法治疗后1个月内,观察组和对照组分别有2例和3例患者出现局部皮肤红斑、瘙痒,经抗组胺药物及激素治疗3 d后均缓解。所有患者在治疗及随访期间均未出现肝肾功能损害、光敏剂过敏、出血、肿瘤组织误吸、气道穿孔、治疗相关死亡等严重不良事件。
2.5.2 注射用紫杉醇(白蛋白结合型)化疗毒副反应:观察组治疗2个化疗周期内,主要血液学毒副反应为白细胞减少(46.7%)和中性粒细胞减少(36.7%),但多为1~2级,患者可耐受,仅发生2例3级白细胞减少和1例3级中性粒细胞减少。主要非血液学毒副反应为胃肠道反应(46.7%)、脱发(43.3%)、乏力(33.3%)、周围神经毒性(23.3%),但均为1~2级,患者可耐受。30例患者均无3~4级不良反应发生,治疗期间均未出现因毒副反应而中断治疗的情况,均未出现过敏反应,且无治疗相关死亡事件发生。总体而言,患者的不良反应可控制,整体耐受性良好。见表5。

表5 观察组患者注射用紫杉醇(白蛋白结合型)化疗毒副反应发生情况[n=30,n(%)]
2.6 两组生存情况的比较 60例患者均无失访,随访率为100%,随访时长5~36个月。观察组和对照组的中位无进展生存期分别为5.4个月(95%CI:3.54,7.16)、4.0个月(95%CI:3.37,6.02),组间差异有统计学意义(χ2=4.683,P=0.031)。观察组和对照组的中位总生存期分别为13.5个月(95%CI:9.98,19.43)、10.4个月(95%CI:9.39,14.05),组间差异有统计学意义(χ2=4.059,P=0.040)。
3 讨 论
研究发现,光动力疗法除了能通过产生活性氧杀伤肿瘤细胞或诱导肿瘤细胞凋亡,还可能通过诱发肿瘤病变组织血管内血栓形成,增加血管活性物质释放,以减少肿瘤病变组织的血供,使其缺血、缺氧,最终导致组织变性、坏死;光动力疗法还能通过增强肿瘤细胞免疫原性来激发较强烈的免疫反应,帮助机体免疫系统识别肿瘤细胞并将其清除[13]。目前,光动力疗法在肺癌治疗中已广泛应用,其可作为姑息性治疗手段应用于晚期肺癌患者,在控制症状、重新开放气道及改善患者生存质量等方面具有重要意义[14]。本研究采用光动力疗法治疗晚期NSCLC致中心气道狭窄患者,结果显示,治疗后患者的气道狭窄情况及EORTC QLQ-C30中躯体功能、疼痛、呼吸困难、整体生存质量评分和肺功能指标均较治疗前显著改善,提示采取光动力疗法治疗晚期NSCLC致中心气道狭窄能获得较好的疗效。光动力疗法的主要不良反应为光敏反应,光敏剂注入患者体内后需要30 d左右才能排出体外,故本研究均要求患者光动力疗法治疗后继续严格避光1个月,结果发现患者不良反应相对轻微,均可耐受,且经对症处理后症状很快消失,表明光动力疗法治疗晚期NSCLC致中心气道狭窄患者的安全性高。
注射用紫杉醇(白蛋白结合型)是一种在传统的紫杉醇基础上添加人血白蛋白为载体的新型化疗药物,其特殊的结构使其能够通过内源性白蛋白通路而与肿瘤组织中富含半胱氨酸的酸性分泌蛋白结合,从而增加紫杉醇在肿瘤局部组织中的浓度,增强了紫杉醇对肿瘤细胞的靶向杀伤作用,同时本品无需蓖麻油作为助溶剂,降低了传统的紫杉醇常见毒性反应的发生风险,提高了用药安全性及患者的可耐受程度。杨科等[15]应用注射用紫杉醇(白蛋白结合型)单药治疗63例一线治疗失败的晚期NSCLC患者,结果显示其客观缓解率达23.81%,较多西他赛和培美曲塞单药二线治疗的客观缓解率(<10%)明显升高;其中位无进展生存期和中位总生存期分别为3.9个月(95%CI:3.1,5.2)、9.3个月(95%CI:7.8,10.4),较多西他赛和培美曲塞单药二线治疗明显延长;主要的2级以上不良反应为血小板减少、中性粒细胞减少、外周神经毒性和脱发,总体毒副作用可耐受。此外,Kotake等[16]应用注射用紫杉醇(白蛋白结合型)单药治疗35例一线或二线化疗失败的晚期NSCLC患者,结果显示其客观缓解率和疾病控制率可达到31.4%与74.3%,中位无进展生存期和中位总生存期分别为3.6个月与11.4个月,整体的毒副反应可耐受。以上研究说明注射用紫杉醇(白蛋白结合型)的抗实体瘤疗效较好,且毒副作用小,耐受性好。
综合治疗是肺癌临床治疗的重要策略,光动力疗法联合手术、放疗、化疗、抗血管生成药物等,除可明显缓解症状外,还能显著改善远期生存情况。研究发现[17],光动力疗法与紫杉醇化疗在直接杀伤人类癌细胞、促进人类癌细胞凋亡等方面具有显著的协同效应。Kimura等[18]应用光动力疗法联合化疗治疗12例晚期NSCLC合并气道狭窄患者,结果显示,所有患者的呼吸困难症状和生活质量均有改善,且患者气道狭窄程度显著降低,阻塞性肺炎的发生风险也明显降低。El-Hussein等[19]联合化疗和光动力疗法治疗肺癌患者,发现二者可以协同增强抑癌作用,显著提高抗肿瘤效果,且安全性高。以上研究结果表明光动力疗法联合化疗是一种安全且有效的治疗方案。注射用紫杉醇(白蛋白结合型)与光动力疗法在治疗晚期NSCLC上有一定优势,但目前尚缺乏二者联合治疗晚期NSCLC致中心气道狭窄的近期疗效、安全性及对远期生存状态的影响的相关研究。为此,本研究将注射用紫杉醇(白蛋白结合型)与光动力疗法联合应用于晚期NSCLC致中心气道狭窄患者的临床治疗中。结果显示,治疗后,观察组的客观缓解率、疾病控制率(分别为40.0%、76.6%)均高于对照组(分别为16.7%、50.0%),气道狭窄程度较同期对照组减轻,肺功能及EORTC QLQ-C30中的躯体功能、疼痛、呼吸困难和整体生存质量评分优于同期对照组,且中位无进展生存期和中位总生存期均较对照组延长(均P<0.05)。这提示采用注射用紫杉醇(白蛋白结合型)联合光动力疗法治疗晚期NSCLC致中心气道狭窄患者的近、远期疗效均优于单用光动力治疗,另外也可说明注射用紫杉醇(白蛋白结合型)与光动力疗法在晚期NSCLC致中心气道狭窄治疗中有协同效应,但二者如何起到协同作用尚有待进一步研究。从安全性角度分析,观察组除了出现可控的光动力疗法相关不良反应外,注射用紫杉醇(白蛋白结合型)化疗的主要毒副反应为骨髓抑制、胃肠道反应、周围神经毒性、脱发、乏力,但多为1~2级,患者耐受性较好,这说明晚期NSCLC致中心气道狭窄患者对注射用紫杉醇(白蛋白结合型)联合光动力疗法治疗的整体耐受性良好。
综上所述,注射用紫杉醇(白蛋白结合型)联合光动力疗法治疗晚期NSCLC致中心气道狭窄的总体疗效确切,能有效解除患者气道狭窄,改善肺通气功能,提高生存质量,并可使患者在远期生存方面获益,且患者耐受性好。
