利妥昔单抗在非霍奇金淋巴瘤患者中的疗效、安全性及对血浆克隆刺激因子的影响
2023-06-25张渝李福原陶丽菊
张渝 李福原 陶丽菊
【摘要】 目的:探究利妥昔单抗在非霍奇金淋巴瘤患者中的疗效、安全性及对血浆克隆刺激因子的影响。方法:将2019年1月-2022年2月右江民族医学院附属医院的80例非霍奇金淋巴瘤患者根据随机数字表法分为对照组40例和观察组40例。对照组进行常规非霍奇金淋巴瘤治疗,观察组则在常规治疗的基础上加用利妥昔单抗。比较两组治疗总有效率、各类不良反应发生率、治疗前后的疾病相关血清指标(LDH、β2-MG及CA125)及血漿克隆刺激因子(G-CSF及GM-CSF)。结果:观察组治疗总有效率高于对照组,差异有统计学意义(P<0.05)。两组的各类不良反应发生率比较,差异均无统计学意义(P>0.05)。治疗前两组的疾病相关血清指标及血浆克隆刺激因子比较,差异均无统计学意义(P>0.05);治疗2、4个周期后两组疾病相关血清指标及血浆克隆刺激因子均低于治疗前,且观察组均低于对照组,差异均有统计学意义(P<0.05)。结论:利妥昔单抗在非霍奇金淋巴瘤患者中的疗效较好,安全性值得肯定,且可显著改善患者的血浆克隆刺激因子,因此在非霍奇金淋巴瘤患者中的应用价值相对较高。
【关键词】 利妥昔单抗 非霍奇金淋巴瘤 克隆刺激因子
Effect and Safety of Rituximab in Patients with Non-Hodgkin's Lymphoma and Influence on Plasma Colony-stimulating Factor/ZHANG Yu, LI Fuyuan, TAO Liju. //Medical Innovation of China, 2023, 20(09): 0-022
[Abstract] Objective: To investigate the effect and safety of Rituximab in the patients with non-Hodgkin's lymphoma and influence for plasma colony-stimulating factor. Method: A total of 80 patients with non-Hodgkin's lymphoma in Affiliated Hospital of Youjiang Medical University for Nationalities from January 2019 to February 2022 were divided into control group 40 cases and observation group 40 cases by the random number table method. The control group received conventional treatment for non-Hodgkin's lymphoma, and the observation group received Rituximab in addition to conventional treatment. The total effective rate, incidence of various adverse reactions, disease-related serum indexes (LDH, β2-MG and CA125) and plasma cloning stimulating factor (G-CSF and GM-CSF) before and after treatment were compared between the two groups. Result: The total effective rate of the observation group was higher than that of the control group, the difference was statistically significant (P<0.05). There were no statistical significance in the incidences of all kinds of adverse reactions between the two groups (P>0.05). There were no significant differences in disease-related serum indexes and plasma clone stimulating factors between the two groups before treatment (P>0.05). After 2 and 4 cycles of treatment, disease-related serum indexes and plasma clone stimulating factors in two groups were lower than those before treatment, and those of observation group were lower than those of control group, with statistical significances (P<0.05). Conclusion: The effect of Rituximab in patients with non-Hodgkin's lymphoma is better, and its safety is worth affirming, it can significantly improve the plasma colony-stimulating factor of patients, so its application value in the patients with non-Hodgkin's lymphoma is relatively higher.
[Key words] Rituximab Non-Hodgkin's lymphoma Colony-stimulating factor
First-author's address: Affiliated Hospital of Youjiang Medical University for Nationalities, Baise 533000, China
doi:10.3969/j.issn.1674-4985.2023.09.005
非霍奇金淋巴瘤是我國较为常见的一类疾病,其相关的诊治研究多见,除表现出局部及全身表现外,乳酸脱氢酶(LDH)、β2微球蛋白(β2-MG)及糖类抗原125(CA125)等疾病相关的血液指标在本类患者中呈现高表达状态,且与疾病的发生发展及变化转归等密切相关[1-2];另外,粒细胞集落刺激因子(G-CSF)和粒细胞-巨噬细胞集落刺激因子(GM-CSF)等克隆刺激因子也在本类患者中呈现高表达状态,因此也是疾病治疗效果的重要参考方面。近年来临床中采用利妥昔单抗治疗本病的研究不断增多,多数研究认为其具有较好的效果[3-5],但是对于非霍奇金淋巴瘤的细致治疗效果研究仍不足,且对血浆克隆刺激因子表达的影响研究不足。因此本研究现探究利妥昔单抗在非霍奇金淋巴瘤患者中的疗效、安全性及对血浆克隆刺激因子的影响,并报道如下。
1 资料与方法
1.1 一般资料 将2019年1月-2022年2月右江民族医学院附属医院的80例非霍奇金淋巴瘤患者根据随机数字表法分为对照组40例和观察组40例。纳入标准:确诊为非霍奇金淋巴瘤;年龄18~75岁。排除标准:合并肝肾功能不全;沟通障碍;合并其他恶性肿瘤;临床资料不完整。所有患者均知情同意本研究并签署知情同意书。本研究经医院医学伦理委员会批准。
1.2 方法 对照组进行常规非霍奇金淋巴瘤治疗,第1天静滴环磷酰胺(生产厂家:山西普德药业股份有限公司,批准文号:国药准字H14023686,规格:0.2 g)750 mg/m2,第1天静推长春新碱(生产厂家:辽宁卫星制药厂,批准文号:国药准字H21023593,规格:1 mg)1.4 mg/m2及吡柔比星(生产厂家:深圳万乐药业有限公司;批准文号:国药准字H10930105,规格:10 mg)40 mg/m2,第1~5天口服泼尼松(生产厂家:新乡市常乐制药有限责任公司,批准文号:国药准字H41020214,规格:5 mg)100 mg/次,1次/d。观察组则在对照组的基础上加用利妥昔单抗(生产厂家:F.Hoffmann-la Roche Limited,批准文号:国药准字S20080045,规格:500 mg),即在上述常规治疗措施前1 d采用利妥昔单抗静滴,剂量为375 mg/m2。两组均以21 d为1个周期。两组均治疗4个周期。
1.3 观察指标与判定标准 统计及比较两组治疗总有效率、各类不良反应发生率、治疗前后的疾病相关血清指标及血浆克隆刺激因子。(1)治疗效果:穿刺活检阴性,淋巴结在1.5 cm以下,且维持4周以上为完全缓解;病灶缩小50%以上,且未出现新的病灶为部分缓解;病灶缩小不足50%,或增大不足25%为稳定;病灶增大25%以上为进展[6]。治疗总有效率=(完全缓解例数+部分缓解例数)/总例数×100%。(2)各类不良反应发生情况:根据WHO化疗毒副反应分级标准对两组患者的各类不良反应发生情况进行评估,对白细胞下降、发热、血红蛋白下降及感染等方面进行评估,其均为0~Ⅳ级,0为无,Ⅰ~Ⅳ级表示由轻到重,其中Ⅲ、Ⅳ级为相对较重[7]。(3)疾病相关血清指标:于治疗前及治疗2、4个周期后分别采集两组的晨起空腹静脉血,每次采集5.0 mL,即刻送检,由两名经验丰富的检验科工作人员进行疾病相关血清指标(LDH、β2-MG及CA125)及血浆克隆刺激因子(G-CSF及GM-CSF)的定量检测,均采用酶联免疫法进行定量检测。
1.4 统计学处理 采用SPSS 23.0软件对所得数据进行统计分析,计量资料用(x±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 对照组男27例,女13例;
年龄39~73岁,平均(56.36±8.19)岁;Ann Arbor分期:Ⅰ、Ⅱ期19例,Ⅲ、Ⅳ期21例。观察组男25例,女15例;年龄39~74岁,平均(56.75±8.31)岁;Ann Arbor分期:Ⅰ、Ⅱ期18例,Ⅲ、Ⅳ期22例。两组非霍奇金淋巴瘤患者的上述基线资料比较,差异均无统计学意义(P>0.05),具有均衡性与可比性。
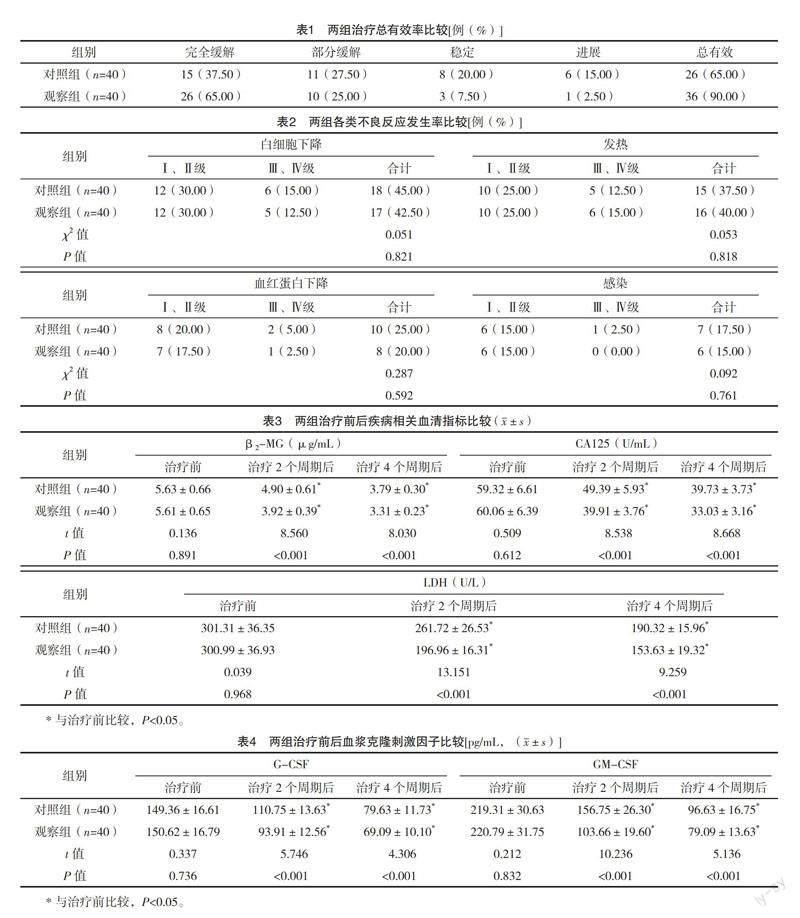
2.2 两组治疗总有效率比较 观察组治疗总有效率高于对照组,差异有统计学意义(字2=7.168,P=0.007),见表1。
2.3 两组的各类不良反应发生率比较 两组的各类不良反应发生率比较,差异均无统计学意义(P>0.05),见表2。
2.4 两组治疗前后疾病相关血清指标比较 治疗前两组的疾病相关血清指标比较,差异均无统计学意义(P>0.05);治疗2、4个周期后两组疾病相关血清指标均低于治疗前,且观察组均低于对照组,差异均有统计学意义(P<0.05)。见表3。
2.5 两组治疗前后血浆克隆刺激因子比较 治疗前两组的血浆克隆刺激因子比较,差异均无统计学意义(P>0.05);治疗2、4个周期后两组的血浆克隆刺激因子均低于治疗前,且观察组均低于对照组,差异均有统计学意义(P<0.05)。见表4。
3 讨论
非霍奇金淋巴瘤主要发生于淋巴器官,其在我国的发病率呈现升高的趋势,而与之相关的各方面研究也不断增多。本病患者除表现出淋巴结肿大及其相关器官的表现外,发热、盗汗等相关表现也相对突出[8-9],与此同时,本类患者的LDH、β2-MG及CA125等指标也呈现异常表达的状态,且研究显示,上述指标与本病的发生发展及变化转归有密切的关系,对于患者的预后具有较高的检测价值,因此对本类患者治疗的过程中,上述疾病相关血液指标的变化监测意义较高。G-CSF及GM-CSF等克隆刺激因子也是在本病患者中呈现异常表达的指标[10-12],其与T细胞介导的免疫反应及B淋巴细胞增殖等多方面有密切的关系,而其在本类患者中的表达与疾病的控制效果有密切的关系,因此可作为非霍奇金淋巴瘤治疗措施可取性的重要参考方面[13-15]。近年来临床中采用利妥昔单抗治疗本病的研究不断增多,多数研究认为其对本病的治疗效果较好,安全性也值得肯定,但是效果差异仍存在[16-17],且对上述克隆刺激因子表达的影响研究不足,故仍有较大的研究空间。
本研究结果显示,利妥昔单抗在非霍奇金淋巴瘤患者中的治疗总有效率高于常规治疗(P<0.05),且其各类不良反应发生率无显著差异(P>0.05),因此认为其疗效较好的同时,安全性也得到有效肯定,而且,患者治疗后的上述疾病相关血清指标及血浆克隆刺激因子均低于治疗前,且均低于常规治疗(P<0.05),因此进一步肯定了其对非霍奇金淋巴瘤的治疗效果。分析原因,利妥昔单抗可有效针对B细胞进行干预,通过抑制B细胞增生来达到控制疾病的目的,对肿瘤细胞起到杀伤作用[18-19],同时其对肿瘤细胞的凋亡具有干预作用,有助于促进其凋亡[20-21],因此对非霍奇金淋巴瘤具有较好的治疗效果。
综上所述,利妥昔单抗在非霍奇金淋巴瘤患者中的疗效较好,安全性值得肯定,且可显著改善患者的血浆克隆刺激因子,因此在非霍奇金淋巴瘤患者中的应用价值相对较高。
参考文献
[1]陈晓,陈茂林,魏晓霞,等.不同临床分期弥漫大B细胞淋巴瘤患者血清β2-MG、LDH、VEGF水平变化及动态监测指导意义[J].医学检验与临床,2021,32(5):57-59.
[2]陈海珠.利妥昔单抗时代弥漫大B细胞淋巴瘤预后相关临床及分子标志物的探索研究[D].北京:北京协和医学院,2022:16-26.
[3]柯维强,陈祥慧,陈小玲,等.自体外周血干细胞移植联合利妥昔单抗治疗弥漫大B细胞淋巴瘤及相关因子的表达[J].中国组织工程研究,2023,27(6):915-920.
[4]单欣,郭赛赛.含利妥昔单抗方案治疗晚期套细胞淋巴瘤临床分析[J].中国临床研究,2022,35(2):167-171.
[5]赵博.利妥昔单抗联合CHOP方案治疗DLBCL的疗效及预后因素分析[J].临床研究,2022,30(6):36-40.
[6]邱流进,刘轩,肖威.盐酸多柔比星脂质体联合利妥昔单抗治疗复发难治性非霍奇金淋巴瘤的临床研究[J].中国医学创新,2022,19(29):17-20.
[7]李茜汝,曹红敏,郭靖雯,等.二线方案联合利妥昔单抗治疗非霍奇金淋巴瘤的疗效观察[J].中国现代药物应用,2022,16(2):196-198.
[8]赵芳,程莉莉,郑重,等.苯达莫司汀联合利妥昔单抗治疗复发滤泡性淋巴瘤的临床分析[J].中华血液学杂志,2022,43(6):513-517.
[9] KANATE A S,KUMAR A,DREGER P,et al.Maintenance therapies for Hodgkin and non-Hodgkin lymphomas after autologous transplantation:a consensus project of ASBMT,CIBMTR,and the lymphoma working party of EBMT[J].JAMA Oncol,2019,5(5):715-722.
[10] CHESON B D,CHUA N,MAYER J,et al.Overall survival benefit in patients with Rituximab-refractory indolent non-Hodgkin lymphoma who received Obinutuzumab plus Bendamustine induction and Obinutuzumab maintenance in the GADOLIN study[J].J Clin Oncol,2018,36(22):2259-2266.
[11] MATASAR M J,CAPRA M,ÖZCAN M,et al.Copanlisib plus Rituximab versus placebo plus Rituximab in patients with relapsed indolent non-Hodgkin lymphoma(CHRONOS-3):a double-blind,randomised,placebo-controlled,phase 3 trial[J].Lancet Oncol,2021,22(5):678-689.
[12]林曉媛,张晓冬.利妥昔单抗联合CHOP化疗方案治疗B细胞非霍奇金淋巴瘤的临床观察[J].中国实用医刊,2022,49(4):93-96.
[13]周令,李战华,李运玲.利妥昔单抗对儿童高分期成熟B细胞非霍奇金淋巴瘤的疗效研究[J].实用癌症杂志,2022,37(1):146-149.
[14]孙颖颖.弥漫大B细胞淋巴瘤患者利妥昔单抗联合化疗治疗效果及其影响因素[J].数理医药学杂志,2022,35(5):698-701.
[15]姬宏利,姬宏娟,丁平.利妥昔单抗联合GDP化疗对非霍奇金淋巴瘤患者TK-1水平、血小板功能恢复及总生存率的影响[J].检验医学与临床,2022,19(21):2962-2966.
[16] MINARD-COLIN V,AUPÉRIN A,PILLON M,et al.
Rituximab for high-risk,mature B-cell non-Hodgkin's lymphoma in children[J].N Engl J Med,2020,382(23):2207-2219.
[17]巫洁.苯达莫司汀联合利妥昔单抗治疗弥漫性细胞淋巴瘤的临床疗效及对NF-κB p50、VEGF的影响[J].中国处方药,2022,20(11):91-93.
[18]潘晓兰,张燕,骆竹媚.沙利度胺联合利妥昔单抗治疗对淋巴瘤患者生存质量的影响[J].实用医院临床杂志,2022,19(1):22-25.
[19]郭怀鹏,秦炜炜,郭欢绪,等.利妥昔单抗治疗新诊断原发性中枢神经系统淋巴瘤的系统回顾和荟萃分析[J].检验医学与临床,2022,19(15):2086-2090.
[20]申晗,高冠论,许艳丽,等.阿卡替尼增强利妥昔单抗生物类似药HLX01对非GCB型DLBCL耐药细胞株的杀伤效果[J].中国病理生理杂志,2022,38(1):11-19.
[21]高苏,陈莉,陈洁,等.重组人粒-巨噬细胞集落刺激因子联合R-CHOP方案治疗初治弥漫大B细胞淋巴瘤效果观察[J].白血病·淋巴瘤,2021,30(12):730-734.
(收稿日期:2023-01-17) (本文编辑:田婧)