儿童重症监护室肺出血患儿发生死亡的影响因素*
2023-06-23饶玉薪陈茂琼孙慧
饶玉薪, 陈茂琼, 孙慧*
(1.贵州医科大附属医院 儿童重症监护室, 贵州 贵阳 550001; 2.贵州医科大学 临床医学院, 贵州 贵阳 550001; 3.贵州医科大学附属医院 新生儿科, 贵州 贵阳 550001)
肺出血是指肺血管壁损伤、变性或伴有肺动脉高压等因素引起的以咯血为主要特征的疾病,如不正确及时诊治可能出现危及生命的并发症,例如窒息、休克、多器官功能障碍综合征(multiple organ dysfunction syndrome,MODS)及弥漫性血管内凝血(disseminated intravascular coagulation,DIC)等[1]。国外研究显示肺出血的死亡率高达 9%~38%[2],其中危重症患者死亡率更高达25%,大咯血死亡率可至50%[3-4]。国内针对儿童肺出血的研究多集中于新生儿[5-7], 对非新生儿期的肺出血的研究较少[8];杨雨航等[9]研究显示,儿童重症监护室(pediatric intensive care unit,PICU)肺出血患儿的发病率为0.66%,提示在PICU儿童肺出血占有一定比例。因此,本研究拟通过分析PICU肺出血患儿的临床资料,探究其病因构成、临床特征及死亡相关因素,旨在提高对儿童肺出血的认识,以达到早期识别、诊断及干预治疗,降低病死率,提高患儿生存质量。
1 对象与方法
1.1 研究对象
选取2013年3月—2022年4月PICU诊断为肺出血的患儿,要求符合《儿童咯血诊断与治疗专家共识》相关肺出血诊断标准[1],年龄28 d~18岁,有血性液体经鼻腔、口腔流出或咳出、气管插管时可从导管中吸出泡沫样血性液体,所有参与本研究患儿的家属或监护人均已知情同意参与本研究,且病例信息完整;排除其他已知原因导致的出血,如鼻腔出血、口腔出血及气道肿瘤引起出血等。本研究获得医院伦理委员会批准(2023362)。
1.2 研究方法
1.2.1一般临床资料 收集84例肺出血患儿性别、年龄、病因(感染性疾病、血液系统疾病、心血管疾病等)、生命体征(心率、呼吸、血压等)及结局(死亡或生存)的资料。
1.2.2临床症状及体征 收集肺出血患儿出现的早期不典型症状(发热、咳嗽、喘息、呼吸困难及消化道出血等)或首发体征(肺部湿性啰音、肝大及脾大等)。
1.2.3实验室检查 记录最接近肺出血发生前的实验室指标,包括血液pH值及氧分压(partial pressure of oxygen,PaO2),血液 Na+、K+、肌酐(serum creatinine,Scr)、尿素氮(blood urea nitrogen,BUN)、白细胞(white blood cell,WBC)、红细胞(red blood cell,RBC)、血红蛋白(hemoglobin,HGB)、血小板(bloodplatelet,PLT)、降钙素原(procalcitonin,PCT)、白细胞介素6(interleukin 6,IL-6)及C反应蛋白(C-reactiveprotein,CRP)等实验室指标。
1.2.4影像学检查 收集肺出血患儿的肺部影像学检查结果,包括有无肺部渗出、胸腔积液、磨玻璃样密度影、气胸、支气管扩张、肺不张及肺实变等,并对肺叶累及范围进行分析。
1.2.5小儿危重症评分(pediatric critical illness score,PCIS) 参考中华儿科学会制定的《危重病儿评分表》[10]评估PICU患儿的病情程度,PCIS包括心率(heart rate,HR)、收缩压(systolic blood pressure,SBP)、呼吸频率(respiratory rate,RR)、PaO2,血液pH、Na+、K+、Scr、BUN、HGB及有无消化道出血等,以上各指标评分累加为PCIS总分,规定PCIS>80分、80~71分及<70分分别定义为非危重症、危重症及极危重症。
1.2.6并发症 收集肺出血患儿住院期间发生的并发症,包括休克、心力衰竭、呼吸衰竭、MODS、DIC、急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)等。
1.2.7呼吸机治疗信息 收集呼吸机治疗患儿的有创呼吸机参数呼气末正压(positive end-expiratory pressure,PEEP)。
1.3 统计学分析
采用SPSS 26.0软件进行统计分析,计量资料用中位数(四分位数间距)[M(P25,P75)]描述,予Mann-WhitneyU检验;计数资料以n(%)表示,予χ2检验、校正χ2检验、Fisher精确检验;影响因素采用多因素logistic回归进行分析,P<0.05认为差异有统计学意义。
2 结果
2.1 一般临床资料
入住PICU肺出血患儿中,生存28例(33.3%)、死亡56例(66.7%),年龄1~13岁、中位年龄5岁,男52例(61.9%)、女32例(38.1%);患儿早期以某项症状或体征首发起病,发热29例(34.5%)、咳嗽19例(22.6%)、喘息48例(33.2%)、呼吸困难26例(30.9%)、消化道出血28例(33.3%)、肺部湿性啰音51例(60.7%)、肝大52例(61.9%)及脾大42例(50.0%),病因构成见表1。
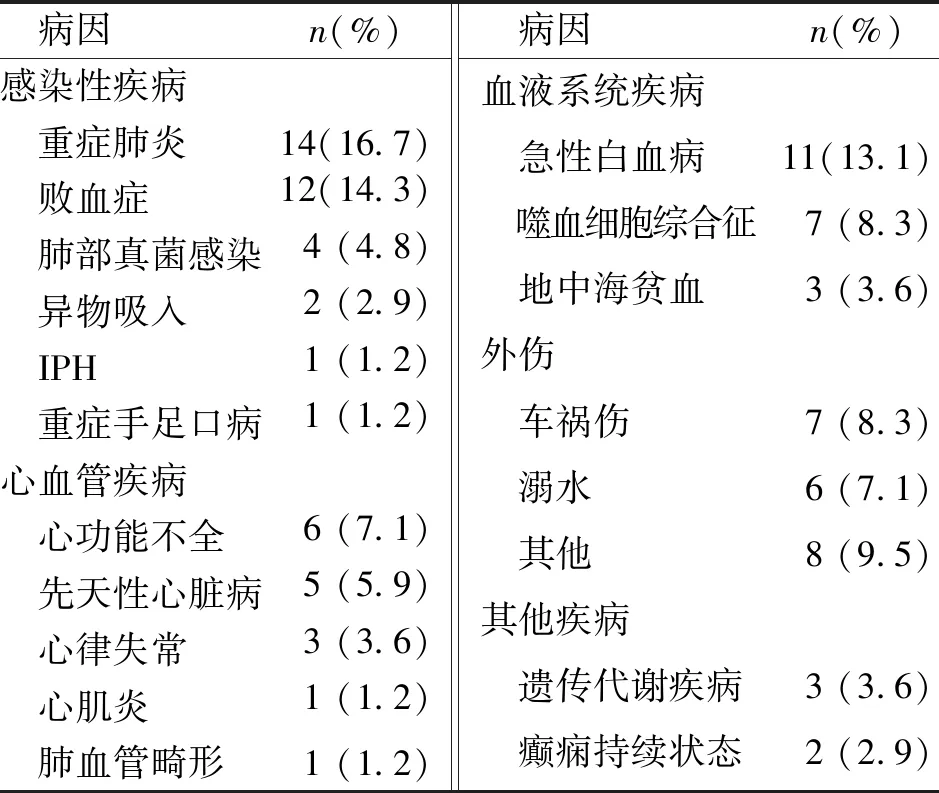
表1 PICU肺出血患儿的病因构成
2.2 肺出血患儿死亡的单因素分析
84例肺出血患儿中发生死亡56例,病死率为66.7%;单因素分析结果显示,死亡组患儿并发休克比例高于生存组,PCIS及PaO2,血液Na+、HGB、PLT水平均低于生存组,但其余指标比较、差异均无统计学意义(P>0.05)。见表2。
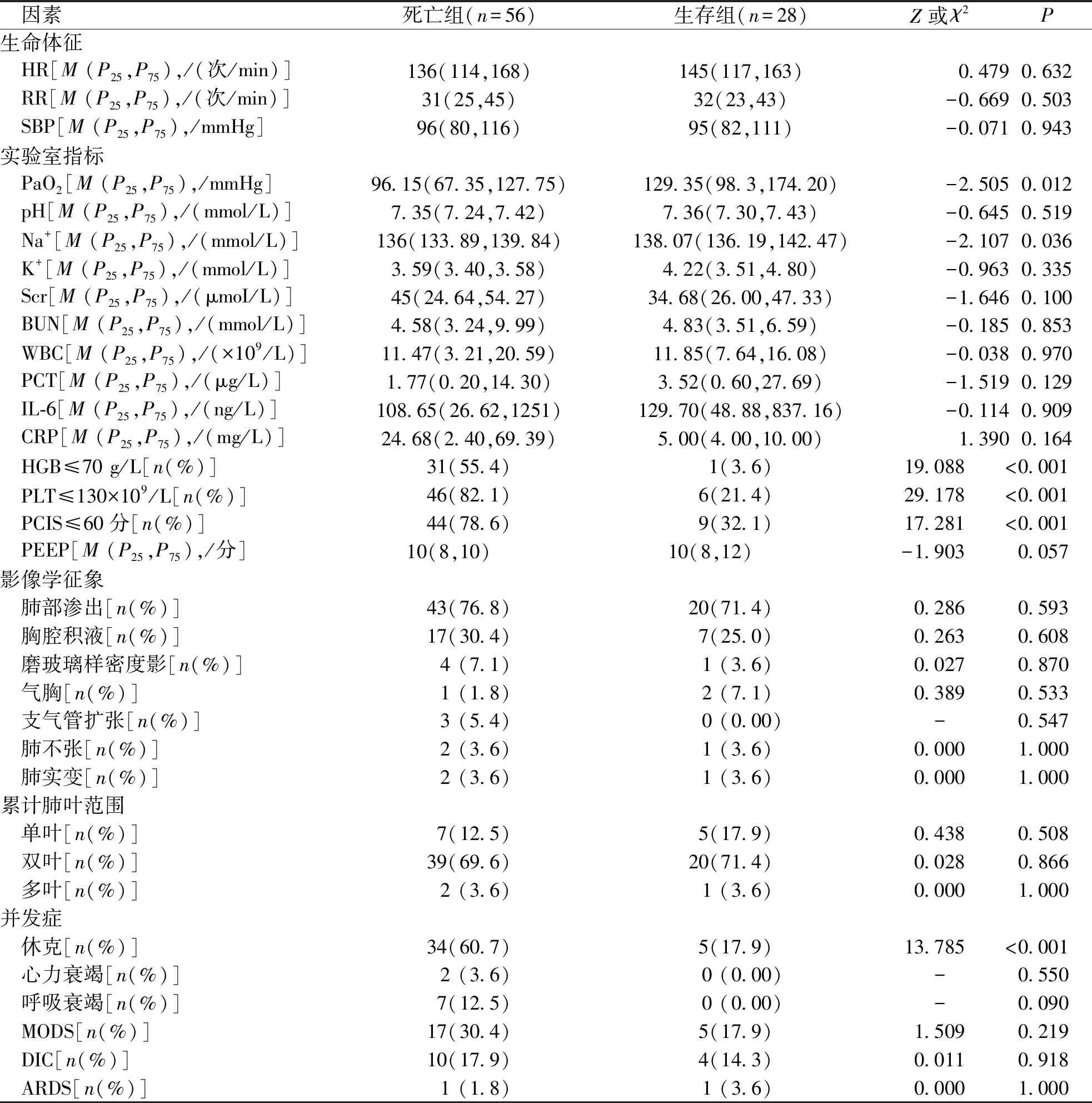
表2 PICU肺出血患儿发生死亡的单因素分析
2.3 肺出血患儿死亡的多因素logistic回归分析
多因素logistic回归分析结果显示,肺出血患儿并发休克(OR=6.381,95%CI为1.274~31.948)、HGB≤70 g/L(OR=29.584,95%CI为2.603~336.233)、PLT≤130×109/L(OR=10.461,95%CI为2.217~49.367)、PCIS≤60分(OR=6.181,95%CI为1.308~29.210)是PICU肺出血患儿死亡的影响因素。见表3。
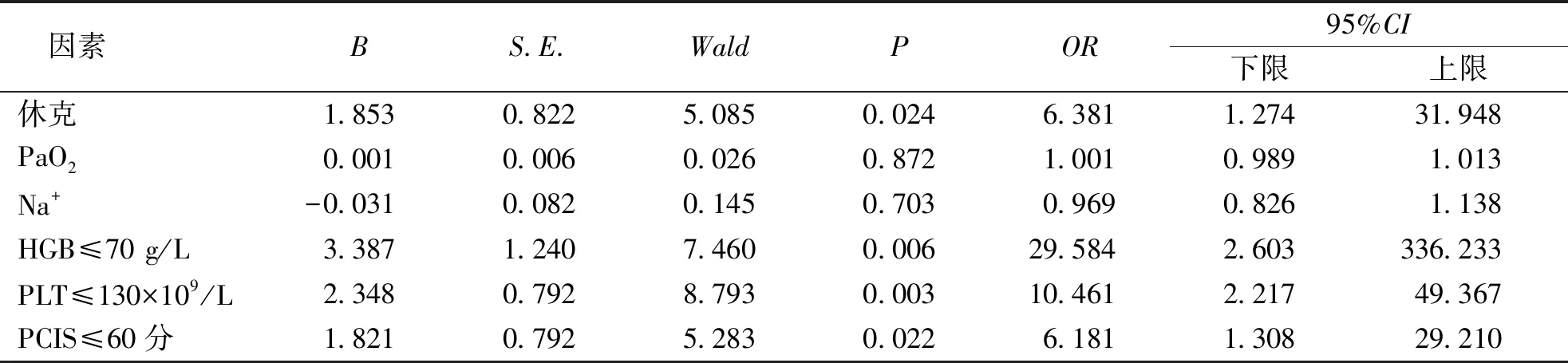
表3 PICU肺出血患儿发生死亡的多因素logistic回归分析
3 讨论
本研究肺出血患者确诊年龄为1~13岁,中位年龄5岁,男女比例差距不大,这与Siu等[11]、De等[12]研究类似,即肺出血好发于5岁以下儿童,且发病率在性别上无明显差异。肺出血可建立在各种原发疾病基础上,不同病因可共存,缺氧、酸中毒、DIC及心力衰竭是新生儿发生肺出血最常见的危险因素,非新生儿期儿童肺出血病因的相关研究报道较少,本研究分析了非新生儿期肺出血患儿的病因,以感染性疾病最常见,主要为肺部感染,这与近年的回顾性研究结论一致[13]。值得注意的是,本中心救治了1例重症手足口病合并肺出血患儿,近年已有多例报道肠道病毒71型感染手足口病,其中有病例以肺出血首发但全程无手足口病表现[14-15];张交生等[8]研究结果显示肺出血患儿原发疾病前3位中血液系统疾病占2位(急性白血病和噬血细胞综合征),本研究结果与该研究结果类似。相关研究显示,白血病患儿常合并导致肺出血的高危因素,如高白细胞状态、化疗药物使用、严重感染、免疫功能缺陷、血小板减少等,肺浸润发生率为29%~62%,病死率高达50%[16]。另外,本研究中重型地中海贫血患儿行骨髓移植后可并发肺出血致死亡,这与相关报道骨髓移植后因血小板降低致肺出血发生病例类似[17];本研究中心血管疾病主要有先天性心脏病及心功能不全,先天性心脏病包括室间隔缺损、动脉导管未闭及法洛四联症等,这与Welsh等[18]、冯丽梅等[19]研究类似。本研究还收录了1例肉碱缺乏症患儿,染色体遗传病可能会导致肺出血水肿。
肺出血患儿早期临床表现不明显,临床症状缺乏特异性,De等[20]研究指出可有1/3患儿未出现咯血表现,只是以不典型临床症状及体征首发,本研究中患儿病初可出现发热、咳嗽、喘息、呼吸困难、消化道出血等临床症状,体征上多出现肺部湿性啰音、肝脾肿大,早期直接出现咯血例数很少,大部分患儿均为住院期间发生肺出血甚至大咯血,这与文献所示疾病初期隐匿,临床表现缺乏诊断价值相符。生化指标对于判断疾病进展极为重要,严重感染可导致WBC、CRP、PCT、IL-6等升高,PLT下降[21-22],本研究结合PCSI,选取肺出血发生前最近的实验室数据,结果显示本研究肺出血患儿发生肺出血前血红蛋白和血小板越低,更容易发生死亡,与王维、代佳佳等[23-24]研究结果类似。肺出血患儿的肺部影像多表现为肺泡弥漫性、充填性、融合性实变影,可因出血期不同而表现不同[25],反映了疾病不断发展变化的过程,本研究肺出血患儿可合并多种影像学征象出现,以肺部渗出最常见,累及多个肺叶,典型磨玻璃样密度影征象较少,这与文献所述疾病早期缺乏特异性影像学征象相符[26],此外,近年超声诊断在儿童肺出血,特别是新生儿领域得到了广泛应用,一项多中心回顾性研究也应用了这项技术[27]。
肺出血出血量大时可出现各种并发症,新生儿领域的相关回顾性研究显示休克、DIC、心衰等并发症是新生儿肺出血死亡的独立危险因素,休克病死率高达50%,非新生儿儿童研究较少,Fan等[28]研究提示休克是肺出血的危险因素,可损伤局部血管的完整性,本研究对本中心肺出血患儿并发症进行了分析,可合并不同并发症,休克最常见,其次是MODS、DIC,并发休克时的死亡率更高,这与文献相似,近年的回顾性研究也显示休克是肺出血患儿死亡的独立危险因素[29],及时评估病情,积极纠正休克对于肺出血患儿住院期间的结局极为关键。另一项极为重要的治疗措施就是预防窒息,呼气末正压机械通气可使引起肺出血的塌陷闭合肺泡重新膨胀,增加肺部功能残气量,纠正缺氧。本研究中患儿大多采取呼吸机治疗,选择呼吸机PEEP值8~12 cmH2O,发现生存组大多选择较高PEEP值,这与相关研究相符[25],强调初设PEEP不宜过低,不仅促进氧合,还可增加肺泡内压力,同时起到压迫止血作用,更好促进出血性肺水肿的吸收。
本中心肺出血患儿治疗无效死亡56例(病死率66.7%),接近目前国内外病死率50%[4,8],分析发现重症监护室肺出血患儿合并休克、HGB≤70 g/L、PLT≤130×109/L、PCIS≤60分是死亡的相关因素,可提供预警参考,PCIS需结合实验室指标进行,可以在肺出血发生前、病情隐匿时,评价疾病综合状态,但因应用的普适性,目前国内研究较少,新生儿领域应用新生儿危重症评分对结局进行预测较多[30],近年国内外重症监护室也在使用APACHEII评分系统对各疾病初期进行评分[31-32]。
