褪黑素片中两种功效成分含量测定方法学研究
2023-06-19李军波欧阳浩栩郭丹李雪峰郁晓艺
李军波,欧阳浩栩,郭丹,李雪峰,郁晓艺
完美(广东)日用品有限公司(中山 528451)
褪黑素是人类和哺乳动物的脑松果体分泌的神经胺类激素之一,具有改善睡眠质量、克服睡眠障碍的功效[1]。近年来,随着对褪黑素研究的不断探索,褪黑素功能的多样性[2-3]和与其他物质的协同作用被逐渐发现[4-6],如小剂量褪黑素在维生素B6的参与下,改善睡眠的作用更佳[7-8]。维生素B6又称吡哆醇,是一种水溶性维生素,为氨基酸、糖及脂类代谢的辅酶[9]。在市场上诸多保健品公司研发了丰富的褪黑素和维生素B6复配产品[10-11]。
对保健品中褪黑素和维生素B6的含量测定中,GB/T 5009.197[12]《保健食品中褪黑素含量的测定》和GB/T 5009.170[13]《保健食品中硫酸硫胺素、盐酸吡哆醇、盐酸、烟酰胺和咖啡因的测定》只能分别检测褪黑素和维生素B6(以吡哆醇计),但GB/T 5009.197[12]与GB/T 5009.170[13]测试范围及方法相近,即均适用于保健食品,均用醇类试剂超声提取,液相色谱紫外测定。现有已报道研究中缺乏对褪黑素片产品中褪黑素和维生素B6检测的方法的全面研究,为提高检测效率,此研究拟参考GB/T 5009.170[13]和GB/T 5009.197[12]的前处理方法,提取褪黑素和维生素B6进行试验研究,建立可同步检测褪黑素和维生素B6的方法,对建立的方法进行全面的方法学研究,同时参考CNAS-GL006:2019《化学分析中不确定度的评估指南》[14]、JJF 1135——2005《化学分析测量不确定度评定》[15]和JJF 1059.1——2012《测量不确定度评定与表示》[16]对建立的方法进行不确定度评价。
1 材料与方法
1.1 主要材料与试剂
≥99.5%褪黑素(中国计量科学研究);100%盐酸吡哆醇(美国Sigma-Aldrich公司);磷酸、无水甲醇、无水乙醇(国药集团化学试剂有限公司);乙腈(色谱纯,德国默克公司);1-癸烷磺酸钠(上海安谱公司)。
1.2 主要仪器与设备
1260高效液相色谱仪(美国Agilent公司),配有可变波长紫外检测器和Openlab色谱工作站;ML204和ML205电子天平(瑞士METTLER TOLEDO公司);Elma P180H超声波清洗器(德国JULABO公司);Milli-Q去离子水发生器(美国Millipore公司)。
1.3 方法
1.3.1 色谱条件
色谱柱:TSK C18色谱柱(4.6 mm×150 mm,5μm);流动相:1-癸烷磺酸钠(1.22 g→850 mL)+乙腈+磷酸=850+150+1;流动相流速:1.0 mL/min;检测波长:褪黑素222 nm,维生素B6280 nm;进样量:10 μL;柱温:30 ℃。
1.3.2 标准曲线绘制
精密称取15.44 mg维生素B6(以吡哆醇计)对照品于50 mL容量瓶中,加20 mL水溶解并定容至刻度,摇匀,得254.0 μg/mL的吡哆醇对照品储备液,备用。精密称取12.95 mg褪黑素对照品于50 mL容量瓶中,加20 mL体积分数为70%乙醇溶解并定容至刻度,摇匀,得257.7 μg/mL的对照品储备液,备用。分别精密吸取10 mL对照品储备液维生素B6和10 mL对照品储备液褪黑素,再加入甲醇+水+磷酸=100+400+0.5混合溶液,定容至25 mL,摇匀。分别取0.25,0.5,1,2,3.5和5 mL混合对照品溶液于10 mL容量瓶中,用甲醇+水+磷酸=100+400+0.5定容至刻度线,即得系列标准溶液。按照1.3.1小节色谱条件上机测定即为对照品标准曲线。
1.3.3 样品提取方法
取10片褪黑素片,研细,精密称定0.5 g(精确至
0.000 1 g),置100 mL量瓶中,加入约80 mL体积分数为70%乙醇溶液超声提取25 min,每隔5 min振摇1次,冷却至室温,加入体积分数为70%乙醇溶液定容至刻度,摇匀。取5 mL提取液,用水定容至10 mL得稀释液。取稀释液过0.45 μm滤膜,取续滤液,即得。
1.3.4 不确定度评定数学模型建立方法
试验的测量模型按式(1)计算。
式中:X为试样中褪黑素或维生素B6的含量,mg/g;c为标准测定液中褪黑素或维生素B6的质量浓度,μg/mL;V为试样的定容体积,mL;f为折算系数,维生素B6以吡哆醇计算折算系数为0.823,褪黑素折算系数为1;m为试样的称样质量,g。
2 结果与分析
2.1 样品制备方法优化
2.1.1 提取溶剂的优化
现有国标GB/T 5009.197[12]和GB/T 5009.170[13]可分别测定褪黑素和维生素B6,故此方法参考现有国标GB/T 5009.197[12]和GB/T 5009.170[13],分别使用体积分数为70%乙醇和甲醇+水+磷酸=100+400+0.5提取褪黑素片中的两种功效成分。选用体积分数为70%乙醇同步提取褪黑素片中褪黑素和维生素B6时,维生素B6色谱峰存在峰分叉的情况如图1所示。通过调节样品进样量和更换不同型号色谱柱仍无法解决维生素B6色谱峰存在峰分叉的问题。当将提取液用水稀释一倍后维生素B6的分叉峰消失,如图1所示。为进一步验证,维生素B6的分叉峰原因,将维生素B6的标样用体积分数为70%和35%的乙醇分别溶解定容后上机测试,测试结果如图2所示。

图1 两种上机溶液的色谱图
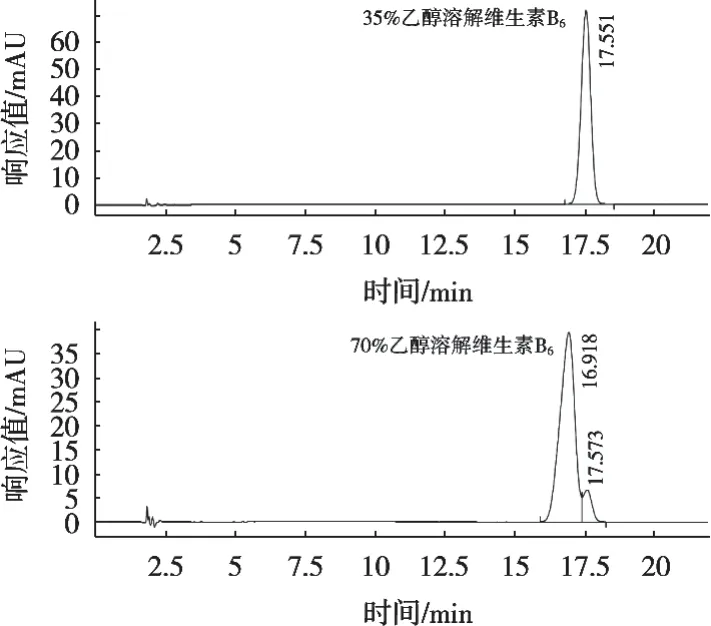
图2 两种溶剂溶解维生素B6的上机色谱图

图3 空白对照与样品色谱图比较
由图1和图2可知,维生素B6的分叉峰消失,可能是维生素B6在体积分数为70%乙醇溶剂中存在溶剂效应,导致色谱峰分叉,该结论与刘丽艳等[17]的研究结论一致。故选择体积分数为70%的乙醇提取褪黑素片中两种功效成分,提取时间为25 min,取提取液5 mL,用水定容至10 mL后,取稀释液过滤后上机测试(前处理方式A)。将该测试结果与使用甲醇+水+磷酸=100+400+0.5提取(前处理方式B),上机测试比对结果进行比对,筛选最佳提取溶剂,比对结果如表1所示。

表1 两种提取方式的结果对比 单位:mg/g
由表1可知,两种前处理方式对维生素B6的提取后含量测定相对偏差为0.4%,无明显差异。而选用甲醇+水+磷酸=100+400+0.5提取,检测结果较体积分数为70%乙醇提取偏低6.9%。体积分数为70%的乙醇提取褪黑素效果更佳,故选取体积分数为70%乙醇提取样品后用水稀释一倍后上机测试,下一步试验按此条件开展试验。
2.1.2 提取时间优化
取同一批褪黑素片样品,分别提取10,25和40 min制成供试品溶液,注入高效液相色谱仪,计算褪黑素与维生素B6含量,结果见表2。由表2可知,25 min条件下提取褪黑素和维生素B6测定含量最高,提取最充分。故选取25 min为方法验证的最终提取时间。

表2 不同提取时间的结果对比 单位:mg/g
2.2 方法性能研究结果
2.2.1 系统适用性结果
用色谱数据处理软件计算褪黑素和维生素B6色谱峰的系统适用性。褪黑素和维生素B6的分离塔板数分别为7 326和13 231均大于5 000,分离度为4.32大于1.5,表明此方法的系统适用性良好。
2.2.2 专属性考察结果
方法专属性对照色谱图如3所示。空白对照溶液色谱图中未见与供试品溶液、对照品溶液色谱图中褪黑素和维生素B6相同保留时间的色谱峰,证明阴性无干扰。
2.2.3 线性范围与定量限结果
按照1.3.1小节条件进行测试,确定各成分的线性范围(如表3所示)。由表3可知,所得褪黑素片中两种成分的标准曲线相关系数满足R>0.999,两种成分在各自范围内均线性良好。各成分的线性范围均为:褪黑素2.54~50.81 μg/mL,维生素B62.55~50.06 μg/mL,按rSN=10确定各成分的定量限,褪黑素0.05 μg/mL,维生素B60.05 μg/mL。

表3 2种成分的标准曲线、线性范围及定量限情况
2.2.4 准确度结果
通过对样品的加标回收试验考察此方法的准确度,取适量微晶纤维素粉末,加入适量的混合对照品,混合均匀制备成片剂。取20片制备好的加标样品,按照最优提取,重复制备7份样品,参考最优的色谱条件进样分析,计算各对照品的加标回收率。各对照品的加标回收率在95%~105%直径,满足GB/T 27417——2017[18]《合格评定化学分析方法确认和验证指南》的要求,表明该方法的准确度高,检测结果准确。具体数据详见表4。
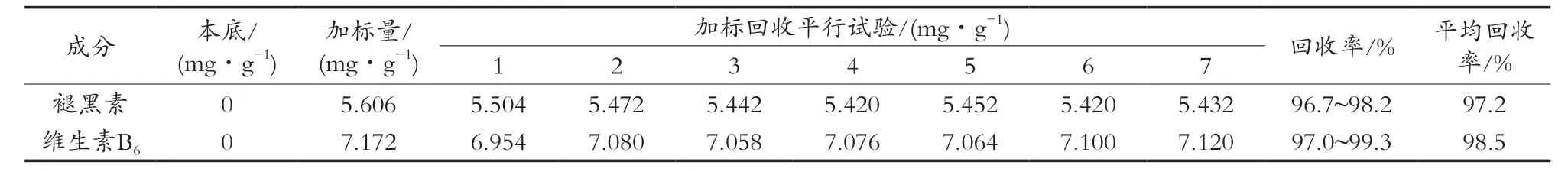
表4 加标回收试验结果
2.2.5 精密度结果
通过对同一批次样品,按照最优提取,重复制备10份样品,参考最优色谱条件进样分析,通过标准曲线分别计算2种功效成分的SRSD(n=10),SRSD值均小于5%,表明该方法的重复性好,精密度高。具体数据详见表5。
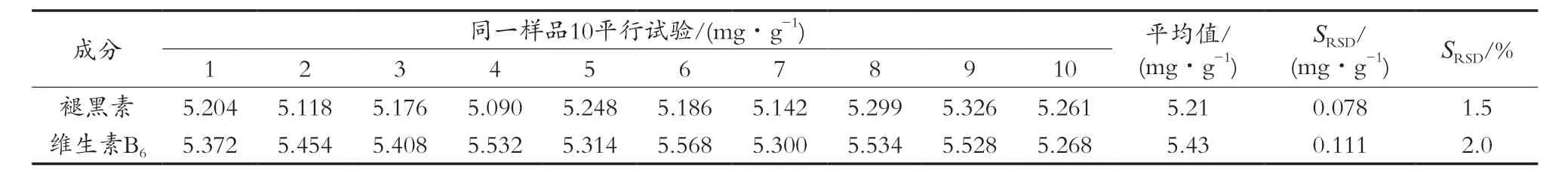
表5 精密度试验结果
中间精密度考察,选取褪黑素片,由试验员A和B分别独立开展6次平行试验,测定褪黑素和维生素B6含量,中间精密度结果如表6所示。由表6可知,该方法测定的褪黑素和维生素B6中间精密度符合方法验证要求。

表6 中间精密度结果
2.2.6 耐用性结果
因此方法在2.1小节中已对前处理方法进行了考察,故此耐用性试验仅针对仪器的色谱条件进行考察。取褪黑素片样品,按1.3.3小节配制成供试品溶液,参考1.3.1小节的色谱条件,分别设置2,5和10 μL进样量,设置25,30和35 ℃柱温条件上机测定,考察此方法的仪器参数耐用性。检测数据详见表7。由表7可知,不同色谱条件下褪黑素和维生素B6测定结果SRSD均小于5%,故此方法具有较好的耐用性。

表7 不同进样量和色谱条件下褪黑素和维生素B6测定结果
2.3 不确定度评定结果
由1.3.4小节不确定度评定数学模型可知,褪黑素和维生素B6的不确定度主要由标准物质、样品前处理过程、重复测定、回收率及液相色谱仪引入。根据建立的模型,采用合成相对标准不确定度按式(2)计算。
式中:urel(x)为合成相对标准不确定度;ur(x1)为由标准物质引入的相对标准不确定度;ur(x2)为由样品提取引入的相对标准不确定度;ur(x3)为由人员操作引入的相对标准不确定度;ur(x4)为由回收率引入的相对标准不确定度;ur(x5)为高效液相色谱仪引起的标准不确定度。
2.3.1 标准物质引入的标准不确定度
褪黑素和维生素B6标准物质的不确定度来源主要是标准溶液配制过程中使用的标准物质、容量瓶、吸量管、天平引入的不确定度。
褪黑素和维生素B6标准品纯度分别为P(m)=99.6%和P(v)=100%,扩展不确定度均为2.0%,按矩形分布,褪黑素和维生素B6纯度带来的不确定度分量按式(3)和(4)计算。
所用天平为十万分之一电子天平,称取12.95 mg褪黑素,15.44 mg维生素B6,该天平经检定合格,校准证书标明扩展不确定度为0.03 mg,k=2,称量时需要去皮,则产生两次称量,其相对标准不确定度按式(5)和(6)计算。
标准溶液配制稀释过程中由容量瓶引入的不确定度,使用50.00 mL和25.00 mL容量瓶各一次,10.00 mL容量瓶6次,根据计量证书所示,50.00,25.00和10.00 mL容量瓶的示值误差不确定度U50=0.02 mL、k=2,U25=0.01 mL、k=2,U10=0.007 mL、k=2,则相对不确定度按式(7)计算。
标准溶液配制稀释过程中使用吸量管1,5和10 mL,根据计量证书所示,1,5和10 mL吸量管的示值误差不确定度分别为:Ux1=0.003 mL、k=2;Ux5=0.01 mL、k=2;Ux10=0.02 mL、k=2。标准母液使用10 mL吸量管2次,工作液有6个点,配制过程中1 mL吸量管使用了3次,吸取体积分别为0.25,0.5,1和5 mL的吸量管使用了3次,吸取体积分别为2,3.5和5 mL,则相对不确定度按式(8)计算。
溶液温度与校准温度不同产生的相对标准不确定度由于此实验室温度在(20±5)℃波动,液体的体积膨胀明显大于容量瓶的体积膨胀,故只考虑前者即可。所使用的容量瓶体积为50 mL,参考甲醇的体积膨胀系数为1.18×10-3℃,按矩形分布,则因温度波动引入的液体体积的相对不确定度为按式(9)计算。
因实验室温度波动范围一致,故后续对温度引起体积变化的不确定将引用此处评估的相对不确定度。综上,标准物质引入的相对标准不确定度按式(10)(11)计算。
2.3.2 样品前处理过程引入的不确定度
试样称量过程使用的万分天平,根据计量证书所示,天平的扩展不确定度U=0.000 5 g,k=2,称量的平均质量为0.512 5 g,称量时需要去皮,则产生两次称量,其引入的相对不确定度按式(12)计算。
试样定容过程中使用100.00 mL和10.00 mL容量瓶,根据计量证书所示,容量瓶的扩展不确定度U100=0.03 mL、k=2,U10=0.007 mL、k=2,定容体积为100.00 mL;引用2.3.1小节溶液温度与校准温度不同产生的相对标准不确定度为0.35%,则样品定容引入的相对不确定度按式(13)计算。
综上,样品前处理引入的相对标准不确定度按式(14)计算。
2.3.3 重复性引入的不确定度
重复测量10次,结果详见2.2.4小节表4,实际检测中测试结果为2次测量结果的平均值,引用表4中的相对标准偏差,则重复性引入的相对不确定度按式(15)和(16)计算。
2.3.4 回收率引入的相对标准不确定度
回收率测试7次,结果详见2.2.5小节表5,褪黑素和维生素B6的平均回收率分别为97.2%和98.5%,则回收率引入的相对不确定度按式(17)和(18)计算。
2.3.5 高效液相色谱仪引入的相对标准不确定度
由高效液相色谱仪的说明书可知,该仪器检测浓度的允许误差为1%,按均匀分布处理。则按式(19)计算。
2.3.6 褪黑素和维生素B6合成总相对不确定度
褪黑素和维生素B6合成总相对不确定度为按式(20)和(21)计算。
2.3.7 褪黑素和维生素B6扩展不确定度
此次试验取包含因子k=2,包含概率P=95%时,褪黑素和维生素B6的扩展不确定度分别为5.10%和4.68%,样品中褪黑素的含量表示为5.21±0.27 mg/g,k=2,维生素B6的含量表示为5.43±0.25 mg/g,k=2。
3 结论
研究表明,褪黑素片中褪黑素和维生素B6可实现同步测定提升日常检测效率。通过对此研究过程的试验数据分析,此方法具有较好的准确度和精密度。此方法不确定度的主要来源为人员操作及回收率引入的随机误差,标准品、天平、移液管、容量瓶、液相色谱仪带入的系统误差。比较相对不确定度分量发现,随机误差对结果影响较大,故检测过程中需要严格规范操作过程并遵守,系统误差中标准物质对结果影响较大,需尽可能选择不确定小的标准物质,同时使用偏差小的量器具和设备、控制实验室温度,提升检测结果的稳定性和可靠性。
