pN0期非小细胞肺癌VEGF、Ki-67、p53表达与淋巴结微转移的相关性
2023-06-15辛运超李彦明郝雁冰
魏 东,辛运超,刘 博,李彦明,郝雁冰
肺癌发病率以及死亡率位居恶性肿瘤的首位,且近年有逐年上升趋势[1]。非小细胞肺癌(non-small cell lung cancer,NSCLC)占肺癌病人的85%以上,虽然随着现代医疗诊治技术的发展,病人5年生存率有明显提高,但约有30%的Ⅰ、Ⅱ期NSCLC病人在肺癌根治术后早期即可出现肿瘤复发及转移,提示在病人区域淋巴结中可能存在肿瘤的微转移,而此类肿瘤微转移通过临床病理诊断难以发现,因此,寻求有效方式诊断病人淋巴结微转移,对于病人后续的治疗及预后改善具有重要临床意义[2-3]。目前对于病理诊断无转移的淋巴结(pN0)期病人,其微转移的诊断尚无公认依据,也无理想标志物进行判断[4-5]。本研究探讨分析pN0期NSCLC血管内皮生长因子(VEGF)、Ki-67、p53表达与淋巴结微转移的关系。现作报道。
1 资料与方法
1.1 临床资料 选择2017年3月至2019年12月在我院术后经常规病理检查证实为pN0期的NSCLC病人93例及手术治疗的非肺癌病人45例。NSCLC病人中男64例,女29例,年龄29~72岁;非肺癌病人中男31例,女14例,年龄25~69岁。2组病人性别、年龄均具有可比性。本研究经我院伦理委员会批准通过。
纳入标准:(1)NSCLC病人经影像学、组织学检查确诊为NSCLC,均接受根治性肺叶切除术;(2)非肺癌病人均在我院进行手术治疗;(3)NSCLC病人清扫至少包括3站纵隔淋巴结,总数不少于6枚。排除标准:(1)合并凝血功能障碍、严重肝肾功能障碍;(2)合并其他部位恶性肿瘤;(3)合并严重免疫系统疾病或感染;(4)全肺切术以及各种姑息性切除病人。
1.3 方法 NSCLC组织及正常肺组织均采用10%甲醛固定,石蜡包埋,常规HE染色,免疫组织化学采用SP法,微波抗原修复,使用PBS代替一抗作为阴性对照组,DAB显色。使用已知的VEGF、Ki-67及p53阳性切片作为阳性对照。VEGF、Ki-67以及p53单克隆抗体均购于福州迈新生物技术公司。
VEGF、Ki-67以及p53以细胞质或细胞膜染色呈棕黄色为阳性,切片染色后选取5个典型视野,由3名检验师分别根据染色深度以及阳性细胞百分比进行评分判断。阳性细胞百分率评分:0%(0分)、≥5%(1分)、≥25%(2分)、≥50%(3分)、≥75%(4分);染色深度评分:未染色(0分)、浅黄(1分)、棕黄(2分)、棕褐色(3分)。两种计分相乘,≤1分为阴性,≥2分为阳性。
淋巴结微转移判断:参照文献[6],使用免疫组织化学法测定病人淋巴结CK20、MUC1表达情况,阳性表达则为淋巴结微转移。
1.4 统计学方法 采用t检验、χ2检验和ROC曲线分析。
2 结果
2.1 NSCLC与正常肺组织VEGF、Ki-67、p53表达比较 NSCLC组织中VEGF、Ki-67和p53表达阳性率均明显高于正常肺组织(P<0.01)(见表1)。
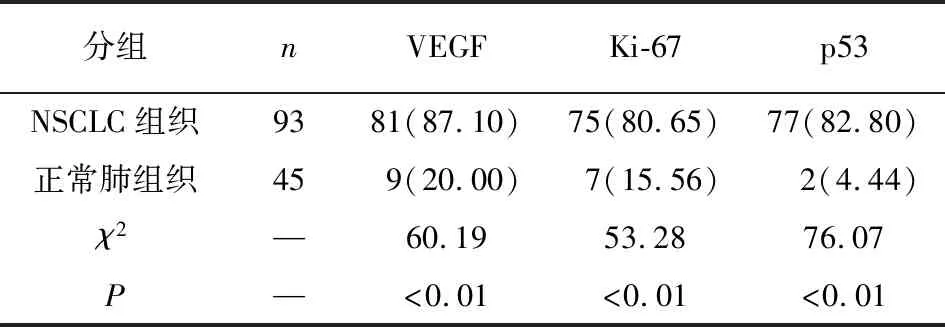
表1 NSCLC组织与正常肺组织VEGF、Ki-67、p53阳性率比较[n;百分率(%)]
2.2 不同特征NSCLC病人VEGF、Ki-67、p53表达比较 不同TNM分期的NSCLC病人VEGF、Ki-67、p53表达阳性率差异均有统计学意义(P<0.05),不同性别、年龄、病理类型、肿瘤最大径及吸烟史NSCLC病人的VEGF、Ki-67、p53表达阳性率差异均无统计学意义(P>0.05)(见表2)。
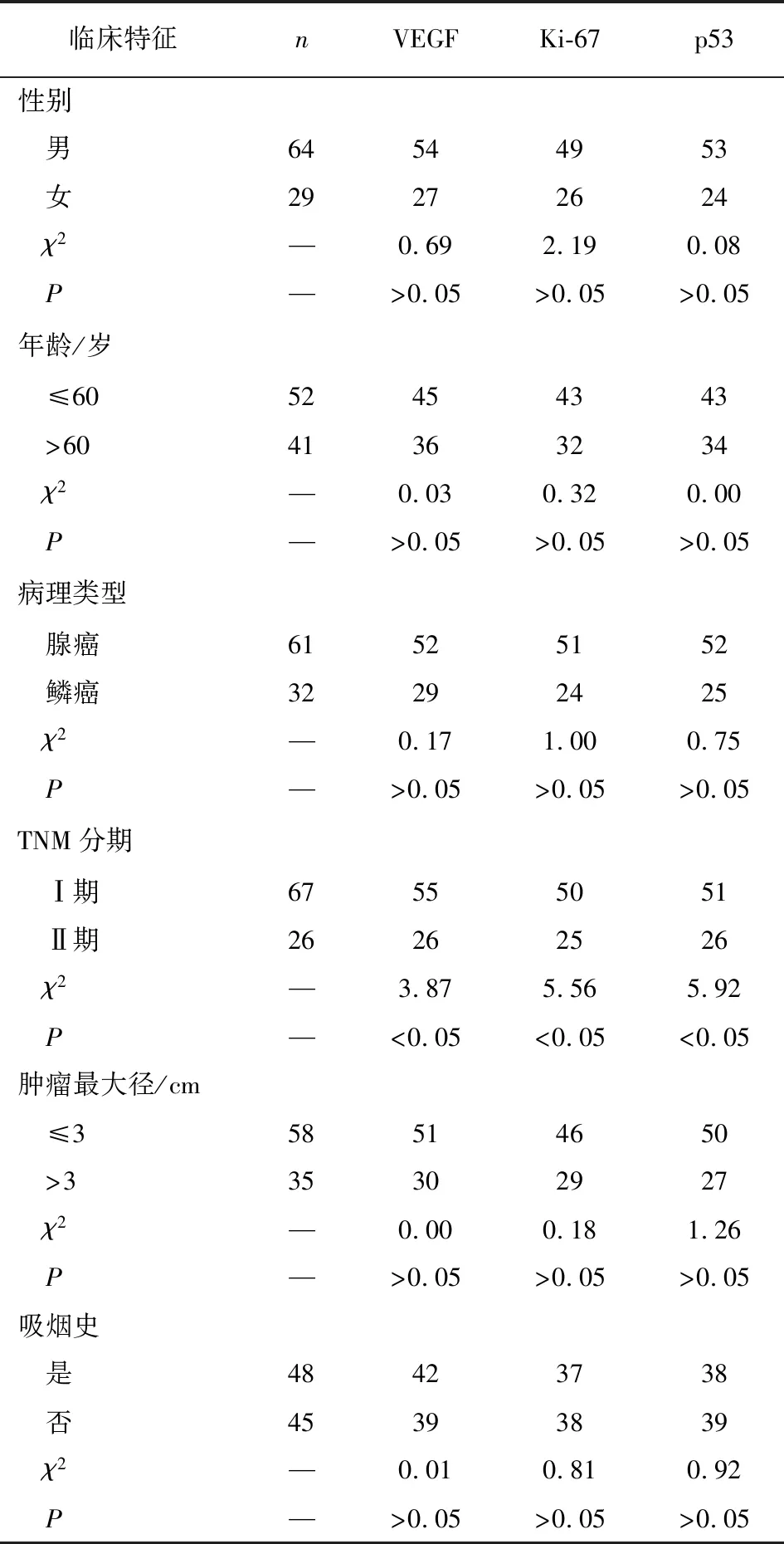
表2 不同特征NSCLC病人VEGF、Ki-67、p53表达比较(n)
2.3 有无淋巴结微转移NSCLC病人VEGF、Ki-67、p53表达比较 淋巴结微转移NSCLC病人VEGF、Ki-67、p53表达评分均明显高于无淋巴微转移病人(P<0.01)(见表3)。

表3 有无淋巴结微转移NSCLC病人VEGF、Ki-67、p53表达评分比较分)
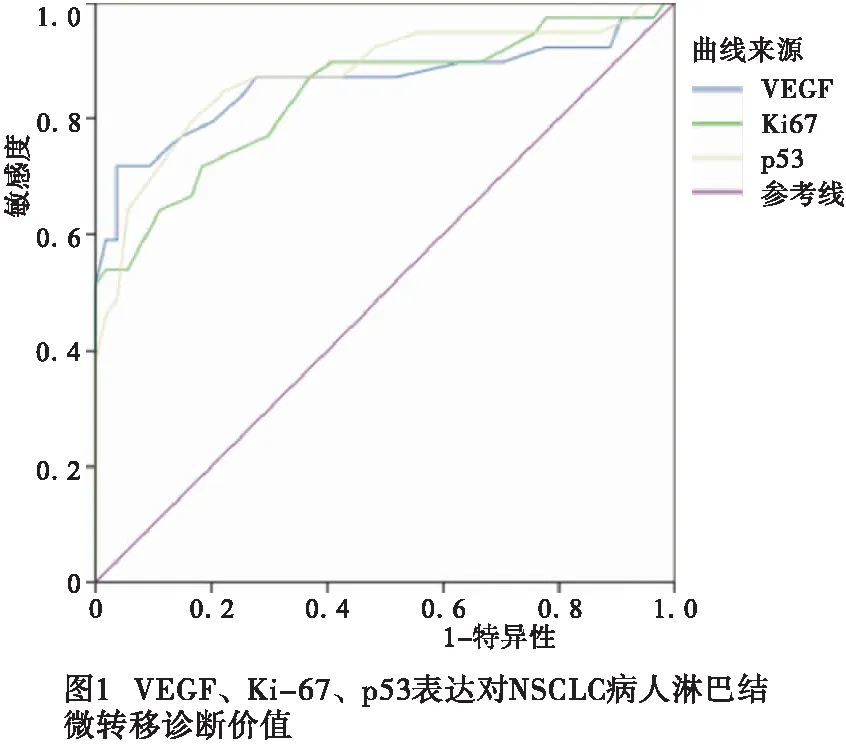
2.4 VEGF、Ki-67、p53评分对NSCLC病人淋巴结微转移诊断价值 ROC曲线分析结果显示,VEGF、Ki-67、p53评分对NSCLC病人淋巴结微转移诊断的AUC分别为0.816、0.877、0.821,有较好诊断价值(见图1)。
3 讨论
肺癌已经成为严重影响我国人民生命健康的重要疾病之一,在肺癌发病进程中,癌细胞转移是导致病人临床预后不良的重要因素,同时也是导致病人死亡的主要原因[7]。对于早中期病人而言,主要采取的治疗方式为肺癌根治性切除术联合淋巴结清扫,手术治疗为肺癌的治愈提供了可能[8]。但是在淋巴结转移病理学确诊之前,可能存在肿瘤转移部分基因的改变,学者推测此类基因的改变可能是淋巴结微转移出现的早期表现,因此检测异常表达基因或其相应的蛋白成为诊断肺癌病人淋巴结微转移的重要依据[9]。
肿瘤的生长以及转移依赖于肿瘤内新生血管的生成,而肿瘤血管的生成受促血管生成因子以及抗血管形成因子的双重调节作用[10]。VEGF是目前认为最直接的参与诱导肿瘤血管形成的相关因子之一,VEGF通过诱导内皮细胞内钙浓度的短暂升高等方式,从而影响内皮细胞基因的表达,加快基底膜的降解,从而发挥相应的促肿瘤血管生成作用[11];此外,VEGF可增加血管通透性,使血浆蛋白发生外渗,从而形成血管化纤维蛋白基质,为内皮细胞的迁移形成网架,而血管内物质的渗漏也为肿瘤的转移提供了基础条件[12]。Ki-67是目前认为最好的肿瘤增殖标志物之一,Ki-67的表达可在一定程度上反映肿瘤的恶性程度以及转移风险,研究[13-14]显示,Ki-67表达与VEGF密切相关,可能也是影响肿瘤血管生成的一个重要因子。p53作为一种肿瘤抑制基因,其基因的突变在肿瘤的发生发展中发挥重要作用[15]。目前p53基因分为野生型(wtp53)以及突变型(mtp53)2种,其中wtp53作为一种抑癌基因表达产物半衰期短且极不稳定,常规免疫组织化学方式难以检出,而mtp53蛋白半衰期长且稳定,容易被检出[16]。因此认为免疫组织化学测出的p53蛋白为突变型p53蛋白,是一种促癌基因的表达蛋白[17]。
本研究探讨分析pN0期NSCLC病人VEGF、Ki-67、p53表达与淋巴结微转移关系,研究结果显示,肺癌组织中VEGF、Ki-67以及p53表达阳性率均明显高于正常肺组织,同时不同TNM分期病人的NSCLC组织中VEGF、Ki-67、p53表达阳性率差异均有统计学意义。与相关研究[18-19]结果一致,提示肺癌组织中可出现VEGF、Ki-67以及p53的异常高表达状态,并且此类肿瘤标志物的表达与病人临床分期具有密切联系,VEGF、Ki-67和p53在NSCLC的发生、发展中具有重要影响作用。此外,本研究对比分析VEGF、Ki-67以及p53表达情况与pN0期病人淋巴结微转移的关系,结果显示,淋巴结微转移NSCLC病人肺组织中VEGF、Ki-67、p53表达评分均明显高于无淋巴微转移病人;ROC曲线分析结果显示,VEGF、Ki-67、p53表达评分对NSCLC病人淋巴结微转移诊断AUC分别为0.816、0.877、0.821。提示VEGF、Ki-67、p53表达与pN0期病人淋巴结微转移有关,并且VEGF、Ki-67、p53表达对pN0期病人淋巴结微转移具有良好诊断价值,可作为临床监测的潜在指标[20]。
综上,pN0期NSCLC病人肺组织VEGF、Ki-67及p53表达与肺癌的发生发展密切相关,且与病人淋巴结微转移有关,可作为病人淋巴结微转移的潜在检测指标。但由于本研究纳入样本量较小,且免疫组织化学评分存在一定的主观性,后续还需进一步扩大样本量,且寻求更为客观的临床检测方式,以提高对病人淋巴结微转移的诊断,改善病人临床预后。
