冲洗液对标准牙根根管内粪肠球菌和白念珠菌混合感染的抗微生物作用比较
2023-06-13张琴琴史般若吴翘楚
吕 盈,徐 瑞,张琴琴,史般若,吴翘楚,魏 昕
微生物感染是牙髓根尖周病的主要病因,当牙体的硬组织受到破坏,例如龋坏、外伤、隐裂等,细菌侵入髓腔和根管并定植,混合菌丛存留于根管内,引起牙髓根尖区的感染和炎症[1]。粪肠球菌是一种革兰氏阳性厌氧球菌,起源于人类的口腔和胃肠道,可以在90%根管治疗后疼痛和继发感染的根管内检出[2]。白念珠菌在21%牙髓原发性感染的根管中被分离出[3],具有良好的环境适应性和强大的毒力特性[4]。在有氧的条件下培养,白念珠菌形成的生物膜提供了低氧微环境,有利于兼性厌氧菌粪肠球菌的生长[5]。鉴于白念珠菌和粪肠球菌在根管内难于彻底去除,混合存在更容易引起顽固性、持续性、反复性感染,增加了根管治疗的失败率并导致根管再治疗的预后风险[6]。对粪肠球菌和白念珠菌两者混合感染的抗微生物研究,有助于克服混合感染所引起的顽固性根尖周病变。目前,对粪肠球菌和白念珠菌两者混合感染根管的研究国内外较少,有待进一步研究。
根管治疗通过机械和化学预备有效地清除根管内的感染物质,之后,通过根管充填和冠部封闭,隔绝微生物,保证了根管治疗的预后效果[1]。化学冲洗作为根管治疗一个重要步骤,采用有效的根管内化学冲洗,可以清除根管内多种微生物,将根管内的感染降至最低。近年来临床常用的冲洗药物有不同浓度的NaClO、0.2%~2.0% CHX等[7]。其中NaClO具有优异的抗菌性能和有机组织溶解能力[8]。CHX具有非常广泛的抗菌谱,对革兰氏阳性菌具有很强的抗菌性,也对酵母菌,某些皮肤藓菌和亲脂类病毒具有活性[9]。NaClO和CHX对标准牙根内的混合感染的抗微生物效果国内外均未见报道,有待进一步研究。
本部分实验分别采用2.5% NaClO、2% CHX溶液和生理盐水作为冲洗液进行根管消毒,评估冲洗液对根管内粪肠球菌和白念珠菌混合感染微生物的清除效果,为牙髓根尖周病的治疗中化学冲洗的选择提供一定的实验依据及临床指导。
1 材料与方法
1.1 试剂和仪器
白念珠菌标准株(SC5314)由上海第二军医大学药学院遗传工程国家重点实验室馈赠。粪肠球菌(ATCC29212)由江苏省口腔疾病研究重点实验室提供。3% NaClO、2% CHX溶液(朗力,中国);3% Tween 80、10%硫代硫酸钠(Sigma,美国);沙堡琼脂培养基(SDA,6.3 g/100 mL);YPD培养液(2%葡萄糖,1%胰蛋白胨,1%酵母提取物);脑心浸脑液肉汤培养基(BHI,OXOID,英国);磷酸盐缓冲液(PBS,诺唯赞,中国);细菌细胞活性测定试剂盒(LIVE/DEAD BacLight Bacterial Viability Kit,Life technologies,美国);2.5%戊二醛固定液(Leagene,中国);YCP系列二氧化碳培养箱(易亮医疗器械有限公司,中国);激光共聚焦扫描显微镜(CLSM, LSM 710,Carl Zeiss,德国);低速精密切割机(Isomet,美国);K锉(Dentsply,美国);NaviTip 30-G needle(Ultradent Products,美国);无菌胰岛素注射器(BD,上海);ProTaper NEXT(DentsplyMaillefer,瑞士);机用马达(VDW,Dentsply,美国);粘结剂(G-aenial Bond,GC,日本);复合树脂(G-aenial,GC,日本)。
1.2 实验方法
1.2.1 离体牙的收集、处理 经南京医科大学附属口腔医院伦理委员会批准(PJ2018-026-001),于2018年10月—2019年5月在南京医科大学附属口腔医院共收集46颗成年人因正畸治疗需要而拔除的单根下颌前磨牙。去除结石和软组织,置于生理盐水中,4 ℃冰箱内保存。纳入标准:①直单根、根尖发育完全;②牙科显微镜下牙齿未见折裂痕;③无充填物或修复体、未接受牙髓治疗;④无牙髓或根尖周病、无牙髓钙化、无发育异常或颌骨相关疾病。
1.2.2 标准牙根模型的制备 去除牙根面的软组织及牙结石,低速切割机于釉牙骨质界下截除冠部,标准化牙根长度为15 mm[10],#15 K锉疏通根管至根尖孔可见,此时的根长减去1 mm即为工作长度。使用ProTaper NEXT预备根管至F3[11],每次换锉,使用1 mL生理盐水冲洗根管[12]。为了去除玷污层,预备结束后使用2 mL 17% EDTA冲洗根管,并将牙根放入17% EDTA溶液中超声荡洗3 min。将标准化牙根依次分别使用无菌水、2.5% NaClO、10%硫代硫酸钠超声荡洗3 min,最后用生理盐水荡洗3 min[13]。干燥根管,流动树脂封闭根尖孔,粘结剂封闭牙根表面[13],防止微生物从根尖孔或根管侧支进入根管内。将所有牙根浸没在BHI液体培养基中,10 000 r/min,离心2 min[13],使得培养基浸入根管内不规则区域,排空多余气体,121 ℃高温高压灭菌20 min备用。消毒完成后牙根取样,置于盛有BHI培养基的试管中培养48 h,若培养基透明,证明灭菌效果可靠,可进行下一步实验;若培养基出现浑浊,说明灭菌效果不可靠,需重新进行高压灭菌。
1.2.3 标准感染牙根模型的制备 取粪肠球菌单克隆菌株于BHI液体培养基中,37 ℃,180 r/min摇床生长3~5 h至对数生长期;收集BHI液体培养基中对数生长状态的细菌,16 000×g离心5 min,无菌PBS洗涤2次,细菌重悬于RPMI 1640培养液中,麦氏比浊仪计数,制备成密度为1 McFarland的标准菌悬液。取白念珠菌单克隆菌株于YPD培养基中,30 ℃,200 r/min摇床过夜达到对数生长期;收集YPD培养液中对数生长状态的真菌,2 100×g离心10 min,无菌PBS洗涤2次,真菌重悬于RPMI 1640培养液中,麦氏比浊仪计数,制备成密度为1×108个/mL的标准菌悬液。将2种菌悬液等比例混合,使用无菌胰岛素注射器在标准化牙根内注入100 μL混合菌液[14],并标准化牙根置入 3 mL混合菌液内,放置在37 ℃,5% CO2培养箱内培养28 d。每两天更换1次新鲜培养基。每次更换培养液,取部分菌液,用BHI固体培养基检测是否有杂菌污染。随后,挑取不同的单菌落革兰氏染色观察微生物是否为粪肠球菌和白念珠菌。感染标准化牙根4周后,使用扫描电镜(SEM)观察标准化牙根感染模型是否建立。
1.2.4 不同冲洗液处理标准感染牙根模型 28 d后,超净台内取出30个牙根,随机分成2.5% NaClO组、2% CHX溶液组和生理盐水组。在根管消毒之前,用3%过氧化氢湿润无菌纱布清洁牙根外表面,再用2.5% NaClO湿润无菌纱布消毒牙根外表面,然后用10%硫代硫酸钠中和2.5% NaClO,并用生理盐水冲洗牙根表面[13],以去除根管外部的微生物,避免影响根管内微生物的取样。随后,使用30号双侧开口冲洗针头和5 mL注射器进行根管冲洗。将橡胶止点放在距离针尖约14 mm处,所有的冲洗液均使用5 mL,缓慢冲洗2 min[15]。冲洗结束后,用1 mL 10%硫代硫酸钠冲洗中和残余的NaClO[13],1 mL 3% Tween 80用于中和CHX[16]。
1.2.5 标准感染牙根模型内微生物的取样 根管内微生物取样分为根管冲洗前(S1)和根管冲洗后(S2)。在根管冲洗前(S1),根管用1 mL生理盐水轻轻冲洗,以去除未附着的微生物,采用3~5个无菌纸捻取菌,每次纸捻停留在根管内1 min[17],1 min后取出纸捻,立即置入装有1 mL生理盐水的EP管中,震荡1 min,之后10倍列梯度稀释[15]。根管冲洗后(S2)的取样方法同S1。取50 mL稀释后的S1、S2菌液,分别接种到粪肠球菌培养基和SDA含有氯霉素的固体培养基中。将培养基放置在37 ℃中培养至48 h,菌落计数。
1.2.6 CLSM样本制备及观察 取培养28 d混合感染的牙根12个,用2.5% NaClO、2% CHX溶液和生理盐水分别处理后,使用玻璃离子封闭根管口。在唇颊侧分别预备一个约0.5 mm深的浅凹槽,不破坏根管内壁牙本质。用锤子和凿子沿凹槽将牙根一分为二:用CLSM观察冲洗液对牙本质小管内微生物的杀菌作用。在避光的条件下,将劈好的牙根用现配的LIVE/DEAD BacLight Bacterial Viability Kit进行染色,暗室下室温孵育15 min。用1 mL PBS轻轻洗去未与牙根表面结合的荧光染色剂,吸干牙根表面的水分,保持牙根干燥,立刻置于CLSM下观察。每个样本随机选取根管内的3个不同区域,镜头放大20倍,步长为5 μm,SYTO 9的激发/发射波长为488/525 nm,propidium iodide(PI)的激发/发射波长为561/642 nm。使用ZEN软件(Carl Zeiss,德国)进行拍摄,绿色荧光表示活菌,红色荧光表示死菌,并测量距离根管内壁牙本质小管内微生物主要的抑制深度。
1.3 统计学方法
对于CFU计数分析,数据进行对数转换并使用ANOVA和Tukey检验进行分析。CLSM数据使用Kruskal-Wallis检验进行分析,成对比较使用Mann-Whitney检验进行分析。使用SPSS 25.0统计学软件进行分析,P<0.05差异有统计学意义。
2 结 果
2.1 标准化牙根感染模型的建立
使用扫描电镜观察标准化牙根感染模型是否建立:未接种微生物之前,牙本质小管内未见微生物。接种混合感染并培养4周后,牙本质小管内可见大量微生物,以粪肠球菌为主,其中可见少量白念珠菌(图1)。
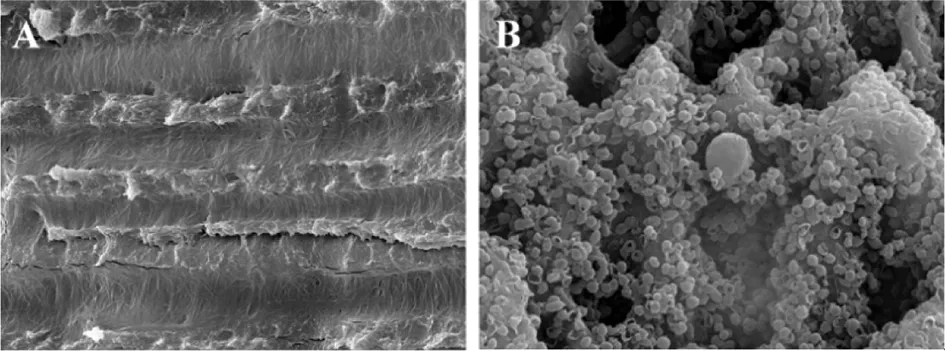
A:接种前;B:接种后
2.2 根管消毒后的粪肠球菌和白念珠菌的清除率
根管内粪肠球菌和白念珠菌的微生物量在冲洗前的(S1)各组之间均无统计学差异(P>0.05)。根管冲洗后,2.5% NaClO和 2% CHX溶液对混合感染根管内粪肠球菌和白念珠菌各自的清除率((S1-S2)/S1)均高于生理盐水(P<0.05),而2.5% NaClO和 2% CHX之间的对混合感染根管内粪肠球菌和白念珠菌各自的清除率无统计学差异(P>0.05)。不同冲洗液对混合感染根管内微生物的清除率见表1。
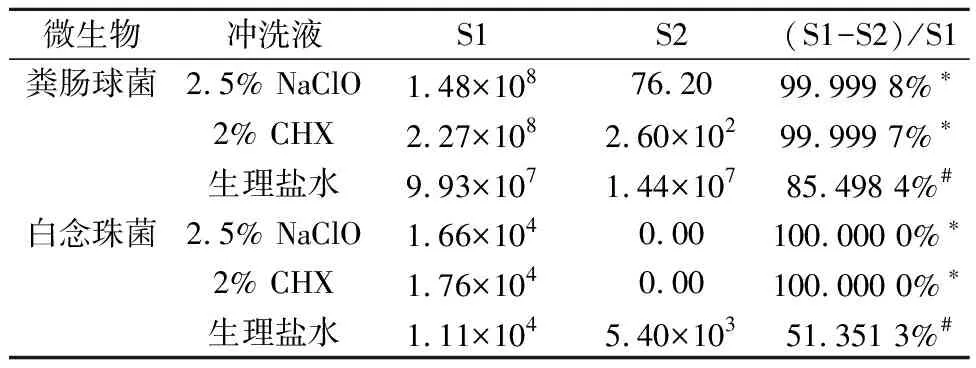
表1 不同冲洗液对混合感染根管内微生物的结果
2.3 CLSM观察
生理盐水组的CLSM图像显示牙本质小管内可见绿色荧光(代表活细菌),而没有任何红色荧光(代表死细菌),即生理盐水对牙本质小管内混合微生物无抑制作用;此外,在生理盐水组中,牙本质小管中的绿色荧光长度在根上、根中和根尖部均超过400 μm。2% CHX组的CLSM图像显示牙本质小管内可见少量的红色和黄色,并伴有大量的绿色荧光。2.5% NaClO组的CLSM图像显示牙本质小管内可见大量红色荧光,并伴有少量黄色荧光。2.5% NaClO在根上、根中、根尖部牙本质小管内的微生物抑制深度显著高于2% CHX(P<0.05);2.5% NaClO对根上、根中和根尖区根管牙本质小管内混合微生物的抑制作用依次递减。2.5% NaClO、2% CHX对于根上部、根中部、根尖区牙本质小管内混合微生物的抑制作用见表2和图2。
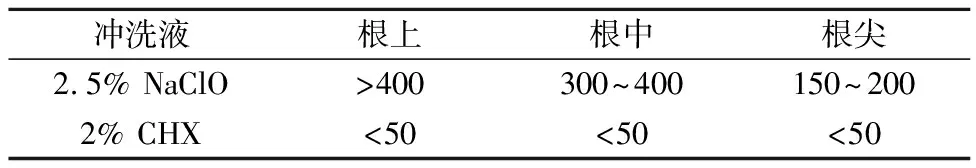
表2 不同冲洗液对于牙本质小管内混合微生物的抑制深度
3 讨 论
根管冲洗是根管治疗成功不可或缺的一部分,其主要目的是控制感染,因此根管冲洗液应具备一定的抗微生物性能[1]。NaClO由于其广谱抗微生物的性能,同时可以促进感染牙髓及其他有机物溶解,在临床上广泛研究。NaClO在临床中可用的浓度范围为0.50%~5.25%,其抗微生物性能和细胞毒性均随浓度升高而升高,为保留其抗微生物性能而尽可能减少其细胞毒性,最广泛研究的浓度为2.5%[7]。CHX虽不能溶解有机组织,但具有显著的抗菌作用和相对较低的毒性作用。本研究对2.5% NaClO、2% CHX溶液在对标准牙根模型中根管混合感染的抗微生物作用进行探讨。
粪肠球菌和白念珠菌混合生物膜的毒性可加剧根尖周病变和骨吸收[18]。本实验在标准牙根模型中建立了粪肠球菌和白念珠菌混合感染的根管模型,这种模型较单一感染的模型更贴近临床实际。混合培养28 d之后,在根管冲洗前对根管内的微生物培养并菌落计数发现,粪肠球菌的生物数量明显多于白念珠菌;同时对建模的混合感染根管CLSM结果表明微生物在牙本质小管中的渗透深度在根上、根中和根尖部均超过400 μm,且牙本质小管内主要以粪肠球菌侵入为主。研究表明,体外建模的酵母菌可以侵入牙本质小管内的深度为10~150 μm[19],而粪肠球菌可以侵入牙本质小管深度400 μm[20],甚至达到700 μm[17]。这可能由于粪肠球菌的直径小于白念珠菌,且根管内空间较小,不适合需氧的白念珠菌的生长,更适合兼性厌氧菌粪肠球菌,因此粪肠球菌可以大量繁殖,这也是粪肠球菌更易造成严重感染的原因。
菌落CFU计数是目前检测根管内微生物清除作用的常用检测方法,但无菌纸捻只能收集主根管内的微生物,对于复杂根管内较隐蔽区域的微生物无法采集。对于牙本质小管内微生物的抑制作用,如果仅是利用菌落CFU计数法检测,在操作过程中可能对微生物细胞壁造成破坏。此外,菌落CFU计数中微生物培养法灵敏度低,若提取的细菌数量不足,则在固体培养基上无细菌生长,并不一定意味着根管内无微生物存活[21]。这是菌落CFU计数的局限性,在分析结果时应予以考虑。从本研究的菌落CFU计数结果显示,2.5% NaClO和2% CHX对根管内混合微生物均有较好的清除作用,且两者对根管内粪肠球菌和白念珠菌的清除效果未见明显统计学差异。Meta分析的结果也表明:同一种镍钛器械预备时,CHX和NaClO用于根管冲洗时,两者对于根管内微生物的清除作用差异无统计学意义[7]。这与本实验的研究结果一致。
本研究中采用CLSM来获得混合感染在根管内的位置(样本中的空间分布)和渗透深度等的完整信息,以弥补菌落计数的不足。CLSM是将生物膜可视化处理的首选,可以在不破坏细胞或组织的状态下,观察其内部结构,并对其进行实时的检测,实现细胞及微生物三维重建和成熟生物膜重建[22]。CLSM的结果表明,2.5% NaClO对根管内微生物的抑制深度在根上部>400 μm,根中部为 300~400 μm,根尖区为150~200 μm;2.5% NaClO对根尖区混合微生物的抑制作用明显低于根上部和根中部,这符合冲洗液渗入根尖区牙本质小管的能力低于其在根上及根中部的研究结论[23]。根尖区牙本质小管的结构似乎和其他部位存在一定的差异[24],这在一定程度上或许可以解释,冲洗液对于根尖区牙本质小管内微生物的抑制作用较差。2.5% NaClO对于根上、根中、根尖区牙本质小管内微生物的抑制深度明显优于2% CHX。2% CHX虽然对于根管内微生物的清除具有一定作用,但对于根管上、中、下三部分的牙本质小管内微生物的抑制作用仅限于牙本质小管的浅层,这或许与根管冲洗液本身的渗透性有关。CLSM的结果也进一步证明,两种冲洗液对牙本质小管内混合微生物均无法完全抑制,对根管内混合感染更有效的冲洗液有待进一步研究。
菌落计数显示2.5% NaClO和2% CHX对于标准牙根感染根管内的微生物的清除作用明显高于生理盐水,CLSM结果进一步显示2.5%NaClO对于牙本质小管内微生物的抑制作用明显优于 2% CHX。2.5% NaClO对于混合感染根管的抗微生物作用最好,可以在临床中用于粪肠球菌和白念珠菌混合感染的冲洗。
