基于FAERS 数据库的福沙匹坦不良事件信号挖掘*
2023-06-11刘迅,陈力,陈乾,肖潇,余瑛
刘 迅,陈 力,陈 乾,肖 潇,余 瑛
(1. 四川省成都市第七人民医院,四川 成都 610041; 2.重庆理工大学药学与生物工程学院,重庆 400054;3. 四川大学华西第二医院,四川 成都 610041; 4. 四川省宜宾市第一人民医院,四川 宜宾 644000)
恶心和呕吐是化学治疗过程中最常见的药品不良反应(ADR),常造成患者拒绝治疗或恐惧治疗,延误治疗时机。福沙匹坦为神经激肽1(NK1)受体拮抗剂,于2008 年被美国食品和药物管理局(FDA)批准用于化学治疗所致恶心呕吐(CINV)。国产仿制药福沙匹坦于2019 年上市,通过静脉途径给药,其生物利用度不受呕吐的影响,也可用于口腔黏膜炎等不宜口服用药的患者或年龄大于6个月的患儿。福沙匹坦已收入美国国立综合癌症网络(NCCN)、美国临床肿瘤学会(ASCO)、中国临床肿瘤学会(CSCO)等化学治疗相关恶心呕吐指南推荐,但国产福沙匹坦的药品说明书记载的ADR 较少,尚无相关系统分析。为此,本研究中主要利用比例失衡法中的报告比值比(ROR)法、比例报告比(PRR)法和综合标准(MCA)法对从FDA不良事件报告系统(FAERS)[1]中收集的数据进行筛选和挖掘,分析福沙匹坦可疑的药品不良事件(ADE)信号,以期为临床安全、合理用药提供参考。现报道如下。
1 资料与方法
1.1 数据来源
所用FAERS 数据库的数据来源于自发呈报,即由报告者(卫生健康人员或患者)自发向数据库报告相关信息[1]。收集其中2016 年第一季度至2021 年第二季度共22 个季度的数据,包括患者基本信息、药品使用信息、ADE、结果、报告来源、报告日期、报告国家等。研究数据以FDA 官网批准和维基百科上所有关于福沙匹坦的商品名及通用名为关键词,从FAERS数据库下载对应季度的ASCII数据包,导入MY SQL数据库,经过demo表去重,核对drug name项符合“福沙匹坦”的ADE。
1.2 数据处理
采用国际医学科学组织理事会《国际医学用语词典》(MedDRA)中ADR 术语集的首选系统器官分类(SOC)和首选语(PT)对ADE 进行分类和描述,下载MedDRA 23.0 版,用于PT、高位语(HLT)、高位组语(HLGT)、SOC编码及中英文映射。
1.3 数据挖掘
目前,国内外用于ADE 信号检测的数据挖掘方法主要是比例失衡法[2]。其原理是比较目标药物- 事件出现频率与背景频率的差异,即在1个包含所有药物事件报告的数据库中,当目标药物事件组合的出现频率明显高于整个数据库的背景频率,且达到设定阈值时,可认为产生了1 个信号[3]。同时,联用比例失衡法中的ROR法、PRR法、MCA法[4-5],可降低假阳性和假阴性信号的数量,提高结果的可靠性。通过比较目标药物福沙匹坦的ADE 报告例数和其他所有药物的报告例数(背景数据)来判断是否失衡,以此挖掘潜在的ADE信号。
1.4 数据计算与筛选
根据比例失衡法四格表(表1)和PT 对应的报告例数计算出相应的ROR值、PRR值、χ2值和95%CI下限(表2),统计信号数,排除不满足要求的报告。数值越大,信号就越强,说明目标药物与目标ADE间的联系越强。
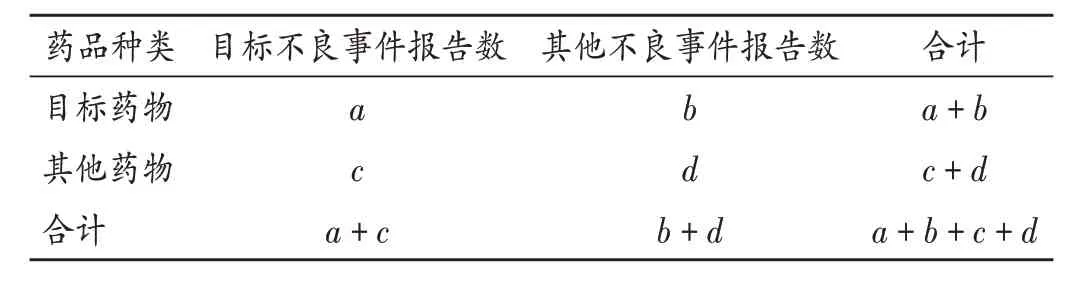
表1 比例失衡法四格表Tab.1 Four grid table of proportional imbalance method
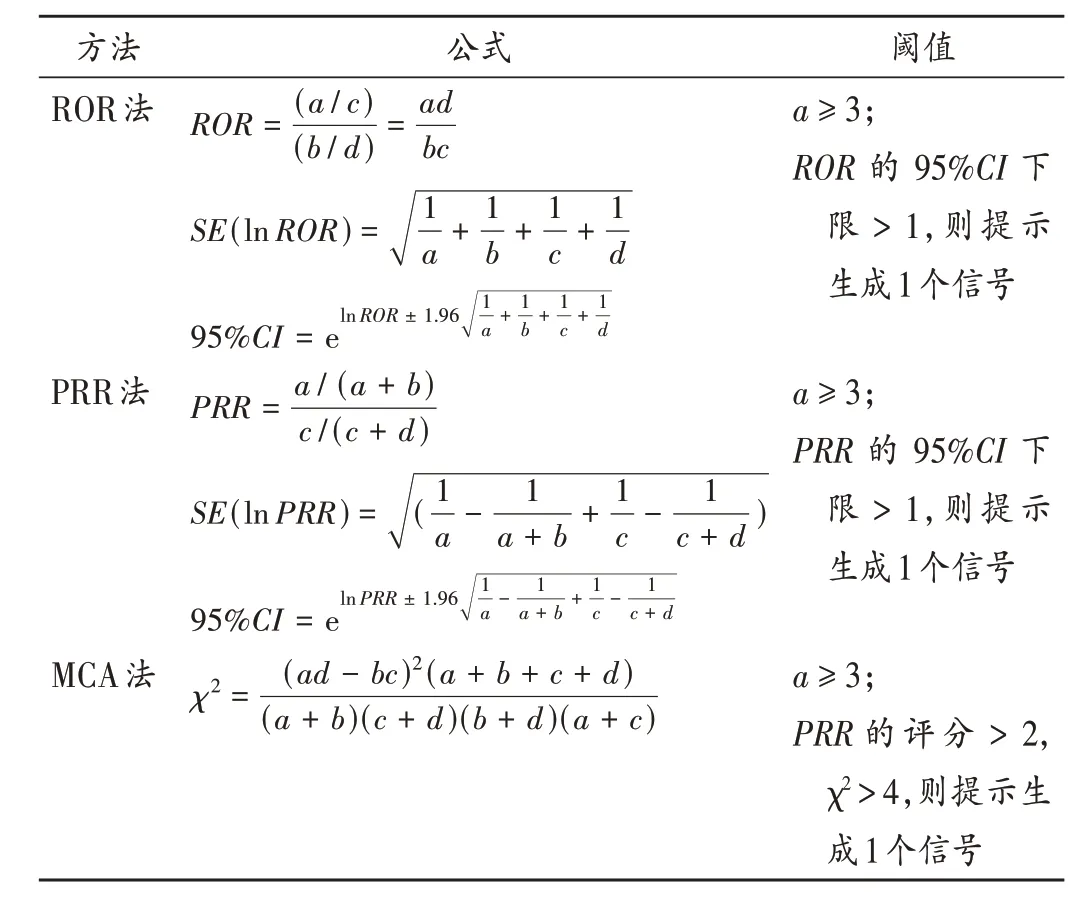
表2 ROR法、PRR法及MCA法的公式及阈值Tab.2 The formulas and thresholds of ROR,PRR and MCA methods
2 结果
2.1 ADE 报告的基本信息
2016 年第一季度至2021 年第二季度的ADE 背景信号7 621 815 份,以Primaryid(ISR 编码)作为唯一识别,多份报告中保留1份,并保留“性别”“年龄”“ADE发生地区”“报告者”4个用药信息中至少有1项的报告,得到首要怀疑药物为福沙匹坦的报告共548 份,PT 共1 992 个。548 份报告中,男女比例约为1∶1;年龄主要集中于50~<70岁,占48.54%;报告居前3位的国家分别为韩国、美国、日本,其中韩国占60.58%;医师、药师、消费者为主要上报人群,分别占65.15%,14.42%,10.40%。详见表3。
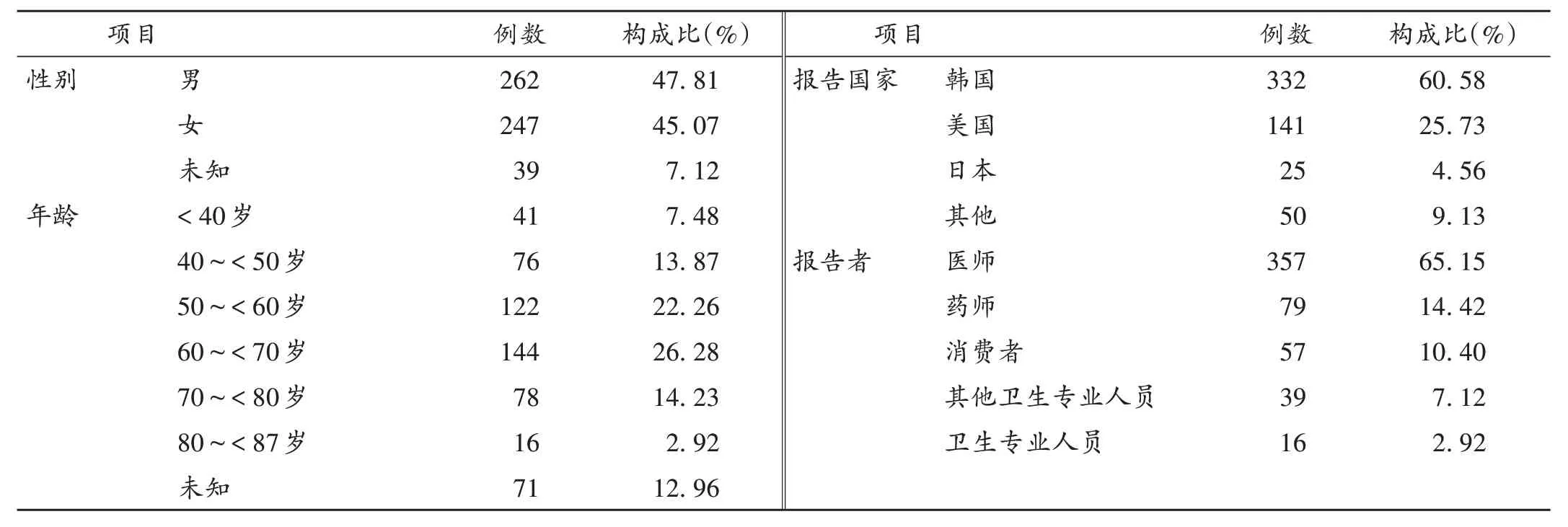
表3 2016年第一季度至2021年第二季度FAERS中福沙匹坦相关ADE报告基本信息(n=548)Tab.3 Basic information of ADE reports related to fosaprepitant from the first quarter of 2016 to the second quarter of 2021 in the FAERS database(n=548)
2.2 ADE 信号挖掘结果
筛选后最终获得福沙匹坦ADE 信号88 条,其中药品说明书未提及的有71 个,PT 报告1 308 个,再对得到的88个ADE信号的发生频次(a值)居前50位和信号强度[95%CI(ROR)下限]居前50位进行PT排序。其中,报告频次最高的ADE 为恶心、发热、呼吸困难;相关性较高的ADE为反射性食管炎、呕逆、静脉炎。详见表4。
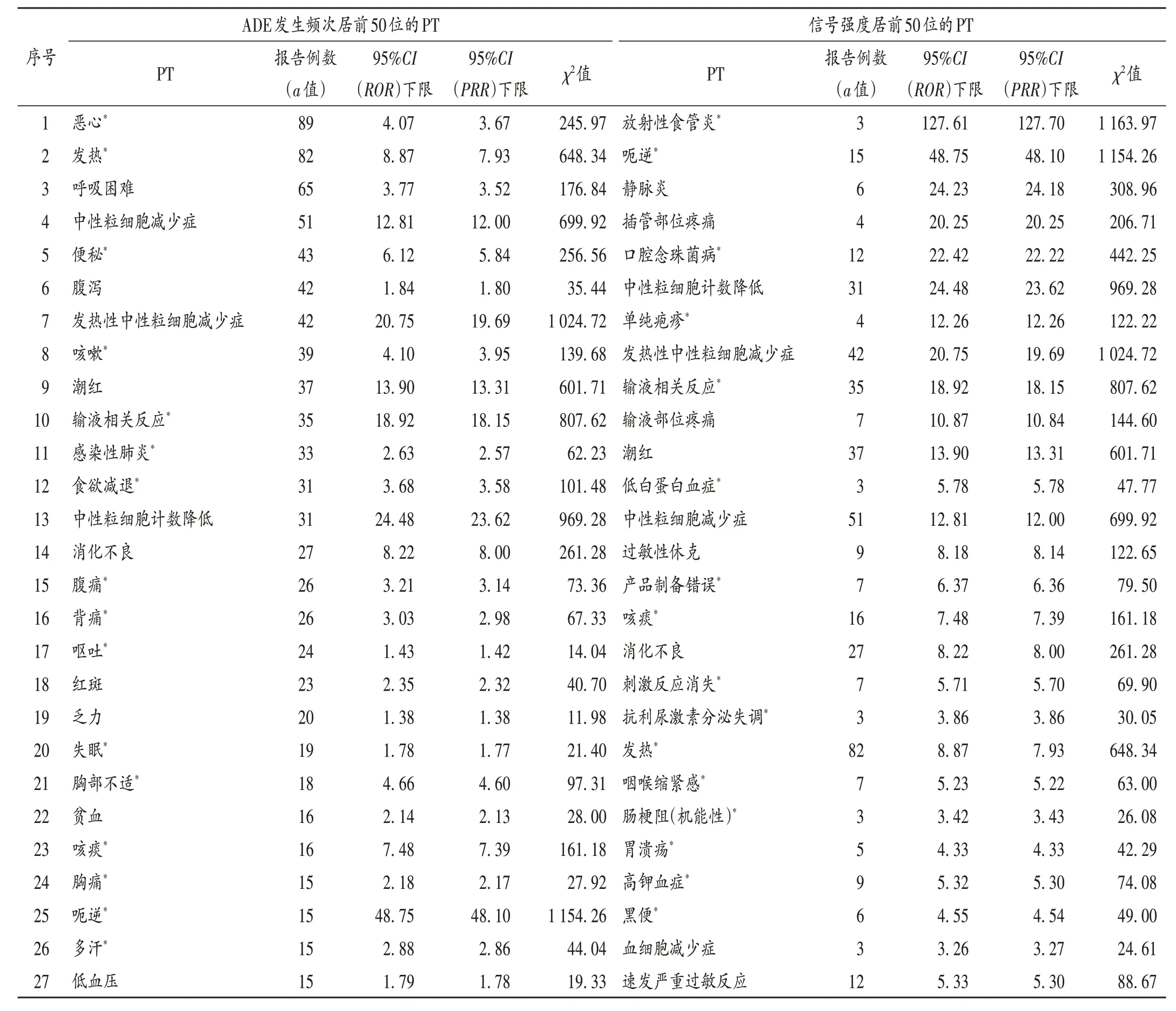
表4 福沙匹坦ADE发生频次居前50位和信号强度居前50位的PTTab.4 The PT sequence of the top 50 bits of the occurrence frequency and the top 50 bits of the signal intensity of ADEs related to fosaprepitant
2.3 ADE 信号累及系统/器官
福沙匹坦88 个ADE 信号累及17 个SOC,分类后各个SOC 的信号数、报告数及构成比见表5。各种胃肠系统疾病的ADE 报告数最多(恶心、便秘、腹泻等),共299份,占22.86%;报告数较多的SOC 还有血液及淋巴系统疾病(中性粒细胞减少症、发热性中性粒细胞减少症、潮红等),全身性疾病及给药部位各种反应(发热、胸部不适、胸痛等),呼吸系统、胸及纵隔疾病(呼吸困难、咳嗽、咳痰)等。

表5 福沙匹坦ADE信号累及系统/器官Tab.5 Systems and organs involved in ADE signals caused by fosaprepitant
3 讨论
3.1 福沙匹坦ADE 发生人群的特点
本研究中共纳入福沙匹坦导致的ADE 报告PT共1 992 个,涉及548 例患者。其中,男女比例约为1∶1;各年龄段都有ADE 的发生,其中50~<70 岁人群占比最高,可能与肿瘤的高发年龄、患者身体机能的下降、联合用药等因素相关;医师、药师、消费者为主要上报人群,通过临床工作者和患者上报ADE 是药品上市后ADR 监测的常用形式之一,监测范围更广,且能提高数据的可利用性。
3.2 与福沙匹坦药品说明书的对比
本研究中对以福沙匹坦为首要怀疑药物的ADE 信号进行筛选,筛选后最终获得88个福沙匹坦信号数,涉及17个SOC,药品说明书未提及的有71个。现有福沙匹坦药品说明书的ADR 未涉及的10 个系统分类包括呼吸系统、胸及纵隔疾病,感染及侵染类疾病,代谢及营养类疾病,心脏器官疾病,肾脏及泌尿系统疾病,内分泌系统疾病,各种肌肉骨骼及结缔组织疾病,各类损伤、中毒及操作并发症,良性、恶性及性质不明的肿瘤(包括囊状和息肉状),精神病类。可见,福沙匹坦现有药品说明书及最新版合理用药信息支持系统中涉及该药的ADR 不全面。本研究结果可作为对药品说明书未涉及的ADR 的补充,提示在临床用药过程中注意可能发生的相关ADE。
3.3 福沙匹坦ADE 信号分析
3.3.1 ADE 信号累及系统/器官
本研究中采用ROR 法、PRR 法和MCA 法分析发现,福沙匹坦较强的ADE 信号为放射性食管炎、呃逆、静脉炎、插管部位疼痛、口腔念珠菌病、中性粒细胞计数降低、单纯疱疹、发热性中性粒细胞减少症、输液相关反应等。其中,放射性食管炎上报例数为3例,但相关性很高,但未查阅到福沙匹坦可能引起放射性食管炎的相关研究及个案报道;呃逆的相关性较高,其产生机制复杂,涉及中枢和外周神经系统的多种神经递质和解剖结构,目前尚无研究报道福沙匹坦可能引起呃逆的机制[6]。
值得注意的是,福沙匹坦用药部位的反应信号相关性较高,表现为静脉炎、插管部位疼痛、输液相关反应、输液部位疼痛。一项关于福沙匹坦与其他药物相互作用的回顾性系统评价显示,因福沙匹坦会导致输注部位反应风险升高,应避免通过相同的外周静脉给予福沙匹坦和蒽环类抗肿瘤药[7]。日本一项关于福沙匹坦输注部位ADE 的回顾性研究表明,在使用高致吐化学治疗方案的乳腺癌患者中,经由中心静脉导管输注福沙匹坦,可减少输注部位的ADE[8]。2019 年的一项关于福沙匹坦相关输液部位反应发生率的报告显示,福沙匹坦稀释至0.6 mg/mL 并超过30 min 输注时,输注部位反应的总体发生率从28.70%降至5.74%,输注部位反应显著降低[9]。建议临床输注福沙匹坦时,可考虑使用更低浓度和控制输注时间在30 min内。
本研究中,报告例数最多的为恶心。恶心定义为上腹部不适和紧迫欲吐的感觉。恶心和呕吐在化学治疗过程中经常一起发生,但恶心和呕吐的神经药理学不同,恶心可独立发生[10],在恶性肿瘤化学治疗过程中较呕吐更常见。目前,对于化学治疗导致恶心的病理生理学机制尚不清楚[11]。NK1受体拮抗剂显著改善了化学治疗相关呕吐[12-15],但预防恶心的作用还不太确定。2017年的相关研究回顾了不同机构14项包含NK1受体拮抗剂的临床随机对照试验,化学治疗相关恶心被设定为临床研究的一部分或次要终点;阿瑞匹坦- 昂丹司琼-地塞米松方案虽在控制化学治疗引起的呕吐方面显著优于昂丹司琼- 地塞米松,但与昂丹司琼- 地塞米松相比,在总体恶心控制方面并不优越[16-17]。一项Ⅲ期临床试验中对福沙匹坦进行了评估,研究组(福沙匹坦-昂丹司琼-地塞米松)较对照组(昂丹司琼-地塞米松)发生严重恶心的患者更少,但恶心发生率无显著差异[18]。在奥沙利铂治疗结直肠癌患者的Ⅲ期临床试验中,使用福沙匹坦或阿瑞匹坦的女性患者未发生恶心的比例更高,表明NK1受体拮抗剂对女性可能有特殊益处[19]。目前,关于NK1类药物对化学治疗相关恶心的防治相关研究尚未得出确切、有效的结论[16]。恶心的病理生理学及更多以恶心为主要疗效终点的临床试验的开展,将有助于确定预防恶心的最有效药物组合。
3.3.2 药物相互作用对福沙匹坦ADE 评价的影响
福沙匹坦通常联合其他药物用于CINV,可用于大于6个月以上的儿童和成人。不论是用于化学治疗相关呕吐,还是用于术后止吐,均涉及众多合并用药,合用如5-羟色胺3(5-HT3)受体拮抗剂、地塞米松、化学治疗药物等。福沙匹坦是细胞色素P450 3A4 酶(CYP3A4)的底物,同时也是弱CYP3A4 抑制剂[20]。一项关于福沙匹坦药物相互作用的系统评价指出,对于接受地塞米松(口服,po)、甲泼尼龙(静脉注射,iv)、咪达唑仑(po/iv)、羟考酮(po)或甲苯磺丁脲(po)的患者,应考虑对相应药物进行剂量调整或使用福沙匹坦以外的止吐剂;接受博舒替尼(po)、卡巴他塞(iv)或环磷酰胺(iv)的患者应考虑使用不具有CYP3A4 活性的NK1受体拮抗剂;对于接受厄洛替尼(po)、帕唑帕尼(po)或塞替哌(iv)的患者,福沙匹坦也不是最优选择[21]。上述药物相互作用不仅对药物治疗效果有影响,也更易产生ADR。使用福沙匹坦时,医师和药师需高度关注药物之间可能的互相作用,以避免或减少ADR的发生。
3.3.3 原发疾病对福沙匹坦ADE 评价的影响
福沙匹坦药品说明书批准的适应证为预防化学治疗或手术引起的恶心和呕吐,但在该不良事件信号挖掘中,在胃肠系统的ADE 信号均占比最大,如恶心、便秘、腹泻、消化不良等,但相关性都不高。因原发疾病的影响,不排除为化学治疗或患者本身疾病进展导致的消化系统不良事件。对于排除原发疾病影响的ADE,应根据患者病情权衡利弊,对症处理,如严重影响生活质量,可考虑停止使用。
本研究为上市后ADE 信号研究,数据来源于真实世界,样本量大,是评价药品安全风险的关键方法,但仍有局限性。FAERS 数据库的部分数据存在缺失、错误、质量不高等情况,研究结果可能出现误差。另外,本研究中为了减少遗漏的信号,联用比例失衡法中的ROR 法、PRR法、MCA法以降低假阳性和假阴性信号的数量,但对于临床中实际判断目标药物与目标ADE 的关联性尚需进一步评估。所得结果与药品说明书较一致,也发现了许多新的ADR;临床工作者需关注福沙匹坦带来的ADR,以便及早采取干预措施,保证患者用药安全、有效,降低用药风险。
