miRNA505-3P在系统性红斑狼疮患者中的表达及临床意义
2023-05-15张燕妮胡玉海
张燕妮,刘 梅,胡玉海
湖北省武汉市汉口医院检验科,湖北武汉 430013
系统性红斑狼疮(SLE)是一种常见的多器官损伤性自身免疫性疾病,多数患者发病较缓慢,但少数可急性发作[1]。研究显示,SLE的发生与外界环境、遗传易感性、药物和激素等多种因素密切相关,但确切发病机制尚未完全明确[2]。因此,探究SLE发病机制,筛选出诊断和预后的生物学标志物,对指导临床早期诊治SLE具有重要临床意义。微小RNA(miRNA)是一类由18~25个核苷酸组成的非编码小RNA,它可通过促进mRNA降解或在翻译水平调控基因的表达而发挥重要作用[3]。miRNA的异常表达与多种自身免疫性疾病的发病密切相关,它们可通过驱动T淋巴细胞、B淋巴细胞等细胞活化,产生特异性自身抗体,形成抗原抗体复合物沉积于组织器官,从而造成慢性炎症损伤[4-5]。miRNA505-3P为一类与慢性炎症密切相关的小RNA,可通过靶向晚期促炎症蛋白质-高迁移率族蛋白B1(HMGB1)发挥促炎作用[6-7]。在狼疮性肾炎患者的研究中发现HMGB1的表达水平与疾病活动度呈显著正相关[8],但目前关于miRNA505-3P在SLE患者中的具体作用研究尚少。因此,本研究通过检测SLE患者血浆中miRNA505-3P的表达水平,进一步评估其对SLE患者的早期诊断效能,并分析miRNA505-3P与SLE疾病活动度的关系,以期为临床诊疗提供新的标志物。
1 资料与方法
1.1一般资料 收集2020年9月至2022年5月首次到武汉市汉口医院就诊并确诊的SLE患者174例作为SLE组,其中男35例、平均(42.3±9.6)岁,女139例、平均(36.6±10.1)岁。根据SLE疾病活动度指数(SLEDAI)评分,将SLE患者分为活动组(SLEDAI评分≥4分)92例和非活动组(SLEDAI评分<4)82例。其中活动组男19例、平均(44.5±8.5)岁,女73例、平均(36.6±10.5)岁;非活动组男16例、平均(39.8±10.8)岁,女66例、平均(36.5±9.5)岁。活动组与非活动组患者性别、年龄比较,差异无统计学意义(P>0.05),具有可比性。另选取同期在本院体检的60例健康体检者作为健康对照组,其中男15例、平均(41.5±9.9)岁,女45例、平均(36.9±9.7)岁。SLE组与健康对照组的性别、年龄比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:所纳入的SLE患者均符合《2020年中华医学会风湿学分会2020中国系统性红斑狼疮诊疗指南》[9]中关于SLE的诊断标准。排除标准:(1)合并肝、肾、心、脑等基础疾病;(2)合并其他感染性疾病;(3)合并其他自身免疫性疾病期或肿瘤等女性;(4)妊娠或哺乳期女性;(5)诊断不明确者。
1.2仪器与试剂 Gentier96R全自动PCR分析系统(西安天隆),5804R台式高速大容量离心机(艾本德),Nanodrop 1000微量分光光度计(赛默飞世尔),BX41荧光显微镜(奥林巴斯),RT-6100全自动酶标分析仪(深圳雷杜),PW-960全自动洗板机(深圳汇松)。miRNA快速提取试剂盒(无锡百泰克生物),反转录试剂盒(大连宝日医),荧光定量PCR试剂盒(大连宝日医),HMGB1酶联免疫吸附试验测定试剂盒(E-EL-H1554c,武汉伊莱瑞特生物),抗核抗体(ANA)、抗双链DNA抗体检测试剂盒(欧蒙医学诊断)。
1.3方法
1.3.1血液标本采集及处理 所有研究对象均于清晨采集空腹静脉血2 mL,置于含有EDTA-K2抗凝真空采血管中,4 ℃条件下3 000 r/min离心5 min,分离血浆于无RNA酶的EP管中,-80 ℃冻存备用。
1.3.2RNA提取与反转录 采用Trizol法提取血浆中总RNA,分光光度计测量A260/A280比值,比值为1.8~2.0的用于后续实验。按照反转录试剂盒说明书将所提取的总RNA反转录为cDNA,-80 ℃冻存备用。
1.3.3miRNA505-3P水平检测 根据Genebank中miRNA505-3P(NC_000023.11)和U6(NR_138085)的基因序列号,采用Primer Premier 5.0软件进行相应引物的设计,并由武汉擎科生物技术有限公司进行合成。miRNA505-3P反转录引物为5′-GCGTCTCAACTGGTGTCGTGGAGTCGGCAATT AGTTGAGACGCAGAAAACCAGC-3′,扩增正向引物为5′-GCGAGCACCGTCAACACT-3′,扩增反向引物为5′-TGGTGTCGTGGAGTCGGC-3′;内参U6正向引物为5′-CGCTTCACGAATTTGCGTGTCAT-3′,反向引物为5′-GCTTCGGCAGCACATATACTAAAAT-3′。PCR反应体系:SYBR Premix 10 μL,cDNA 2 μL,正、反向引物各1 μL,ddH2O 6 μL,循环条件为95 ℃ 10 min,95 ℃ 15 s,58 ℃ 15 s,72 ℃ 20 s,共40个循环,每个标本设置3个复孔,U6为内参,通过2-ΔΔCt计算miRNA505-3P在血浆中的表达水平,公式:ΔΔCt=[(实验组目的基因Ct-实验组内参基因Ct)-(对照组目的基因Ct-对照组内参基因Ct)]。
1.3.4抗核抗体(ANA)、抗双链DNA抗体检测 采用间接免疫荧光法进行检测,操作步骤严格按照试剂说明书进行。ANA阳性为抗体滴度≥1∶100,并根据观察相应的荧光模型,抗双链DNA抗体阳性为抗体滴度≥1∶10。

2 结 果
2.1SLE组与健康对照组miRNA505-3P和HMGB1水平比较 SLE组miRNA505-3P和HMGB1水平明显高于健康对照组,差异均有统计学意义(P<0.05)。见表1。

表1 SLE组与健康对照组miRNA505-3P和HMGB1水平比较M(P25,P75)
2.2活动组与非活动组miRNA505-3P和HMGB1水平比较 活动组miRNA505-3P和HMGB1水平明显高于非活动组,差异有统计学意义(P<0.05)。见表2。

表2 活动组与非活动组miRNA505-3P和HMGB1水平比较M(P25,P75)
2.3SLE患者中miRNA505-3P水平与SLEDAI评分及HMGB1水平的相关性分析 Pearson相关性分析结果显示,miRNA505-3P水平与SLEDAI评分及HMGB1水平呈显著正相关(r=0.734 4、0.647 5,P<0.05)。
2.4miRNA505-3P对SLE的诊断效能 ROC曲线分析结果显示,miRNA505-3P诊断SLE的曲线下面积(AUC)为0.969 9(95%CI:0.950 0~0.989 8),当miRNA505-3P最佳截断值为0.765 0时,诊断SLE的录敏度为96.67%,特异度为83.33%。见图1。

图1 miRNA505-3P诊断SLE的ROC曲线
2.5不同临床病理参数的SLE患者miRNA505-3P水平比较 以miRNA505-3P的最佳截断值(0.765 0)为分界值,将SLE患者分为高表达组(miRNA505-3P水平≥0.765 0)和低表达组(miRNA505-3P水平<0.765 0),结果显示,高表达组与低表达组患者的年龄、性别和是否累及肾脏情况比较,差异均无统计学意义(P>0.05),但两组ANA阳性、抗双链DNA抗体阳性比例和SLEDAI评分比较,差异均有统计学意义(P<0.05)。见表3。

表3 不同临床病理参数的SLE患者miRNA505-3P水平比较[n(%)]
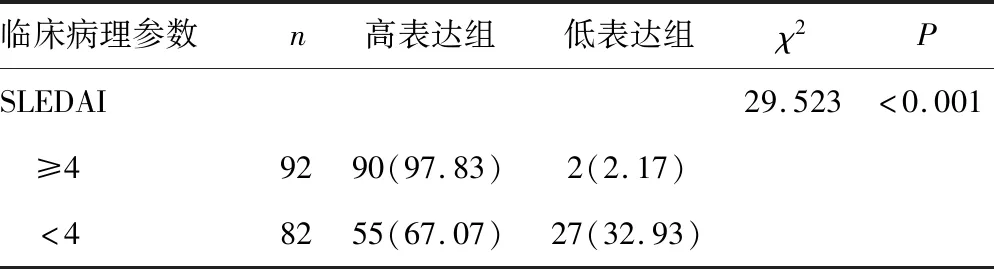
续表3 不同临床病理参数的SLE患者miRNA505-3P水平比较[n(%)]
3 讨 论
SLE为一种由多因素参与的系统性自身免疫性疾病,致病原因尚不明确,但具有明显的性别倾向,好发于女性。有研究显示在外界相关因素作用下SLE患者体内免疫功能严重紊乱,机体表现为以ANA为代表的多种自身抗体的出现,并与相应抗原形成抗原抗体复合物,沉积于不同组织和器官,造成组织器官的损伤,其中肾脏受累是SLE常见的严重并发症[10]。尽管SLE患者的治疗及护理得到了较明显的改善,但由于该病病因复杂,病情缓解后常易复发,因此该病的预后仍无法令人感到满意[11]。目前对SLE的致病机制研究尚不清楚,临床上对SLE的诊断也主要依靠患者的临床表现和相关自身抗体标志物(如ANA、抗双链DNA抗体等),故易导致对患者病情诊断的延误。因此进一步探明其发病机制,发现新的灵敏度和特异度较好的生物标志物,进行早期诊断,并针对相应靶点进行早期干预治疗显得十分必要。
有研究显示,miRNA在自身免疫性疾病、炎症及肿瘤等疾病中发挥着巨大作用[12]。也有研究发现多种miRNA在SLE疾病进展中发挥着重要作用,如miR-146a可通过下调巨噬细胞中泛素连接酶等转录因子的活性,进而影响细胞内Ⅰ型干扰素的释放,促进SLE患者体内炎症基因的过度表达[13]。Let-7 miRNAs可通过调节核转录因子的激活发挥对先天免疫系统的负性调节作用,在狼疮性肾炎患者中高表达[14]。miRNA505-3P作为近年来新发现的一个肿瘤抑制miRNA,可通过mTOR途径调控细胞代谢、生长、增殖及存活,并起到中心调控的作用[15],而mTOR抑制剂也是目前临床上治疗SLE患者的有效药物[16]。但目前少见miRNA505-3P在SLE患者中作用的相关报道,因此本研究通过检测SLE患者与健康对照组中miRNA505-3P水平,发现miRNA505-3P在SLE患者中表达显著增高,且活动期SLE患者miRNA505-3P水平显著高于非活动期。这表明miRNA505-3P的异常表达可能与SLE的发生、发展密切相关,提示miRNA505-3P可能是诊断SLE(尤其是活动性SLE)的一种重要生物标志物。Pearson相关分析显示,SLE患者miRNA505-3P水平与SLEDAI评分呈正相关。ROC曲线分析miRNA505-3P对SLE的诊断价值发现,miRNA505-3p对SLE诊断的AUC为0.969 9(95%CI:0.950 0~0.989 8),当miRNA505-3P最佳截断值为0.765 0时,诊断SLE的灵敏度为96.67%,特异度为83.33%,说明miRNA505-3P对SLE的诊断具有较高的诊断价值,尤其是活动性SLE。通过比较不同临床病理参数的SLE患者血浆中miRNA505-3P发现miRNA505-3P高表达组与低表达组患者的ANA阳性、抗双链DNA抗体阳性和SLEDAI评分比较,差异均有统计学意义(P<0.05)。这说明miRNA505-3P在SLE患者的发病过程中起着重要作用。
有研究表明,miRNA505-3P可通过靶向HMGB1抑制胶质瘤细胞中p-AKT的表达从而抑制抑制胶质瘤细胞的增殖、侵袭与迁移,在神经胶质瘤的发生、发展中起着重要作用[17]。但在SLE中miRNA505-3P是否也是通过HMGB1促进SLE的发生、发展,尚不清楚。本研究通过对研究对象HMGB1水平进行检测,发现SLE组HMGB1水平显著高于健康对照组,活动期患者HMGB1水平也显著高于非活动期,这与黎明娟[8]在研究狼疮性肾炎时发现肾炎活动期患者血浆中HMGB1水平高于稳定期患者,且SLE患者中HMGB1水平与疾病活动度呈正相关是一致的,提示HMGB1可能也参与了SLE的发生、发展过程,而且对狼疮性肾炎的发生也起着至关重要的作用。
HMGB1为高迁移率族蛋白家族成员之一,研究显示HMGB1在自身免疫性疾病、炎症、免疫调节、细胞分化、肿瘤侵袭迁移等多方面发挥这着重要作用[18]。黄莉等[19]在儿童SLE发病机制的研究中发现HMGB1可能通过CD14/Toll样受体4(TLR-4)受体参与儿童SLE发病。通过Pearson相关分析发现,SLE患者miRNA505-3P水平与HMGB1水平呈正相关,说明SLE患者HMGB1水平也与SLE活动度密切相关。因此,笔者推测在SLE患者发病过程中miRNA505-3P有可能也是通过调控HMGB1的表达,进一步导致SLE的发生。但本研究尚未对此结论进行验证,且SLE患者中miRNA505-3P对HMGB1的相应调控机制,本研究也未进行研究,有待下一步深入探讨。
综上所述,SLE患者血浆中miRNA505-3P水平显著增高,其水平与SLE活动度密切相关,有望作为SLE患者活动期辅助诊断的生物标志物。在SLE患者发病过程中miRNA505-3P有可能通过作用于HMGB1促进机体免疫功能的紊乱,但具体机制有待进一步研究。
