喉垂直部分切除术治疗声门型喉癌的临床疗效分析
2023-05-09龚洪立施勇陶磊张明吴海涛曹鹏宇周健周梁
龚洪立,施勇,陶磊,张明,吴海涛,曹鹏宇,周健,周梁
(复旦大学附属眼耳鼻喉科医院 耳鼻咽喉头颈外科,上海 200031)
喉癌居头颈癌发病率和死亡率第二位,占全身恶性肿瘤的1%,主要的病理类型是鳞状细胞癌(96%~98%),主要的类型是声门型(63%)[1]。2020年我国的流行病学数据统计喉癌的发病率为1.84/100 000,死亡率为1.0/100 000,在肿瘤发病率和死亡率均排第21位[1]。从2003—2012年,我国喉癌的发病率和死亡率均有所下降[1-2]。喉癌的治疗策略包括手术、放疗、化疗、靶向治疗和免疫治疗,根据患者肿瘤评估和全身情况采取单一或联合治疗方案,目的是在根治肿瘤、保证患者生存率的前提下,尽量保留患者的喉功能,提高生活质量[3]。目前手术仍然是我国喉癌患者的主要治疗方案,可结合辅助治疗[4]。对于病变主要位于一侧声带的声门型喉癌,喉垂直部分切除术(vertical partial laryngectomy,VPL)是主要的开放性手术方式。本研究拟通过中心的大样本量临床数据分析保留喉功能的VPL治疗声门型喉癌的远期临床疗效,为喉癌在国内的规范化临床诊疗提供数据支撑。
1 材料与方法
1.1 临床资料
本组数据为单中心、回顾性研究,根据纳排标准收集2005年1月—2010年12月在本中心接受VPL为主要治疗方案的声门型喉癌患者。临床变量为记录患者就诊时的年龄、性别、吸烟饮酒史、既往病史、癌前病变、TNM分期、临床分期、手术切缘、术后辅助治疗及肿瘤面积。肿瘤面积的计算采用术后病理的测量数据,计算肿瘤长度乘以宽度得出。本组患者548例,男537例(98.0%),女11例(2.0%);年龄34~89岁,平均年龄(59.0±9.4)岁。吸烟396例(72.3%),饮酒304例(55.5%)。84例(15.3%)患者既往伴高血压,20例(3.6%)患者伴糖尿病,9例(1.6%)患者伴高血压和糖尿病。28例(5.1%)患者既往伴声带白斑,1例(0.2%)患者伴喉淀粉样变,2例(0.4%)患者伴喉乳头状瘤。524例(95.6%)患者主诉声嘶就诊,3例(0.5%)患者喉梗阻急诊气管切开。所有患者术前均无放/化疗。
入组标准:①声门型喉癌;②首选治疗方案是VPL;③病理为鳞状细胞癌。排除标准:①患者病史资料不完整;②术前接受辅助治疗;③既往外院治疗后复发或转移。术后通过对患者进行定期门诊随访和电话随访,记录患者术后的生存时间、生活质量和喉功能的恢复情况。平均随访时间(104.9±33.2)个月。
1.2 诊疗方案
1.2.1 手术治疗 所有患者术前均行增强CT和电子纤维喉镜检查,评估肿瘤的部位和范围以及临床TNM分期。临床TNM分期按照第7版AJCC分期指南。T1期169例(30.8%),T2期316例(57.7%),T3期63例(11.5%)。临床Ⅰ期168例(30.7%),Ⅱ期310例(56.6%),Ⅲ期66例(12.0%),Ⅳ期4例(0.7%)。根据肿瘤分型、分期确定治疗方案。治疗方案经多学科会诊讨论,与患者及家属充分沟通后确定。本研究中VPL主要适用于肿瘤位于一侧声带或涉及前联合(T1);一侧声带稍涉及声门上和声门下结构(T2);一侧声带涉及声门旁间隙(T3);术前评估支撑喉镜下喉部结构暴露较差的患者。手术切除范围向下不涉及环状软骨,向上不涉及杓会厌襞,保证足够的安全切缘,并送检切缘组织。缺损修复采取甲状软骨膜或颈前带状肌筋膜。术前根据TNM分期和增强CT结果显示颈部是否有可疑淋巴结转移决定淋巴结清扫术,本组7例患者接受根治性颈部淋巴结清扫,30例接受功能性颈部淋巴结清扫术。根据原发肿瘤侵犯的解剖结构范围、颈部淋巴结转移的情况以及术后病理结果,决定术后是否行放/化疗。适应证包括:手术切缘小于5 mm,切缘肿瘤阳性,N2或N3淋巴结病变,淋巴结侵犯包膜外、神经和血管癌栓。
1.2.2 术后康复 术后予以鼻饲饮食,1周后评估颈部和喉部情况,如无异常开始先固体食物(面包、香蕉、馒头)训练试吃,再半流质饮食,最后流质饮食,如饮水无异常则拔鼻饲管出院。3个术后康复时间段的定义为①经口进食时间:从手术以后到开始训练经口进食的时间;②进食训练时间:从开始训练经口进食到进食流质无呛咳并拔除鼻饲管时间;③术后康复时间:从手术以后到出院的时间段。
1.3 统计学分析
数据录入建库和分析采用SPSS 23.0软件统计。组间差异性采用t检验,Chi-Squareχ2检验和Kruskal-Wallis秩和检验。各组间的生存率的比较采用Kaplan-Meier检验,组间差异性比较采用Log Rank法。分析本组患者预后的指标包括总生存率(overall survival,OS)和无病生存率(disease free survival,DFS)。OS定义时间范围为患者手术后至任何原因死亡;DFS定义时间范围为患者手术后至原发灶复发,颈部淋巴结转移,远处转移或死亡。3、5、10年的OS和DFS均采用寿命表法计算。利用Cox模型排除混杂因素评价影响声门型喉癌患者生存指标的危险因素,计算风险比(hazard ratio, HR)和95%的置信区间(confidence interval, CI)。P<0.05为差异具有统计学意义。
2 结果
2.1 手术治疗
本组患者为声门型喉癌接受VPL为主的治疗,临床变量见表1。术后病理确诊肿瘤切缘阳性21例(3.8%),切缘<5 mm 42例(7.7%)。67例患者术后接受辅助治疗,平均放疗剂量为(66.0±3.7)Gy。
2.2 术后康复
患者平均经口进食时间为(9.7±1.7)d,平均进食训练时间为(1.1±0.8)d;平均术后康复时间为(12.7±2.3)d。颈前气管切开造口处门诊随访喉镜检查黏膜无水肿则连续堵管48 h,如无呼吸困难则拔管蝶形胶布封口或局麻下缝合造口。鼻饲管拔管率为100%。
2.3 并发症处理
术后近期并发症包括出血1例(0.2%),切口感染4例(0.7%),肺炎2例(0.4%),通过及时止血,抗炎后恢复。远期并发症包括喉部肉芽肿56例(10.2%)通过CO2激光切除,喉狭窄20例(3.6%)需再次行气管切开术。
2.4 复发转移处理
术后原发灶复发21例(3.8%),颈部淋巴结转移13例(2.4%),远处转移2例(0.4%),同时出现局部和颈部转移7例(1.3%)。原发灶复发予以全喉切除术,颈部淋巴结转移予以根治性颈部淋巴结清扫术15例(2.7%)和改良根治性颈部淋巴结清扫术5例(0.9%),2例患者挽救性手术后辅以放化疗(0.4%),远处转移至综合性医院治疗。
2.5 生存率
本组548例患者的3、5、10年OS分别为:96.5%,92.1%和83.3%。3、5、10年的DFS分别为:93.2%,88.0%和79.6%。不同组别患者的3、5、10年的OS和DFS具体数据见表2。

表1 本组548例声门型喉癌患者的临床信息 [例
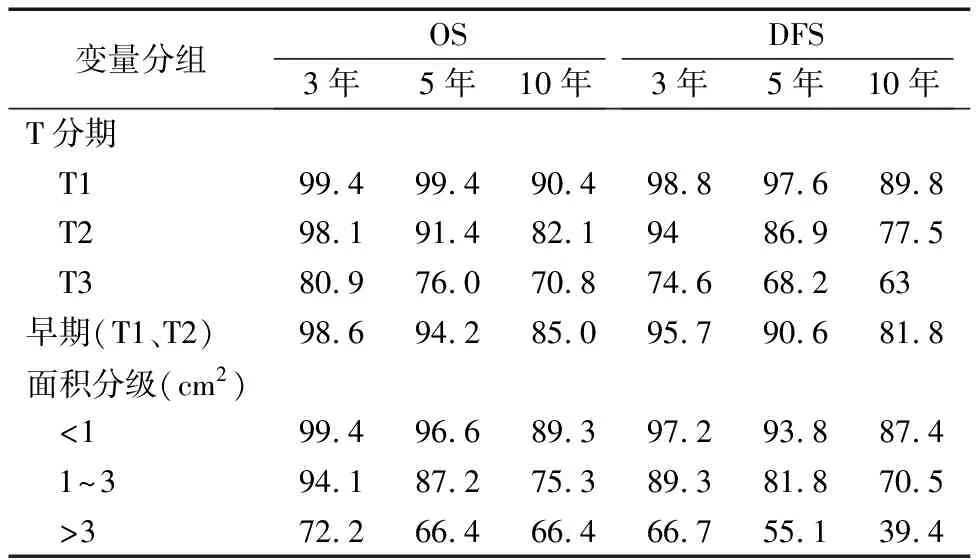
表2 不同分组患者的OS和DFS (%)
2.6 临床变量分析
与T1期比较,T分期较晚患者的OS和DFS降低(P<0.001)(图1)。采用肿瘤面积评价声门型喉癌的实体肿瘤大小,与较小肿瘤面积组比较,较大肿瘤面积患者的OS和DFS降低(P<0.001)(图1)。与N0期比较,伴有颈部淋巴结转移(N1、N2)患者的OS降低(P=0.03)。临床早期(Ⅰ、Ⅱ)患者的生存率优于晚期(Ⅲ、Ⅳ)患者(图2)。T1期89.9%的患者肿瘤面积≤1 cm2。在T2期和T3期内分析3组肿瘤面积患者的生存率,因T2期肿瘤面积>3 cm2的患者6例,组间统计分析OS时结果产生偏移,仅列出<1 cm2和1~3 cm2两组患者的数据发现肿瘤面积较大患者的OS和DFS较差(P<0.001)(图3)。
2.7 影响预后的因素
采用Cox模型系统的分析影响本组患者生存率的变量。单因素分析发现T分期、年龄大于70岁、较大肿瘤面积、N+是影响预后的因素,颈部淋巴结转移(N1、N2)是影响OS的危险因素(HR=2.89,95%CI[1.06-7.88],P=0.038),但多因素分析无统计学意义。通过多因素回归模型分析发现较晚的T分期、年龄>70岁、较大肿瘤面积是影响OS和DFS的危险因素(表3)。
3 讨论
喉癌威胁患者的生命,影响发音、呼吸、吞咽功能,降低生活质量。近年喉癌治疗的方案取得进展并逐渐在国内医院规范化。对于手术治疗,主张完整切除肿瘤的同时尽量保留喉功能,在不降低生存率的前提下,提高患者术后的生活质量。VPL能够完整切除肿瘤的同时保留喉功能,具有较理想的临床疗效。
对于早期声门型喉癌,可选择经口CO2激光、放疗、手术,这些治疗方案的肿瘤学疗效无明显差异[5-7]。CO2激光治疗早期声门型喉癌,5年生存率达92.6%[5]。国际上CO2激光治疗喉癌的5年OS范围为84%~92%,根治性放疗的5年OS范围为79%~91%,两种治疗方案的2年OS均可达到100%,但CO2激光治疗的患者术后生存率和保喉率可能要优于根治性放疗[8]。目前国内早期喉癌选择根治性放疗的患者较少。对于支撑喉镜下肿瘤暴露差,病变侵犯一侧声带,前联合和喉旁间隙的病例,可考虑开放性手术VPL,该术切除肿瘤后可根据解剖结构缺损,利用甲状软骨膜、颈前带状肌膜瓣等进行修复,重建喉功能。保留喉功能的开放性手术治疗喉癌,术后5年OS和DFS分别为89.3%和83.9%,这些方案适用于我国早期喉癌患者,且术者易操作,临床上可广泛推广[6,9]。近期研究报道VPL治疗T1b期声门型喉癌患者的术后5年OS为97.4%,5年喉功能保留率为94.8%,认为涉及前联合的声门型喉癌采用VPL,具有良好的临床效果[10]。本组数据的T1期声门型喉癌的5年OS和DFS分别为99.4%和97.6%,与国外报道数据相似,综合国内、外数据认为VPL的临床疗效较理想。
开放性喉癌手术的术后并发症包括出血、感染、肉芽肿和喉狭窄等。术后24 h内出血常为术中止血不彻底,环甲动脉或喉上动脉出血,以及气管造口处血管和气管筒反复摩擦破裂出血。术腔感染少见,可为关闭术腔时颈前带状肌漏缝,痰液分泌物渗入术腔,形成喉瘘,术中置引流管可显著降低感染。有研究认为VPL术后不置鼻饲管能明显促进患者的康复,术后采用全静脉营养,第3天即可开始进食训练,患者无明显呛咳和感染,可缩短气管造口处堵管时间和住院时间,提高生活质量[11],而本组患者术后均置鼻饲管。本中心目前的原则是鼻饲1周左右开始训练经口进食,开放性手术引起咽喉黏膜水肿,早期进食和拔除鼻饲管刺激加重局部炎症,黏膜水肿导致局部感觉迟钝引起食物误呛导致肺炎可能。因VPL保留了双侧杓状软骨、杓会皱襞、会厌等结构,对吞咽功能影响较小,1周后患者训练1~2 d即可正常进食。部分患者术后喉肉芽肿可在堵

表3 Cox模型分析影响OS和DFS的危险因素
管后经口鼻气流冲击而逐渐缩小,严重者可行CO2激光切除。对于喉狭窄,可考虑气管切开后激光切除瘢痕再置T型硅胶管置10个月左右取出,也可考虑喉裂开肌皮瓣前壁加宽等方案解决[12]。
研究报道影响喉癌预后的因素包括T分期,N分期,病理分期,复发转移,高龄,吸烟、饮酒和HPV病毒感染等[13-15]。崔捷等[14]通过多因素分析发现年龄>65岁、T分期、N+、术后原发灶/造瘘口复发、术后颈淋巴结复发是影响声门型喉癌患者生存率的独立危险因素。宋小霞等[15]通过多因素分析发现年龄>60岁、复发、临床分期明显降低患者的生存率。我们通过回归模型排除混杂因素后发现影响本组喉癌患者生存率的因素包括T分期较晚、较大肿瘤面积和高龄。本研究将50~70岁年龄段以10年分段细化分组,发现年龄>70岁是影响预后因素,临床医生在术后帮助患者康复时要注意高龄患者感染肺炎的可能,术前胸部CT平扫评估肺部情况,包括慢性肺炎、肺大泡、支气管扩张等基础疾病,这些基础疾病术中也可能影响全身麻醉实施。此外,本研究认为术后病理肿瘤面积是影响预后的危险因素,既往T分期是没有考虑实体肿瘤体积的因素,本组数据发现肿瘤面积越大的患者OS和DFS下降,在同一T分期患者中,肿瘤体积越大的患者OS和DFS下降。因此,临床医生在判断患者预后的时候,可考虑既往研究和本中心报道的这些因素,实现更加精确的随访和预防。
总结,VPL主要针对T1、T2期声门型喉癌,和肿瘤侵犯声门旁间隙的T3病变,术前评估切除范围不会涉及环状软骨和杓会厌襞,不影响喉功能的重建。本研究系统的分析了T1、T2和经选择的部分T3期声门型喉癌患者接受VPL的远期临床疗效,发现T分期越晚,肿瘤体积越大和高龄是影响患者生存率的危险因素。该手术方案具有理想的远期生存率和术后生活质量,患者术后并发症较少,通过规范术式操作,可进行广泛的临床推广应用。
