中药丹参及其制剂心宁片丹参素质量控制研究
2023-04-11岳玲燕邓竹君涂雨佳何桂英
岳玲燕 龙 平 邓竹君 涂雨佳 陈 可 何桂英
太极集团四川绵阳制药有限公司,四川绵阳 621000
丹 参(salviae miltiorrhizaeradixet rhizoma) 来源于唇形科植物丹参Salvia miltiorrhizaBge.的干燥根和根茎[1],其具有活血祛瘀,通经止痛,清心除烦,凉血消痈的功效[2]。长期以来主要靠人工栽培,山东为道地产区,其次四川中江、河北、安徽、山西、陕西亦有栽培[3]。《中华人民共和国药典》2020年版丹参质量控制只有丹参酮类和丹酚酸B两类成分[1],丹参素作为丹参药材的重要组成成分,在丹参类药物制剂中应用广泛[4],比如临床上用于冠心病、心绞痛等症[5-8]的心宁片,其质量标准要求对丹参素含量进行控制,但该处方中君药丹参并未对丹参素进行质量控制及检验方法介绍[9],且该制剂检测丹参素方法较复杂,所以通过本试验研究出一种适合中药丹参及心宁片中丹参素检测方法,用于指导心宁片生产非常有必要,为心宁片工艺生产提供参考依据,有效控制心宁片中丹参素的质量,从而保障心宁片产品质量的均一性。
1 材料与方法
1.1 试药试剂
对照品丹参素钠(批号:110855-201915,含量以97.8%计)购于中国食品药品检定研究院;色谱级甲醇购自百灵威化学技术有限公司;分析级甲醇、乙醇、盐酸、醋酸、氢氧化钠均购自成都市科隆化学品有限公司;水为屈臣氏蒸馏水,购自广州屈臣氏食品饮料有限公司。丹参药材样品采收于河北丰润、亳州谯城、山东莒县、山东临朐,且均为栽培品,经绵阳市食品药品检验所魏云主任中药师鉴定为正品。心宁片样品收集于生产企业A、B,规格均为0.4 mg/片(糖衣片)。
1.2 仪器
Agilent1260型高效液相色谱仪(安捷伦科技有限公司),MSA6.6S-CE型微量电子天平(sartorius)、ME204E型电子天平[梅特勒-托利多仪器(上海)有限公司],YR-500A型多功能粉碎机(永康市五瑞工贸有限公司)等。
2 方法与结果
2.1 色谱条件及系统适用性试验
迪马 C18为填充柱(150 mm×4.6 mm,5 μm);以甲醇-0.6%的醋酸溶液(5∶95)为流动相;检测波长为280 nm;流速为1 ml/min;柱温25℃。理论板数按丹参素钠峰计算应不低于3000。
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取丹参素钠对照品10.62、12.00 mg,分别置10 ml的量瓶中,加甲醇适量溶解,再加甲醇至刻度,摇匀,分别制成质量浓度为1.0386、1.1736 mg/ml的对照品溶液储备液。
2.2.2 供试品溶液的制备 (1)取丹参粉(过二号筛)约2.5 g,精密称定,置具塞锥形瓶中,精密加水60 ml,称定重量,加热回流2.5 h,放冷,再称定重量,用水补足减失的重量,摇匀,用 0.45 μm 微孔滤膜滤过,取续滤液,作为丹参供试品溶液。(2)取心宁片20片,除去包衣研细,取约1.0 g,精密称定,同上法操作,制成心宁片供试品溶液。
2.2.3 阴性样品溶液的制备 按2.2.2项下方法,制备阴性样品溶液。
2.3 方法学考察
2.3.1 专属性试验 取2.2.1项下对照品溶液储备液(浓度 1.1736 mg/ml)1 ml,置 10 ml量瓶中,加甲醇至刻度,摇匀,制成对照品溶液,再分别取2.2.2、2.2.3项下供试品溶液、阴性样品溶液,按2.1项下色谱条件测定,进样量10 μl,测定结果阴性样品溶液对测定成分无干扰,专属性良好。见图1~4。

图1 对照品溶液色谱图
图2 阴性样品溶液色谱图

图3 丹参供试品溶液色谱图

图4 心宁片供试品溶液色谱图
2.3.2 线性关系考察 精密吸取2.2.1项下对照品溶液储备液(浓度1.0386 mg/ml)1 ml,分别置5、10、20、25、50 ml量瓶中,加甲醇至刻度,摇匀,制成不同质量浓度对照品溶液,按2.1项下色谱条件依次进样10 μl,记录色谱图峰面积,以峰面积为纵坐标,对照品溶液浓度为横坐标,绘制标准曲线,结果显示丹参素钠的线性回归方程Y=6.768 61×103X-32.770 21,线性范围0.020 77~0.207 73 mg/ml,相关系数R2=0.999 95,丹参素钠在浓度范围内与其峰面积呈现良好的线性关系。见图5。

图5 峰面积与对照品溶液浓度的线性标准曲线
2.3.3 精密度试验 精密吸取丹参素钠对照品溶液(浓度 0.1039 mg/ml)10 μl,按 2.1 项下色谱条件连续进样6次,记录峰面积,相对标准偏差(relative standard deviation,RSD)=0.50%,n=6,表明仪器精密度良好。
2.3.4 重复性试验 取同一丹参样品、心宁片样品,按2.2.2项下方法分别平行制备6份供试品溶液,按2.1项下色谱条件依次检测,计算含量,丹参和心宁片中丹参素平均含量分别为 6.48、3.25 mg/g,RSD分别为0.78%、0.86%,表明该方法重复性良好。
2.3.5 稳定性试验 取同一供试品溶液,分别在0、2、4、8、12 h进行测定,记录峰面积并计算 RSD,结果丹参素钠峰面积RSD为1.60%,表明供试品溶液在制备后12 h内稳定。
2.3.6 加样回收率试验 精密称取已知含量的丹参药材供试品、心宁片供试品各9份,分别精密加入一定量丹参素钠对照品,按2.2.2中供试品溶液方法进行制备,分别进样,测定峰面积,计算回收率,丹参素钠的平均回收率分别为95.2%、93.4%,RSD分别为1.30%、1.93%,结果见表1~2。

表1 中药材丹参加样回收率试验结果

表2 心宁片加样回收率试验结果
2.3.7 样品测定 取9批丹参样品、6批心宁片样品,分别按2.2.2供试品溶液方法制备,进行丹参素含量测定并计算,结果见表3~4。
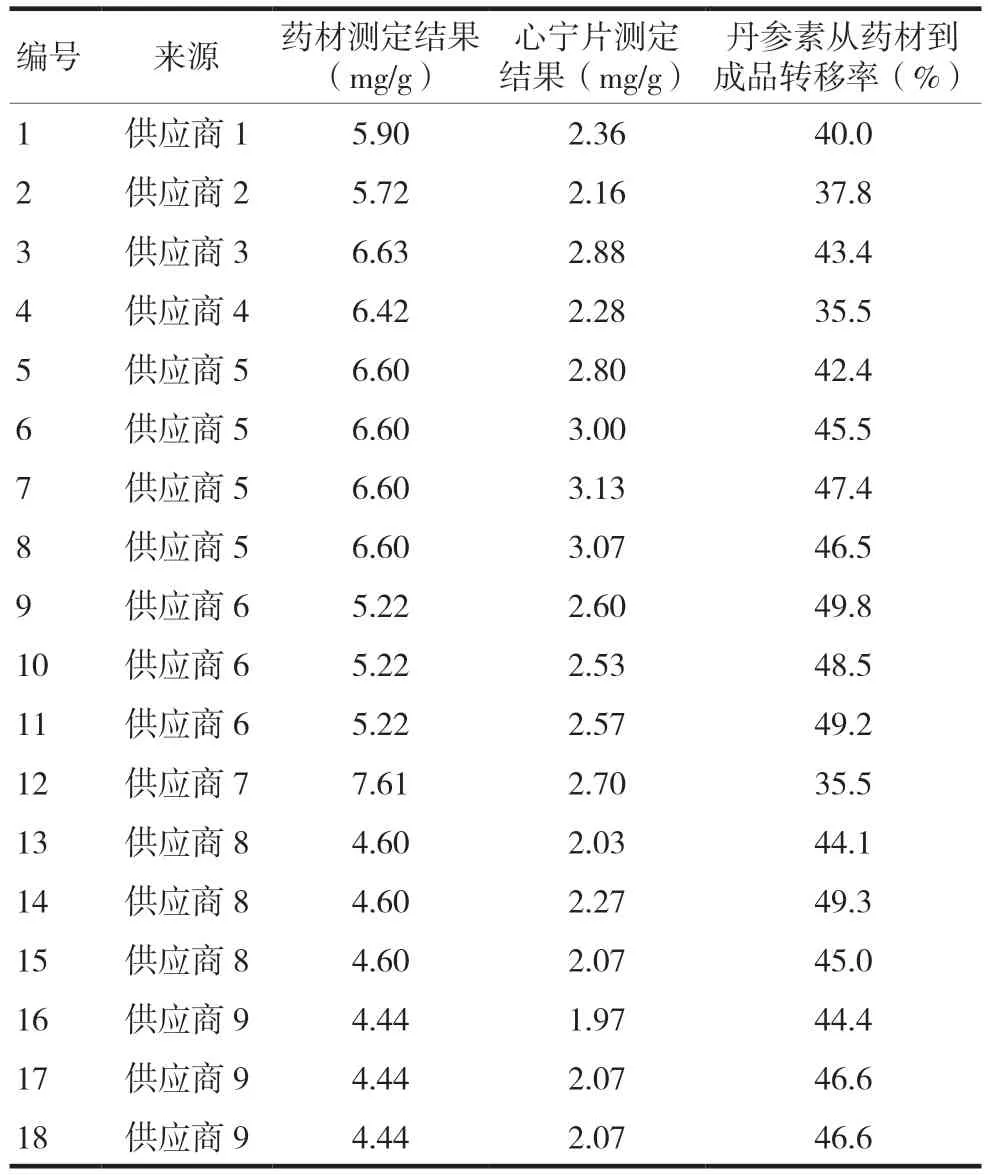
表3 不同批次丹参及对应心宁片中丹参素的含量

表4 不同批次心宁片两种方法测定丹参素含量结果比较(mg/g)
投料前对9批丹参药材进行丹参素含量测定,含量范围为4.44~7.61 mg/g,对应18批成品丹参素含量范围为1.97~3.07 mg/g,平均转移率为44.3%。通过以上数据结合心宁片质量标准计算,建议丹参含丹参素不得少于0.375%,更能保证心宁片丹参素含量符合质量标准要求。
对6批心宁片进行丹参素含量测定,本法含量范围为2.56~3.80 mg/g,药典方法含量范围为2.00~2.88 mg/g,可知本方法优于药典方法,可用于心宁片丹参素含量检测,有效控制其质量。
3 讨论
3.1 丹参素提取方式
试验分别采用了加碱回流提取、加水回流提取、水提醇沉提取和加水超声提取四种方法,结果表明加水回流提取所得丹参素含量最高,效果最佳。结合心宁片生产中丹参药材提取方式,加水回流提取更符合心宁片生产工艺要求。
查阅丹参中丹参素测定的文献[10-13],多数文献只研究丹参药材丹参素含量测定,并未结合实际生产,涉及丹参的中成药质量标准,制法项多采用加水提取方式,较少采用超声提取和水提醇沉提取方式,可能是因为大生产考虑生产成本及可操作性。
3.2 丹参素的提取时间
试验摸索1、2、2.5和3 h加水回流提取时间,结果表明2.5 h加水回流提取所测定的丹参素含量最高,所以确定2.5 h为最佳提取时间。
3.3 丹参素测定色谱条件
试验摸索了检测波长为 278、279、280、281、282、283 nm的色谱条件,结果表明280 nm条件下供试品的吸收强度最大,故确定280 nm为最佳检测波长。
根据文献资料[9,14]对丹参素的检测方法比较,流动相多为一定比例的甲醇与醋酸溶液。本实验对流动相甲醇-冰醋酸-二甲基甲酰胺-水[15](2∶1∶2∶95)和甲醇-0.6%的醋酸溶液(5∶95)进行对比考察,结果表明后者检测出的色谱峰无杂质峰干扰,故选择甲醇-0.6%的醋酸溶液(5∶95)为测定流动相。
试验对35、30、25℃三个柱温条件进行了考察,结果表明柱温25℃时色谱峰峰型最好,故确定柱温为25℃。
3.4 丹参素提取溶剂
文献显示[14],在丹参药材中,丹参素以丹参素钠的形式存在,是丹参水溶性成分中的主要药效成分之一,结合心宁片生产中丹参的提取工艺,确定本研究提取溶剂为水。
4 结论
综上所述,本法测定结果准确,重复性好、灵敏度高,与其他研究文献比较不足在于回流提取时间较长。通过同一检测方法控制丹参及心宁片丹参素质量,从源头把关追踪溯源,确保心宁片丹参素含量达到《中华人民共和国药典》标准要求。
