不同乳基婴幼儿配方乳粉的理化性质和表面组成
2023-04-06尹乾隆高文浩王筱迪滕翔宇
李 萌,尹乾隆,高文浩,王筱迪,滕翔宇,2,刘 宁,2,*
(1.东北农业大学食品学院,乳品科学教育部重点实验室,黑龙江 哈尔滨 150030;2.哈尔滨腾凝科技有限公司,黑龙江 哈尔滨 150030)
婴儿配方乳粉被定义为一种可以模拟母乳[1],并可以完全或部分替代母乳的婴儿食品[2]。一般来说,婴幼儿配方乳粉主要通过平衡宏量营养素(蛋白质、脂肪和碳水化合物)和微量营养素(维生素和矿物质)制备。婴幼儿配方乳粉的成分因婴儿及幼儿生长发育阶段而异[3],第1阶段产品适用于0~6 月龄的婴儿,第2阶段产品适用于6~12 月龄的儿童,第3阶段产品适用于1 周岁以上的儿童。不同阶段婴幼儿配方乳粉成分的组成往往会影响其配方在加工、贮存和运输过程中的物理及化学稳定性。
制备婴幼儿配方乳粉时,通常先将乳液与原料和配料混合均匀,再经均质、剪切、浓缩、喷雾干燥制成。乳液的形成和稳定通常由蛋白质作为主要乳化剂实现,特别是油包水型乳液[4]。蛋白质对粉末的物理性质具有决定作用。在婴幼儿配方乳粉制备过程中,均质过程中脂肪球受湍流、空化和气泡影响[5],会被破坏形成新的脂肪球,并被酪蛋白和乳清蛋白重新吸附达到稳定状态;蒸发浓缩过程中,空洞引起的大量水蒸气蒸发是造成脂肪球破裂的最可能原因[6];而喷雾干燥阶段的高温使浓缩物中的水分被迅速蒸发,干物质聚集形成粉末颗粒。与蛋白质和乳糖相比,脂肪由于液滴较大,输送速率慢,造成了脂肪在粉末表面比例较高[7]。乳糖作为粉末表面的另一主要成分,在一般状态下呈非晶态玻璃状,但易受周围环境影响。在低于玻璃化转变温度(glass transition temperature,Tg)时,乳糖分子的流动性非常稳定,不会发生明显变化[8]。在高于Tg的条件下,乳糖分子的流动性随着基质黏度的降低而增加,导致其重新配置成高度有序的晶体结构,新形成的乳糖结晶会破坏脂肪球使其产生更多的游离脂肪[9]。当配方乳粉中脂肪丰富时,蛋白质桥接脂肪球状簇形成[10],并一定程度影响粉末的复合溶解度。
近年来,羊乳婴幼儿配方乳粉越来越受欢迎,并呈现一定规模。羊乳与牛乳相比,乳清蛋白含量较高,酪蛋白含量较低,且酪蛋白中β-酪蛋白含量较高,羊乳脂肪酸构成中短链脂肪酸含量较高,这些特点表明羊乳较牛乳更宜作为母乳替代品,更有利于婴幼儿消化、吸收和促进婴幼儿生长发育[11-12]。然而,对羊乳婴幼儿配方乳粉理化性质及表面成分的研究却很少,主要集中于牛乳婴幼儿配方乳粉蛋白质和碳水化合物等理化性质的报道。因此,本实验对羊乳婴幼儿配方乳粉的理化性质及表面成分进行研究,并与牛乳婴幼儿配方乳粉进行比较分析,以期为羊乳婴幼儿配方乳粉的加工和生产提供理论支持。
1 材料与方法
1.1 材料与试剂
羊乳和牛乳婴幼儿乳粉均购自哈尔滨当地超市,为相同厂址的同一品牌乳粉,贮藏时间(检测时间-生产时间)均小于1 个月,包装标示主要成分见表1。1段、2段和3段羊乳和牛乳婴幼儿乳粉分别记作G1、G2、G3和C1、C2、C3。
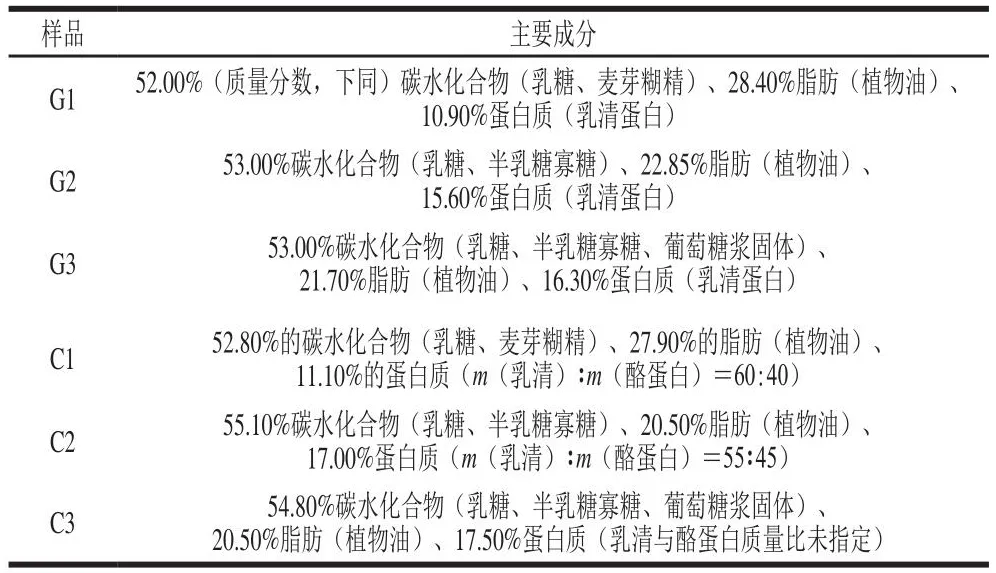
表1 婴幼儿配方奶粉的主要成分Table 1 Major ingredients of infant formula
十二烷基硫酸钠聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electropheresis,SDSPAGE)凝胶配制试剂盒 上海碧云天生物技术有限公司;水杨酸甲酯 美国Nu-Chek-Prep公司;甲醇(色谱纯) 美国Fisher Scientific公司;氯仿、硫酸、正己烷均为色谱纯。
1.2 仪器与设备
BSA124S-CW分析天平 德国Sartorius公司;HX204水分分析仪 瑞士Mettler Toledo公司;AquaLab 4TE水分活度计 美国AquaLab公司;Thermo Plus EVO TG-DTA差示扫描量热(differential scanning calorimetry,DSC)仪 日本Nippon Neoku公司;SmartLab SEX射线衍射仪 日本Rigaku公司;恒温磁力搅拌器 上海梅颖浦仪器仪表制造有限公司;YS3010色度分光光度计深圳市三辉创电子有限公司;Nexsa X射线光电子能谱(X-ray photoelectron spectroscopy,XPS)仪美国Thermo Fisher Scientific公司;7000D三重四极杆气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)仪 美国Agilent公司;S-3400N扫描电子显微镜 日本Hitachi公司;全自动多功能X射线衍射仪(X-ray diffractomer,XRD) 日本Shimadzu公司。
1.3 方法
1.3.1 水分质量分数和水分活度测定
称量2.0~2.5 g样品,放入铝托盘中,采用由水分分析仪测定样品水分质量分数。使用水分活度计测定水分活度(aw)。
1.3.2 玻璃化转变温度的测定
采用DSC仪测定婴幼儿配方乳粉Tg。将5~15 mg粉末样品装入样品盘,密封在坩埚中,以空坩埚作为对照,高纯氮气为载气(50 mL/h)。参照Kelly等[13]的方法进行加热和冷却,0 ℃平衡,以5 ℃/min从0 ℃加热到100 ℃,然后以10 ℃/min冷却到0 ℃,再以5 ℃/min升温至到120 ℃,在最后的加热步骤中测定Tg。
1.3.3 乳糖结晶度的测定
使用XRD仪在Cu Kα辐射下测定样品乳糖结晶度。将1~2 g粉末样品装入样品容器中,然后以0.02°为步长,从6°扫描至90°,测定结晶部分的衍射强度。采用DIFFRAC.Eva软件(4.2版)分析衍射强度谱。
1.3.4 溶解度的测定
在室温下,将5 g婴幼儿配方乳粉粉末溶解于95 mL水中,用磁力搅拌器(500 r/min)搅拌1 h。将溶液静置15 min,然后将其转移到预先称质量的离心管中,1 000 r/min离心5 min,以分离不溶性物质。去除奶油层后,氮气连续进入离心管,去除残留水分,直至离心管质量不变。溶解度按式(1)计算。
1.3.5 色度的测定
采用色度计测定样品的亮度(L*)值和黄度(b*)值。测定前,仪器采用标准参考板(L*=96.90、a*=0.21、b*=1.93)进行校准。
1.3.6 蛋白、脂肪、碳水化合物和灰分质量分数的测定
采用凯氏定氮法测定乳粉中的蛋白质量分数。脂肪质量分数采用国际标准ISO 488—2008《牛奶 脂肪含量的测定 Gerber乳脂计》测定。按照Masum等[14]的马弗炉高温燃烧法测定粉体灰分质量分数。碳水化合物质量分数通过100%减去蛋白质和脂肪质量分数计算得到[15]。
1.3.7 蛋白质组成分析
采用SDS-PAGE对不同乳基婴幼儿配方乳粉中蛋白质进行鉴定。在还原条件下,用4%~15%的预制聚丙烯酰胺凝胶进行电泳。将12 μL 3 mg/mL样品溶液与12 μL溴苯酚蓝混合,在100 ℃下加热5 min,冷却至环境温度(25 ℃)待测。将加热后的10 μL样品溶液和5 μL Marker分别加载到预制凝胶上。SDS-PAGE条件:12%分离胶、5%浓缩胶,浓缩凝胶和分离凝胶分别在80 V和120 V恒压电泳1 h。电泳完成后用考马斯亮蓝R-250染料溶液在恒温振动筛(40 r/min)上染色2 h。随后,定时更换去污液以去除污渍。用凝胶成像系统分析电泳条带。
1.3.8 X射线光电子能谱测量表面成分
由于乳粉粉末表面几乎被恒定成分(蛋白质、乳糖和脂肪)所覆盖,这3 种主要物质由碳、氮和氧组成,因此利用XPS分析样品表面碳、氮和氧的相对组成。采用热K-alpha源,粉末样品用双面胶带固定在硅废料上,以确定粉末表面(~10 nm)的相对原子组成[16]。在检测时,环境温度25 ℃、相对湿度40%,操作程序按Gaiani等[17]的方法,以1 eV和50 ms停留时间为单位进行扫描。利用式(2)~(4)分别计算表面蛋白、乳糖和脂肪的相对含量[17]。
式中:IC、IO、IN分别为样品中测得的碳、氧和氮的相对含量/%;αP、α’L、α”F分别为样品中的蛋白、乳糖和脂肪的相对含量/%;ICp、ICL、ICF分别为标准品(酪蛋白、无水乳脂和一水乳糖)中蛋白、乳糖和脂肪的碳元素相对含量/%;IOp、IOL、IOF分别为标准品(酪蛋白、无水乳脂和一水乳糖)中蛋白、乳糖和脂肪的氧元素相对含量/%;INp、INL、INF分别为标准品(酪蛋白、无水乳脂和一水乳糖)中蛋白、乳糖和脂肪的氮元素相对含量/%。
1.3.9 表面游离脂肪提取及脂肪酸测定
按照Tham等[18]的方法并略作修改,提取表面游离脂肪。将3 g婴幼儿配方乳粉放置于装有滤纸(Whatman 4)的玻璃漏斗中,用5 mL正己烷沿滤纸边缘滴加洗涤,洗涤5 次,间隔15 s。收集约25 mL的滤液于玻璃培养皿中,并放置在通风柜中蒸发有机溶剂,将玻璃培养皿在60 ℃烤箱中烘干,直至质量稳定。玻璃培养皿质量增加量与样品质量之比为婴幼儿配方乳粉表面游离脂肪酸的质量分数。
采用GB 5009.168—2016《食品安全国家标准 食品中脂肪酸的测定》中改进的乙酰氯-甲醇法分析样品表面和总脂肪酸组成。表面脂肪酸按上述方法提取,然后用乙酰氯-甲醇进行甲基化。检测总脂肪酸时,婴幼儿配方乳粉直接进行甲基化。将甲酯化样品与一定量的水杨酸甲酯混合,作为GC-MS的内标。注射体积为1 µL,分流比为1∶30。样品采用配备火焰离子化检测器的GC-MS仪和DB-5MS极性柱(30 m×0.25 mm,0.25 µm)进行检测。GC-MS条件:初始温度50 ℃,以10 ℃/min升至220 ℃,维持20 min;载气为氦气,流速1.1 mL/min;入口温度280 ℃,离子源温度230 ℃;电子电离源,电子能量70 eV。
1.3.10 扫描电子显微镜观察粉末表面微观形貌
参考Huang Shan等[19]的方法用配备钨丝的场发射扫描电子显微镜分析粉末的表面形貌。粉末样品通过将粉末安装在碳黏接片上制备,在18 mA下溅射镀金60 s,在30 kV加速电压下检测,获得不同放大倍数的图像,观察粉末表面形貌。
1.4 数据处理与分析
所有实验均做3 次重复,所得结果以平均值±标准差表示,使用SPSS 26.0软件进行统计分析,采用Student’sttest进行显著性分析,P<0.05为显著差异。用Origin Pro 2019b 9.6.5.169软件作图。
2 结果与分析
2.1 不同乳基婴幼儿配方乳粉的理化性质
2.1.1 不同乳基婴幼儿配方乳粉的水分质量分数和aw
水分质量分数和aw是影响婴幼儿配方粉稳定的关键因素。如图1A所示,两种乳基婴幼儿配方乳粉的水分质量分数差异显著(P<0.05),羊乳婴幼儿配方乳粉整体水分质量分数较低,说明羊乳基比牛乳基对降低配方乳粉中水分质量分数更为有利。如图1B所示,两种乳基婴幼儿配方乳粉的aw与水分质量分数呈相同的变化趋势,即水分质量分数越高,aw越高。具有较高水分质量分数和aw的婴幼儿配方乳粉更易出现无定形乳糖吸湿产生结块的现象,导致粉末氧化变质速率加快,促进美拉德反应[20],与Cheng Hong等[21]的研究结果一致。
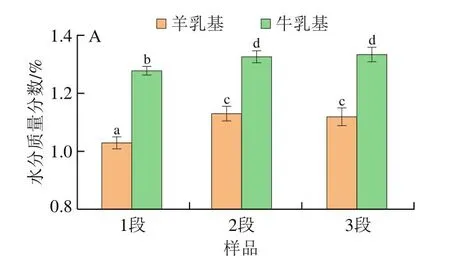
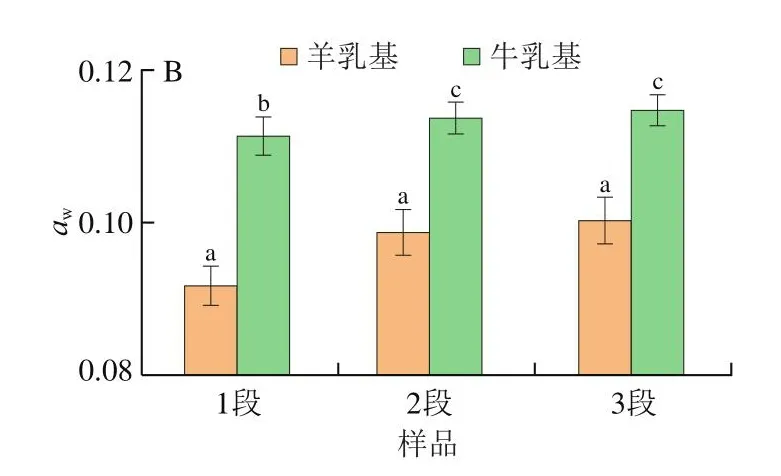
图1 不同乳基婴幼儿配方乳粉的水分质量分数(A)和aw(B)Fig.1 Water content (A) and water activity (B) of infant formula
2.1.2 不同乳基婴幼儿配方乳粉的玻璃化转变温度
Tg是无定形乳糖由“亚稳定”玻璃化状态向橡胶化状态转变的温度,是乳粉结块的重要指标。DSC曲线在80 ℃左右开始出现下降时由仪器对下降曲线作切线,切点温度即为Tg。由图2A可知,羊乳婴幼儿配方粉各阶段Tg均显著高于牛乳样品(P<0.05),且羊乳和牛乳配方乳粉均为1段Tg高于2段和3段。羊乳婴幼儿配方乳粉Tg整体高于牛乳婴幼儿配方乳粉可能与aw相关,aw越低,Tg越高,这与Tham等[22]的研究结果一致。此外,先前的研究也报道了部分结晶的乳清粉中乳糖的结晶被延迟[23],这是由于蛋白质的存在,这些蛋白质在分子水平上影响乳糖-乳糖相互作用,进而影响玻璃化转变,所以Tg在样品间表现出的差异也可能是因为蛋白组成不同。而两组样品均表现为1段较2段和3段Tg高的原因可能归结为麦芽糊精的存在,在相同条件下含有麦芽糊精的婴幼儿配方乳粉Tg会高于不含麦芽糊精的婴幼儿配方乳粉[24]。以往研究认为Tg对粉末的稳定性有显著影响[25]。Tg越低,粉末的分子流动性越大,黏度越低,有利于乳糖的结晶。随着乳糖结晶的形成,粉末容易变质,美拉德反应加剧,表面游离脂肪增加,出现粉末团聚。Tg越高,乳糖结晶发生越晚,乳粉稳定性越好。由于羊乳婴幼儿配方乳粉的Tg较高,乳糖结晶的发生较牛乳乳粉延迟,从而使羊乳婴幼儿配方乳粉在贮存过程中较牛乳婴幼儿配方乳粉更稳定。
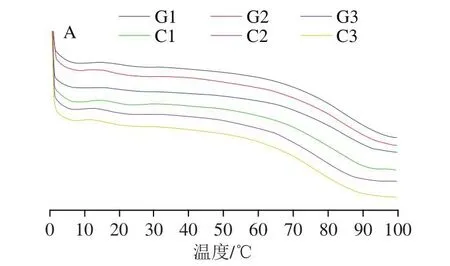
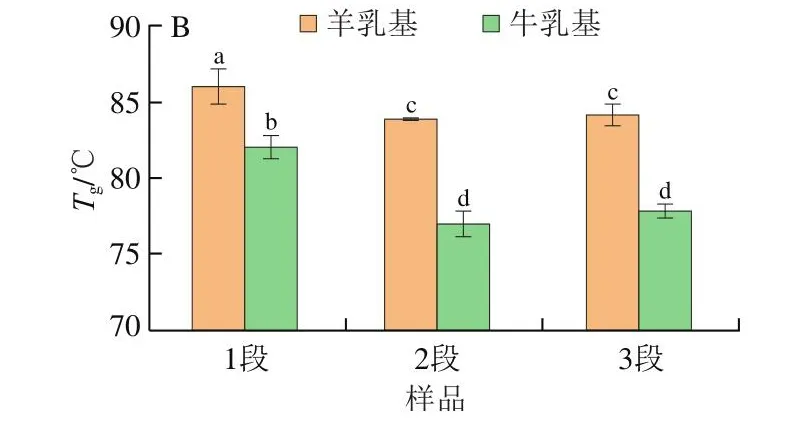
图2 不同乳基婴幼儿配方乳粉的DSC曲线(A)和Tg(B)Fig.2 DSC curve (A) and Tg (B) of infant formula powders made from different milks
2.1.3 不同乳基婴幼儿配方乳粉的乳糖结晶度和溶解度
研究发现,α-乳糖一水合物和无水α∶β乳糖晶体(物质的量比5∶3)结晶峰的特征峰分别在19.1°和20.1°处[22,26],用峰值高度量化乳糖的结晶度。本研究中所有配方粉中均没有检测到显著的结晶峰。如图3A显示,所有粉末的结晶度均无显著差异(P>0.05),表明婴幼儿配方乳粉粉末中乳糖均以无定形状态存在,没有明显的结晶,说明不同来源的乳基对配方乳粉的乳糖结晶度没有影响。如图3B所示,婴幼儿配方乳粉的溶解度在92%~95%范围内,两种乳基婴幼儿配方乳粉均表现出1段配方乳粉溶解度显著大于2段和3段配方乳粉(P<0.05),2段和3段间无显著差异(P>0.05)。产生这种现象的原因可能是1段配方乳粉中含有麦芽糊精,2段和3段配方乳粉的成分和乳糖结晶度相似导致其溶解度差异不显著[27]。
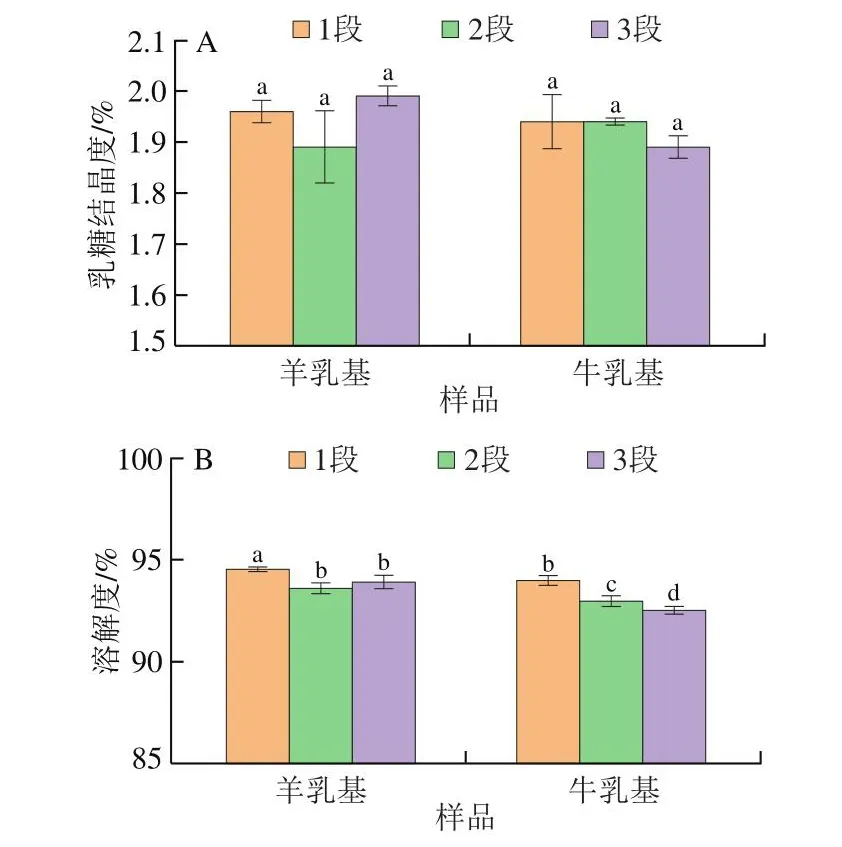
图3 不同乳基婴幼儿配方乳粉的乳糖结晶度(A)和溶解度(B)Fig.3 Lactose crystallinity (A) and solubility (B) of infant formula
2.1.4 不同乳基婴幼儿配方乳粉的色度
配方粉的颜色变化作为美拉德反应的伴随反应,能够反映美拉德反应的进程。如图4A所示,除3段羊乳婴幼儿配方乳粉外,其余样品L*值均差异不显著(P>0.05)。如图4B所示,b*值在各婴幼儿配方乳粉中差异显著(P<0.05),较高的b*值表明发生美拉德反应的可能性更大。羊乳婴幼儿配方乳粉的b*值在各阶段均显著低于牛乳婴幼儿配方乳粉(P<0.05),这与aw变化趋势一致。Cheng Hong等[21]研究证明,aw对婴儿配方乳粉的褐变至关重要,在aw较高时,乳糖更容易吸收水分并结晶,进一步促进美拉德反应,使乳粉黄色加深。
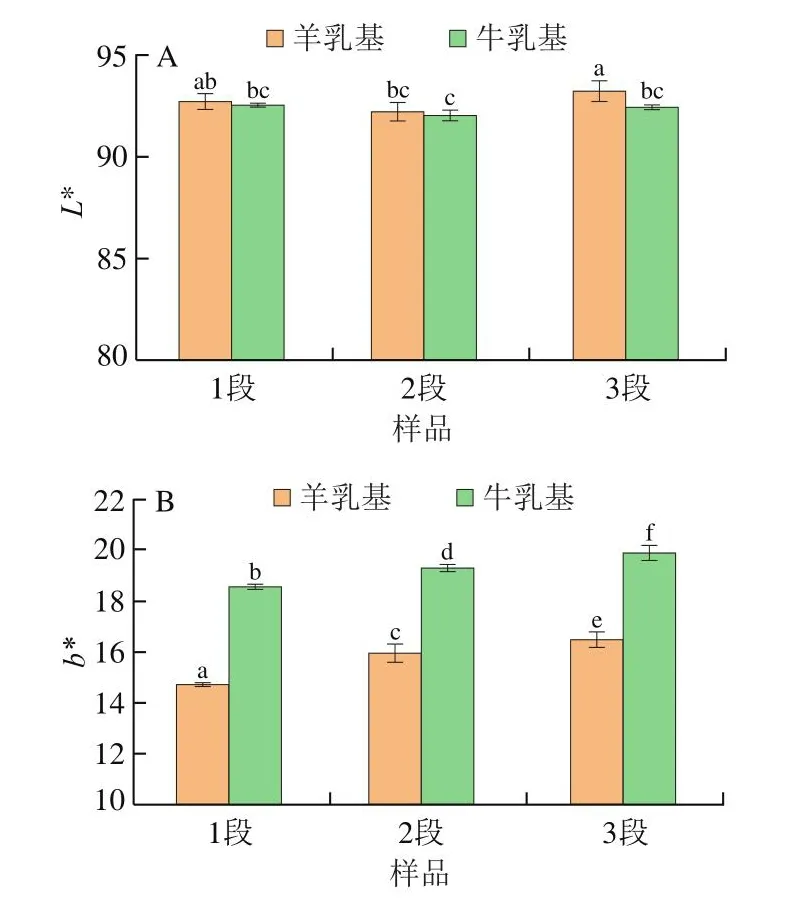
图4 不同乳基婴幼儿配方乳粉的色度Fig.4 Color parameters of infant formula made from different milks
2.2 不同乳基婴幼儿配方乳粉的表面组成和总体组成
2.2.1 不同乳基婴幼儿配方乳粉的化学组成
如表1所示,在相同阶段,牛乳婴幼儿配方乳粉蛋白质量分数在略高于羊乳婴幼儿配方乳粉,两者脂肪、碳水化合物和灰分质量分数无明显差异;随着阶段的改变,2段和3段羊乳与牛乳婴幼儿配方乳粉的蛋白质量分数明显高于1段,而脂肪质量分数较低,碳水化合物及灰分质量分数未发生明显改变。
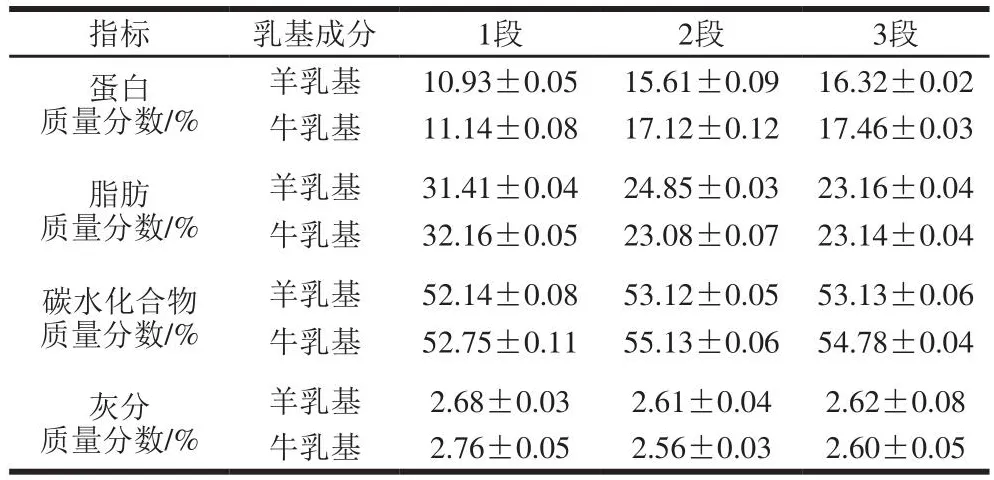
表1 不同乳基婴幼儿配方乳粉的组成Table 1 Composition of goat and cow milk infant formula
2.2.2 不同乳基婴幼儿配方乳粉的蛋白质成分特性
如图5所示,不同乳基婴幼儿配方乳粉中乳清蛋白组成无显著差异,而酪蛋白组成有明显不同,在羊乳婴幼儿配方乳粉中发现了较多的β-酪蛋白。在乳液的蒸发浓缩和均质过程中,蛋白质优先吸附在新形成的脂肪球表面,使乳液形成稳定的体系,因此在制备粉末时,油相应稳定在粉体内部,尽量减少向表面迁移,防止造成粉末发生严重的物理和化学变化。不同蛋白质组成对吸附性能有影响,乳清蛋白主要由α-乳白蛋白和β-乳球蛋白组成[28],α-乳清蛋白和β-乳球蛋白虽然同样能吸附在脂肪表面,但在含有β-酪蛋白的体系中,β-酪蛋白会优先吸附在脂肪表面形成较为稳定的结构[4,29-30]。研究发现,在均质过程中,酪蛋白胶束比乳清蛋白更容易吸附在脂肪界面[31]。Ye Aiqian等[6]研究也发现,蒸发过程中脂肪小球表面的酪蛋白含量显著增加,而乳清蛋白含量增加相对较少。蛋白质包覆于脂肪小球表面形成颗粒,提高脂肪小球颗粒稳定性,从而减缓后期粉末颗粒性能变差。因此,不同乳基婴幼儿配方乳粉中酪蛋白的差异可能对乳粉的表面脂肪组成和游离脂肪含量有决定性影响。
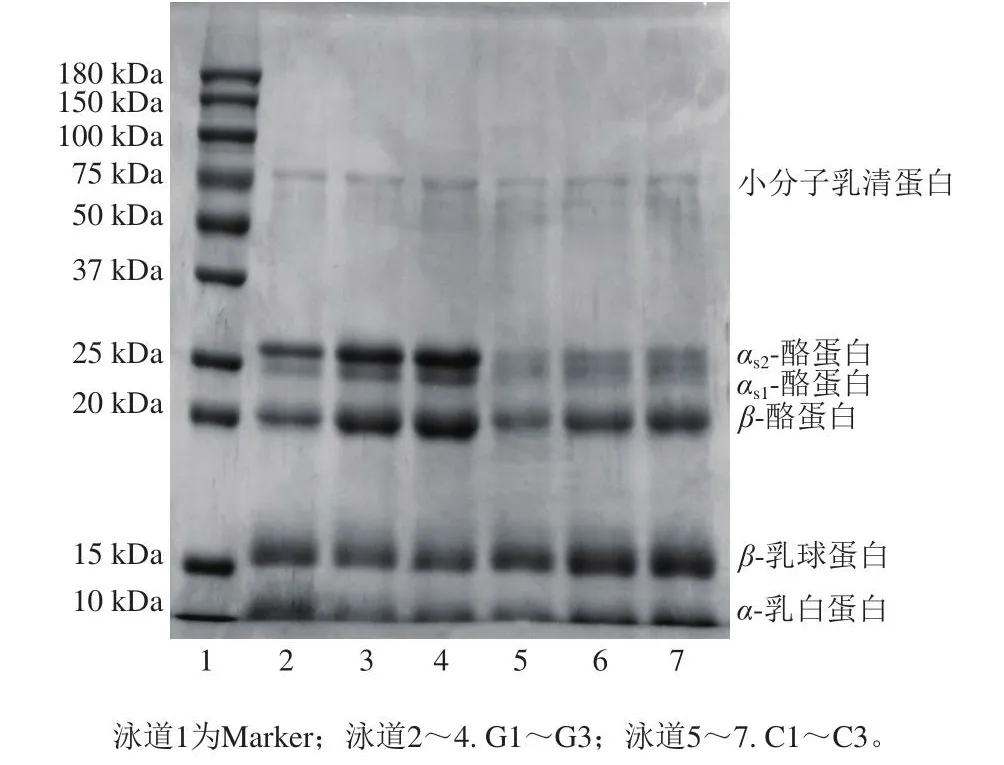
图5 不同乳基婴幼儿配方乳粉的还原型SDS-PAGE图谱Fig.5 Reducing SDS-PAGE patterns of infant formula powders made from different milks
2.2.3 不同乳基婴幼儿配方乳粉的表面成分分析
粉末的表面组成对颗粒的团聚、脂肪氧化和溶解性有重要意义。如图6所示,颗粒表面成分主要为脂肪(>50%),其次为乳糖(>20%)和蛋白质(11%~18%)。乳粉颗粒表面脂肪相对含量过高通常是喷淋过程中乳脂组分迁移速率不同造成的,高分子质量组分的扩散系数较小,其向中心的迁移速率较慢,与其他成分相比,脂肪的分子质量较小,迁移速率较快,因此脂肪在颗粒的表面堆积。受乳组分迁移速率的影响,其他组分在总体组成和表面组成上也存在差异,尤其是乳粉中乳糖在总体组分中的相对含量约为50%(表1),而表面组成中乳糖相对含量仅约为20%。早期研究已有关于颗粒表面成分和总体成分差异的报道[32-33]。不同乳基婴幼儿配方乳粉的表面脂肪相对含量存在显著差异,不同阶段羊乳婴幼儿配方乳粉的表面脂肪相对含量均显著低于牛乳婴幼儿配方乳粉(P<0.05)。婴幼儿配方乳粉表面存在大量脂肪,使粉末颗粒黏度改变,易形成团聚[34]。表面脂肪相对含量的增加也会增加乳粉的氧化酸败敏感性[35]。与牛乳婴幼儿配方乳粉相比,羊乳婴幼儿配方乳粉具有显著较低的表面脂肪相对含量和显著较高的表面乳糖相对含量。本实验中各配方乳粉乳糖均处于无定形状态,粉末表面被无定形乳糖所覆盖会阻止内部脂肪向外迁移,这与羊乳婴幼儿配方乳粉较低的表面脂肪相对含量相互印证。
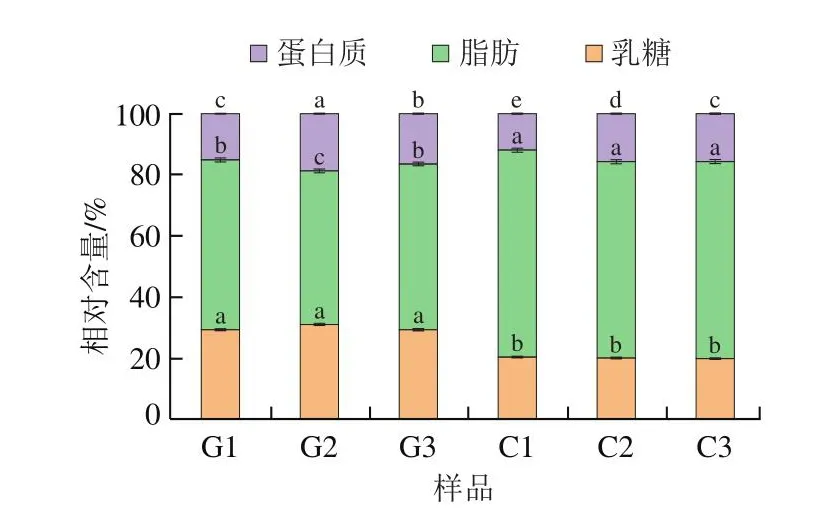
图6 不同乳基婴幼儿配方乳粉的表面成分Fig.6 Surface composition of infant formula made from different milks
2.2.4 不同乳基婴幼儿配方乳粉的游离脂肪酸组成
由图7可知,不同乳基婴幼儿配方乳粉中提取的表面游离脂肪质量分数具有显著差异(P<0.05)。羊乳婴幼儿配方乳粉的表面游离脂肪酸质量分数显著低于牛乳婴幼儿配方乳粉(P<0.05)。而造成这种差异的原因是不同乳基婴幼儿配方乳粉蛋白组成不同,导致颗粒稳定性不同。羊乳婴幼儿配方乳粉中β-酪蛋白含量较高,β-酪蛋白优先吸附在脂肪球表面,使释放到表面的脂肪量较少。
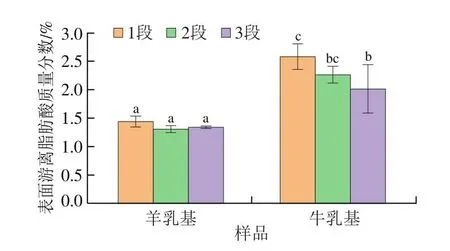
图7 不同乳基婴幼儿配方乳粉的表面游离脂肪酸质量分数Fig.7 Surface free fatty acid composition of infant formula powders made from different milks
使用GC-MS分析牛乳与羊乳婴幼儿配方乳粉总脂肪酸和表面游离脂肪酸组成,如表2所示,与总脂肪酸组成相比,表面游离脂肪酸中饱和脂肪酸(月桂酸(C12:0)、肉豆蔻酸(C14:0)、棕榈酸(C16:0)和硬脂酸(C18:0))相对含量较高;在总脂肪酸中不饱和脂肪酸含量较高,特别是油酸(C18:1)和亚油酸(C18:2)[35],这一现象可能与颗粒表面蛋白的相互作用有关[36],此外,由于脂肪酸之间形成了共晶相,也可能与共晶相中的分子相互作用有关[37]。与羊乳婴幼儿配方乳粉相比,牛乳婴幼儿配方乳粉表面游离脂肪酸中含有较多的不饱和脂肪酸,特别是油酸(C18:1);不饱和脂肪酸的存在使配方乳粉粉末更易被氧化,导致在贮存过程中产生异味[38],且不饱和脂肪酸熔化温度较低,易与脂肪酸链桥接产生结块[39]。该结果说明羊乳婴幼儿配方乳粉较牛乳婴幼儿配方乳粉稳定性更好。
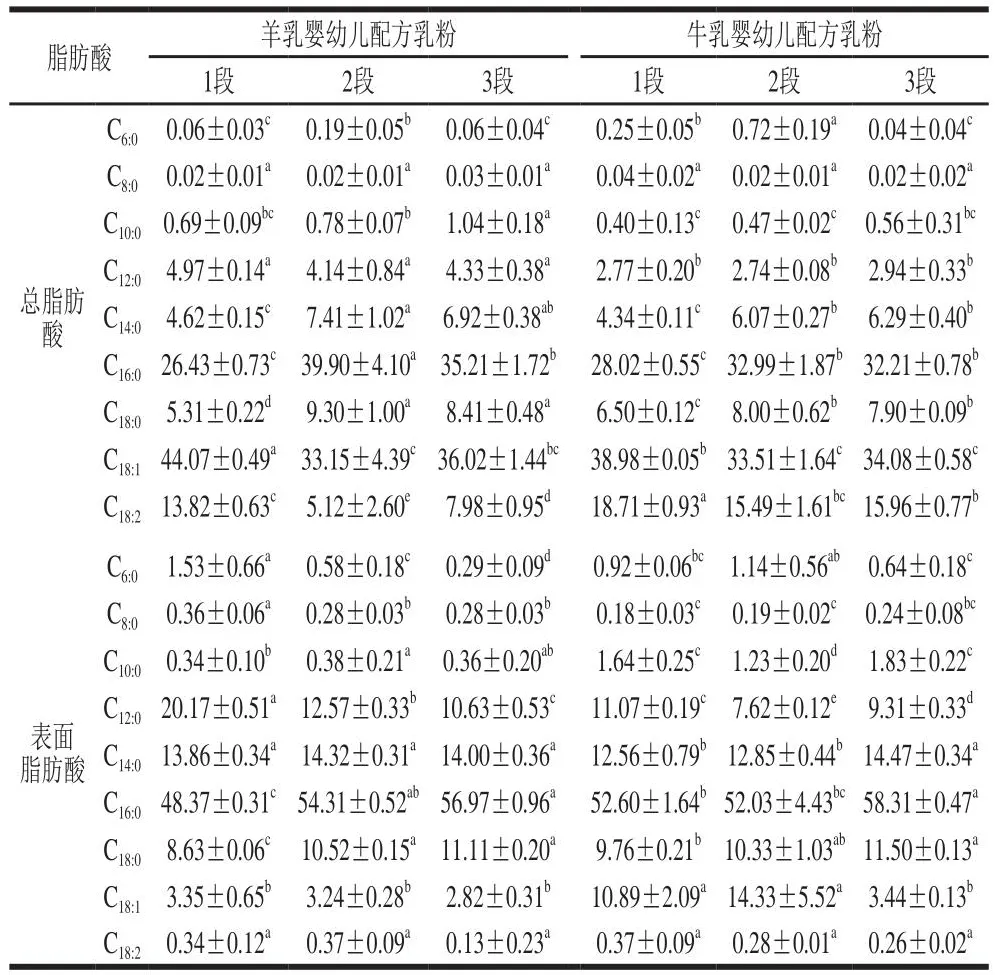
表2 不同乳基婴幼儿配方乳粉的总脂肪酸和表面游离脂肪酸组成及相对含量Table 2 Fatty acid composition of total fat and surface free fat in goat and cow milk infant formula%
2.2.5 不同乳基婴幼儿配方乳粉表面微观形貌
如图8所示,羊乳婴幼儿配方乳粉中,与2段和3段样品相比,1段样品颗粒更团聚。而牛乳婴幼儿配方乳粉1段和3段样品较2段样品中颗粒更团聚。牛乳婴幼儿配方乳粉的颗粒总体较羊乳婴幼儿配方乳粉更团聚、更致密。这可能是由于牛乳婴幼儿配方乳粉具有较低的Tg和较高的表面游离脂肪质量分数。羊乳和牛乳婴幼儿配方乳粉不同阶段样品颗粒的表面微观形貌没有明显差异,但牛乳婴幼儿配方乳粉粉体颗粒表面的粗糙度明显高于羊乳婴幼儿配方乳粉。上述结果表明,羊乳婴幼儿配方乳粉低Tg和高表面脂肪质量分数有利于粉末团聚,而表面粗糙度较高是由于乳糖晶体的存在[40]。
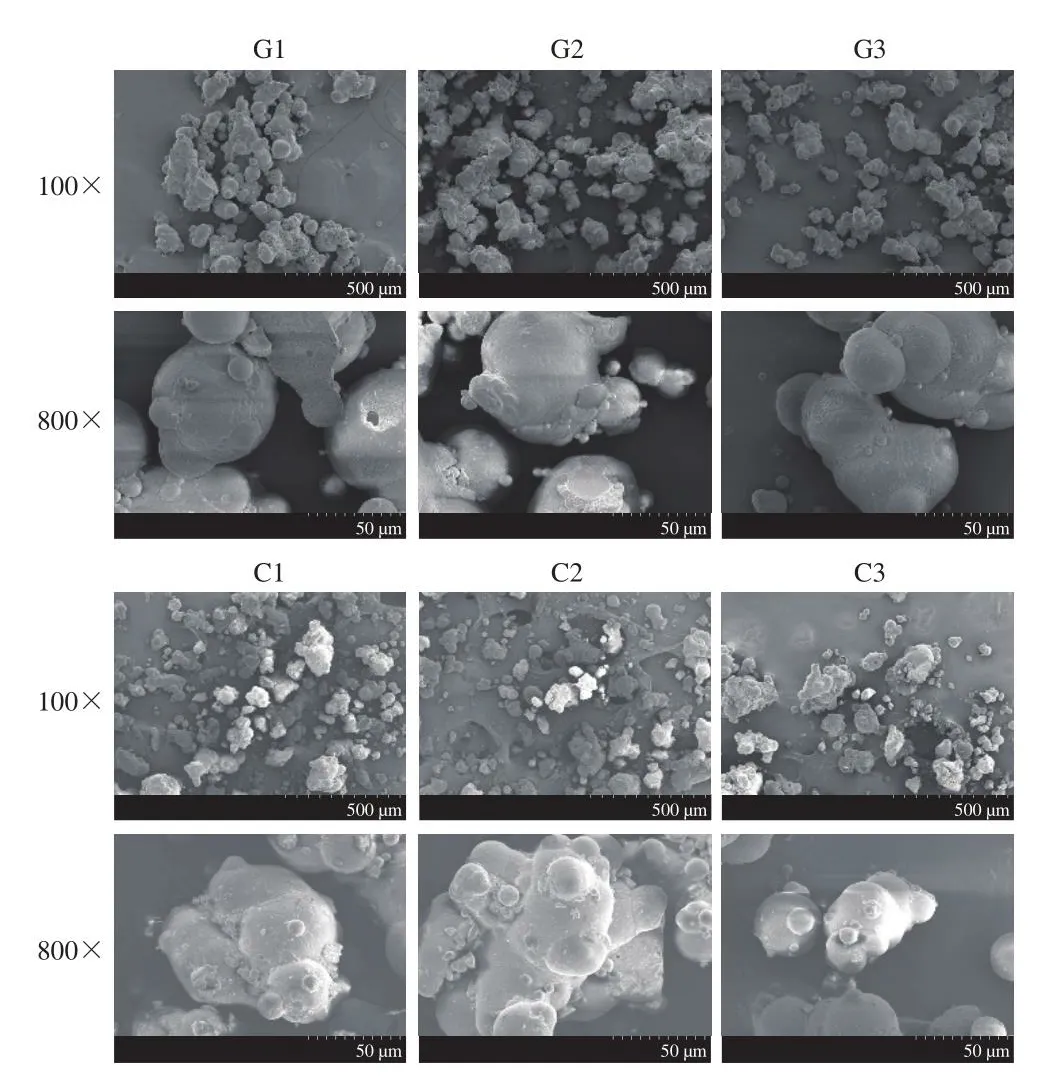
图8 不同乳基婴幼儿配方乳粉的表面微观形貌Fig.8 SEM images of goat and cow milk infant formula
3 结 论
羊乳婴幼儿配方乳粉与牛乳婴幼儿配方乳粉相比,水分质量分数和aw、b*值较低,Tg较高,说明与牛乳婴幼儿配方乳粉相比,羊乳婴幼儿配方乳粉理化性质较好。本研究中所有婴幼儿配方乳粉的乳糖结晶度相似且极低,表明乳基的不同对乳糖结晶度无影响。通过SDSPAGE分析发现,羊乳配方乳粉中β-酪蛋白含量较高,酪蛋白的含量差异影响了乳粉粉末表面成分的组成;XPS结果证实,羊乳婴幼儿配方乳粉具有较高的表面蛋白质相对含量以及较低的脂肪相对含量,表面游离脂肪酸质量分数也证实了这一趋势。通过GC-MS进一步分析表面游离脂肪酸和总脂肪酸组成,发现婴幼儿配方乳粉中均表现出表面游离脂肪酸饱和总脂肪酸相对含量较高,以油酸(C18:1)为代表的不饱和脂肪酸相对含量较低。通过SEM观察发现,与羊乳婴幼儿配方乳粉相比,牛乳婴幼儿配方乳粉由于表面脂肪含量较高,其粉末颗粒更团聚、更致密。这些发现将为开发基于羊乳的婴幼儿配方乳粉提供较好的理论指导,有助于生产更稳定的羊乳配方乳粉。
