乳腺癌和鼻咽癌病人子器官剂量评估方法辅助放疗调强计划的优化
2023-03-25李静毅具天波
周 平,杨 蕾,詹 翔,李静毅,具天波,詹 希
1.西南医科大学附属医院 放射科(泸州646000);2.西南医科大学附属医院 肿瘤科(泸州646000);3.西南医科大学 护理学院(泸州 646000)
放射治疗现已成为癌症综合治疗的重要组成部分。50%~70%肿瘤病人的治疗手段包括放射疗法,其已成为治愈癌症的主要治疗方法[1-3]。调强放疗(intensity modulated radiotherapy,IMRT)技术提高了肿瘤区域剂量,有效保护正常组织,提高病人的生活质量[4-7]。在现阶段IMRT 计划的制作过程中,计划质量很大程度取决于医务人员的个人经验,制作稳定的高质量IMRT计划仍是物理师和医师所面临的挑战[8]。对于不同病人,其肿瘤浸润生长与危及器官(organ at risk,OAR)的解剖结构不同,如何优化放疗计划,与病人个体化的解剖结构紧密相关[9-10]。由于乳腺癌及鼻咽癌癌肿特殊的解剖结构关系和肿瘤生物学行为特点,IMRT成为了临床应用广泛的治疗方式。从大数据中总结出适合IMRT计划个体化的经验,由这些经验提供的客观数据对临床计划进行评估与权衡极为重要[11-12]。本研究充分考虑到IMRT 计划剂量分布与OAR 和靶区之间的特殊几何结构关系,试图在现有计划系统的基础上利用一种全新的方法来评价IMRT 计划中OAR 的剂量,以减少人为经验误差对计划质量的影响,从而提高放疗计划质量。
1 对象与方法
1.1 病例选择及一般资料
回顾性分析西南医科大学附属医院肿瘤科2017年1月至2018年12月接受IMRT治疗的乳腺癌保乳术后(n=19)与鼻咽癌病人(n=55)的放疗计划资料,与病人签署相关知情同意书,以乳腺癌保乳术后病人的患侧肺以及鼻咽癌病人的内耳、口腔、腮腺、喉、环后区咽、食管等OAR 进行研究。其中乳腺癌不同分期的病例数为:I期5例,II期14例;鼻咽癌不同分期的病例数为:II期3例,III期39例,IV期13例。
1.2 纳入与排除标准
乳腺癌组纳入标准:①女性,年龄18~70 岁;②按照2017 年国际抗癌联盟(Union for International Cancer Control,UICC)公布的第8 版分期标准分期为Tis,T1~2N0M0 期的早期乳腺癌保乳术后病人;③病理确诊为导管原位癌、浸润性导管癌;④切缘阴性;⑤美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分0~1分。
鼻咽癌组纳入标准:①年龄18~70 岁;②病理组织或细胞学确诊为鼻咽癌;③根据2017年美国癌症联合委员会(American Joint Committee on Cancer,AJCC)第8 版标准分期为T2-4/N0-4M0 期;④病人为首程治疗;⑤ECOG评分0~1分。
排除标准:①妊娠、哺乳期妇女;②育龄期男女拒绝采用合适的避孕措施;③合并多器官、系统严重病症及精神病病人;④合并有不受控制神经病变(2 级或以上)或精神病病人;⑤既往5年以内有恶性肿瘤病史并接受过放射治疗;⑥无法完成放射治疗或随访。
1.3 靶区及危及器官的勾画
乳腺癌:同一医师根据国际辐射单位和计量委员会(International Commission on Radiation Units and Measurements,ICRU)50 和62 号报告[13-14]勾画临床靶区(clinical target volume,CTV)包括可见的腺体组织以及参考定位时所作标记,根据术腔边界金属夹勾画瘤床区(gross tumor volume tumor bed,GTVtb)包括可见血清肿以及保乳术中钛夹位置。GTVtb 与CTV 外扩5 mm形成计划肿瘤靶区(planning gross tumor volume tumor bed,PGTVtb)与 计 划 靶 区(planning target volume,PTV),皮肤方向内缩0.3 cm。PGTVtb 处方剂量为60.00 Gy,单次剂量2.40 Gy ;PTV 处方剂量为50.00 Gy,单次剂量2.00 Gy。
鼻咽癌:根据2010 鼻咽癌调强放疗靶区及剂量设计指引专家共识[15],有五年临床经验的影像医师勾画出GTV和CTV,所有GTV与CTV外扩3 mm 形成PGTV与PTV,PGTV 处方剂量为70.00 Gy,单次剂量2.00~2.25Gy;PTV1 处方剂量为60.00~66.00 Gy,单次剂量1.80~2.05Gy;PTV2 处方剂量为50.96~56.00 Gy,单次剂量1.80 Gy。同时勾画出内耳、口腔、腮腺、喉、环后区咽、食管等OAR。
1.4 危及器官限制要求
不同危及器官的平均剂量见表1。

表1 不同危及器官的平均剂量比较Table 1 Comparison of average dose of different endangered organs.
1.5 调强计划设计
运用Pinnacle 9.10(Pinnacle3,version 9.10m,Philips Medical Systems)放疗计划平台,采用直接子野优化方法进行调强治疗计划设计。以乳腺癌保乳术后调强计划为例:在计划优化之前,利用计划平台脚本程序将PTV 外扩为宽度为0.5 cm 的n 个环,分别编号为ring 1~ring n。将ring1~ring n 与患侧肺相交区域分别编号为ring 1 ∩lung~ring n ∩lung,将该区域作为患侧肺独立的子器官(sub-lung)进行参数优化,其中ring 1 ∩lung定义为sub-lung 1,ring 2 ∩lung定义为sub-lung 2,以此类推。通过对各个病人子器官的等效均一计量(equivalent uniform dose)大小与权重的不断调整,在保证靶区处方剂量满足评估要求的前提下,使得患侧肺的吸收剂量尽量低,由于优化时子器官数量较多,其权重参数应调整到相对于靶区权重较小的值。
对于鼻咽癌由于所研究的OAR 体积较小,外扩环的宽度为0.3 cm。最后统计出病人各OAR子器官的归一化平均剂量(Dsub-OARmean/D 处方,其中Dsub-OARmean 为子器官的平均剂量,乳腺癌D 处方为PTV处方剂量,鼻咽癌D处方为PTV2的处方剂量)的均值。病人乳腺癌保乳术后患侧肺的子器官与鼻咽癌左侧内耳的子器官分别如图1与图2所示。
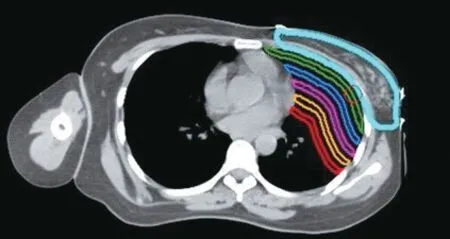
图1 某例乳腺癌保乳术后病人患侧肺的子器官设计Figure 1 Design of the sub-organs of the affected lung of a patient with breast cancer after breast-conserving surgery
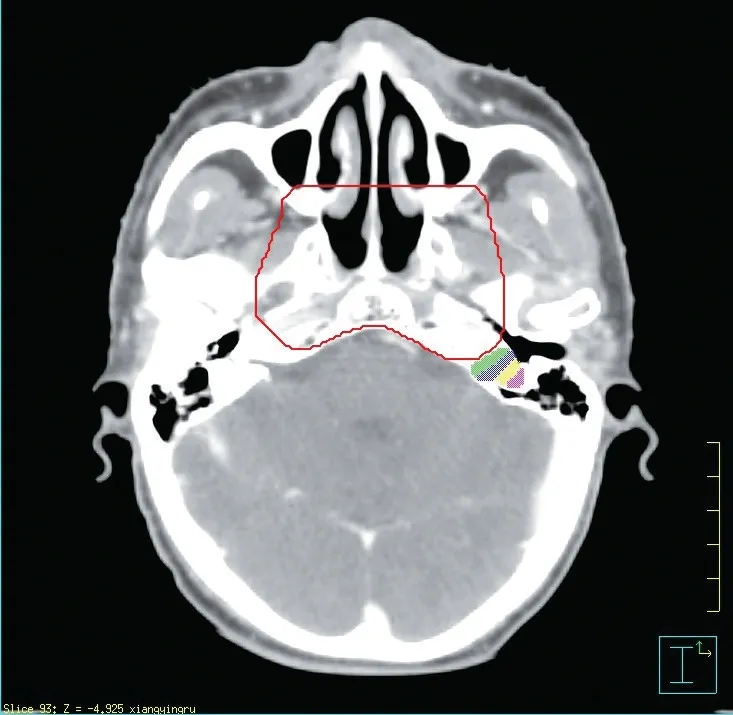
图2 某例鼻咽癌左侧内耳子器官设计Figure 2 Design of the sub-organs of the inner ear of a patient with nasopharyngeal carcinoma
1.6 数据拟合
从病人IMRT 治疗计划中寻找OAR 子器官平均剂量与其到靶区表面最短距离的相关因素,建立数学模型,利用matlab软件(R2017a)对相关数据进行拟合,得出公式。
1.7 统计学方法
采用SPSS 23.0软件对数据进行分析,计量资料用均数±标准差()表示,计数资料用频数(n)和百分比(%)表示。各个OAR 的体积和OAR 子器官平均剂量、OAR 子器官归一化平均剂量均值其到靶区表面最短距离均为正态分布的连续变量,采用Pearson法进行相关性分析,并给出相关系数r和P值,检验水准α=0.05,P<0.05为差异有统计学意义(双尾)。通过成组t检验对两组间均值差异性进行分析,P<0.05为差异有统计学意义。
2 结果
不同OAR 子器官平均剂量与OAR 体积之间无统计学意义相关性(Pearson 分析,P >0.05)。不同OAR各子器官的归一化平均剂量均值与其到靶区表面最短距离呈负相关性(Pearson 分析,P<0.01),其相关系数(r)见表2。病人各个危及器官子器官归一化平均剂量均值与各子器官到靶区表面最短距离轨迹图分别见表2、图3。
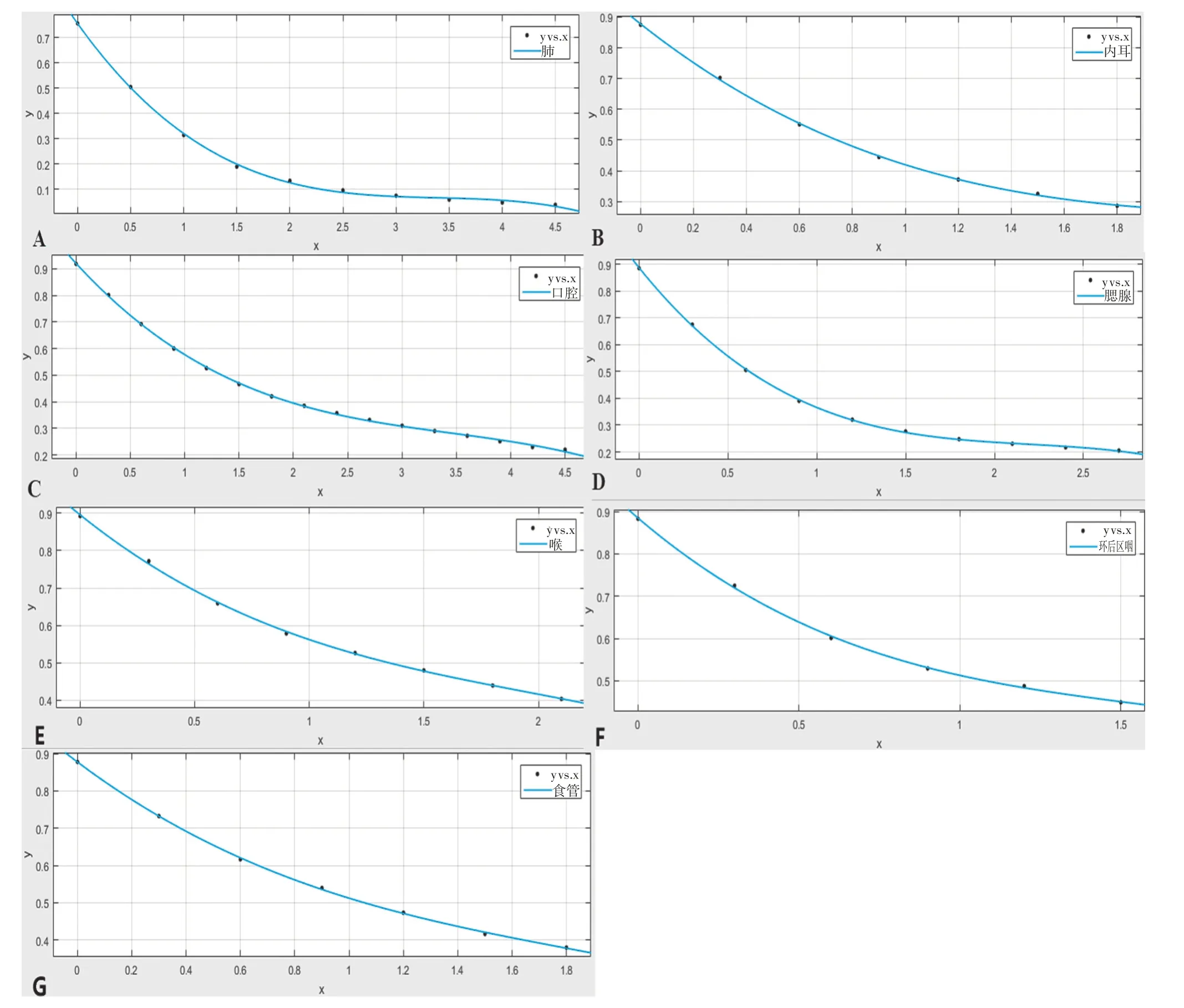
图3 不同危及器官子器官归一化平均剂量均值与各子器官到靶区表面最短距离轨迹图Figure 3 The average value of normalized mean dose of different OARs and the trajectory diagram of the shortest distance from each sub-organ to the surface of the target area
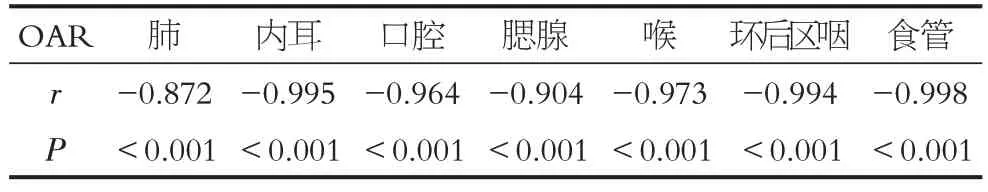
表2 不同QAR各子器官归一化平均剂量均值与各子器官到靶区表面最短距离的相关系数Table 2 Correlation coefficient between the normalized average dose of each sub-organ of different QAR and the shortest distance from each sub-organ to the surface of the target area
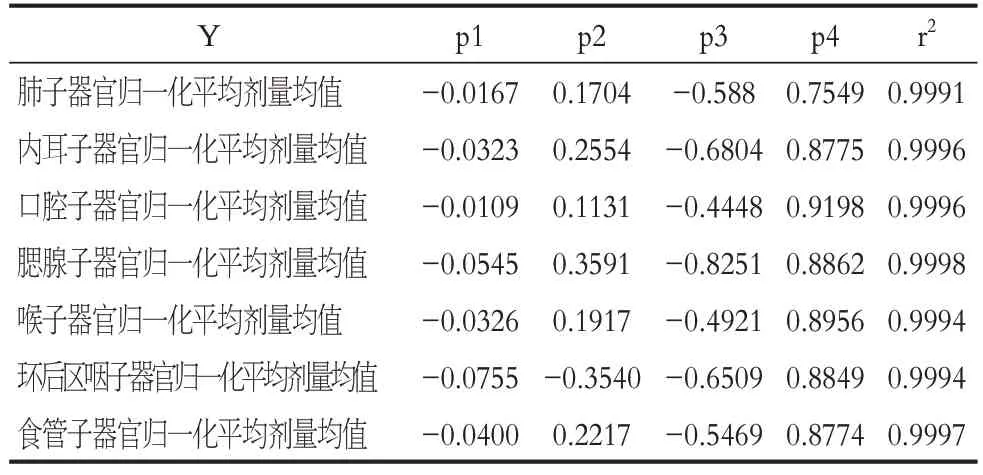
表3 权重因子与可决系数(r2)取值Table 3 The value of weight factor and coefficient of determination(r2)
3 讨论
IMRT 技术已经被广泛应用于鼻咽癌和乳腺癌保乳术后的临床治疗中[16-18],故本研究以乳腺癌保乳术后与鼻咽癌IMRT 计划为例,将OAR 分割为多个子器官,统计出不同OAR 子器官的归一化平均剂量均值。各子器官归一化平均剂量均值与各子器官到靶区表面最短距离呈负相关性,进而对各个OAR 子器官归一化平均剂量均值与各子器官到靶区表面最短距离轨迹图进行数据拟合得到相应拟合公式,在制作放疗计划前,可以通过拟合公式预测出子器官的平均剂量,对放疗计划进行质量控制,从可决系数(r2)均大于0.99 可知,拟合公式的拟合优度非常好。
在实际计划优化中,设定score=100×(1-δ),将score作为OAR子器官剂量评分标准,并将score阈值设定为90 分,将score 值低于90 分的子器官作为独立OAR 进行优化。将子器官作为独立OAR 优化时可采用uniform dose 作为优化条件,不断调节其大小与权重,在满足靶区处方评估条件前提下获得满意的score值,减少人为误差因素对调强放疗计划的影响,以获得更为精确的放射治疗计划。常规方法中,常常将OAR分割为多个子器官,较为繁琐且误差较大,但通过计划平台自带脚本程序可全自动化获得子器官,极大程度提高效率[19-21]。在实际优化中,也并不需要将所有的危及器官子器官都作为优化条件,选取其中一部分进行优化评估也可以显著改善危及器官剂量,从而节约优化时间。调强放疗中OAR 剂量评估方法是近年来研究的热点[22-27],本研究方法较为简单,在现有计划系统基础上即可完成,并不需要复杂的数学计算以及购买新的优化模块。
本研究局限性在于放疗计划是由单中心获得。在进一步的研究中,需要加入更多放疗中心、不同的放疗计划系统以及更大的数据采集组计划样本,建立放疗计划样本库,获得更为精确的OAR 子器官的归一化平均剂量均值。
4 结论
本研究提出了一种较简便的调强放疗计划OAR剂量评估的方法,并对其进行验证,减少调强放疗计划中人为主观因素对OAR 剂量的影响。本方法对不同调强计划系统、不同调强实现技术以及不同病种的OAR 剂量评估均适用,大多数放疗中心在现有调强计划系统与现有调强技术基础上即可应用到实际的调强优化计划中。
(利益冲突:无)
