桧木醇衍生物的合成及抑菌活性
2023-03-14叶久辉周海玉李婕宁冯俊涛高艳清马志卿
桂 阔, 叶久辉, 李 璇, 周海玉, 李婕宁,冯俊涛, 雷 鹏, 高艳清, 马志卿
(西北农林科技大学 植物保护学院,陕西省生物农药工程技术研究中心,陕西 杨凌 712100)
天然产物特有的结构和生物活性多样性,增强了其作为先导化合物进行新农药创制的可行性[1-2]。然而,天然产物具有分离困难、含量少、稳定性差等缺点,限制了其直接作为农药使用[2]。因此,选取具有一定活性的天然产物进行结构修饰与改造,是发现新型绿色农药先导化合物的重要途径[3]。以天然产物为先导开发的农用杀菌剂有很多,如嘧菌酯、咯菌腈、氟吗啉等,其中嘧菌酯是以杀菌天然活性化合物strobilurin A 为先导进行结构改造而发现的甲氧基丙烯酸酯类杀菌剂[4]。
桧木醇 (1,图式1) 是一种从柏科植物中提取的具有䓬酚酮骨架的单萜类天然化合物,具有广泛的生物活性,如抗癌[5]、抗炎[6]、抗病毒[7]、杀虫[8]和抗菌[9-11]等。此外,桧木醇具有较好的安全性,已应用于化妆品、食品和保健品等行业[12]。Wang 等报道了桧木醇能够有效地控制葡萄和苹果贮藏期的灰霉病[13]。Morita 等研究了桧木醇对大肠杆菌和金黄色葡萄球菌的抑菌作用机理,发现其能有效影响供试菌细胞膜的通透性和呼吸作用[14]。本课题组前期研究表明,桧木醇对炭疽病菌具有较好的抑制活性,可以控制香蕉在储存过程中炭疽病的发生[15]。为了发现结构简单、活性更高的绿色抑菌新分子,本研究以桧木醇为先导化合物,引入酯键或醚键,设计合成了17 个新型桧木醇衍生物3、5 和6 (合成路线见图式1),并测定了其对5 种植物病原菌的抑制活性。
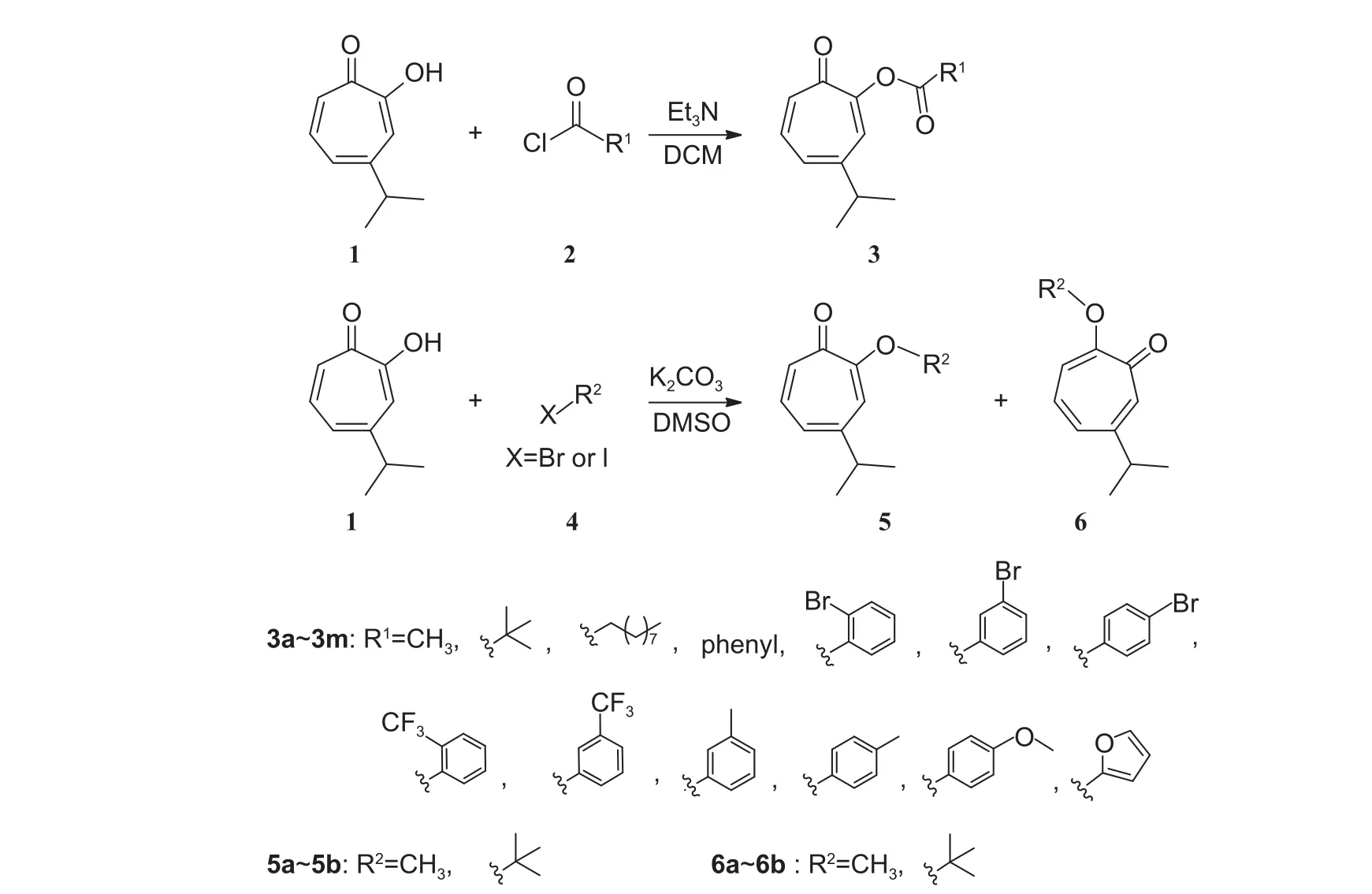
图式1 目标化合物的合成路线Scheme 1 Synthetic route of the target compounds
1 实验部分
1.1 仪器与试剂
Bruker AVANCE III 500 MHz 或 400 MHz 核磁共振仪 (以CDCl3为溶剂,TMS 为内标);AB SCIEX Triple TOF5600 高分辨质谱仪;X-6 型数字熔点仪 (北京泰克仪器有限公司);柱层析硅胶(0.050~0.074 mm,200~300 目) 和薄层层析硅胶板 (GF254型) 均购自青岛海洋化工厂;所用试剂均为市售分析纯或化学纯,除特别注明外未经无水处理。
1.2 化合物的合成
1.2.1 目标化合物3 的合成 参考文献方法[16]进行。在25 mL 单口瓶中,加入0.16 g 桧木醇 (1 mmol)、0.2 mL 三乙胺 (1.4 mmol) 和10 mL 二氯甲烷,0 ℃搅拌下缓慢滴加2 mL 含酰氯 (1.5 mmol)的二氯甲烷溶液。滴加完毕后室温反应1 h,薄层色谱(TLC,V(石油醚) :V(乙酸乙酯) =4 : 1) 监测至反应终点。用饱和食盐水 (10 mL) 洗涤,有机相用无水硫酸钠干燥。旋转蒸发浓缩,柱层析纯化 (V(石油醚) :V(乙酸乙酯)= 8 : 1),干燥后得目标化合物3。
1.2.2 目标化合物5 和6 的合成 参考文献方法[17]进行。在25 mL 单口瓶中,加入0.16 g 桧木醇 (1 mmol)、0.25 g 碳酸钾 (1.8 mmol)和2 mL 二甲基亚砜,室温搅拌10 min 后升温至60 ℃。加入0.12 mL 卤代烷 (2 mmol),保温反应5 h, TLC(V(石油醚) :V(乙酸乙酯) = 1 : 1) 监测至反应终点。用饱和食盐水 (10 mL) 洗涤,有机相用无水硫酸钠干燥。旋转蒸发浓缩,柱层析纯化 (V(石油醚) :V(乙酸乙酯)= 1 : 1),干燥后得目标化合物5 和6。
目标化合物的结构均经核磁共振和高分辨质谱的验证,相关数据如下。
乙酸桧木酯 (3a):黄色油状液体,产率 46%.1H NMR(500 MHz, CDCl3),δ: 7.16 (s, 1H), 7.13~7.04 (m, 2H), 6.96(d,J= 9.6 Hz, 1H), 2.83~2.78 (m, 1H), 2.36 (s, 3H), 1.24 (d,J= 6.8 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 168.31,38.35, 22.86, 20.72.HRMS: C12H14NaO3[M + Na]+, 计算值229.0835, 测试值 229.0836.
三甲基乙酸桧木酯 (3b):黄色油状液体,产率 20%.1H NMR (500 MHz, CDCl3),δ: 7.14~7.02 (m, 3H), 6.94 (d,J= 9.0 Hz, 1H), 2.83~2.77 (m, 1H), 1.39 (s, 9H), 1.24 (d,J=5.7 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 176.03, 39.19,38.31, 27.28, 22.89.HRMS: C15H21O3[M + H]+, 计算值249.1485, 测试值249.1485.
正癸酸桧木酯 (3c):红色油状液体,产率 94%.1H NMR (400 MHz, CDCl3),δ: 7.18~7.01 (m, 3H), 6.95 (d,J= 9.4 Hz, 1H), 2.83~2.76 (m, 1H), 2.62 (t,J= 7.6 Hz, 2H),1.81~1.73 (m, 2H), 1.46~1.39 (m, 2H), 1.33~1.26 (m, 10H),1.23 (d,J= 6.8 Hz, 6H), 0.88 (t,J= 6.7 Hz, 3H).13C NMR(125 MHz, CDCl3),δ: 178.70, 171.12, 160.20, 137.44, 132.45,127.85, 123.53, 122.54, 38.32, 34.08, 33.95, 31.85, 29.39,29.26, 29.06, 24.73, 22.83, 22.65, 14.07.HRMS: C20H30NaO3[M + Na]+, 计算值 341.2087, 测试值 341.2091.
苯甲酸桧木酯 (3d):棕色油状液体,产率 32%.1H NMR (500 MHz, CDCl3),δ: 8.19 (d,J= 7.6 Hz, 2H), 7.61 (t,J= 7.4 Hz, 1H), 7.48 (t,J= 7.6 Hz, 2H), 7.25 (s, 1H), 7.20 (d,J= 10.5 Hz, 1H), 7.10 (s, 1H), 6.99 (d,J= 9.8 Hz, 1H),2.84~2.79 (m, 1H), 1.25 (d,J= 6.8 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 168.25, 164.00, 155.45, 154.82, 133.72,132.96, 132.72, 130.33, 129.77, 128.98, 128.54, 128.18, 38.18,22.77.HRMS: C17H17O3[M + H]+, 计算值 269.1172, 测试值269.1177.
2-溴苯甲酸桧木酯 (3e):棕色油状液体,产率 86%.1H NMR (400 MHz, CDCl3),δ: 8.19 (d,J= 7.5 Hz, 1H), 7.72(d,J= 7.6 Hz, 1H), 7.45~7.38 (m, 2H), 7.28~7.21 (m, 2H),7.11 (t,J= 10.3 Hz, 1H), 7.01 (d,J= 10.1 Hz, 1H), 2.87~2.80(m, 1H), 1.26 (d,J= 6.9 Hz, 6H).13C NMR (125 MHz,CDCl3),δ: 163.12, 134.50, 133.36, 132.72, 130.58, 127.33,122.58, 38.41, 22.92.HRMS: C17H16BrO3[M + H]+, 计算值347.0277, 测试值 347.0280.
3-溴苯甲酸桧木酯 (3f):黄色固体,产率 57%,熔点56.9~57.0 ℃.1H NMR (500 MHz, CDCl3),δ: 8.31 (s, 1H),8.10 (d,J= 7.9 Hz, 1H), 7.73 (d,J= 7.8 Hz, 1H), 7.36 (t,J=7.9 Hz, 1H), 7.25 (s, 1H), 7.20 (d,J= 10.7 Hz, 1H), 7.10 (t,J= 10.4 Hz, 1H), 7.00 (d,J= 10.0 Hz, 1H), 2.84~2.79 (m,1H), 1.24 (d,J= 7.0 Hz, 6H).13C NMR (125 MHz, CDCl3),δ:168.42, 162.84, 136.65, 136.25, 133.41, 133.05, 132.56,131.80, 130.94, 130.13, 129.98, 129.09, 128.65, 122.59, 38.43,22.91.HRMS: C17H15BrNaO3[M + Na]+, 计算值 369.0097,测试值 369.0096.
4-溴苯甲酸桧木酯 (3g):白色固体,产率 65%,熔点89.8~91.0 ℃.1H NMR (500 MHz, CDCl3),δ: 8.03 (d,J= 8.4 Hz, 2H), 7.62 (d,J= 8.2 Hz, 2H), 7.25 (s, 1H), 7.20 (d,J=10.6 Hz, 1H), 7.09 (t,J= 10.5 Hz, 1H), 6.99 (d,J= 9.8 Hz,1H), 2.84~2.79 (m, 1H), 1.24 (d,J= 7.1 Hz, 6H).13C NMR(125 MHz, CDCl3),δ: 163.44, 131.98, 131.91, 128.94, 127.98,38.39, 22.90.HRMS: C17H16BrO3[M + H]+, 计算值 347.0277,测试值 347.0278.
2-三氟甲基苯甲酸桧木酯 (3h):黄色固体,产率 56%,熔点 76.7~78.1 ℃.1H NMR (400 MHz, CDCl3),δ: 8.16~8.13(m, 1H), 7.74~7.67 (m, 1H), 7.60~7.58 (m, 2H), 7.21~7.09 (m,2H), 7.02 (s, 1H), 6.92 (d,J= 9.5 Hz, 1H), 2.78~2.71 (m, 1H),1.16 (d,J= 6.9 Hz, 6H).13C NMR (125 MHz, CDCl3),δ:163.62, 131.97, 131.83, 131.40, 129.79, 129.01 (q,J= 32.5 Hz), 126.65 (q,J= 3.25 Hz), 123.37 (d,J= 272.5 Hz), 38.37,22.84.HRMS: C18H16F3O3[M + H]+, 计算值337.1046, 测试值 337.1041.
3-三氟甲基苯甲酸桧木酯 (3i):黄色固体,产率 61%,熔点 75.2~76.2 ℃.1H NMR (400 MHz, CDCl3),δ: 8.38 (s,1H), 8.30 (d,J= 7.7 Hz, 1H), 7.81 (d,J= 7.7 Hz, 1H), 7.57 (t,J= 7.8 Hz, 1H), 7.21~7.13 (m, 2H), 7.06 (t,J= 10.4 Hz, 1H),6.95 (d,J= 10.0 Hz, 1H), 2.80~2.73 (m, 1H), 1.20 (d,J= 6.9 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 162.88, 133.70,131.27 (q,J= 32.5 Hz), 130.19 (q,J= 11.25 Hz), 129.96,129.26, 127.39 (q,J= 11.25 Hz), 123.64 (d,J= 271.25 Hz),38.43, 22.89.HRMS: C18H15F3NaO3[M + Na]+,计算值359.0866, 测试值 359.0870.
3-甲基苯甲酸桧木酯 (3j):黄色油状液体,产率 21%.1H NMR (500 MHz, CDCl3),δ: 7.95~7.89 (m, 2H), 7.36 (d,J= 7.6 Hz, 1H), 7.30 (t,J= 7.6 Hz, 1H), 7.18 (d,J= 10.8 Hz,1H), 7.12 (d,J= 10.6 Hz, 1H), 7.02 (t,J= 10.5 Hz, 1H), 6.91(d,J= 10.0 Hz, 1H), 2.77~2.71 (m, 1H), 2.35 (s, 3H), 1.18 (d,J= 6.8 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 164.33,138.34, 134.49, 131.01, 128.92, 128.44, 127.70, 38.40, 22.91,21.28.HRMS: C18H18NaO3[M + Na]+, 计算值 305.1148, 测试值 305.1153.
4-甲基苯甲酸桧木酯 (3k):黄色固体,产率 67%,熔点 86.5~88.0 ℃.1H NMR (400 MHz, CDCl3),δ: 8.00 (d,J=8.0Hz, 2H), 7.23~7.16 (m, 3H), 7.12 (d,J= 10.6 Hz, 1H), 7.02(s, 1H), 6.90 (d,J= 9.8 Hz, 1H), 2.78~2.71 (m, 1H), 2.35 (d,J= 7.2 Hz, 3H), 1.18 (d,J= 6.9 Hz, 6H).13C NMR (125 MHz,CDCl3),δ: 164.21, 144.55, 130.58, 129.26, 126.25, 38.41,22.92, 21.81.HRMS: C18H18NaO3[M + Na]+, 计算值 305.1148,测试值 305.1151.
4-甲氧基苯甲酸桧木酯 (3l):黄色固体,产率 21%,熔点87.1-88.1 ℃.1H NMR (500 MHz, CDCl3),δ: 8.16 (d,J=9.0 Hz, 2H), 7.25~7.11 (m, 3H), 6.98 (d,J= 9.0 Hz, 3H), 3.89(s, 3H), 2.86~2.81 (m, 1H), 1.27 (d,J= 6.9 Hz, 6H).13C NMR(125 MHz, CDCl3),δ: 164.04, 163.83, 132.64, 121.31, 113.84,55.53, 38.35, 22.89.HRMS: C18H18NaO4[M + Na]+, 计算值321.1097, 测试值 321.1096.
糠酸桧木酯 (3m):棕色油状液体,产率 43%.1H NMR(400 MHz, CDCl3),δ: 7.64 (d,J= 22.9 Hz, 1H), 7.40 (d,J=2.3 Hz, 1H), 7.25 (t,J= 23.6 Hz, 2H), 7.12 (t,J= 10.1 Hz,1H), 7.02 (d,J= 9.5 Hz, 1H), 6.56 (d,J= 22.0 Hz, 1H),2.86~2.80 (m, 1H), 1.26 (d,J= 6.8 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 155.36, 147.16, 143.36, 120.00, 112.14,38.22, 22.71.HRMS: C15H14NaO4[M + Na]+, 计算值 281.0784,测试值281.0785.
2-甲氧基-4-异丙基-2,4,6-环庚三烯-1-酮 (5a):棕色油状液体,产率 53%.1H NMR (400 MHz, CDCl3),δ: 7.22~7.17 (m, 1H), 7.12 (d,J= 12.1 Hz, 1H), 6.79 (d,J= 8.5 Hz,1H), 6.69 (s, 1H), 3.97 (s, 3H), 2.90~2.83 (m, 1H), 1.28 (d,J=6.9 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 179.96, 164.49,154.32, 137.07, 134.71, 124.64, 114.08, 56.04, 38.87, 23.35.HRMS: C11H14NaO2[M + Na]+, 计算值 201.0886, 测试值201.0881.
2-壬氧基-5-异丙基-2,4,6-环庚三烯-1-酮 (5b):黄色油状液体,产率 41%.1H NMR (500 MHz, CDCl3),δ:7.10~7.06 (m, 1H), 7.02 (d,J= 12.0 Hz, 1H), 6.67 (d,J= 8.5 Hz, 1H), 6.61 (s, 1H), 3.99 (t,J= 6.8 Hz, 2H), 2.79~2.73 (m,1H), 1.87~1.81 (m, 2H), 1.44~1.38 (m, 2H), 1.32~1.27 (m,2H), 1.23~1.19 (m, 14H), 0.81 (t,J= 6.7 Hz, 3H).13C NMR(125 MHz, CDCl3),δ: 180.18, 164.30, 154.09, 136.62, 135.03,124.43, 115.02, 69.27, 38.97, 31.85, 29.46, 29.36, 29.22,28.72, 25.95, 23.43, 22.64, 14.08.HRMS: C19H31O2[M + H]+,计算值 291.2319, 测试值291.2318.
2-甲氧基-6-异丙基-2,4,6-环庚三烯-1-酮 (6a):棕色油状液体,产率 44%.1H NMR (400 MHz, CDCl3),δ: 7.19 (s,1H), 7.05 (t,J= 10.5 Hz, 1H), 6.82 (d,J= 11.2 Hz, 1H), 6.70(d,J= 9.9 Hz, 1H), 3.94 (s, 3H), 2.82~2.75 (m, 1H), 1.23 (d,J= 7.0 Hz, 6H).13C NMR (125 MHz, CDCl3),δ: 180.30,164.81, 157.80, 134.29, 131.68, 129.41, 111.66, 56.15, 38.39,23.05.HRMS: C11H14NaO2[M + Na]+, 计算值 201.0886, 测试值 201.0884.
2-壬氧基-6-异丙基-2,4,6-环庚三烯-1-酮 (6b):黄色油状液体,产率 42%.1H NMR (500 MHz, CDCl3),δ: 7.10 (s,1H), 6.89 (dd,J= 11.2, 9.9 Hz, 1H), 6.68 (dd,J= 11.2, 1.7 Hz,1H), 6.55 (d,J= 9.9 Hz, 1H), 3.95 (t,J= 6.9 Hz, 2H),2.73~2.67 (m, 1H), 1.86~1.80 (m, 2H), 1.41~1.35 (m, 2H),1.30~1.26 (m, 2H), 1.24~1.18 (m, 8H), 1.16 (d,J= 6.8 Hz,6H), 0.81 (t,J= 6.9 Hz, 3H).13C NMR (125 MHz, CDCl3),δ:180.39, 164.53, 157.30, 134.41, 131.64, 128.99, 112.35, 69.32,38.36, 31.87, 29.48, 29.34, 29.24, 28.63, 25.94, 23.08, 22.66,14.10.HRMS: C19H31O2[M + H]+, 计算值 291.2319, 测试值291.2319.
1.3 生物活性测试
采用菌丝生长速率法[18]测定目标化合物对5 种植物病原菌的抑制活性。供试菌种分别为水稻纹枯病菌Rhizoctonia solani、番茄灰霉病菌Botrytis cinerea、油菜菌核病菌Sclerotinia sclerotiorum、苹果树腐烂病菌Valsa mali和黄瓜炭疽病菌Colletotrichum orbiculare,由陕西省生物农药工程技术研究中心提供。试验药剂为目标化合物3a~3m、5a、5b、6a、6b 和桧木醇 (1)。每处理设置3 次重复。选取在50 μg/mL 时抑制率大于90%的化合物,等倍降低质量浓度后再次测定其抑菌活性,计算EC50值和95%置信限。
2 结果与讨论
2.1 目标化合物的合成
酯类目标化合物3 可由桧木醇 (1) 和相应的酰氯 (2) 在三乙胺作缚酸剂的条件下进行合成。桧木醇 (1) 在碳酸钾的存在下与卤代烷进行反应,由于烯醇式和酮式的互变异构,因此醚化产物会有两种异构体,经分离提纯即可获得醚类目标化合物5 或6。为丰富酯类目标化合物的结构,酰氯选择脂肪链酰氯和芳香环酰氯,前者主要选用不同链长及支链的脂肪链,后者选用取代或未取代的苯环和呋喃环,取代基有吸电子基、供电子基,取代方式有邻位、间位和对位。
2.2 化合物的波谱分析
以高活性化合物3m (图式2) 为例。七元环上3,4,5,7 位质子的吸收峰化学位移值 (δ) 为7.25~7.02 的3 处峰;呋喃环上18 位碳上1 个质子的吸收峰为7.64 处的双峰,靠近羰基16 位碳上质子化学位移值在7.40 处,受邻近碳上氢的影响,裂分为双重峰,δ6.56 处的质子为呋喃环上17 位碳上的质子的吸收峰;11 和12 位异丙基上甲基质子的吸收峰化学位移值在1.26 处,裂分为双重峰,10 位碳上质子的吸收峰是2.83 处的多重峰。
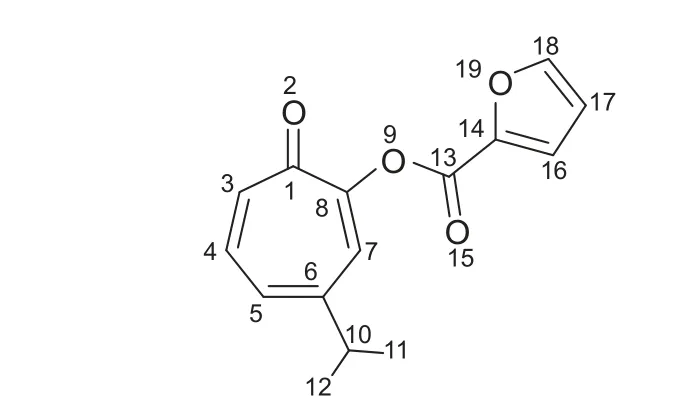
图式2 化合物3m 的化学结构式Scheme 2 Structure of compound 3m
醚类化合物存在两种位置异构体,以化合物5a 和6a 为例。通过NOESY (nuclear overhauser effect spectroscopy) 谱图(图1) 看出:化合物5a 的7 位碳上氢δ6.69 (s, 1H) 和甲氧基上氢δ3.97 (s, 3H) 之间存在明显的关联,证明化合物5a 为图1A 所示结构;化合物6a 的3 位碳上氢δ6.82 (d, 1H)和甲氧基上氢δ3.94 (s, 3H)之间关联明显,可以确定化合物6a 为图1B 所示结构。而酯类化合物只生成一种异构体,以化合物3a 为例,通过NOESY 谱图看出,其7 位碳上氢δ7.15 (s, 1H)和乙酰基上的甲基氢δ2.36 (s, 3H)处存在一定的关联,因此可以确定酯类化合物的结构。相应的NOESY 谱图见附加材料。

图1 化合物5a (A)和6a (B)的NOESY 图谱Fig.1 NOESY spectrum of 5a (A) and 6a (B)
2.3 抑菌活性
抑菌活性测定结果见表1 和附加材料图S38。从中看出,在50 μg/mL 下,目标化合物对5 种供试病原菌表现出中等到优异的抑菌活性。其中:对水稻纹枯病菌、油菜菌核病菌、苹果树腐烂病菌和黄瓜炭疽病菌均有部分化合物能够完全抑制菌丝的生长,表现出与桧木醇类似的高活性;化合物3j 和6a 对番茄灰霉病菌表现出大于90%的抑制率,优于桧木醇。表明以桧木醇作为先导化合物进行结构衍生有可能会发现高抑菌活性新分子。

表1 目标化合物在50 μg/mL 下离体抑菌活性Table 1 In vitro antifungal activities of target compounds at 50 μg/mL
初步构效关系分析表明,酯类化合物的抑菌活性整体上优于醚类化合物。对于醚类化合物,化合物5b 对4 种供试菌的抑制率均高于50%,而5a 均低于30%,化合物6a 和6b 也符合此趋势,说明碳链越长对抑菌活性越有利 (5b > 5a,6b > 6a)。化合物6a 对5 种供试菌的抑制活性均高于5a,例如6a 对番茄灰霉病菌的抑制率为93.4%,而化合物5a 对该菌的抑制率仅为27.5%;化合物6b 的抑菌活性也整体优于5b,说明在相同碳链长度的条件下,化合物6 的活性优于5。对于酯类化合物,脂肪链 (3a~3c)、杂环 (3m) 和未取代的苯环 (3d)对水稻纹枯病菌、油菜菌核病菌和苹果树腐烂病菌的抑制率均大于95%;化合物3j 和3l 对5 种菌的抑制率均高于80%,说明苯环上取代基为供电子基时对活性有利。
EC50值测定结果 (表2) 显示:桧木醇对水稻纹枯病菌、番茄灰霉病菌、油菜菌核病菌、苹果树腐烂病菌和黄瓜炭疽病菌的EC50值在2.00~12.1 μg/mL 之间。对所测定的5 种病原菌均有部分化合物表现出较桧木醇更优的活性。对苹果树腐烂病菌和黄瓜炭疽病菌,多数化合物的EC50值大于5 μg/mL。化合物3a 和3d 对水稻纹枯病菌,3j 对番茄灰霉病菌,3c、3j 和3m 对油菜菌核病菌的EC50值均小于3 μg/mL,值得对其进行深入研究。
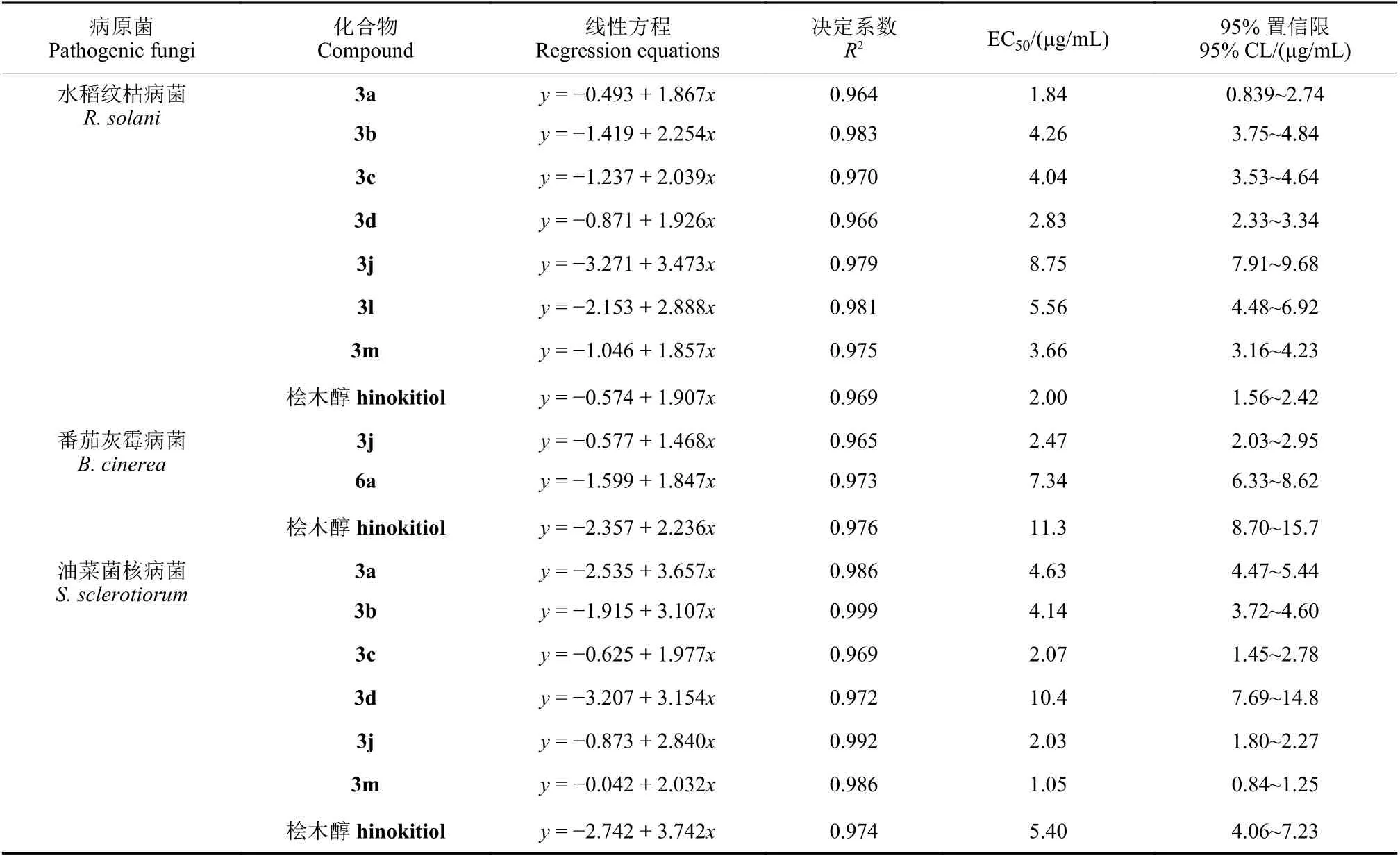
表2 部分目标化合物对5 种病原菌的EC50 值Table 2 EC50 values of some target compounds against five pathogenic fungi
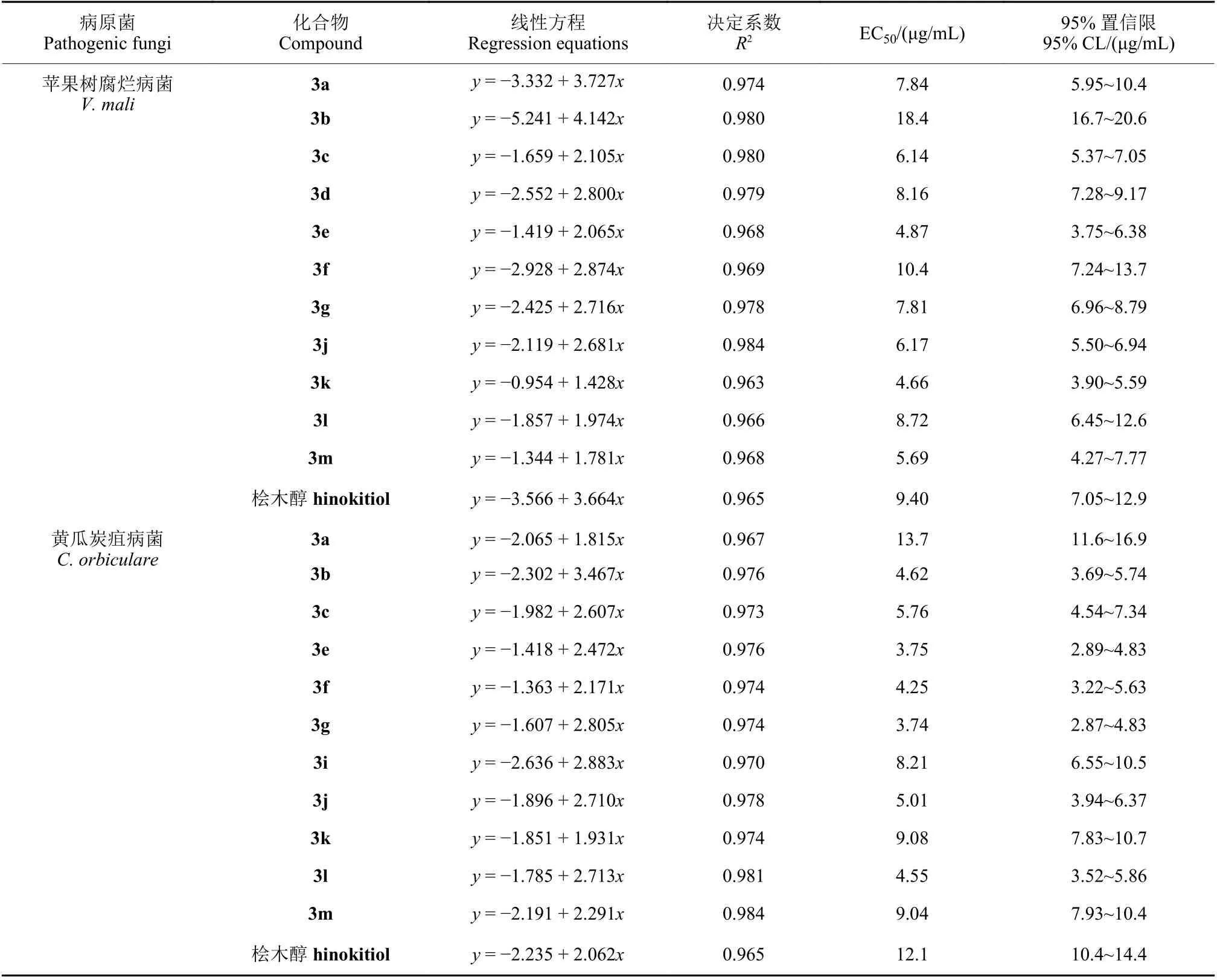
续表2Table 2 (Continued)
3 结论
本文设计合成了17 个新型桧木醇酯类和醚类衍生物,并研究了它们的抑菌活性及构效关系。活性结果表明,桧木醇及目标化合物对水稻纹枯病菌、番茄灰霉病菌、油菜菌核病菌、苹果树腐烂病菌和黄瓜炭疽病菌表现出较好的抑菌活性。化合物3a对水稻纹枯病菌、3j对番茄灰霉病菌、3m对油菜菌核病菌的EC50值分别为1.84、2.47和1.05 μg/mL,与桧木醇(2.00、11.3、5.40 μg/mL)相比表现出更优的抑菌活性。本文结果表明,桧木醇可以作为杀菌剂创制的有效药效团,化合物3a、3j和3m具有结构简单、活性较高等特点,可以作为先导化合物进一步优化研究。
(责任编辑: 金淑惠)
