短指软珊瑚Sinularia sp.的多骨架类型萜类成分和生物活性研究
2023-03-10陈俊锟崔晚香万佩里姚励功梁林富郭跃伟
陈俊锟,崔晚香,卜 庆,万佩里,姚励功,梁林富*,郭跃伟*
1.中南林业科技大学材料科学与工程学院,湖南 长沙 410004
2.中国科学院上海药物研究所 新药研究国家重点实验室,上海 201203
在生物分类学上,短指属软珊瑚(Sinularia)属于刺胞动物门(Cnidarians,也称腔肠动物门Coelenterata)珊瑚虫纲(Anthozoa)八放珊瑚亚纲(Octocorallia)软珊瑚目(Alcyonacea)软珊瑚科(Alcyoniidae)无脊椎动物,是构成海底珊瑚礁的主要底栖海洋生物之一[1]。它们生存能力强,在我国东海、南海等各大海域均有分布。受高压、高盐度、低营养、低(恒)温、低(无)光照、缺氧等复杂恶劣的海洋生存环境的影响,短指属软珊瑚次级代谢产物有着丰富的化学结构多样性,涵盖萜类、甾体、生物碱、长链烷基糖苷、神经酰胺、精胺等各种结构类型,其中研究最热门的一类次级代谢产物是萜类化合物[1-2]。最近,Zeng 等[3]从短指属软珊瑚Sinularia nanolobata得到双环 [13.1.0]十五烷型新骨架二萜sinunanolobatone A,并具有显著的抗炎活性。由于短指属软珊瑚的萜类成分不仅结构新颖,而且活性显著,受到国内外合成化学家的广泛关注和青睐[4-5]。
为了开发利用我国的海洋资源,寻找具有生物活性及药用前景的海洋天然产物,研究人员前期对我国南海短指属Sinularia、肉芝属Sarcophyton等种属的软珊瑚开展了一系列的研究,发现了不少结构新颖的萜类,并具有显著的抗炎、免疫抑制等活性[3,6-10]。鉴于此,本研究对采自中国南海海域的软珊瑚Sinulariasp.进行了系统的化学成分和生物活性研究,共分离鉴定15 个合物(图1),分别为1β-hydroxy-4(15),5E,10(14)-germacratriene (1)、(7R*)-opposit-4(15)-ene-1β,7-diol(2)、15-hydroxyα-cadinol(3)、nephalbidol(4)、isodauc-6-ene-10β,14-diol(5)、pubinernoid A(6)、norcembrene 5(7)、norcembrenolide 2(8)、sinularcasbane O(9)、scabrolide D(10)、5-epi-sinuleptolide(11)、sinuleptolide(12)、ineleganolide(13)、yonarolide(14)和dihydrosinularin(15)。其中,化合物3 和6 为首次从软珊瑚科软珊瑚中分离得到,1、2 和5为首次从短指属软珊瑚中分离得到。同时,开展了化合物对人肺腺癌A549 细胞、人结肠癌HT-29 细胞、人肝癌SNU-398 细胞和人胰腺癌Capan-1 细胞的细胞毒活性和与糖脂代谢密切相关的乙酰辅酶A羧化酶1(acetyl-CoA carboxylase,ACC1)与ATP-柠檬酸裂解酶(ATP citrate lyase,ACL)的酶抑制活性测试。
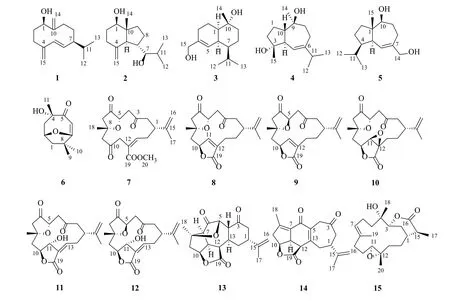
图1 化合物1~15 的化学结构Fig.1 Chemical structures of compounds 1—15
1 仪器与材料
Bruker DRX-400 型核磁共振仪(德国Bruker公司);Finnigan-MAT-95 型质谱仪(美国Finnigan公司);Perkin-Elmer 241MC 型旋光仪(美国Perkin-Elmer 公司);Shimadzu LC-6AD 型制备液相色谱仪(日本岛津制作所);Shimadzu SPD-20A 型紫外检测器(日本岛津制作所);Sephadex LH-20凝胶(瑞典Amersham Biosciences 公司);柱色谱硅胶(200~300、300~400 目,青岛海洋化工有限公司);GF254薄层色谱硅胶板(烟台江友硅胶开发有限公司);色谱级甲醇、乙腈为DiKMA 有限公司产品;其他有机试剂均为分析纯,购自国药集团化学试剂有限公司。
实验材料于2017年5月采自我国南海西瑁岛海域,采集后立即冷冻备用。由中国科学院南海海洋研究所的黄晖研究员鉴定为短指软珊瑚Sinulariasp.。样品标本(17-XD-55)保存于中国科学院上海药物研究所国家新药研究重点实验室。
2 提取与分离
将冷冻的软珊瑚(干质量315 g)切碎,室温下用丙酮超声提取3 次,提取液减压浓缩悬浮于500 mL 水中,分别用等体积的乙醚和正丁醇各萃取3次,收集的有机相萃取液分别减压蒸馏后得到黑褐色的乙醚相浸膏(10.0 g)和黄棕色的正丁醇相浸膏(5.3 g)。
乙醚相浸膏通过硅胶柱色谱,石油醚-乙醚(98∶2→90∶10→80∶20→70∶30→60∶40→50∶50)梯度洗脱,分为7 个组分A~G。组分C 经硅胶柱色谱,石油醚-乙醚(90∶10)等度洗脱,再经半制备HPLC,以乙腈-水(80∶20)洗脱得到化合物1(1.2 mg,tR=8.4 min)。组分D 依次经Sephadex LH-20 凝胶柱色谱(石油醚-二氯甲烷-甲醇2∶1∶1)、硅胶柱色谱(200~300 目,石油醚-乙醚80∶20)和半制备HPLC(乙腈-水70∶30)洗脱得到化合物2(2.0 mg,tR=5.7 min)。组分E 先后经Sephadex LH-20 凝胶柱色谱(石油醚-二氯甲烷-甲醇2∶1∶1)、硅胶柱色谱(200~300 目,二氯甲烷-乙醚80∶20)和半制备HPLC(甲醇-水90∶10)洗脱得到化合物3(1.6 mg,tR=12.0 min)。组分F经硅胶柱色谱,二氯甲烷-乙醚(50∶50)等度洗脱得到5 个亚组分F1~F5。亚组分F2 经半制备HPLC(乙腈-水50∶50)洗脱得到化合物4(3.8 mg,tR=9.2 min)。亚组分F4 先后经硅胶柱色谱(二氯甲烷-甲醇50∶50)和半制备HPLC(甲醇-水40∶60)洗脱得到化合物11(4.6 mg,tR=17.9 min)和12(4.7 mg,tR=21.7 min)。亚组分F5 依次经硅胶柱色谱(200~300 目,二氯甲烷-甲醇90∶10)和半制备HPLC(乙腈-水40∶60)洗脱得到化合物5(1.7 mg,tR=14.7 min)和6(1.5 mg,tR=15.2 min)。组分G经硅胶柱色谱(200~300 目),二氯甲烷-甲醇(90∶10)等度洗脱得到共4 个亚组分G1~G4。亚组分G1 经半制备HPLC(甲醇-水85∶15)洗脱得到化合物7(5.1 mg,tR=4.2 min)。亚组分G2 先后经硅胶柱色谱(200~300 目,二氯甲烷-甲醇70∶30)和半制备HPLC(乙腈-水38∶62)得到化合物8(5.4 mg,tR=18.2 min)和9(5.1 mg,tR=19.4 min)。亚组分G3 依次经硅胶柱色谱(200~300 目,二氯甲烷-甲醇60∶40)和半制备HPLC(乙腈-水50∶50)洗脱得到化合物10(9.2 mg,tR=11.2 min)和15(2.4 mg,tR=13.4 min)。亚组分G4 先经硅胶柱色谱(200~300 目,二氯甲烷-乙醚85∶15)得到化合物13(4.3 mg)和待纯化组分,再经半制备HPLC(甲醇-水50∶50)得到化合物14(1.2 mg,tR=10.4 min)。
3 结构鉴定
化合物1:无色油状物;[α]20D-30.0(c0.06,CHCl3);EI-MSm/z220 [M]+;1H NMR(400 MHz,CDCl3)δ:5.99(1H,d,J= 15.7 Hz,H-5),5.43(1H,dd,J= 10.3,15.7 Hz,H-6),5.27(1H,s,H-14a),5.00(1H,s,H-14b),4.92(1H,s,H-15a)4.84(1H,s,H-15b),3.77(1H,dd,J= 3.9,11.9 Hz,H-1),0.89(3H,d,J= 6.7 Hz,H-12),0.81(3H,d,J= 6.8 Hz,H-13);13C-NMR(125 MHz,CDCl3)δ:76.0(C-1),36.2(C-2),29.8(C-3),146.8(C-4),129.7(C-5),138.0(C-6),52.5(C-7),36.1(C-8),34.5(C-9),153.5(C-10),31.8(C-11),20.8(C-12),20.5(C-13),110.6(C-14),112.8(C-15)。以上数据与文献报道基本一致[11],故鉴定化合物1 为1β-hydroxy-4(15),5E,10(14)-germacratriene。
化合物2:无色油状物;[α]20D+70.4(c0.06,CHCl3);EI-MSm/z238 [M]+;1H-NMR(400 MHz,CDCl3)δ:4.95(1H,s,H-15a),4.81(1H,s,H-15b),3.59(1H,dd,J= 4.7,11.2 Hz,H-1),3.23(1H,brd,J=9.8 Hz,H-7),1.00(3H,d,J= 6.9 Hz,H-13),0.91(3H,d,J= 6.8 Hz,H-12),0.67(3H,s,H-14);13C-NMR(125 MHz,CDCl3)δ:79.0(C-1),31.9(C-2),34.9(C-3),148.9(C-4),56.4(C-5),39.4(C-6),82.7(C-7),26.0(C-8),37.3(C-9),49.5(C-10),31.3(C-11),20.5(C-12),14.7(C-13),12.3(C-14),107.6(C-15)。以上数据与文献报道基本一致[12],故鉴定化合物2 为(7R*)-opposit-4(15)-ene-1β,7-diol。
化合物3:无色油状物;[α]20D-16.8(c0.16,MeOH);EI-MSm/z238 [M]+;1H-NMR(400 MHz,CDCl3)δ:5.79(1H,brs,H-5),3.99(1H,d,J= 13.2 Hz,H-15a),3.96(1H,d,J= 13.2 Hz,H-15b),1.12(3H,s,H-14),0.92(3H,d,J= 6.9 Hz,H-12),0.78(3H,d,J= 6.9 Hz,H-13);13C-NMR(125 MHz,CDCl3)δ:50.4(C-1),22.1(C-2),26.6(C-3),138.4(C-4),123.8(C-5),39.8(C-6),46.6(C-7),22.1(C-8),42.3(C-9),72.5(C-10),25.9(C-11),15.3(C-12),21.6(C-13),20.8(C-14),67.5(C-15)。以上数据与文献报道的基本一致[13],故鉴定化合物 3 为 15-hydroxy-α-cadinol。
化合物4:无色油状物;[α]20D-11.0(c0.10,CHCl3);EI-MSm/z238 [M]+;1H-NMR(400 MHz,CDCl3)δ:5.50(1H,brd,J= 5.0 Hz,H-5),1.27(3H,s,H-14),1.21(3H,s,H-15),0.99(3H,d,J= 6.7 Hz,H-12),0.97(3H,d,J= 6.7 Hz,H-13);13C-NMR(125 MHz,CDCl3)δ:21.5(C-1),40.5(C-2),80.2(C-3),50.3(C-4),121.3(C-5),149.6(C-6),25.3(C-7),42.6(C-8),75.3(C-9),50.7(C-10),37.3(C-11),21.1(C-12),21.3(C-13),21.4(C-14),22.5(C-15)。以上波谱数据与文献报道的基本一致[14],鉴定化合物4 为nephalbidol。
化合物5:无色油状物;[α]20D+11.9(c0.05,MeOH);EI-MSm/z238 [M]+;1H-NMR(400 MHz,CDCl3)δ:5.76(1H,d,J= 6.7 Hz,H-6),4.06(2H,s,H-14),3.40(1H,dd,J= 1.8,11.0 Hz,H-10),0.91(3H,d,J= 6.0 Hz,H-12),0.89(3H,d,J= 6.0 Hz,H-13),0.66(3H,s,H-15);13C-NMR(125 MHz,CDCl3)δ:48.5(C-1),39.0(C-2),27.1(C-3),47.5(C-4),44.5(C-5),127.0(C-6),139.1(C-7),25.5(C-8),29.3(C-9),83.7(C-10),29.3(C-11),23.7(C-12),20.2(C-13),68.2(C-14),14.0(C-15)。以上波谱数据与文献报道基本一致[15],鉴定化合物5 为isodauc-6-ene-10β,14-diol。
化合物6:无色油状物;[α]20D+12.9(c0.05,MeOH);EI-MSm/z196 [M]+;1H-NMR(400 MHz,CDCl3)δ:5.69(1H,s,H-6),4.35(1H,m,H-2),1.78(3H,s,H-11),1.47(3H,s,H-9),1.28(3H,s,H-10);13C-NMR(125 MHz,CDCl3)δ:47.5(C-1),66.8(C-2),45.7(C-3),86.5(C-4),183.2(C-5),113.0(C-6),171.6(C-7),35.9(C-8),26.5(C-9),30.5(C-10),27.0(C-11)。以上波谱数据与文献报道基本一致[16],鉴定化合物6 为pubinernoid A。
化合物7:白色固体;[α]20D-57.7(c0.50,CHCl3);EI-MSm/z362 [M]+;1H-NMR(400 MHz,CDCl3)δ:6.75(1H,t,J= 7.7 Hz,H-13),4.95(1H,s,H-16a),4.71(1H,s,H-16b),4.41(1H,dd,J= 3.5,9.4 Hz,H-5),3.72(3H,s,H-20),1.79(3H,s,H-17),1.37(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:39.6(C-1),45.8(C-2),206.9(C-3),45.6(C-4),75.9(C-5),215.1(C-6),45.8(C-7),80.5(C-8),49.6(C-9),206.4(C-10),44.9(C-11),128.2(C-12),140.3(C-13),29.1(C-14),144.9(C-15),112.2(C-16),22.0(C-17),28.9(C-18),167.7(C-19),52.1(C-20)。以上波谱数据与文献报道基本一致[7,17],鉴定化合物7 为norcembrene 5。
化合物8:白色固体;[α]20D-31.0(c0.05,CHCl3);EI-MSm/z332 [M]+;1H-NMR(400 MHz,CDCl3)δ:7.22(1H,s,H-11),5.13(1H,s,H-10),4.81(1H,s,H-16a),4.68(1H,s,H-16b),4.15(1H,dd,J= 3.5,8.4 Hz,H-5),1.66(3H,s,H-17),1.32(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:43.2(C-1),40.9(C-2),207.9(C-3),46.8(C-4),74.8(C-5),212.9(C-6),48.3(C-7),78.8(C-8),45.7(C-9),78.4(C-10),150.8(C-11),131.3(C-12),20.9(C-13),27.7(C-14),145.9(C-15),113.2(C-16),18.2(C-17),25.4(C-18),174.2(C-19)。以上波谱数据与文献报道基本一致[17],鉴定化合物8 为norcembrenolide 2。
化合物9:白色固体;[α]20D+29.5(c0.50,CHCl3);EI-MSm/z332 [M]+;1H-NMR(400 MHz,CDCl3)δ:7.22(1H,s,H-11),5.17(1H,s,H-10),4.87(1H,s,H-16a),4.74(1H,s,H-16b),4.46(1H,dd,J=2.0,11.0 Hz,H-5),1.66(3H,s,H-17),1.34(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:38.9(C-1),41.8(C-2),208.6(C-3),50.3(C-4),77.8(C-5),212.7(C-6),51.3(C-7),79.5(C-8),44.2(C-9),79.1(C-10),151.8(C-11),131.3(C-12),20.2(C-13),29.3(C-14),145.5(C-15),113.2(C-16),18.5(C-17),28.0(C-18),174.5(C-19)。以上波谱数据与文献报道基本一致[18],鉴定化合物9 为sinularcasbane O。
化合物 10:白色固体;[α]20D-58.3(c0.24,CHCl3);EI-MSm/z348 [M]+;1H-NMR(400 MHz,CDCl3)δ:4.93(1H,s,H-16a),4.86(1H,s,H-16b),4.74(1H,t,J= 6.0 Hz,H-10),4.19(1H,dd,J= 4.0,5.6 Hz,H-5),3.95(1H,s,H-11),1.68(3H,s,H-17),1.46(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:40.8(C-1),48.2(C-2),207.6(C-3),44.8(C-4),75.0(C-5),213.8(C-6),49.4(C-7),79.1(C-8),42.4(C-9),75.9(C-10),62.7(C-11),60.7(C-12),21.3(C-13),26.4(C-14),145.8(C-15),112.7(C-16),18.7(C-17),25.6(C-18),174.0(C-19)。以上波谱数据与文献报道的基本一致[19],鉴定化合物10 为scabrolide D。
化合物11:无色晶体(甲醇);[α]20D+12.5(c0.30,CHCl3);EI-MS:m/z348 [M]+;1H-NMR(400 MHz,CDCl3):δH6.46(1H,dd,J= 4.8,10.8 Hz,H-13),4.87(1H,s,H-16a),4.80(1H,s,H-16b),4.63(1H,d,J=7.6 Hz,H-10),4.60(1H,s,H-11),4.27(1H,dd,J=2.5,8.8 Hz,H-5),1.82(3H,s,H-17),1.46(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:39.8(C-1),42.5(C-2),205.6(C-3),46.2(C-4),75.1(C-5),214.6(C-6),51.5(C-7),79.4(C-8),43.4(C-9),83.4(C-10),75.2(C-11),132.6(C-12),145.3(C-13),28.6(C-14),147.4(C-15),110.6(C-16),21.8(C-17),26.6(C-18),168.6(C-19)。以上波谱数据与文献报道基本一致[7,20],鉴定化合物11 为5-epi-sinuleptolide。
化合物12:无色晶体(甲醇);[α]20D-67.9(c0.30,CHCl3);EI-MSm/z348 [M]+;1H-NMR(400 MHz,CDCl3)δ:6.52(1H,dd,J= 6.0,10.8 Hz,H-13),4.85(1H,s,H-16a),4.79(1H,s,H-16b),4.66(1H,d,J=6.8 Hz,H-10),4.60(1H,s,H-11),4.39(1H,dd,J=3.1,9.9 Hz,H-5),1.82(3H,s,H-17),1.48(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:41.8(C-1),48.1(C-2),208.3(C-3),44.7(C-4),76.9(C-5),213.1(C-6),52.0(C-7),79.5(C-8),42.4(C-9),83.9(C-10),75.6(C-11),131.8(C-12),145.4(C-13),31.6(C-14),148.0(C-15),110.5(C-16),21.2(C-17),29.6(C-18),169.1(C-19)。以上波谱数据与文献报道基本一致[7,20-21],鉴定化合物12 为sinuleptolide。
化合物13:无色晶体(甲醇);[α]20D+39.0(c0.40,CHCl3);EI-MSm/z330 [M]+;1H-NMR(400 MHz,CDCl3)δ:5.12(1H,t,J= 7.4 Hz,H-10),5.07(1H,s,H-5),4.94(1H,s,H-16a),4.62(1H,s,H-16b),1.71(3H,s,H-17),1.28(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:40.4(C-1),44.4(C-2),206.4(C-3),49.8(C-4),77.5(C-5),212.2(C-6),62.5(C-7),91.1(C-8),45.5(C-9),83.1(C-10),43.8(C-11),47.1(C-12),33.2(C-13),32.7(C-14),146.0(C-15),113.8(C-16),22.6(C-17),20.2(C-18),176.1(C-19)。以上波谱数据与文献报道基本一致[7,22],鉴定化合物13为ineleganolide。
化合物 14:白色固体;[α]20D-40.9(c0.10,CHCl3);EI-MSm/z312 [M]+;1H-NMR(400 MHz,CDCl3)δ:5.01(1H,t,J= 4.6 Hz,H-10),4.86(1H,s,H-16a),4.83(1H,s,H-16b),3.95(1H,m,H-11),3.59(2H,s,H-4),3.44(1H,d,J= 8.2 Hz,H-12),1.82(3H,s,H-17),2.09(3H,s,H-18);13C-NMR(125 MHz,CDCl3)δ:41.4(C-1),47.1(C-2),207.9(C-3),39.6(C-4),134.2(C-5),183.4(C-6),126.5(C-7),150.7(C-8),45.8(C-9),80.9(C-10),50.1(C-11),47.6(C-12),149.2(C-13),38.5(C-14),146.9(C-15),111.1(C-16),21.5(C-17),15.7(C-18),172.5(C-19)。以上波谱数据与文献报道基本一致[7,23],鉴定化合物14为yonarolide。
化合物 15:白色固体;[α]20D-78.3(c0.20,CHCl3);EI-MSm/z336 [M]+;1H-NMR(400 MHz,CDCl3)δ:5.07(1H,t,J= 7.6 Hz,H-7),4.02(1H,d,J= 9.2 Hz,H-3),2.90(1H,t,J= 5.7 Hz,H-11),1.80(3H,s,H-19),1.61(3H,s,H-20),1.48(3H,s,H-18),1.38(3H,d,J= 7.0 Hz,H-17);13C-NMR(125 MHz,CDCl3)δ:37.3(C-1),23.4(C-2),31.6(C-3),59.4(C-4),63.4(C-5),25.8(C-6),36.2(C-7),134.1(C-8),126.4(C-9),38.6(C-10),35.2(C-11),94.1(C-12),74.8(C-13),28.1(C-14),42.8(C-15),175.2(C-16),17.7(C-17),25.6(C-18),15.9(C-19),16.9(C-20)。以上波谱数据与文献报道基本一致[24],鉴定化合物15为dihydrosinularin。
4 生物活性测试
文献曾报道了化合物7~15 开展过细胞毒活性的测试。本研究中对化合物1~6 进行抗肿瘤活性筛选,结果表明,这6 个化合物均对A549、HT-29、SNU-398 和Capan-1 细胞没有表现出有明显的细胞毒活性。
为探索降二萜类化合物更广泛的生物活性,也为解决我国面临的高血脂、肥胖、糖尿病问题提供指导,开展了ACC1[25]和ACL[26]抑制活性实验,但本结果中所有化合物均未表现出明显的酶抑制活性。
5 讨论
短指软珊瑚作为珊瑚家族的重要成员之一,不仅每年从中分离的结构新颖的化合物数目可观,而且有一些化合物是有强烈生物活性,这与其生存的非常独特的海洋环境是密切相关的[1]。本课题对采自中国南海西瑁岛海域的短指属Sinularia的一个未明确种名的软珊瑚的化学成分开展了系统性的研究,共分离鉴定了15 个化合物。化合物1~5 为倍半萜类化合物,其骨架类型分别为大根香叶烷型(germacrane)、oppositane 型、杜松烷型(cadinane)、愈创木烷型(guaiane) 和异胡萝卜烷型(isodaucane)。化合物6 为罕见的反Bredt 规则的双环桥烯型单萜。化合物7~14 为降二萜,其中7~12 的骨架类型是C-4 降西松烷型,13 是inelegane型,14 是yonarane 型。化合物15 为西松烷型(cembrane)二萜。这15 个化合物的骨架类型多达10 种,充分证明了短指属软珊瑚的萜类成分结构的多样性和复杂性,本研究进一步充实了对该属软珊瑚的化学多样性的认知。其中,化合物3 和6 为首次从软珊瑚科软珊瑚中分离得到,1、2 和5 为首次从短指属软珊瑚中分离得到。另外通过对比化合物8~12 的碳谱数据,发现化合物8、10 和11 的C-5和C-18 化学位移小于化合物9 和12 的,差值在δ2~3。引起化学位移显著变化的是由于C-5 构型改变引起的。这一规律与其他文献报道的降二萜化合物的性质符合[7,27]。
利益冲突所有作者均声明不存在利益冲突
