一种新型聚合物VDE用于快速吸附水中的硝酸盐
2023-03-09吴汾奇
胡 伟,祝 凯,吴汾奇 ,李 燕
(1.吉林大学 地下水资源与环境教育部重点实验室,长春130021;2.吉林大学 新能源与环境学院,长春130021)
硝酸盐的污染问题已受到人们广泛关注.近年来,由于人们频繁的工业和农业活动,使大量的含硝酸盐废水进入地下水和地表水体,极大破坏了生态环境.超标的硝酸盐不仅会导致湖泊中藻类的疯狂生长,产生水体的富营养化[1],而且对人们的饮用水安全也构成了威胁,如婴幼儿不慎饮用硝酸盐含量超标的水,硝酸盐在人体内会转化为毒性更强的亚硝酸盐[2],导致儿童食道癌和高铁血红蛋白症.因此,为保护人们的安全,美国环保署(EPA)规定饮用水中含硝酸盐氮的最大质量比为10 mg/L.
目前,应用广泛的处理硝酸盐废水技术一般包括生物反硝化法[3]、零价铁还原[4]、反渗透法[5]、电渗析法[6]和催化还原法[7].但这些方法均存在局限性,如生物法处理周期长、零价铁还原法易产生副产物导致环境二次污染、反渗透和电渗析法处理成本较高、耗能大且不可再生.吸附法因其制备和操作简单、效果好、处理速度快和可再生性等特点而备受关注.常见的吸附剂[8]包括活性炭[9-11]、黏土吸附剂[12]、农业副产物[13-14]、工业废渣吸附剂[15-16]、离子交换树脂[17]、合成的有机聚合物[18]和层状双氢氧化物等无机化合物[19].但由于硝酸盐在废水中具有较高的稳定性、溶解性及其较小的电荷密度,因此其沉淀和吸附的趋势较低.

为提高吸附剂对硝酸盐的吸附量,仍需改进合成材料和方法.研究表明,乙烯基咪唑中的咪唑基团是一种氮取代芳香杂环化合物,可与卤代烷烃发生季铵化反应,从而使其带正电荷,与负离子发生静电吸附作用,但其尚未应用于水中硝酸盐吸附剂的研究.此外,该聚合物吸附剂与离子交换树脂相比,不需进行有机骨架的氯甲基化和三乙胺、乙二胺等胺类化合物的胺化反应,提高了材料的合成效率,减少了合成过程所需的时间,避免了过多繁杂的合成步骤及产生有毒的中间产物[23-25].二溴癸烷作为长链烷烃可与咪唑基团发生季铵化反应,使咪唑基团带正电,乙二醇二甲基丙烯酸酯作为交联剂可使乙烯基咪唑相互交联,形成高度交联的聚合物.因此,本文采用乙烯基咪唑和二溴癸烷作为合成硝酸盐吸附剂的主要材料,简单快速地合成了乙烯基咪唑/二溴癸烷/二甲基丙烯酸乙二醇(vinylimidazole/dibromodecane/ethylene dimethacrylate,VDE)有机聚合物吸附剂,确定了吸附剂的最佳配比,对材料的结构进行表征,并研究反应的最佳剂量比、pH值和温度条件以及材料的重复利用性.
1 实 验
1.1 材 料
乙二醇二甲基丙烯酸酯(EGDMA)、乙烯基咪唑、二溴癸烷、过硫酸钾均购自上海麦克林生物化学有限公司;氢氧化钠(NaOH)、盐酸(HCl)、硝酸钠(NaNO3)、氯化钠(NaCl)和N,N-二甲基甲酰胺均购自北京化工厂.所用试剂均为分析纯试剂.
1.2 VDE的合成
VDE通过自由基交联共聚法合成,步骤如下: 首先,将50 mL水和N,N-甲基甲酰胺的混合液(体积比为1∶10)放入三颈烧瓶中.充分混匀后,依次向混合液中加入10 mmol的乙烯基咪唑、10 mmol二溴癸烷、交联剂EGDMA(相对于混合物质的量的50%)和100 mg引发剂过硫酸铵.其次,将混合液在磁力搅拌器上充分搅拌10 min.为避免空气中氧气对聚合反应的影响,在室温下通入惰性氮气30 min以驱除溶液中的氧气.将三颈烧瓶用橡胶塞密封并用氮气保存,置于75 ℃的油浴锅中8 h.最后,反应完全可得到白色的胶状体VDE,烘干后用研钵将其碾成细小颗粒.合成的聚合物用乙醇和去离子水洗涤3~5次,以去除残留的溶剂和药剂,清洗干净后,将VDE置于冷冻干燥机中干燥24 h.
1.3 表征和离子检测

1.4 吸附实验
除特别说明外,所有批量吸附实验均在室温下进行.将50 mL硝酸盐溶液(初始质量浓度为50 mg/L)和160 mg的VDE依次加入200 mL四口试剂瓶中,置于恒温摇床中120 r/min摇晃1 h,VDE吸附完成后,先用注射器抽取含有吸附剂VDE的上清液,再用45 μm的滤膜过滤并进行测定,平行实验两份.为研究乙烯基咪唑和二溴癸烷的最佳配比,控制交联剂EDGMA和引发剂过硫酸铵的物质的量保持不变(EDGMA相对于混合物质量的50%,过硫酸铵为100 mg),改变乙烯基咪唑与二溴癸烷的物质的量比例,分别合成n(乙烯基咪唑)∶n(二溴癸烷)=1∶1,1∶2,1∶0.5的吸附剂,合成的吸附剂依次命名为VDE-1,VDE-2和VDE-0.5,并在50 mL硝酸盐(10,20,50,80,100 mg/L)溶液中加入160 mg吸附剂VDE-1,VDE-2和VDE-0.5.为确定吸附剂在实际应用中的最佳剂量,分别将不同质量(0.8,1.6,2.4,3.2,4 mg)的VDE加入体积为1 L,质量浓度为100 mg/L的硝酸盐溶液中.此外,用0.1 mol/L HCl和0.1 mol/L NaOH调节硝酸盐溶液的初始pH值(2~10),研究pH值对VDE吸附硝酸盐的影响.在吸附动力学实验中,将VDE加入硝酸盐溶液中,并在吸附过程中以不同的时间间隔(1~60 min)抽取0.5 mL等分试样溶液.分别在温度为15,25,35 ℃条件下,对配置不同初始质量浓度(10,20,50,80,100 mg/L)的硝酸盐溶液进行吸附等温线实验.为研究吸附剂的可重复利用性,选择0.2 mol/L NaCl溶液作为解吸试剂,将已吸附硝酸盐的VDE加入0.2 mol/L NaCl溶液中解析1 h,使硝酸盐与溶液中的Cl-发生离子交换反应,解析完成后,再将吸附剂VDE用抽滤机抽滤,并再次加入含50 mg/L的硝酸盐溶液中进行吸附实验.共进行5次吸附/脱附实验.
1.5 数据分析
在序批式吸附实验中,VDE对硝酸盐的吸附量可通过
qe=(ρ0-ρe)V/m
(1)
计算,其中qe为平衡时VDE吸附硝酸盐的量(mg/g),ρ0为硝酸盐的初始质量浓度(mg/L),ρe为溶液中VDE吸附达到平衡时的硝酸盐质量浓度(mg/L),V为溶液体积(L),m为VDE的质量(g).
使用准一级方程
qt=qe[1-exp{-K1t}]
(2)
和准二级方程
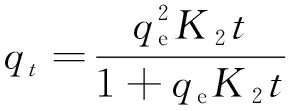
(3)
分析吸附机制和吸附过程的决定速率步骤,其中qt表示时间t时的硝酸盐吸附量(mg/g),K1(min-1)和K2(g·(mg·min)-1)分别为准一级和准二级速率常数,t为VDE接触时间(min).
用Langmuir和Freundlich两种等温线吸附模型进一步描述吸附过程[26].Langmuir 等温吸附方程为
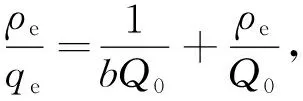
(4)
Freundlich 等温吸附方程为

(5)
其中Q0为最大单层覆盖吸附量(mg/g),b为Langmuir等温线常数(L/mg),KF为Freundlich等温线常数((mg·g-1)/(mg·L-1)n),n为吸附强度,R为通用气体常数(8.314 J/(mol·K-1)),T为绝对温度(K).
吸附的热力学参数计算方法[27]为
Kc=55.5×1 000×b,
(6)
ΔG⊖=-RTlnKc,
(7)

(8)
其中Kc为热力学平衡常数,ΔG为Gibbs能量变化(kJ/mol), ΔH为焓变(kJ/mol),ΔS为熵变(kJ/(mol·K)).
2 结果与讨论
2.1 最佳配比

图1 VDE-1,VDE-2,VDE-0.5对硝酸盐的吸附量Fig.1 Adsorption capacity of VDE-1,VDE-2 and VDE-0.5 on nitrate
吸附剂配比直接决定功能单体的嫁接率,从而决定硝酸盐吸附位点的多少.不同物质的量比的乙烯基咪唑和二溴癸烷对硝酸盐吸附量如图1所示.由图1可见,随着硝酸盐平衡质量浓度的增大,VDE-1,VDE-2和VDE-0.5的吸附量增大.在整个硝酸盐的平衡质量浓度梯度范围内(5~70 mg/L),VDE-1对硝酸盐的吸附量均大于VDE-2和VDE-0.5,当硝酸盐的平衡质量浓度为70 mg/L时,VDE-1对硝酸盐的吸附量可达17.46 mg/g,VDE-2和VDE-0.5的吸附量分别为16.62,15.72 mg/g.表明当n(乙烯基咪唑)∶n(二溴癸烷)=1∶1时,在吸附剂上的咪唑基团与二溴癸烷发生季铵化反应的程度高于其他两种比例,在EDGMA物质的量确定的条件下,继续增加乙烯基咪唑的量,很难再与交联剂EDGMA发生交联反应.因此,实验选用乙烯基咪唑与二溴癸烷最佳物质的量比为1∶1,用于进行后续实验.
2.2 材料的表征
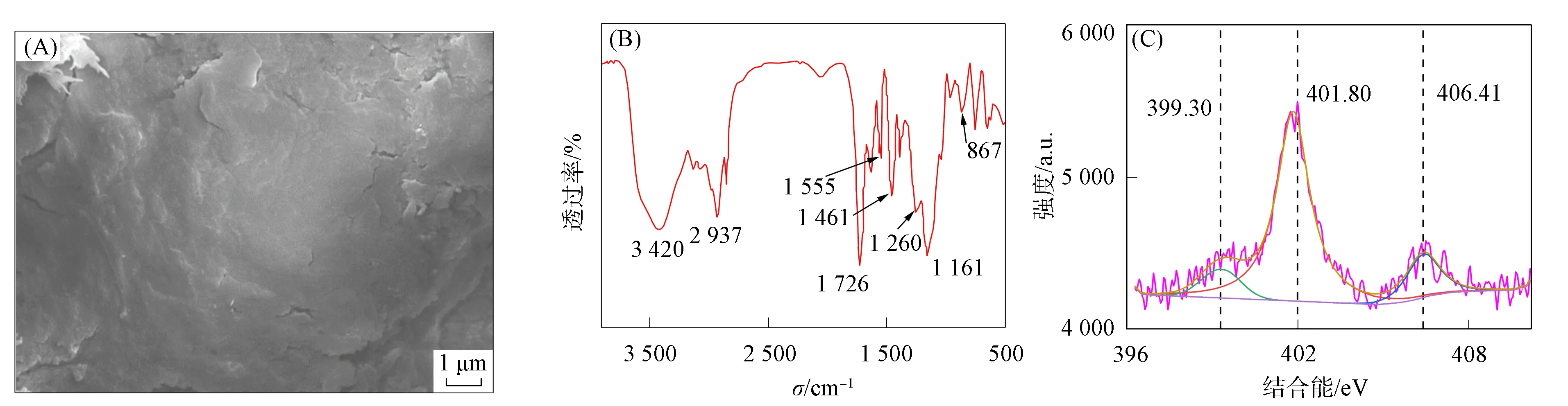
图2 VDE在吸附前的SEM照片(A),FT-IR(B)和XPS(C)Fig.2 SEM image (A),FT-IR (B) and XPS (C) of VDE before adsorption

2.3 投加量的影响
吸附剂的投加量是影响吸附剂处理硝酸盐废水出水浓度和吸附量的重要参数.不同VDE投加量对硝酸盐的吸附量及去除率的影响如图3所示.由图3可见,在含有100 mg/L的硝酸盐溶液中,当投入吸附剂VDE的量由0.8 g/L增加至4 g/L时,硝酸盐的去除率从41.38%增加至80.4%.可见,随着吸附剂投加量的增加,硝酸盐的去除率增大,这是由于投入较多的吸附剂,增加了硝酸盐溶液中VDE的吸附位点以及较大的表面积所致.随着吸附剂的增加,硝酸盐的吸附量降低,这是由于在一定质量浓度硝酸盐溶液中投加吸附剂,在初始阶段,由于吸附剂表面存在大量的吸附位点,因此硝酸盐在吸附剂表面与溶液间形成浓度差的推动下迅速到达VDE表面,在第二阶段,随着溶液中硝酸盐质量浓度的降低,其驱动力下降,使硝酸盐与吸附剂VDE间的离子交换过程速率减慢.此外,VDE颗粒空隙中存在固液界面膜阻力,硝酸盐无法到达吸附剂内部的空隙表面,使VDE中存在大量未饱和的吸附位点,导致吸附量下降,与Hu等[34]的研究结果相符.综合考虑去除率、吸附量以及经济因素,VDE的最佳投加量为3.2 g/L,此时去除率可达76.43%.
2.4 pH值的影响
溶液中pH值的影响是检测吸附材料性能的一项重要指标.不同pH值对VDE吸附硝酸盐的影响如图4所示.
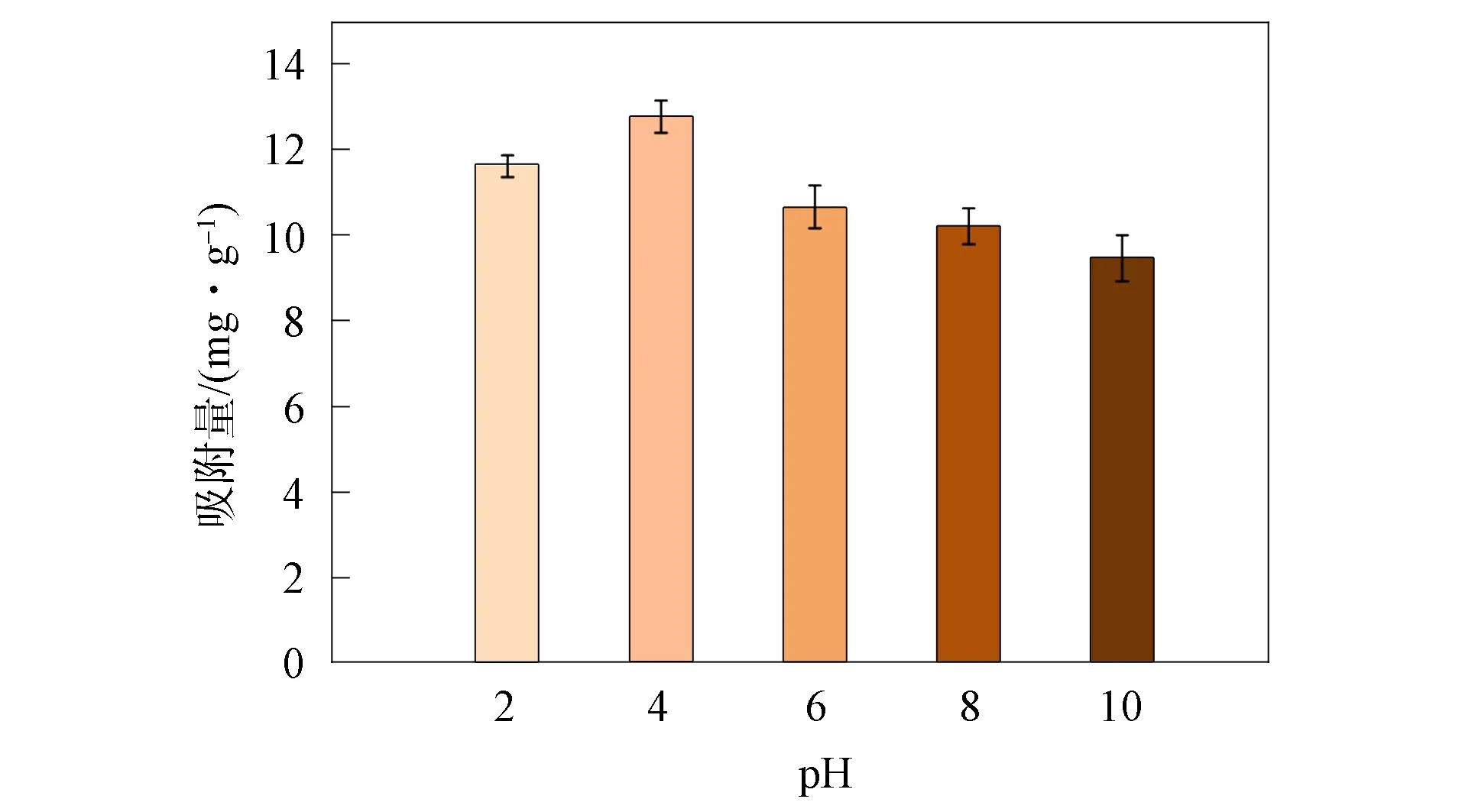
图4 不同pH值对VDE吸附硝酸盐的影响Fig.4 Effect of different pH values on adsorption of nitrate by VDE
由图4可见,随着pH值的增加,吸附剂VDE的吸附量呈先增加后迅速下降的趋势.当pH值从2上升到4时,硝酸盐的吸附量逐渐增加到最大值12.78 mg /g,表明在pH=4的条件下,由于吸附剂VDE中的咪唑基团可能与氢离子结合而带正电荷,因此增加了VDE的吸附位点,进而增大了对硝酸盐的吸附量[35].此外,pH=2时的吸附量是pH=4时吸附量的90.09%,表明在强酸条件下,VDE可能部分结构被破坏,导致VDE的吸附位点减小,吸附量略有降低.当pH值为6和8时,吸附量分别为最大吸附量的83.49%和80.0%,表明吸附剂在近似中性条件下有较好的稳定性.当pH值进一步升高,吸附量降低,可能是由于VDE中咪唑基团的氮正原子与H+间的结合作用减弱,从而发生脱质子化作用所致.在pH=10的碱性条件下,吸附量降低为最大吸附量(pH=4)的74.11%,其原因可能是: 1) 由于OH-与硝酸盐竞争吸附位点,将吸附剂咪唑基团上已吸附的硝酸盐置换下来;2) 过多的OH-中和了吸附剂中的正电荷,使其失去吸附效果,因此吸附剂VDE的吸附位点减少,硝酸盐的吸附量下降.Sowmya等[24]研究的季铵盐ADVEGR树脂在pH=2~8内吸附量基本不发生变化,其最大吸附量约为10 mg/g,但当pH>8时,其吸附量迅速下降,与本文研究的VDE在近似中性pH值范围内对硝酸盐吸附量几乎不发生变化相符.表明本文的吸附剂在中性及弱酸性条件下可获得较稳定的吸附量,其中吸附位点受氢离子影响较小,而在高浓度OH-存在时会受影响,吸附量与最大吸附量相比下降了25.89%.与Tsuchiya等[9]研究的改性活性炭和Chatterjee等[21]研究的交联壳聚糖相比,VDE在pH=2~10的条件下均能维持良好的稳定性,吸附量随着pH值变化波动较小.
2.5 吸附动力学
硝酸盐吸附动力学参数是评估VDE吸附硝酸盐快慢的一个重要指标.VDE吸附硝酸盐过程的准一级和准二级动力学模型及颗粒扩散模型的拟合曲线如图5所示.由图5(A)可见,硝酸盐的吸附量随时间的增加而上升.在0~4 min内,其吸附量最大为8.27 mg/g,且吸附速率迅速增大.在4~10 min内,VDE对硝酸盐的吸附速率逐渐下降,相应的吸附曲线逐渐缓和,硝酸盐的吸附量由8.27 mg/g上升至11.47 mg/L.在10 min后,硝酸盐的吸附量基本保持不变,这是由于吸附剂VDE中的吸附位点基本达到饱和,导致吸附量也达到了最大值.由图5(B)可见,根据颗粒内扩散模型,在整个吸附过程中,前4 min内吸附最快,即快速吸附阶段,这是由于硝酸盐在VDE固液界面间浓度差的推动下,迅速涌向吸附剂VDE表面并与吸附位点结合所致.4 min后,由于扩散推动力减弱,因此硝酸盐的吸附速率变小,直到10 min后不再发生变化.与Song等[36]研究的NDP-2,D201,purolite A300离子交换树脂的吸附过程相符.
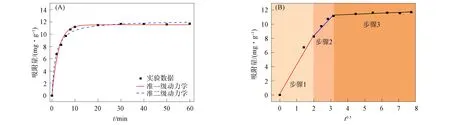
图5 VDE吸附硝酸盐过程的准一级和准二级动力学模型(A)及颗粒扩散模型(B)的拟合曲线Fig.5 Fitting curves of quasi-primary and quasi-secondary kinetic models (A) and particle diffusion model (B) for process of adsorption of nitrate by VDE


表1 VDE对硝酸盐吸附的动力学参数
2.6 等温吸附
采用Langmuir和Freundlich等温模型拟合实验数据,研究吸附量与平衡质量浓度的相互关系,结果如图6所示.由图6可见,在相同剂量的VDE下,随着硝酸盐初始质量浓度的增加,VDE吸附量增加.在相同硝酸盐初始质量浓度下,随着温度的上升,VDE对硝酸盐的吸附量下降.VDE对硝酸盐吸附的Langmuir和Freundlich等温模型参数列于表2.由表2可见,与Langmuir吸附等温模型相比,Freundlich模型对VDE整个吸附过程的拟合效果较好,在不同温度下(15,25,35 ℃)的相关系数均大于或等于0.99.表明硝酸盐在VDE表面上的吸附是表面不均匀的多分子层吸附.在Freundlich模型中,随着温度上升,KF值逐渐降低,表明VDE对硝酸盐的吸附过程是放热过程[38].在15 ℃条件下,Langmuir模型拟合的最大吸附量Qmax=28.31 mg/g.
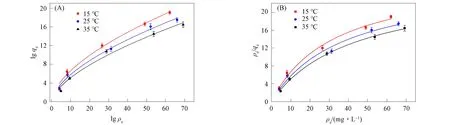
图6 VDE吸附硝酸盐的Langmuir(A)和Freundlich(B)等温模型拟合曲线Fig.6 Fitting curves of Langmuir (A) and Freundlich (B) isothermal model for adsorption of nitrate by VDE
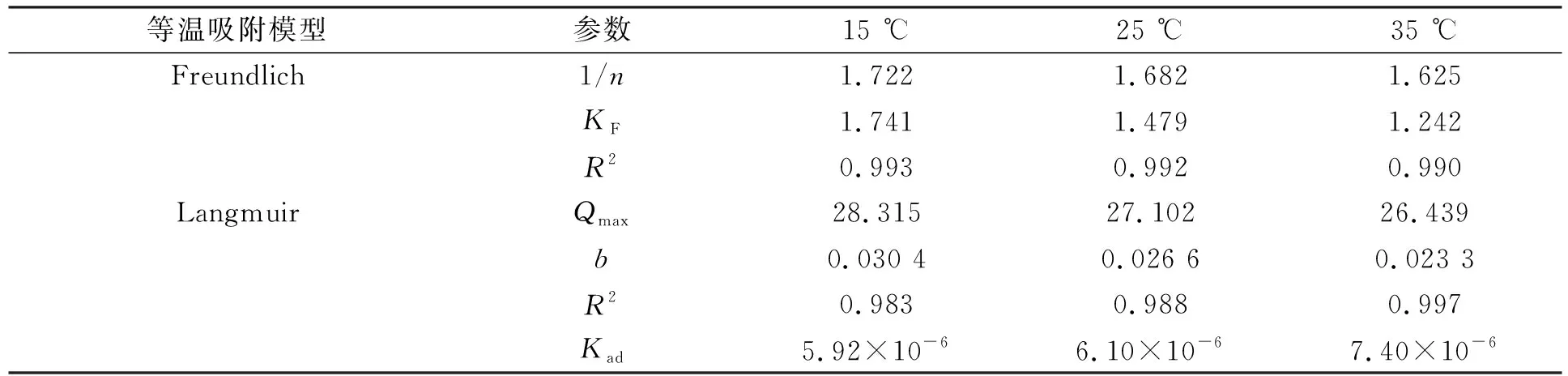
表2 VDE对硝酸盐吸附的Langmuir和Freundlich等温模型参数
2.7 吸附热力学
VDE对硝酸盐吸附的热力学参数列于表3.由表3可见,随着温度的增加,Gibbs自由能ΔG⊖变小,表明吸附剂VDE对硝酸盐的吸附反应是自发进行的.由lnKd与1/T的线性关系公式可得吸附过程产生的焓变ΔH⊖=-9.823 kJ/mol,表明吸附剂VDE对硝酸盐的吸附过程是一个放热反应,即在低温环境下可促进该吸附反应进行.吸附过程的熵变ΔS⊖=63.12 kJ/(mol·K),表明随着吸附反应的进行,VDE固液界面上的硝酸盐吸附反应向混乱度增加的方向进行,且升高温度更易于吸附反应进行[27].

表3 VDE对硝酸盐吸附的热力学参数
2.8 重复利用性的影响

图7 重复利用性对VDE吸附硝酸盐的影响Fig.7 Effect of reusability on adsorption of nitrate by VDE
重复利用性对VDE吸附硝酸盐的影响如图7所示.由图7可见,在整个循环过程中,随着解析次数的增加,VDE吸附硝酸盐的吸附量基本保持不变,当解析第5次时,其吸附量为10.19 mg/g,仍可达到首次使用吸附量(10.67 mg/g)的95.5%,表明VDE重复利用率较高且吸附剂中的吸附位点是可逆的,具有较好的稳定性,VDE并未随使用次数的增加而使表面吸附位点减少,与Yang等[39]研究的季铵盐改性纳米复合材料的重复利用率相符.
综上所述,针对硝酸盐污染的问题,本文合成了一种新型的聚合物乙烯基咪唑/二溴癸烷/二甲基丙烯酸乙二醇,通过扫描电子显微镜、Fourier变换红外光谱仪和X射线光电子能谱对其结构进行表征,并研究其在含硝酸盐水溶液的最佳剂量比、pH值、吸附温度、吸附时间以及重复利用性.结果表明,在15 ℃,pH=4时,VDE对硝酸盐氮的吸附量通过Langmuir模型拟合为28.31 mg/g,该吸附过程在10 min可达到平衡,且符合准一级和准二级动力学拟合模型,相关系数R2>0.99.此外,通过吸附热力学模型计算,VDE的吸附过程属于放热反应.在5次吸附/脱附实验后,其吸附量仍可达到首次使用吸附量的95.5%,表明该材料可有效净化低质量浓度的硝酸盐废水,具有一定的应用前景.
