舒肝解郁胶囊治疗抑郁症的系统评价再评价
2023-02-15马华萍韩振蕴胡文悦常泽王育纯胡玉立
马华萍 ,韩振蕴 ,胡文悦 常泽 王育纯 胡玉立
1.北京中医药大学,北京 100029; 2.北京中医药大学深圳医院(龙岗),广东 深圳 518100
抑郁症是一种严重的情绪障碍,以情绪低落、精力降低、失去兴趣为主要特征,常伴有焦虑、认知障碍、精神运动发育迟缓,甚至有自杀倾向[1]。世界卫生组织(WHO)报道,2015年全球抑郁症患者总数为3.22亿,其中中国抑郁症患者约5 400万人[2]。根据我国抑郁症社会负担与经济负担组织的研究结果显示,我国每年抑郁症疾病支出至少为300亿人民币,占精神疾病总负担的47%,占全部疾病负担的6.2%,在中国疾病经济负担排位中居第2位[3]。2008年时抑郁症被WHO列为全球疾病负担的第三大原因,预计到2030年将排名第一[4]。抑郁症对患者的心理健康有严重影响。
舒肝解郁胶囊是国内首个获得批准用于治疗抑郁症的中成药[5],自2009年上市以来,广泛应用于治疗轻中度抑郁症及卒中后抑郁[6-7]、轻中度抑郁障碍共病焦虑障碍[8-9]、其他疾病(如高血压、阿尔茨海默病等)伴发轻中度抑郁障碍[10-11]等,积累了丰富的临床证据。越来越多研究关注舒肝解郁胶囊的药理学作用机制[12-13]和成分测定[14]的基础研究。目前已有较多被认为是当前最高级别证据的系统评价(systematic review,SR)/Meta分析(Meta-analysis,MA)对舒肝解郁胶囊治疗抑郁症的疗效和安全性进行评价,但尚无研究对这些SR/MA的质量进行再评价分析,无法得知证据概貌。本研究对已公开发表的SR/MA及其结局指标的方法学质量、报告质量及证据水平进行综合评价,以期为舒肝解郁胶囊的临床应用提供循证参考。
1 资料与方法
1.1 纳入标准
①研究对象:评价舒肝解郁胶囊治疗抑郁症的随机对照试验(RCT)疗效和安全性的SR/MA,其中抑郁症包括原发、继发或合并其他疾病。②干预措施:治疗组单用舒肝解郁胶囊或舒肝解郁胶囊联合其他抗抑郁治疗;对照组采用安慰剂、空白对照或西医治疗。③结局指标无限制。
1.2 排除标准
①数据重复发表、数据不完整及无法获得全文的研究,网状Meta分析;②仅为描述性的系统综述;③SR/MA的质量评价或方法学研究的文献。
1.3 检索策略
计算机检索中国知识资源总库(CNKI)、万方数据知识服务平台(万方数据)、中文科技期刊数据库(维普网)、中国生物医学文献数据库(CBM)、PubMed、Web of Science、Cochrane Library,并查询Clinical Trials.gov和中国临床试验注册中心两大临床试验注册系统,收集舒肝解郁胶囊治疗抑郁症的中英文文献。检索时间范围自建库至2022年2月,同时追溯纳入研究的参考文献以补充获取相关文献。检索采用主题词与自由词相结合的方式,中文检索词主要为舒肝解郁胶囊、安佳欣、抑郁症、抑郁障碍、抑郁发作、系统评价、meta分析、荟萃分析等;英文检索词主要为 Shugan Jieyu Capsule、 Depression、 Major depressive disorder、 MDD、 systematic review、system evaluation、Meta-analysis、Meta analysis等。根据各数据库检索特征调整检索策略。
1.4 文献筛选和数据提取
由2名研究者独立完成文献检索,并将初检文献导入NoteExpress3.0自动筛重,阅读文献题目和摘要,对文献进行筛选。使用Excel2016设计文献信息汇总表,对最终纳入的文献提取以下信息:第一作者姓名和发表年份、疾病类型、干预措施、偏倚风险评估工具、主要研究结论、基金信息等。交叉核对结果,若意见不统一则与第三方讨论解决。
1.5 评价方法
1.5.1 方法学质量评价
采用AMSTAR-2工具[15]评价纳入研究的方法学质量,共16个条目,其中重要条目为条目2、4、7、9、11、13、15。评价结果以“是”“部分是”“否”表示。根据重点条目和非重点条目结果对纳入研究方法学质量进行评级,无或仅有1个非关键条目不满足为高级,超过1个非关键条目不满足为中级,1个关键条目不满足且伴或不伴非关键条目不满足为低级,超过1个关键条目不满足且伴或不伴非关键条目不满足为极低级。
1.5.2 报告质量评价
采用PRISMA声明[16-17]评价纳入SR/MA的报告质量,共27个条目。评分原则:每个条目完整报告计1分,部分报告计0.5分,未报告计0分,满分27分:21~27分为报告相对完全,15~20分为报告有一定缺陷,<15分为有相对严重的信息缺陷。
1.5.3 证据质量评价
采用GRADE系统[18]从局限性、不一致性、间接性、不精确性、发表偏倚5个方面评价纳入系统评价的主要结局指标证据质量,证据质量分为高级、中级、低级、极低级。
1.5.4 疗效评价
采用描述性统计方法报告纳入SR/MA的结局指标定量分析结果,以标准差(SMD)、加权平均偏差[(W)MD]、比值比(OR)或相对风险(RR)等的点估计值和95%置信区间(CI)等形式汇总报告。
2 结果
2.1 检索结果
初检出相关文献56篇,经逐层筛选后排除重复文献25篇,阅读题目及摘要后排除非SR/MA文献、网状Meta分析等,初步纳入14篇文献,通过全文阅读,排除数据不完整的研究,最终纳入11篇文献[19-29]。
2.2 文献基本信息
纳入11篇SR/MA中10篇[19-26,28-29]为中文,1篇为英文[27],发表时间2013-2021年。每篇纳入的原始文献数量6~24篇,总样本量354~2 398例。11篇SR/MA均纳入RCT。5篇[20,24-26,28]的试验组干预措施仅为舒肝解郁胶囊,其余研究的试验组干预措施为舒肝解郁胶囊单用或联合安慰剂或其他抗抑郁药。所有纳入SR/MA均未报告结局指标随访时间。仅使用Cochrane偏倚风险评估工具对纳入研究进行质量评价5篇[19,23,26-28],使用Jadad量表3篇[20,25,29],两者均使用3篇[21-22,24]。有基金支持4篇[19-22],未报告是否有基金支持7篇[23-29]。纳入研究基本特征见表1。
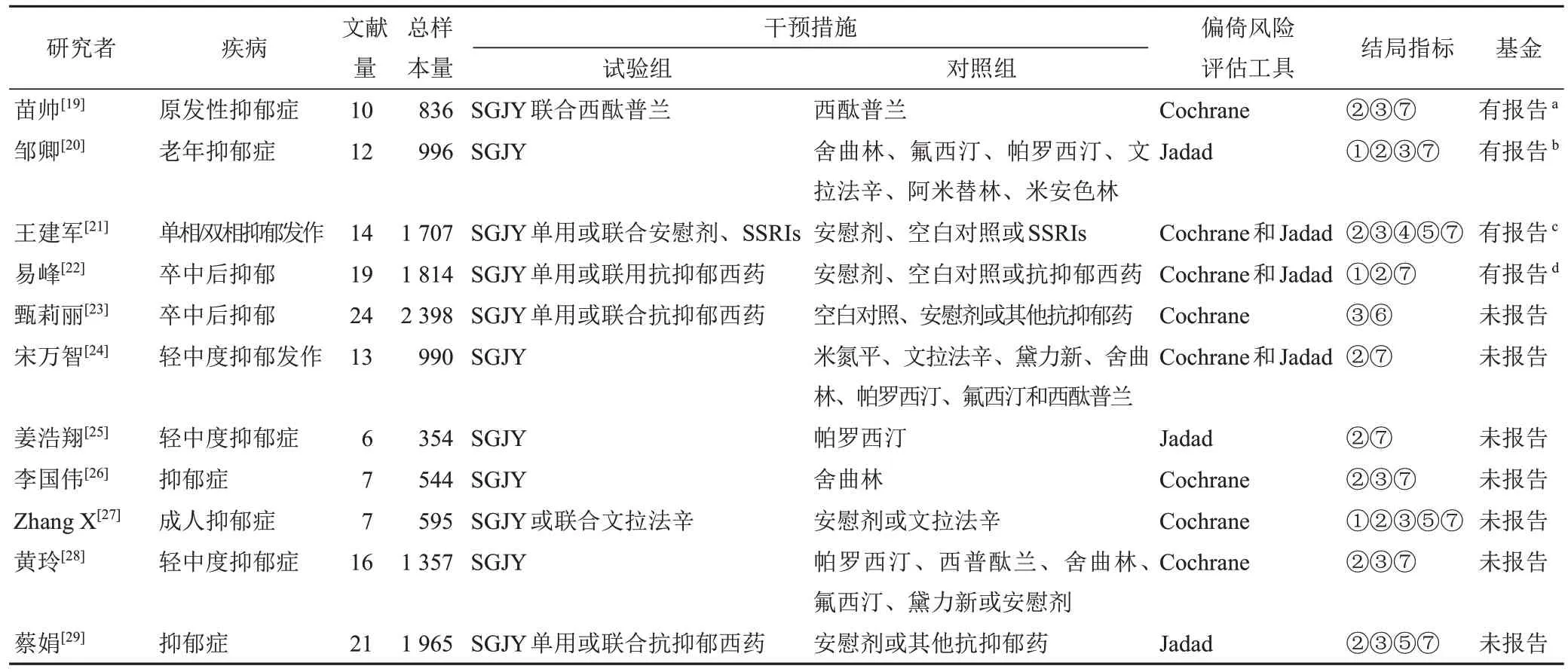
表1 11篇舒肝解郁胶囊治疗抑郁症SR/MA基本信息
2.3 方法学质量评价
AMSTAR-2评价结果显示,条目1(100%)、条目5(100%)、条目6(100%)、条目8(81.8%)、条目11(100%)和条目15(72.7%)的完全报告率均>70%,条目2(50%)、条目4(50%)和条目9(63.6%)的报告率50%~70%,条目12(9.1%)、条目13(27.3%)和条目14(9.1%)的报告率<30%,而其他条目的报告率均为0%。11篇SR/MA中仅1篇[22]存在1个关键条目(条目7)不符合,合并3个非关键条目(条目3、10、16)不符合,其方法学质量为低质量;其余10篇SR/MA存在1个以上关键条目不符合,合并多个非关键条目不符合,方法学质量为极低质量。各条目评价结果见表2。
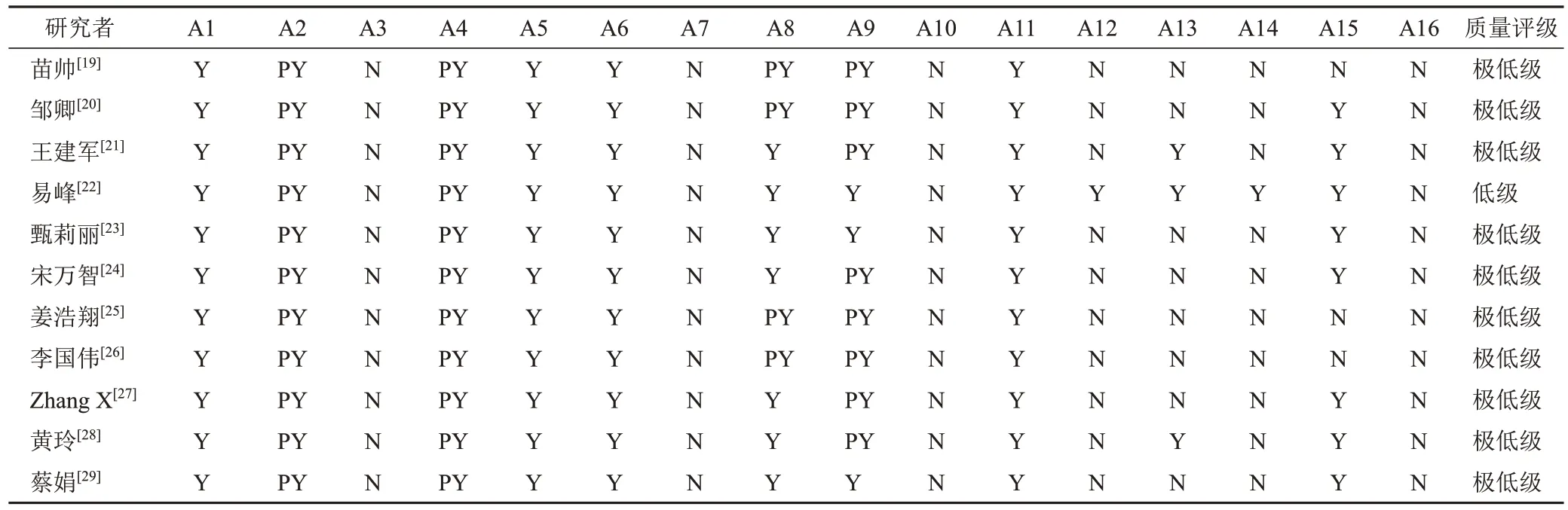
表2 11篇舒肝解郁胶囊治疗抑郁症SR/MA方法学质量评价
2.4 文献报告质量评价
经PRISMA声明进行报告质量评价后,9篇[19-24,27-29]报告质量评分15~20分,报告有一定缺陷;2篇[25-26]评分<15分,报告信息相对缺陷严重。11篇均对“标题”“目的”“研究选择”“概括效应指标”“结果综合”5个条目的内容报告完全,但均未报告“方案和注册”,其余条目有不同程度的报告不够全面。各条目评价结果见表3。
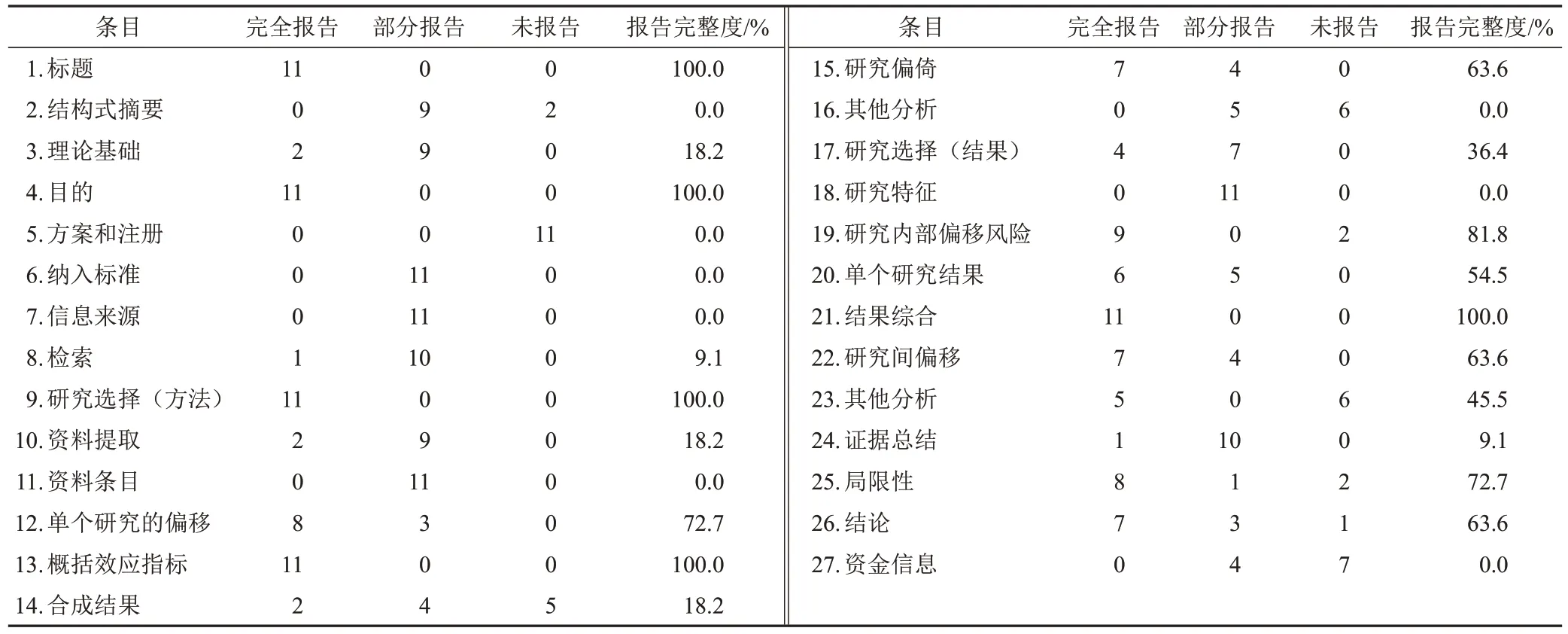
表3 11篇舒肝解郁胶囊治疗抑郁症SR/MA报告质量评价(篇)
2.5 结局指标
纳入的SR/MA中报告的结局指标共36个,每个结局指标的综合效应值见表4;运用GRADE系统对每个结局指标进行质量评价,结果见表5。
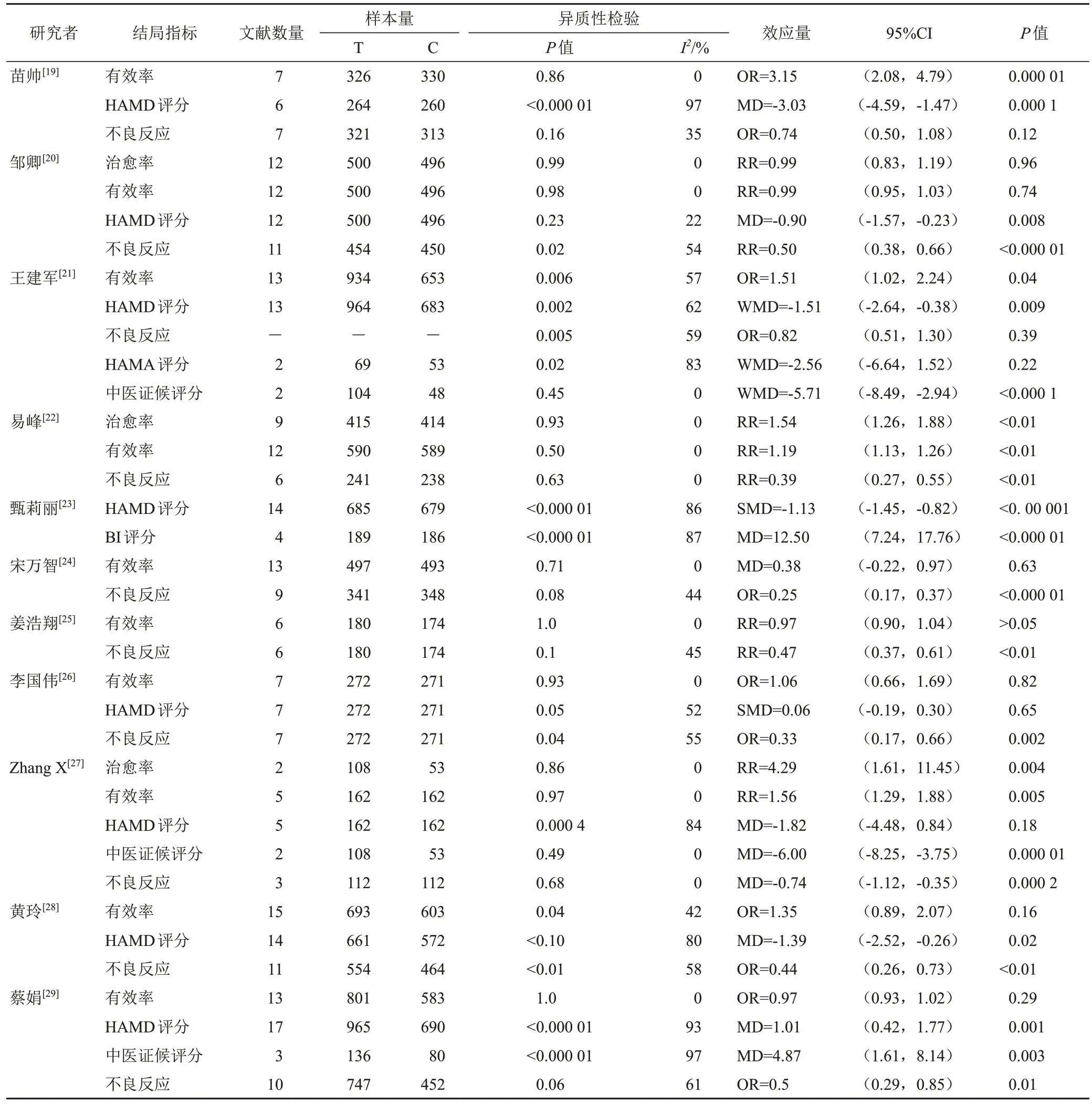
表4 舒肝解郁胶囊治疗抑郁症的SR/MA中不同结局指标的综合效应值
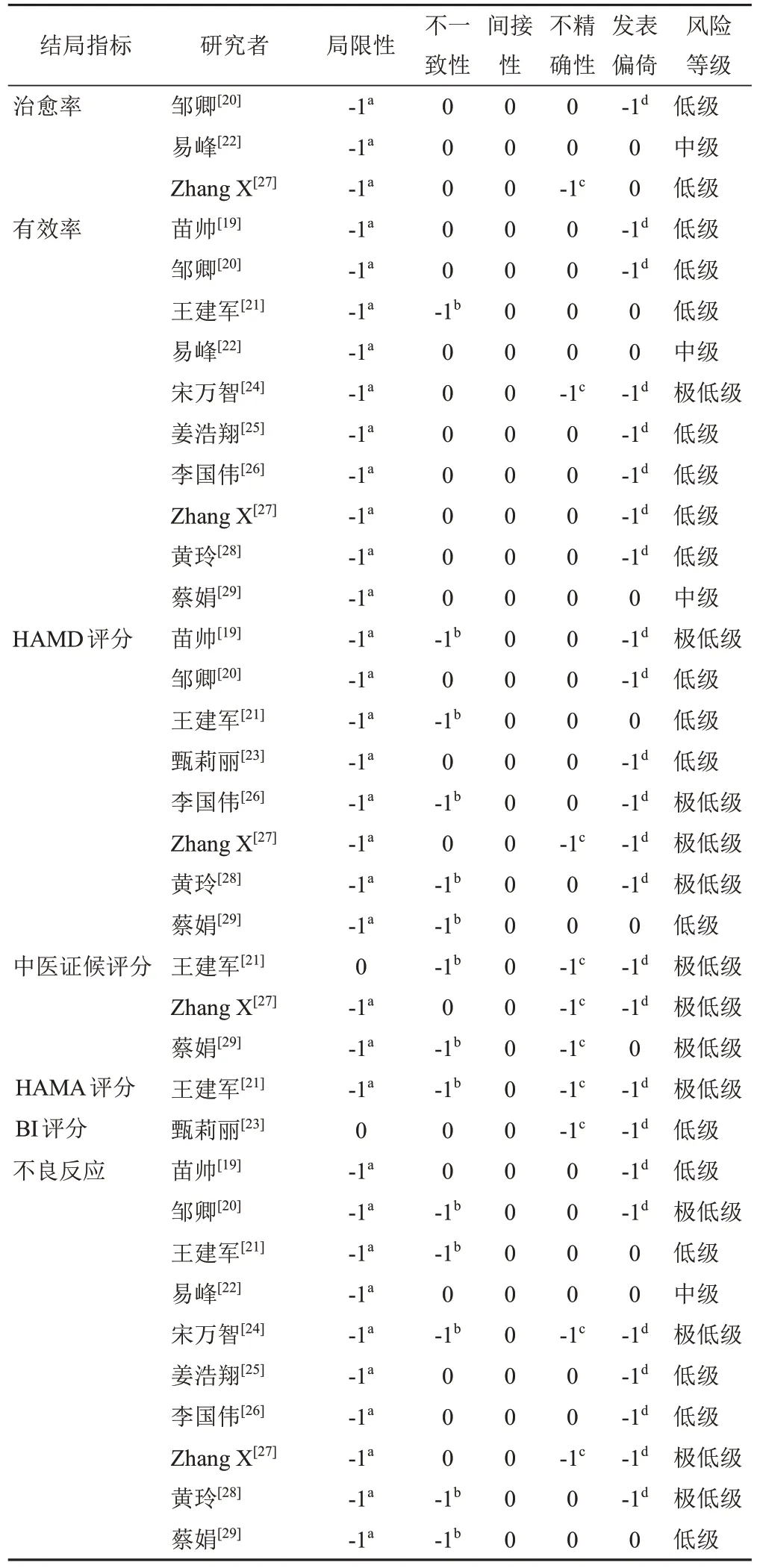
表5 纳入研究的结局指标GRADE分级
2.5.1 治愈率
3篇[20,22,27]报告了治愈率,其中1篇[20]为低级证据,研究表明单用舒肝解郁胶囊与其他抗抑郁药物(舍曲林、氟西汀、帕罗西汀、文拉法辛、阿米替林、米安色林等)相比,治愈率相当,差异无统计学意义。1篇[22]为中级证据,研究结果为舒肝解郁胶囊联用其他抗抑郁药的治愈率优于其他抗抑郁药组。1篇[27]表明舒肝解郁胶囊组的治愈率优于安慰剂组,为低级证据。
2.5.2 有效率
10篇[19-22,24-29]报告了有效率,舒肝解郁胶囊联合其他抗抑郁药的疗效优于单用其他抗抑郁药,而单用舒肝解郁胶囊与其他抗抑郁药相比疗效相当。其中2篇[22,29]为中级证据,7篇[19-21,25-28]为低级证据,1篇[24]为极低级证据。
2.5.3 汉密顿抑郁量表评分
8篇[19-21,23,26-29]报告了 HAMD 评分,其中 4篇[20-21,23,29]为低级证据,4篇[19,26-28]为极低级证据。结果显示单用舒肝解郁胶囊或联合其他抗抑郁药时,对HAMD评分改善率均高于对照组。
2.5.4 汉密顿焦虑量表评分
1篇[21]报告了HAMA评分,为极低级证据。该研究表明舒肝解郁胶囊组与对照组相比,能改善患者的HAMA评分。
2.5.5 中医证候评分
3篇[21,27,29]对中医证候评分进行报告,均为极低级证据。研究表明舒肝解郁胶囊治疗抑郁症,与安慰剂相比,能有效改善患者的中医证候评分。
2.5.6 BI量表评分
1篇[23]报告了BI量表评分,为低级证据。研究提示使用舒肝解郁胶囊联合其他抗抑郁药(米氮平、帕罗西汀、西酞普兰)或常规治疗,可有效改善卒中后抑郁症患者的BI量表评分,且优于对照组。
2.5.7 不良反应
10篇[19-22,24-29]报告了不良反应,1篇[22]为中级证据,5篇[19,21,25-26,29]为低级证据,4篇[20,24,27-28]为极低级证据。2篇[19,22]提及舒肝解郁胶囊与其他抗抑郁药联用时的不良反应,与单用其他抗抑郁药相比无明显差别,表明舒肝解郁胶囊联合其他抗抑郁药时,不会增加不良反应。7篇[20,24-29]的研究中单用舒肝解郁胶囊在不良反应方面低于其他抗抑郁药物,不良反应以头晕、恶心、食欲减退症状更常见,未报道严重不良反应。1篇[21]研究报道舒肝解郁胶囊的中枢神经系统和胆碱能系统不良反应,与对照组差异无统计学意义,而舒肝解郁胶囊组消化系统不良反应发生率低于对照组。
3 讨论
系统评价再评价是以同一疾病或同一健康问题的病因、诊断、治疗或预后方面的相关SR/MA为研究对象,运用综合方法对其质量及证据级别进行评定的一种研究方法,有利于证据资料的集中,可为证据使用者提供证据概况,并为临床决策提供更为可靠的证据[30-31]。
AMSTAR-2是系统评价方法学质量评价工具,具有较好的评价者间一致性和实用性,其适用范围包括基于RCT或非RCT或两者都有的系统评价[32]。本研究经AMSTAR-2的16个条目评价后,1篇SR/MA[22]方法学质量为低质量;其余10篇均为极低质量,无中高质量研究,所纳入的研究方法学质量都有待提高。主要存在以下问题:①纳入研究均未将前期研究方案(包括PICOs化的研究问题、需检索的数据库、纳排标准、数据信息提取等内容)进行提前注册或发表在杂志上,也未详细解释在计划实施过程中与前期计划方案是否有不一致处。②纳入的SR/MA均只提及纳入研究设计类型,但未对选择此研究类型的原因予以解释。③未对灰色文献、相关临床试验数据库或未发表的相关报告等进行检索,可能导致检索不全面。④均未提供文献筛选过程中被排除的文献清单,仅简述排除理由。⑤未报告纳入原始研究的资金相关信息,无法判断资金是否会对评价结果产生偏倚。⑥多数SR/MA未在讨论和解释结果时提及单个偏倚风险对结果的影响。⑦多数SR/MA未对存在明显异质性的结局指标进行亚组分析或敏感性分析探究异质性来源,仅简单根据异质性检验P<0.1和I2>50%结果选择随机效应模型对异质性资料数据进行合并分析,降低了研究质量和可信度。⑧虽然4项SR/MA[19-22]报告了资金来源,但均未申明是否存在利益冲突。
PRISMA声明旨在帮助作者改善SR/MA分析的报告质量,其适用于各类型SR,特别是干预性研究的SR;此外,PRISMA还可用于评价SR的报告质量[33]。参照PRISMA声明对纳入的SR/MA的报告质量进行评价,得出纳入研究普遍报告信息不完全,其中2篇SR/MA[25-26]报告信息相对缺陷严重。需从以下方面完善报告内容:①多数研究未明确该SR是对已有SR的更新,还是新的SR;②未对研究中的亚组分析、敏感性分析、回归分析等进行解释说明;③部分研究无文献筛选流程图或未给出Meta分析后的森林图;④未报告每一个主要结局证据强度,也未分析其与主要利益相关群体(如医务工作者、患者及政策决策者等)的关联性;此外,关于研究方案的注册、充分检索文献、信息提取完全(包括随访时间、文献出处、原始研究资金信息等)、探究可能的异质性来源,以及资金和利益冲突管理相关的内容与AMSTAR-2重合,不再详述。
GRADE系统是目前国际认可度最高的证据质量评价与推荐分级标准。运用GRADE系统对纳入的11个SR/MA的36个结局指标(共7类)进行证据分级,除治愈率中有1个中级证据、有效率中有2个中级证据,不良反应中有1个中级证据,其他结局指标多是低级甚至极低级的证据,证据质量有待提高。降级最多的因素是研究局限性,主要是半随机或假随机等随机方法不正确、未实施分配隐藏和盲法、选择性报告结局等,即在RCT方法学设计上存在较大缺陷;其次在不一致性(因纳入研究异质性高、可信区间重叠较少,但未从患者、干预措施、对照措施、结局等方面探究异质性来源和给出合理解释)、不精确性(纳入研究较少,样本量较少,导致可信区间不够窄)、发表偏倚(漏斗图不对称,或纳入研究较少,发表偏倚不清楚)方面也出现降级。
综合11篇SR/MA结果表明,舒肝解郁胶囊治疗抑郁症疗效较好,能有效降低抑郁症患者的HAMD评分、中医证候评分等,并能辅助改善卒中后抑郁患者的生活质量;单用舒肝解郁胶囊疗效与其他抗抑郁药(包括舍曲林、帕罗西汀、氟西汀、西酞普兰、米氮平、文拉法辛、黛力新等)相当,且不良反应较其他抗抑郁药少,而联用其他抗抑郁药时疗效优于单用其他抗抑郁药,且不会增加不良反应,安全性较好,但临床使用时需注意其中枢神经系统、胆碱能系统不良反应。研究中使用剂量为1.44 g/d,干预疗程多为6~8周,但因无随访信息,无法判断舒肝解郁胶囊治疗抑郁症的长期疗效。本研究纳入了舒肝解郁胶囊治疗抑郁症相关SR/MA,无论原发性抑郁或继发性抑郁,因目前缺乏舒肝解郁胶囊治疗原发性抑郁及继发性抑郁的横向比较,尚不能得知舒肝解郁胶囊对二者的疗效差异。
纳入SR/MA的结局指标多为根据HAMD减分率判断的治愈率、有效率及HAMD评分,而目前有3种HAMD量表版本HAMD-17、HAMD-21和HAMD-24,并且HAMD减分率标准也不相同,有可能会造成异质性较高,建议尽可能细分亚组进行Meta分析。此外,辨证是中医治疗的关键,但大部分研究都未报告与中医特征相关的指标。有2篇SR/MA[21,27]虽报告了中医证候量表评分这一结局指标,但未说明量表来源和细节;在蔡娟[29]研究里,中医证候量表评分纳入的原始研究中有说明根据《中药新药临床研究指导原则(试行)》[34]以肝郁脾虚型抑郁症的中医证候学标准为基础,结合临床经验,制定肝郁脾虚型抑郁症的自拟症状分级量化评分表[35],但因未进行标准化论证该量表的信度和效度,因此无法客观评价舒肝解郁胶囊治疗抑郁症的中医证候改善效果。
本研究尚存在一定局限性:由于仅纳入公开发表且被数据库收录的中、英文SR/MA,可能会有灰色文献漏检;可能受发表杂志版面限制,部分研究未能报告完全,使报告质量评价结果可能低于实际情况;纳入的SR/MA质量不高,评价结果可能存在偏倚。
4 结语
本研究表明,虽然SR/MA提示舒肝解郁胶囊能有效改善患者的抑郁症状,降低HAMD评分、中医证候评分等,且不良反应少,安全性较高。但由于SR/MA纳入的原始研究方法学质量欠佳,使证据水平较低,多为低级或极低级证据,因此,舒肝解郁胶囊治疗抑郁症的有效性和安全性仍需更多设计和实施严谨的高质量临床试验进一步验证,也为系统评价提供高质量、高水准的原始文献。相关SR/MA的制作应重视报告规范,遵循AMSTAR-2量表和PRISMA声明相关条目实施。
