左甲状腺素联合131I治疗甲状腺功能亢进症的临床研究
2023-02-14张学敏张高潮宋晏冯昭刘佳楹陈正福
张学敏,张高潮,宋晏,冯昭,刘佳楹,陈正福
(三二〇一医院核医学科,陕西 汉中 723000)
甲状腺功能亢进症高发于女性,患者以消瘦、食欲亢进、甲状腺肿大等为主要表现,同时伴随眼部综合征、心力衰竭等多种并发症,更有甚者出现甲状腺危象[1-2]。弥漫性甲状腺肿(Graves病)是引发甲亢的主要原因,约占总发病率的80%[3]。临床治疗甲亢以纠正代谢紊乱、缓解甲状腺亢进为基本原则,多采用131I、抗甲状腺药物及手术干预,其中131I主要适用于甲状腺肿大Ⅱ度以上患者,抗甲状腺药物主要适用于轻中度甲亢患者[4]。近年来多项研究指出,左甲状腺素辅助治疗可明显提高甲亢的临床疗效。如,江巍等[5]证明给予68例甲亢患者小剂量131I及左甲状腺素联合治疗,可有效降低甲状腺自身抗体水平;李静[6]发现与甲硫咪唑单一治疗相比,左甲状腺素联合治疗儿童甲亢的消肿效果更明显。为探究更多甲亢患者的治疗可能性,本研究拟分析左甲状腺素联合131I的干预效果。
1 资料与方法
1.1 一般资料
回顾性分析2018年3月至2021年3月三二〇一医院收治的334例甲亢患者的临床资料,依据治疗方式不同分为观察组和对照组,每组均纳入167例患者。纳入标准:(1)经临床超声、血液生化等检查确诊,并符合《内科学》[7]中甲亢的诊断标准:高代谢症状及体征、甲状腺肿大、血清促甲状腺激素(thyroid stimulating hormone,TSH)水平降低、甲状腺激素水平升高;(2)年龄45~75岁,入组前未接受抗甲状腺类药物、放射碘及相关外科手术治疗者;(3)临床资料完整者。排除标准:(1)131I及左甲状腺素过敏者;(2)合并骨质疏松症、血液疾病及恶性肿瘤者;(3)合并其他甲状腺疾病或因其他疾病引发甲亢者;(4)服用免疫抑制剂或影响钙磷代谢的药物者。两组一般资料比较,差异无统计学意义(P>0.05)。见表1。
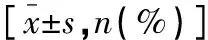
表1 两组一般资料比较
1.2 方法
1.2.1 对照组 患者接受甲亢常规治疗及131I干预。患者入组后均采用常规抗感染、补钙、镇静安神治疗,叮嘱患者注意休息,避免情绪激动,低碘饮食,注意补充维生素,少食刺激性食物;碘(131I)化钠口服液空腹口服,服用剂量=[甲状腺重量(g)×(每克甲状腺计划量)]/24 h碘摄入量;连续给药3个月。
1.2.2 观察组 患者在对照组的基础上接受左甲状腺素钠片联合治疗。常规治疗及131I用法用量同对照组;同时接受德国默克Merck KGaA公司左甲状腺素钠片口服治疗,起始剂量为12.5 μg/d,第2周增加至25 μg/d,连续给药3个月;治疗过程中密切关注患者是否出现心律不齐、胸闷等不良反应,及时处理。
1.3 观察指标
(1)比较两组患者治疗前及治疗后的血清甲状腺激素水平、甲亢相关蛋白及抗体水平、血脂水平:两组患者于治疗前后留取清晨空腹外周静脉血,高速离心,留取上层血清,采用Maglumi 2000全自动化学发光免疫分析仪,以免疫化学发光法检测甲状腺球蛋白抗体(anti-thyroglobulinantibodies,TgAb)、甲状腺球蛋白(thyroglobulin,Tg)、甲状腺过氧化物酶抗体(thyroid peroxidase antibody,TPOAb)、TSH、游离三碘甲状腺原氨酸(free triiodothyronine 3,FT3)、游离四碘甲状腺素(free triiodothyronine 4,FT4)水平;采用全自动化学分析仪检测总胆固醇(total cholesterol,TC)、高密度脂蛋白胆固醇(high density liptein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low density liptein cholesterol,LDL-C)水平;(2)甲状腺体积:采用彩色多普勒超声检测仪检测两组治疗前及治疗后的甲状腺长、宽、厚,并计算甲状腺体积;(3)记录两组用药期间肝损伤、皮肤过敏、继发甲减等不良反应发生情况。
1.4 统计学分析
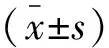
2 结果
2.1 两组患者治疗前后血清甲状腺激素水平比较
观察组治疗后的血清TSH水平高于同组治疗前及对照组(P<0.05),血清FT3、FT4水平低于同组治疗前及对照组(P<0.05)。见表2。
2.2 两组患者治疗前后甲状腺体积比较
观察组治疗前的甲状腺体积为(19.78±5.42)cm3,治疗后的甲状腺体积为(9.21±2.03)cm3;对照组治疗前的甲状腺体积为(19.82±5.64)cm3,治疗后的甲状腺体积为(10.64±2.52)cm3;观察组治疗后的甲状腺体积小于对照组(t=5.711,P<0.05)。
2.3 两组患者治疗前后甲亢相关蛋白及抗体水平比较
观察组治疗后的血清TPOAb、TgAb、Tg水平低于同组治疗前及对照组(P<0.05)。见表3。
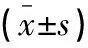
表2 两组患者治疗前后血清甲状腺激素水平
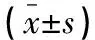
表3 两组患者治疗前后甲亢相关蛋白及抗体水平
2.4 两组治疗前后血脂水平比较
治疗前,两组血清TC、HDL-C、LDL-C水平比较,差异无统计学意义(P>0.05);治疗后,观察组血清HDL-C水平高于同组治疗前及对照组(P<0.05),血清TC、LDL-C水平低于同组治疗前及对照组(P<0.05)。见表4。
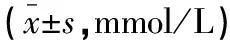
表4 两组治疗前后血脂水平
2.5 两组治疗期间不良反应发生情况比较
观察组治疗期间皮肤过敏5例,肝功能损伤3例,白细胞减少两例,心律不齐3例,头痛两例,其他6例,总不良反应发生率为12.57% (21/167);对照组皮肤过敏3例,肝功能损伤两例,恶心5例,继发甲减3例,白细胞减少1例,其他4例,总不良反应发生率为10.78% (18/167);两组治疗期间不良反应发生率比较,差异无统计学意义(χ2=0.261,P>0.05)。
3 讨论
甲亢是由甲状腺激素分泌异常引发的代谢亢进及交感神经兴奋的内分泌疾病,机体甲状腺激素的分泌水平受垂体、下丘脑等多种反馈机制的调节,当分泌过多时,可诱发甲亢[8]。131I治疗甲亢效果明确、复发少、费用低,该疗法可通过甲状腺的碘摄取能力及β射线,以抑制甲状腺素的分泌,从而改善甲状腺功能,控制疾病进展[9]。131I治疗不会增加白血病、肿瘤等疾病发生率[10]。但部分患者接受131I治疗后易出现甲状腺功能减退及甲状腺相关性眼病等不良反应,应重视临床随访,及时处理并发症[11]。本研究给予甲亢患者左甲状腺素联合131I疗法,获得良好干预效果,为甲亢的临床治疗提供新思路。
本研究发现左甲状腺素联合131I治疗在改善甲状腺激素水平方面显著优于131I单独治疗,观察组患者治疗后的血清TSH、FT3、FT4水平较对照组明显改善。血清TSH、FT3、FT4水平是诊断甲状腺疾病及评估患者预后的重要指标[12-13]。左甲状腺素钠片口服后主要在小肠上端被吸收,在机体中转化为三碘甲状腺素,通过与相关受体结合调节垂体-甲状腺轴,以改善甲亢症状,与甲状腺片相较,左甲状腺素钠片的生物活性更高,起效稳定性好,常用于甲亢的辅助治疗[14]。Tg主要由甲状腺滤泡上皮细胞分泌,生理状态下,其水平由甲状腺大小决定,当机体Tg水平减退时提示甲状腺功能受损[15]。TgAb及TPOAb是诊断及评估甲状腺疾病的标志物,TPOAb可催化甲状腺激素,引起甲状腺组织损伤,TgAb本身无破坏作用,但其与Tg结合后作用于Fc受体,起到破坏甲状腺细胞的作用[16]。本研究显示观察组患者治疗后的TPOAb、TgAb、Tg水平及甲状腺体积显著低于对照组,左甲状腺素联合131I治疗甲亢可有效保护甲状腺功能。
本研究中,两组患者治疗后的血清HDL-C、TC、LDL-C水平较治疗前明显改善,且以观察组较为显著,与刘义粉等[17]研究结论基本一致,证明左甲状腺素可调节血脂,改善代谢,分析原因可能与左甲状腺素可诱导特殊酶系的新生蛋白质的合成,调节机体蛋白质、脂肪、无机盐等代谢平衡的作用相关。此外,本研究还表明观察组皮肤过敏、肝功能损伤、心律不齐等不良反应发生率为12.57% (21/167),对照组继发甲减、白细胞减少等不良反应发生率为10.78% (18/167),组间比较,差异无统计学意义,提示左甲状腺素治疗甲亢,安全性高,具有良好的临床应用基础。
综上,左甲状腺素联合131I治疗甲亢疗效确切,安全性高。该疗法可有效控制甲状腺肿大,调节血脂及甲状腺激素水平,降低血清TPOAb、TgAb、Tg水平,保护甲状腺功能。
