磁性四氧化三铁纳米粒的制备、表面改性及表征*
2023-01-30王高强卯明艳余开湖
王高强,卯明艳,余开湖,2**
(1.湖北科技学院医学部药学院,湖北 咸宁 437100;2.咸宁市中心医院)
在医药领域,针对氧化铁的研究很多,这主要是因为氧化铁比其他磁性材料具有更好的靶向性、生物兼容性、生物降解性和生物安全性[1]。氧化铁在自然界中自然存在,也可以在实验室中合成。超顺磁性氧化铁纳米粒(SPIONS)是一种新型的超顺磁性纳米材料,已广泛应用于磁共振成像、肿瘤热疗、靶向给药系统等领域[2]。SPIONS在生物分布、代谢速度、热稳定性以及矫顽力等理化性质方面展现出优异的稳定性,上述性质主要取决于SPIONS的粒径、磁性、结构以及表面偶联、枝接的材料[3],其高渗透性和滞留效应以及超顺磁性有助于它们在靶点上的大量富集和实现靶向给药,从而达到精准治疗目的。
研究表明[4],在纳米粒子上负载各种治疗和诊断试剂可以特异性地识别靶细胞,或调节纳米粒子的电荷并靶向识别基团,使其更容易进入靶细胞。磁性纳米球结构中的壳层大多都具有良好的生物相容性,对人体不会造成伤害,没有毒副作用,磁性纳米微球的磁核可以很方便的从人体内自然排出。磁性载体的生物相容性和生物降解性在生物医学方面更为重要,因此,磁性载体在生物医学治疗中具有非常广阔的前景。
本文主要研究柠檬酸/四氧化三铁纳米粒的合成方法,不仅可以在病变细胞周围富集,而且具有高饱和磁化强度(Ms)的超顺磁性,简化纳米粒子的纯化,提高纯化效率,并且它的靶向性在外加磁场的作用下,可以作为靶向药物载体,应用在生物医学研究的多个方面,包括治疗药物、基因靶向和放射性核素的递送、热疗和造影剂在磁共振成像(MRI)中的应用等[5]。
1 材料与方法
1.1 试剂与仪器
所需的实验试剂名称、规格及厂家见表1。具体实验设备与仪器见表2。

表1 具体实验试剂

表2 设备与仪器
1.2 实验方法
1.2.1 磁性四氧化三铁纳米粒(SPIONS)的制备
将1.5g乙酰丙酮铁Fe(Acac)3加入15mL二苄醚和15mL油胺溶液中,于三颈圆底烧瓶中混合均匀,期间匀速充入氮气,置于集热磁力搅拌器上,油封隔绝空气,维持30min。加热至100℃维持1h,然后以15℃/10min并维持5min,将温度升至295℃。当出现3次白雾现象后停止反应,冷却至室温后,用无水乙醇洗涤,重复3次直至上清无浑浊,收集产物,置于真空干燥箱中,调节温度至50℃进行干燥过夜。
1.2.2 柠檬酸四氧化三铁纳米粒(SPIONS@CA)的制备
三颈圆底烧瓶内加入10mL DCB、10mL DMF充分混合,取120mg干燥的SPIONS加入混合液中,超声分散均匀,通入氮气,持续搅拌。称取0.1g CA加入其中,升温至110℃,持续反应24h后停止加热,待其自然降至常温,加入过量乙醚沉淀产物,以磁铁分离产物,去除上清,适量丙酮洗涤产物3次,磁体分离,50℃真空干燥,获得CA修饰氧化铁纳米粒(SPIONS@CA),终产物置于干燥锅内保存待用。
1.3 测试及表征
1.3.1 X射线衍射(XRD)
取少许干燥样品,用玛瑙研钵研细,平铺于载玻片上,X射线衍射仪进行分析测定。测量参数:加速电压40kv,电流30mA,测量2θ角范围为10°~80°,Cu-Kα靶。XRD数据图谱用Origin 2019 b进行分析处理绘图。
1.3.2 傅立叶变换红外光谱(FT-IR)
SPIONS、SPIONS@CA、CA红外表征:各称取2mg干燥样品,分别与100mg KBr置于红外灯下干燥。充分混匀,倒入玛瑙研钵中继续研磨,用液压仪制成薄片,在红外光谱仪中进行检测。
1.3.3 粒径及Zeta电位测试
分别取少量样品超声分散于2mL RO水中,超声功率40%,每次5min,共15min。取超声分散后溶液50μL加入2mL RO水中,经两倍稀释后用动态光散射仪(DLS)分析粒度分布及Zeta电位。通过Scherrer公式计算出制得样品的平均粒径D:
D=Kλ/(βcosθ)
D:平均粒径;K:形态因子(一般取0.89);λ:X射线波长(0.15406nm);β:衍射峰半高度;θ:布拉格衍射角。
2 结 果
2.1 X射线衍射(XRD)
为了确定制得的产品是否为Fe3O4,对其进行XRD测定。图1为样品XRD谱图。从谱图来看,衍射峰的位置、强度结果与Fe3O4标准数据基本吻合,2θ=30.46°、35.35°、43.68°、54.31°、57.13°、63.75°处的六个衍射峰分别对应(220)、(311)、(400)、(422)、(511)和(440)的六个晶体面,这说明通过高温热解法制得的产物为Fe3O4,并具备立方晶体结构。
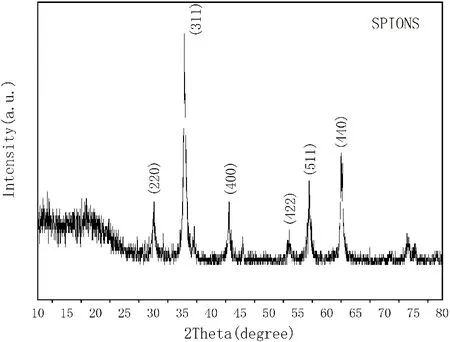
图1 Fe3O4的XRD谱图
2.2 傅立叶变换红外光谱(FT-IR)
为验证CA与Fe3O4纳米粒接枝成功,对纯CA、未经CA改进的Fe3O4、CA改进的Fe3O43种样品进行测定,相应的的红外光谱如图2所示。
从图2(a)曲线可以看出,在波数584cm-1处的吸收峰是由Fe-O键的振动引起的,此为Fe3O4的特征吸收峰;从图2(b)曲线可以看出,在波数596cm-1处的吸收峰是由Fe-O键的振动引起的,也是Fe3O4的特征吸收峰,在波数1357cm-1、1608cm-1处的吸收峰是-CO键的特征吸收峰,显示Fe3O4纳米粒子表面成功修饰上了CA,证明CA分子成功包覆在Fe3O4纳米粒子表面;从图2(c)曲线可以看出,在3495cm-1、1695cm-1、1394cm-1处的振动吸收峰分别为CA分子当中-OH的振动吸收峰以及-CO的振动吸收峰。由此,也可以表明CA分子确实修饰在了Fe3O4纳米粒上面。

图2 CA、SPIONS@CA、SPIONS的红外光谱图
2.3 粒径及Zeta电位测试
高温热解法制备的Fe3O4纳米粒表面包覆有油胺,导致其疏水性强,在极性较大的溶液中容易沉淀,不利于其在生物体中的应用。为了便于Fe3O4纳米粒长时间参与生物体内的血液循环,所以它的表面要用CA进行修饰,以促进Fe3O4纳米粒由疏水性向亲水性转变,实现Fe3O4纳米粒在水溶液中的均匀分散。SPIONS和SPIONS@CA的粒径测量结果见图3。
如图3(a)所示,合成的SPIONS粒径为(91.24±7)nm;图3(b)所示,SPIONS@CA的粒径为(119.41±7)nm,PDI(多分散指数)=0.223,分散均匀。粒径分布较窄,可见包覆CA之后,粒径增大了30nm左右。
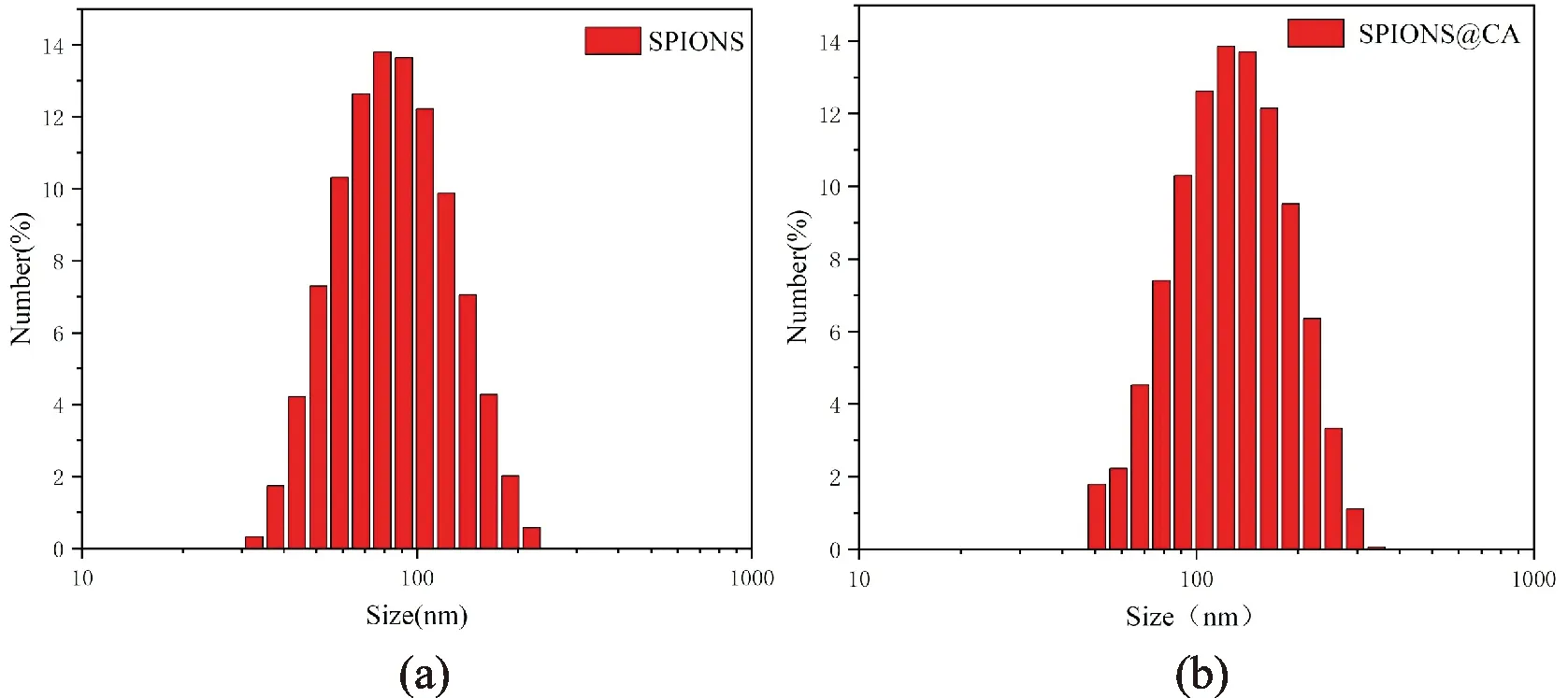
图3 SPIONS、SPIONS@CA的粒径分布图
通过图4(a)SPIONS和图4(b)SPIONS@CA的Zeta电势结果可知,合成的SPIONS和SPIONS@CA的Zeta电势分别为-37.53mV和-20.6mV,包覆CA之后,Zeta电势明显增大。粒径和电势的结果在一定程度上可以说明CA和SPIONS的成功包覆。
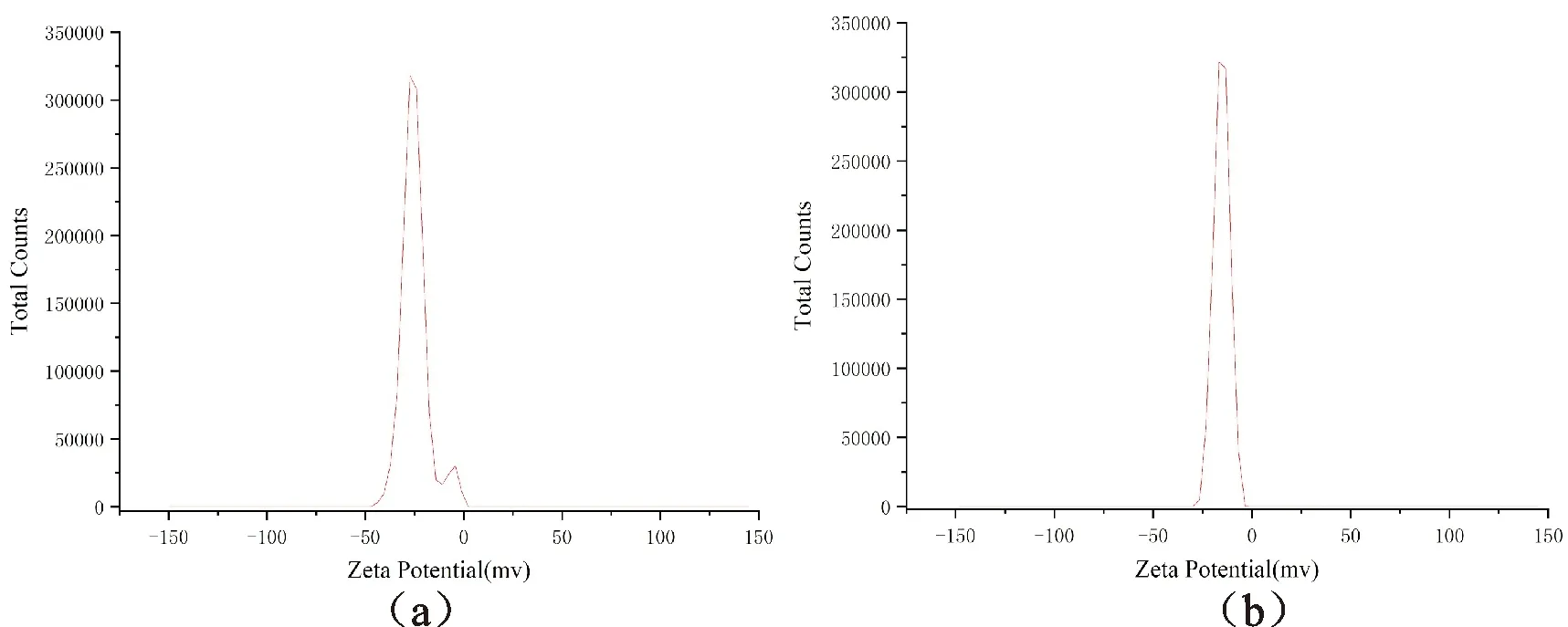
(a)SPIONS电势分布;(b)SPIONS@CA电势分布
3 讨 论
高温热解法基本原理需要有机金属前驱体(organometallic precursor)在高温下分解,同时在体系中引入合适的表面活性剂[6],来调控粒子的成核和生长。常用的金属-有机前体一般为金属乙酰丙酮络合物,如Fe(CO)5、Co2(CO)8等[7]。表面活性剂一般用长链脂肪族羧酸、长链族脂肪胺、有机磷化合物,如油酸、油胺等[8]。由于该反应需要使用化学性质比较活泼的金属-有机前体,因此,经常需要不断地向反应体系中持续通入氮气以去除空气,反应条件相对苛刻;而且由于反应过程中需要用到一些有毒试剂,如有机金属-前体等,环境友好性较差,因此,整个实验过程需要在通风厨中进行。
该方法合成的四氧化三铁纳米粒由于其特定的结构设计,在表面大多都有强疏水基团覆盖,使其在生物医学领域的应用受到了限制,不能直接用于科研或临床需要。在合成纳米颗粒的表面修饰过程中,磁性纳米颗粒的化学稳定性和单分散性,促进了功能分子的进一步连接,扩大了其应用空间,因此,对四氧化三铁纳米粒表面进行修饰改性,增加修饰基团是不可或缺的一步。另一方面,由于反应是在高温下进行的,反应体系是非极性溶剂,以及表面活性剂分子的应用[9],所有这些因素使得最终样品的晶体形状和粒度分布都比较理想,此外,产品的产量也相当可观[10]。
磁球药物载体是纳米技术和现代医药学相融合的产物,具有尺寸效应小、优良的靶向性、生物相容性、生物降解性和功能基团等优点,因此,它有望解决传统药物在循环系统中无法滞留并达到有效浓度、无法达到特定靶点、无法在机体内某一部位形成高浓度聚集而没有毒副作用等问题。目前,常用的磁性材料有Fe-Co合金、Fe2O3、Fe3O4等,对其采用适当的方式可以很方便地得到纳米级的磁性材料。由于磁性颗粒表面覆盖有功能基团,它们可以连接生物活性物质,同时,磁性颗粒表面的特定靶向分子也可以通过靶向分子与细胞表面的特定受体结合进入细胞,从而实现安全有效的靶向治疗、基因治疗、生物医学同位素标记等[11]。
本实验首先以乙酰丙酮铁Fe(Acac)3为原料,以二苄醚和油胺溶液为溶剂,以柠檬酸为稳定剂,使用高温热解法制备柠檬酸改进的Fe3O4纳米粒,并分别用X射线衍射仪、傅立叶变换红外光谱仪、激光粒度仪等仪器对其进行表征;下一步工作,将会把柠檬酸改进的Fe3O4纳米粒与FUNDC1-TTC融合蛋白进行偶联,继续运用前述方法以及考马斯亮蓝染色进行表征与验证。
本研究使用高温热解法制备出Fe3O4@CA纳米粒子,制备和纯化方法简单,成本低。通过用柠檬酸对Fe3O4进行修饰后,柠檬酸可以很好地包覆在Fe3O4纳米粒子表面。在Fe3O4纳米粒子表面增添羧基基团后,后续可进行相关蛋白的偶联工作,为制备新型的纳米药物载体提供了一种新的方法,同时对磁球靶向载药系统的研究也有进一步的推动作用。磁球靶向载药系统在外加磁场的作用下,可以通过动脉或者静脉注入的方式,把携带药物的载体一同运输到机体病变的部位或者细胞靶点,使其在病变部位富集并产生效应。但为了治疗深层组织或器官,则需要对磁球的磁场强度做进一步的改善,又因为微球表面的涂层会大大降低磁性微球的磁性,所以要使磁球的磁强得到进一步增强是比较困难的,而且粒径大小的控制也是亟待解决的问题。
