柱前衍生化法评价注射用奥美拉唑钠中EDTA-2Na·2H2O含量差异
2023-01-17刘晓强汪嘉丽张岩琛
刘晓强,汪嘉丽,张岩琛
(常州市食品药品纤维质量监督检验中心,江苏 213102)
奥美拉唑是苯咪唑的衍生物,属于第一代H+/K+-ATP酶(质子泵)抑制剂,能够有效抑制胃酸的分泌,临床上广泛用于治疗酸相关性疾病[1-3]。奥美拉唑易溶于碱而不溶于水,故临床注射剂均使用其钠盐。目前制备静脉给药制剂时,一般使用不锈钢容器和管道,某些药物如奥美拉唑钠在受热时与金属容器、管道、滤器等较长时间接触后,会导致溶液颜色变深,添加适量的EDTA-2Na等金属离子络合剂,可防止主药与金属离子发生反应,减少溶液变色[4-5]。
EDTA-2Na与钙离子结合成可溶的络合物引起钙的减少,静脉制剂中使用依地酸二钠会导致血钙下降[6-7],因此,需密切关注和严格控制静脉给药制剂中依地酸二钠的用量。同时,基于药物一致性评价要求,建立适当的方法确定仿制药与原研制剂中EDTA-2Na含量差异也十分必要。
1 仪器与试药
1.1 仪器XS105DU电子天平(瑞士Mettler Toledo);LC-20D高效液相色谱仪(含双高压泵、自动进样器、柱温箱、UV检测器、色谱工作站,日本岛津公司)。
1.2 试药EDTA-2Na·2H2O(国药集团化学试剂有限公司,批号20200701);试验用水(去离子纯净水,实验室自制);磷酸二氢铵(国药集团化学试剂有限公司,批号20190318,含量≥99.5%);硫酸铜(分析纯,GENERAL-REAGENT,批号P1587678);乙腈(色谱纯,Merck Company,批号JA091830);注射用奥美拉唑钠[规格:40 mg/支;生产企业A,批号A1、A2、A3;生产企业B,批号B1、B2、B3;生产企业C,批号C1、C2、C3;生产企业D(原研厂家),批号D1、D2、D3;生产企业E,批号E1、E2、E3]。
2 方法与结果
2.1 色谱条件 色谱柱:十八烷基硅烷键合硅胶为填充剂(Titank C18,250 mm×4.6 mm,5μm);流动相A:0.5 %磷酸二氢铵(用磷酸调pH至3.0),流动相B:乙腈,按表1进行梯度洗脱。检测波长为254 nm,柱温为30℃,流速为1.0 ml/min,进样量为20μl[8]。
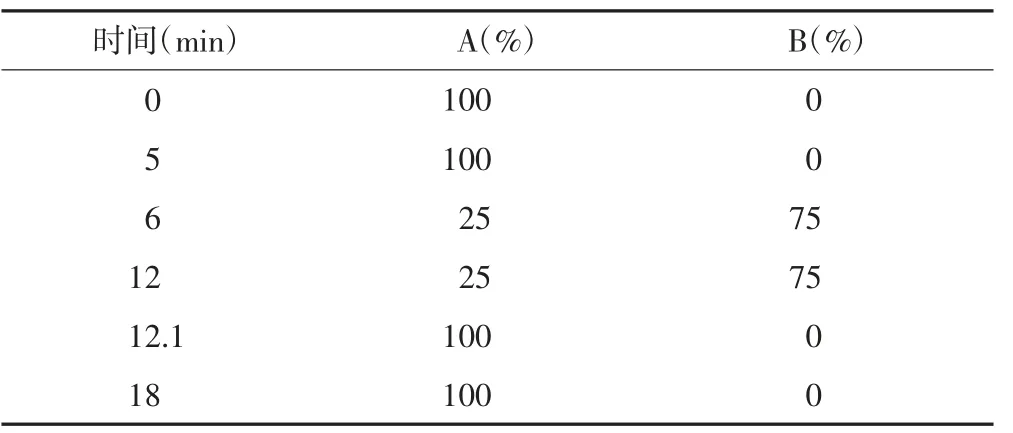
表1 梯度洗脱程序
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取EDTA-2Na·2H2O对照品约100 mg,置100 ml量瓶中,加水溶解并稀释至刻度,摇匀,即得浓度为1 mg/ml的对照品储备液。依次精密量对照品储备液2、2、3、5、5和5 ml,分别置200、100、100、100、50和25 ml量瓶中,精密加入0.04 mol/L的硫酸铜溶液适量(定容体积的2%),加水溶解并定容至刻度,摇匀即得10、20、30、50、100和200μg/ml的标准曲线溶液。
2.2.2 供试品溶液的制备 精密称取本品1支量,置50 ml量瓶中,精密加入0.04 mol/L的硫酸铜溶液1 ml,加水稀释至刻度,摇匀,过滤,取续滤液。
2.3 专属性试验 取空白溶剂水、2% 0.04 mol/L的硫酸铜溶液、浓度为30μg/ml的对照品溶液和供试品溶液,分别按“2.1”项下色谱条件进样,采集色谱图。结果,空白溶剂水、2% 0.04 mol/L的硫酸铜溶液均未在待测成分EDTA-2Na·2H2O处出峰,不干扰检测。见图1。

图1 空白溶剂(A)2% 0.04 mol/L的硫酸铜(B)对照品(C)供试品(D)HPLC色谱图
2.4 线性试验 按照线性标准溶液的制备方法分3 d分别进行溶液制备和HPLC分析,记录色谱图,绘制标准曲线,以对照品峰面积(A)对浓度(C)作权重回归计算,结果分别为:A=10 080.35C+10 477.44(r=0.999 9)、A=11 289.69C+1 0437.27(r=0.999 9)、A=12 689.26C+10 434.81(r=0.999 9)。结果表明EDTA-2Na·2H2O在10~200μg/ml的范围内线性关系良好,均符合要求。
2.5 检测限与定量限 定量限溶液:精密量取对照品储备液5 ml,置50 ml量瓶中,加水溶解并稀释至刻度,摇匀,得浓度为100μg/ml的EDTA-2Na·2H2O溶液,精密量取3 ml,置100 ml量瓶中,精密加入0.04 mol/L的硫酸铜溶液2 ml,加水溶解并稀释至刻度,摇匀,即得(3μg/ml)。检测限溶液:精密量取上述浓度为100 μg/ml的EDTA-2Na·2H2O溶液2 ml,置200 ml量瓶中,精密加入0.04 mol/L的硫酸铜溶液4 ml,加水稀释至刻度,摇匀,即得(1μg/ml)。分别按“2.1”项下色谱条件进样,测得定量限溶液EDTA-2Na·2H2O的信噪比为15.17;检测限溶液EDTA-2Na·2H2O的信噪比为4.68,满足检测要求。
2.6 重复性试验 分别取6份供试品溶液(批号为A1)各20μl,按照“2.1”项下色谱条件进样,结果RSD为0.33%,表明重复性良好。
2.7 中间精密度试验 连续3 d分别由3人制备样品溶液各6份,依次用3台不同品牌仪器取20μl进样,按照“2.1”项下色谱条件测定,并计算含量。3 d的RSD依次为0.33%、0.51%和0.54%,总RSD为0.44%,该检测方法中间精密度良好。
2.8 准确度(加样回收率)试验 取本品1支,加水溶解并转移至50 ml量瓶中,依次分别精密加入对照品储备液0.75、1.5和2.25 ml,精密加入0.04 mol/L的硫酸铜溶液1 ml,加水稀释至刻度,摇匀,即得,平行制备3份。依次取上述溶液各20μl进样,记录色谱图。计算公式:测得加入浓度=测得浓度-样品浓度,加样回收率=测得加入浓度/加入浓度×100%。结果EDTA-2Na·2H2O平均回收率为100.47%,RSD为0.78%,且平行性良好,该方法准确度良好。见表2。

表2 EDTA-2Na·2H2O加样回收率测定结果
2.9 耐用性试验
2.9.1 柱温耐用性 依次改变柱温(35和45℃),取浓度为30μg/ml的标准曲线溶液进样20μl,连续进样6次,EDTA-2Na·2H2O与相邻色谱峰之间的分离度以及进样精密度均符合要求。
2.9.2 流动相比例耐用性 依次改变初始流动相比例为A∶B(99∶1)及A∶B(98∶2),初始比例为A∶B(99∶1)时,EDTA-2Na·2H2O与相邻色谱峰之间的分离度以及进样精密度均符合要求。初始比例为A∶B(98∶2)时,分离度已不符合要求。
2.9.3 流动相pH耐用性 依次改变A相pH值(2.5和3.5),取标准线性3溶液进样20μl,pH为2.5时,连续进样6次,EDTA-2Na·2H2O与相邻色谱峰之间的分离度以及进样精密度均符合要求。pH为3.5时,EDTA-2Na·2H2O与相邻色谱峰之间的分离度不符合要求。
2.9.4 流速耐用性 依次改变流速为0.8和1.2 ml/min,当流速为0.8 ml/min时,分离度不符合要求,流速为1.2 ml/min时,EDTA-2Na·2H2O与相邻色谱峰之间的分离度以及进样精密度均符合要求。
2.9.5 仪器及色谱柱耐用性 依次改变仪器品牌型号和色谱柱品牌型号(Waters 2695+XBridge C18,250 mm×4.6 mm,5μm;Agilent 1200+XTerra C18,250 mm×4.6 mm,5μm),取标准线性3溶液进样20μl,连续进样6次,EDTA-2Na·2H2O与相邻色谱峰之间的分离度以及进样精密度均符合要求。
2.10膜过滤试验 取本品1支,加水溶解并转移至50 ml量瓶中,精密加入0.04 mol/L的硫酸铜溶液1 ml,加水稀释至刻度,摇匀即得。分别取初滤液、弃去1、2、3、4、5、6、7、8和9 ml滤液进样。结果表明,EDTA-2Na·2H2O无明显膜吸附现象。
2.11 样品测定 分别取前述5个厂家15个批次的注射用奥美拉唑钠适量,按“2.2.2”项下方法制备供试品溶液,依次取20μl进样,按外标法计算含量。结果市售各厂家(A、B、C、E)与原研厂家(D)EDTA-2Na·2H2O含量均在1.4 mg/支左右。见表3。

表3 5个厂家注射用奥美拉唑钠中EDTA-2Na·2H2O含量差异比较
3 讨论
EDTA-2Na在C18色谱柱上保留较弱,出峰时间与死时间相近,色谱峰存在明显的前沿峰,同时,在分析过程中部分Na离子会解离出来,色谱峰峰型较差,同时EDTA-2Na在紫外光谱区响应较弱,无特征吸收峰,无法直接测定EDTA-2Na。EDTA-Cu较EDTA-2Na更稳定,色谱保留更强,且有明显的紫外特征吸收(254 nm)。因此选择柱前衍生化法将EDTA-2Na转换成EDTA-Cu,以获得更好的峰型及色谱分离。本试验中,对照品溶液澄清无色,样品溶液较浑浊,需过滤后进样。查阅相关文献后发现奥美拉唑钠在pH<7时不稳定,易降解产生浑浊[9-11]。经测定,2% 0.04 mol/L的硫酸铜溶液pH值约为4左右。在方法学验证时,虽已验证过EDTA-2Na·2H2O对照品溶液48 h内稳定,但由于样品溶液浑浊,且样品溶液中硫酸铜色谱峰消失,因此并未将稳定性考查内容置于正文中。同时也建议在样品测定时,样品临用新配,确保数据的真实性和稳定性。
本试验同时选用了实验室自制纯化水和屈臣氏去离子水溶解上述15个批次的所有样品,结果采用屈臣氏去离子水和实验室自制纯化水所制得的样品从外观上看,无论是颜色还是浑浊程度均无明显差异;从测定结果看,采用屈臣氏去离子水和实验室自制纯化水所制得的样品含量无明显差异。从上述结果可以推断,实验室自制纯化水中所含的各类离子等物质均不影响EDTA-2Na·2H2O含量测定。
本次试验共测定5个厂家15个批次的样品,其中原研厂家3个批次,仿制厂家12个批次。上述15个批次EDTA-2Na·2H2O含量均为1.4 mg/支左右。其中,A、D和E三个厂家批次间差异更小,生产工艺更稳定。
本方法在建立及验证的过程中均采用的杂化硅胶柱,未尝试其他类型C18柱,故建议在测定时也采用同类型色谱柱,同时建议采用25 cm柱长的色谱柱,避免EDTA-2Na·2H2O与相邻杂质分离度不符合要求。同时该方法流速、流动相比例、流动相pH值均不宜调整,若奥美拉唑钠在所采用的C18柱上出峰较晚,可以适当增加流速,或增加高有机相比例持续时间。
