半胱氨酸和甘氨酸丰富蛋白1对膀胱癌细胞增殖、细胞周期及β-catenin/c-Myc通路的影响
2023-01-14张镜伟马胜利谢程国
张镜伟,马胜利,谢程国
广州市第一人民医院南沙医院泌尿外科,广州 511458
膀胱癌的发病率、病死率均较高,是最常见的泌尿系统恶性肿瘤之一[1-2]。研究显示,早期诊断、个体化治疗和随访可以明显延长患者的生存期[3]。尽管临床上在诊断和治疗方法中做了很大的努力,但膀胱癌患者的复发率依旧很高,晚期患者的临床预后也很差[4]。因此,寻找膀胱癌患者早期诊断和临床治疗的特异性分子标志物具有重要意义。半胱氨酸和甘氨酸丰富蛋白1(cysteine and glycine rich protein 1,CSRP1)属于LIM结构域超家族,LIM结构域可以在许多不同的蛋白质中找到,其在细胞结构、细胞黏附、细胞运动以及信号转导中发挥重要作用[5-6]。CSRP1主要表达于细胞质,具有促进细胞增殖的功能;同时,该蛋白还是非常重要的肿瘤分子标志物[7-9]。现已证实,CSRP1在多种肿瘤中均出现了表达失衡,例如结直肠癌、前列腺癌等[10-14]。随着研究的深入,CSRP1有可能成为新型分子标志物,对肿瘤的发生、发展有较大的提示意义。但是,目前CSRP1在膀胱癌中的研究尚未见文献报道,故本研究探讨CSRP1对膀胱癌细胞增殖、细胞周期及β-catenin/c-Myc通路的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2014年1月至2017年1月在广州市第一人民医院南沙医院就诊的膀胱癌患者。纳入标准:①经病理学检查确诊为膀胱癌;②术前未行放化疗等抗肿瘤治疗;③临床资料完整。排除标准:合并其他恶性肿瘤。根据纳入、排除标准,共纳入30例膀胱癌患者,收集30例患者的膀胱癌组织以及相应的癌旁组织。本研究经医院伦理委员会批准通过,所有患者均知情同意并签署知情同意书。
1.2 主要材料与试剂
RPMI1640培养基、DMEM培养基及胎牛血清均购自美国Gibco公司,荧光定量聚合酶链反应(polymerase chain reaction,PCR)反转录和扩增试剂盒均购自Takara公司,MTS细胞增殖定量检测试剂盒购自美国Promega公司,电化学发光(electrochemiluminescence,ECL)荧光底物试剂盒购自美国Pierce公司,Lipofectamine LTX购自Invitrogen公司。c-Myc、CSRP1、β-catenin、GAPDH抗体均购自美国Abcam公司。倒置荧光显微镜购自OLYMPUS公司,电热恒温水槽购自上海精宏实验设备有限公司,生物安全柜(超净工作台)、细胞培养箱均购自Thermo Scientific公司,全自动细胞计数分析仪购自Nexcelom Bioscience公司,立式全自动灭菌器购自Cirrus公司,普通PCR仪购自BioRAD公司,荧光定量PCR仪购自杭州博日科技有限公司。
1.3 研究方法
1.3.1 细胞培养 人正常尿路上皮细胞系SVHUC和膀胱癌细胞系5637、T24均购自中科院上海细胞所。人正常尿路上皮细胞系SVHUC在无角质细胞血清培养基(keratinocyte serum free medium,K-SFM)+1%青霉素和链霉素中培养;5637细胞和T24细胞在RPMI1640完全培养基(10%胎牛血清+1%双抗)中培养。所有细胞在37℃标准细胞培养条件下(5%CO2,95%湿度)生长。
1.3.2 免疫组化 对临床膀胱癌样本石蜡包埋的组织切片进行免疫组化分析,按照免疫组化步骤检测膀胱癌组织及癌旁组织中CSRP1的表达情况,结果用免疫活性评分(immunoreactivity score,IRS)表示,即阳性细胞百分比评分乘以染色强度评分。阳性细胞百分比评分方法:阳性细胞百分比0~5%为0分,6%~25%为1分,26%~50%为2分,51%~75%为3分,>75%为4分;染色强度评分方法:未染色为0分,淡黄色为1分,深黄色或者棕黄色为2分,棕褐色为3分。根据IRS评分可将CSRP1表达分成4个等级:阴性(0~3分),弱阳性(4~6分),阳性(7~9分),强阳性(10~12分)。
1.3.3 实时荧光定量PCR 取对数生长期细胞,采用Trizol/氯仿/异丙醇法提取细胞总RNA,通过核酸蛋白定量仪测定所提取RNA的浓度及纯度;然后参照Takara公司的PrimeScriptRTReagent Kit试剂盒说明书,将总RNA(1 μg)逆转录成cDNA;参照Takara公司的PrimeScript™RT Master Mix试剂盒说明书,以cDNA为模版进行PCR扩增。42℃预变性,60 min;70 ℃,15 min。PCR 反 应条件:94 ℃,45 s;55 ℃,50 s;72 ℃,75 s;共40个循环。所需引物序列详见表1。采用公式2-ΔΔCt对数据进行处理分析,得到各个基因的相对表达量。

表1 引物序列
1.3.4 蛋白质印迹(Western blot)法 收集对数生长期的SVHUC、5637及T24细胞,用预冷磷酸盐缓冲液(phosphate buffered solution,PBS)洗涤细胞3次,然后加入1×Cell Lysis Buffer裂解细胞,经超声、离心后去掉其他细胞成分,使用微量核酸蛋白定量仪测定各蛋白样品的浓度及纯度;加入5×十二烷基硫酸钠(sodium dodecylsulfate,SDS)加样缓冲液在沸水中煮沸10 min以使蛋白充分变性;配置10%的SDS聚丙烯酰胺凝胶进行电泳分离,然后转膜,封闭,并在4℃与一抗孵育过夜;二抗室温孵育2 h,采用化学发光法检测CSRP1蛋白表达情况,并进行灰度值分析。
1.3.5 细胞转染CSRP1-siRNA序列为5'-CTGTTGTGGGAATGAAGAGAGTTTG-3',阴性对照序列为 5'-GCUUCGCGCCGUAGUCUATT-3',由上海吉玛公司合成。取对数生长期的T24细胞,接种于6孔板中。利用转染试剂LipofectamineTM2000,将scramble-siRNA(10 μg)和CSRP1-siRNA(10 μg)分别转染至T24细胞中。转染6~8 h后将无抗生素的RPMI1640培养基换成加入抗生素的RPMI1640培养基,继续培养48 h(用于检测mRNA的表达)或72 h(用于检测相关蛋白的表达)。
1.3.6 MTS细胞增殖实验 通过细胞转染,将T24细胞分成3组:空白对照组、scramble-siRNA组(si-NC组)和实验组(si-CSRP1组)。然后将100 μl完全培养基中的2000个3组细胞接种到96孔板中,在37℃、5%CO2条件下培养1~5天,然后每个时间点在培养基中加入10 μl MTS,37℃孵育4 h后,490 nm波长下测定每孔光密度(optical density,OD),根据结果绘制细胞生长表。
1.3.7 流式细胞术检测细胞周期 利用流式细胞仪检测细胞周期,取对数生长期的si-NC组和si-CSRP1组T24细胞,用D-Hanks清洗3遍后加入不含胎牛血清的培养基静置过夜,然后用预冷PBS清洗3次,使用预冷75%乙醇固定细胞,放置于4℃冰箱内过夜;上机前离心去除乙醇,PBS洗涤3次后,加入100 μl RNase A溶液37℃水浴中放置30 min;然后加 400 μl的碘化丙啶(propidium iodide,PI)4℃避光染色1 h;流式细胞仪根据测定的DNA含量确定细胞周期分布。
1.4 统计学分析
采用SPSS 18.0软件对数据进行统计分析,计量资料以均数±标准差(±s)表示,多组间比较采用方差分析,两组间比较采用两独立样本t检验,组内比较采用配对t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 CSRP1在膀胱癌组织中的表达水平及临床意义
采用免疫组化检测膀胱组织标本中CSRP1的表达水平,CSRP1在肿瘤组织中的表达水平为(8.20±2.58),明显高于癌旁组织中的(3.93±1.98),差异有统计学意义(t=16.837,P<0.01)(图1)。按照IRS评分将膀胱癌患者分成CSRP1高表达组(IRS评分≥8分)和CSRP1低表达组(IRS评分<8分),生存曲线分析显示CSRP1高表达组患者的总生存率低于CSRP1低表达组患者(χ2=5.532,P=0.019)(图2)。不同肿瘤大小、肿瘤分级膀胱癌患者的CSRP1表达情况比较,差异均有统计学意义(P<0.05);不同年龄、性别膀胱癌患者的CSRP1表达情况比较,差异均无统计学意义(P>0.05)(表 1)。

表1 不同临床特征膀胱癌患者CSRP1表达情况的比较

图1 免疫组化检测膀胱癌组织及癌旁组织中CSRP1蛋白表达情况(免疫组化染色,×400)
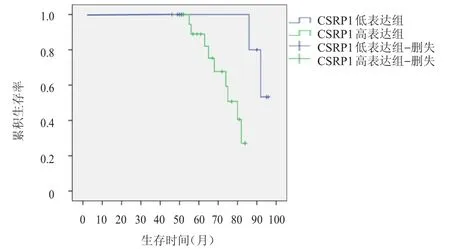
图2 CSRP1高表达组(n=19)与CSRP1低表达组(n=11)膀胱癌患者的生存曲线
2.2 CSRP1在膀胱癌细胞中的表达水平
在细胞水平,分别采用实时荧光定量PCR和Western blot法检测细胞中CSRP1mRNA和蛋白水平。结果显示,CSRP1在人正常尿路上皮细胞SVHUC和膀胱癌细胞T24、5637中的mRNA表达水平分别为(1.025±0.014)、(6.537±0.009)、(8.487±0.043),差异有统计学意义(F=20 762.951,P<0.01),提示膀胱癌细胞中CSRP1mRNA水平高于人正常尿路上皮细胞;膀胱癌细胞T24、5637中CSRP1蛋白表达水平均高于人正常尿路上皮细胞SVHUC(图3)。
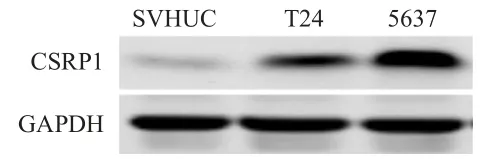
图3 Western blot法检测膀胱癌细胞T24、5637和人正常尿路上皮细胞SVHUC中CSRP1蛋白表达情况
2.3 沉默CSRP1表达对膀胱癌细胞增殖和细胞周期的影响
转染CSRP1siRNA序列至T24细胞中沉默CSRP1表达,CSRP1蛋白表达降低(图4A)。相比si-NC组细胞,si-CSRP1组细胞G1期细胞百分比从57.60%提高到71.59%,而S期细胞百分比则由30.15%降低到19.22%(图4B)。与空白对照组和si-NC组相比,不同时间点si-CSRP1组细胞OD值均降低,差异均有统计学意义(P<0.05)(表2)。
表2 不同时间点3组CSRP1细胞OD值的比较(±s)

表2 不同时间点3组CSRP1细胞OD值的比较(±s)
注:*与si-CSRP1组比较,P<0.05
空白对照组si-NC组si-CSRP1组F值P值0.362±0.002*0.334±0.001*0.308±0.012 55.207 0.000 0.513±0.003*0.525±0.003*0.363±0.003 2687.939 0.000 0.652±0.025*0.668±0.010*0.460±0.017 119.39 0.000 0.912±0.016*0.971±0.018*0.626±0.021 296.729 0.000组别24 h 48 h 72 h 96 h

图4 沉默CSRP1表达对CSRP1蛋白表达和细胞周期的影响
2.4 沉默CSRP1表达对β-catenin/c-Myc信号通路的影响
si-CSRP1组细胞中β-catenin、c-MycmRNA和蛋白表达水平均明显低于si-NC组细胞,差异均有统计学意义(P<0.01)。(表3、图5)
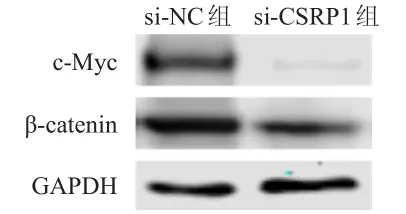
图5 Western blot法检测si-NC组和si-CSRP1组细胞中β-catenin、c-Myc蛋白表达情况
表3 si-NC组和si-CSRP1组细胞中β-catenin、c-Myc mRNA表达水平的比较(±s)

表3 si-NC组和si-CSRP1组细胞中β-catenin、c-Myc mRNA表达水平的比较(±s)
组别si-NC组si-CSRP1组t值P值c-Myc 1.040±0.053 0.461±0.036 15.733 0.000 β-catenin 1.012±0.010 0.330±0.030 37.182 0.000
3 讨论
本研究探讨了CSRP1在膀胱癌组织中的表达情况及临床意义,发现CSRP1在膀胱癌组织中的表达高于癌旁组织,且CSRP1高表达与膀胱癌患者预后不良有关。与正常尿路上皮细胞相比,膀胱癌细胞中CSRP1表达上调。为了确定CSRP1在膀胱癌中的作用,本研究转染靶向CSRP1基因的siRNA沉默其表达,发现沉默CSRP1后抑制了膀胱癌细胞的增殖能力,诱导细胞出现G1/S期阻滞。这些结果提示CSRP1与膀胱癌的发生发展有关,可能是防治膀胱癌的新靶点。
机制研究显示,沉默CSRP1可以明显抑制β-catenin/c-Myc信号通路。据报道,WNT/β-catenin信号通路在膀胱癌细胞的自我更新和增殖中发挥重要作用[15]。β-catenin蛋白N-末端的缺失可以避免其被糖原合酶激酶-3β(glycogen synthase kinase-3β)结合和降解,将N-末端缺失的β-catenin蛋白导入膀胱癌细胞中可以促进其增殖和克隆形成[16]。本研究中应用siRNA沉默T24中CSRP1基因后,β-catenin蛋白表达水平下降,说明CSRP1可能通过β-catenin促进膀胱癌细胞增殖。同时检测了β-catenin下游蛋白c-Myc的表达水平,与β-catenin结果一致,沉默CSRP1基因后,c-Myc蛋白表达水平也出现了下降。原癌基因c-Myc在许多肿瘤中过表达,包括膀胱癌。c-Myc在膀胱癌细胞增殖和分化中发挥重要作用,被报道参与调控膀胱癌细胞的增殖[17]。c-Myc还可以调节其下游细胞周期相关蛋白cyclin D1(调节G1/S检测点最关键的蛋白)和cyclin E2(G1末期细胞从G1期向S期转换过程中的限速调节因子)的表达,从而促进与S期相关的靶分子的表达、DNA复制的完成,促进细胞从G1期至S期进展[18-20]。本研究发现,CSRP1沉默可以下调c-Myc表达水平,诱导膀胱癌细胞周期G1/S期阻滞,抑制膀胱癌细胞的生长,说明CSRP1可能通过β-catenin/c-Myc通路介导细胞周期蛋白上调来促进膀胱癌细胞的增殖。
综上所述,CSRP1在膀胱癌组织及细胞中呈高表达,沉默CSRP1可能通过抑制β-catenin/c-Myc通路下调c-Myc的表达,从而诱导细胞周期G1/S期阻滞并抑制膀胱癌细胞增殖。因此,CSRP1可能在膀胱癌发生、发展过程中发挥重要作用。但是,本研究中后期仅采用了一个膀胱癌细胞系,也缺乏体内动物实验,CSRP1影响细胞周期蛋白的潜在机制也有待进一步深入研究。
