开滦集团社区心房颤动人群全因死亡及其相关因素的观察*
2023-01-09邢爱君王艳秀刘学伟董申许继波刘英孙玉艳吴云涛赵海燕吴寿岭
邢爱君 王艳秀 刘学伟 董申 许继波 刘英 孙玉艳 吴云涛 赵海燕 吴寿岭
心房颤动(简称房颤)是临床常见的心律失常,全世界房颤患者约有数千万[1]。由于人口老龄化及冠心病、高血压等房颤传统危险因素的增加,房颤的患病率也在增加。欧洲一项研究显示,1998~2008年间20岁以上人群房颤的患病率由1.6%升至1.9%[2]。我国资料也显示60岁以上人群房颤的年发病率为4.9‰,患病率达到1.8%[3],预计至2050年房颤患病人数将增加2倍[4-5]。
房颤本身并不是一种良性的心律失常[6]。与非房颤人群相比,房颤患者卒中增加5倍[7]、心力衰竭(简称心衰)增加3 倍[8]、痴呆和死亡增加2 倍[7]。英国一项全因死亡调查显示,由房颤直接或间接致死人数占全因死亡人数的21.4%[9]。国内研究也发现急诊房颤患者1年全因死亡率为13.8%[10]。目前治疗房颤的主要目的之一是预防卒中及相关死亡,忽视了其他导致房颤患者死亡的原因。而且研究对象多为住院患者,不能反映社区房颤患者全因死亡情况。本研究(项目编号:20210929)以开滦研究(注册号:CHiCTR-TNC-11001489)人群中非瓣膜性房颤或心房扑动(简称房扑)患者作为研究对象,旨在探讨社区房颤患者全因、心血管死亡情况及其危险因素。
1 资料与方法
1.1 研究对象
2006~2007年度由开滦总医院等11家医院对开滦(集团)有限责任公司101 510例在职和离退职工进行健康体检。入选标准:①参加了2006~2007年度健康体检的开滦在职和离退职工;②完成常规12导联心电图检查,且心电图提示:P波消失,代之以大小不等、形状各异、不规则的细小的f波(f波频率300~600次/分);R-R 间距绝对不等[11];③二级甲等以上医院诊断为阵发性房颤者:初次或≥2次房颤发作,每次持续时间<7 d且此次心电图为窦性心律者。排除标准:①风湿性心脏病;②先天性心脏病;③甲状腺机能亢进性心脏病;④接受瓣膜置换术者。本研究经开滦总医院道德伦理委员会批准、入选患者签署知情同意书。
1.2 基线资料收集及方法
见本课题组已发表文献[12]。
1.3 相关定义
根据1998年世界卫生组织推荐标准诊断糖尿病[13]:①空腹血糖≥7.0 mmol/L;②既往诊断糖尿病,现在服用或未服用降糖药物治疗者。根据2010年《中国高血压防治指南》推荐标准诊断高血压[14]:①收缩压≥140 mm Hg 和(或)舒张压≥90 mm Hg;②既往诊断高血压病,现在服用或未服用抗高血压药物治疗者。卒中:包括缺血性和出血性卒中,均由二级甲等以上医院经头颅CT 和/或核磁诊断。心肌梗死:由二级甲等以上医院诊断者。心衰:由二级甲等以上医院诊断,且NYHA 分级为Ⅱ~Ⅳ级者。根据2006年《中国成人超重和肥胖症预防与控制指南》[15]诊断超重:24 kg/m2≤体质指数(BMI)<28 kg/m2,肥胖:BMI≥28 kg/m2。
CHADS2评分[11]:①心衰1分;②高血压病1分;③年龄>75岁1分;④糖尿病1分;⑤已知缺血性卒中(脑梗死或短暂性脑缺血发作)2分,总分为6分。0分为低危组,1分为中危组,≥2分为高危组。
估算肾小球率过滤(eGFR)计算方法[16]:根据2006年中国肾脏病膳食改良试验(MDRD)公式计算:eGFR=175×[血肌 酐]-1.234×[年龄]-0.179×[女性×0.79]。
1.4 随访及死亡确定方法
1.4.1随访方法 设计房颤流行病学调查表,内容包括初诊房颤时间、药物治疗、是否住院、生活自理、是否死亡等。课题组专人每半年对入选者或家属进行一次电话随访,每2年对入选者进行一次面对面随访。住院期间死亡者由经过培训的医务人员调取住院病历,根据ICD~10疾病编码确定死因。非住院死亡者与所在工作单位工会和(或)户口所在地的派出所核实。至2013年12月31日完成末次随访。
1.4.2全因、心脑血管、非心脑血管死亡确定 ①全因死亡:排除交通事故、自杀、他杀等非正常死亡的所有死亡;②心脑血管死亡:由经过培训的医务人员到所在医院调取住院资料,根据国际疾病分类编码ICD~10确定心、脑血管疾病死亡,包括I11、I20~I25、I40、I42、I46、I50~I52、I60~I69;③非心脑血管死亡:除心脑血管死亡之外的全因死亡。
1.5 统计学处理
体检资料由各医院终端录入,通过网络上传至开滦医院计算机室服务器,形成oracle数据库。随访资料经EpiData录入,采用双份录入,并由开滦总医院心血管实验室研究人员核实。应用SPSS13.0进行统计学分析。正态计量资料用均数±标准差(±s)表示,组间比较用方差分析,两两比较用LSD 法。高敏C 反应蛋白(hs-CRP)呈偏态分布,经对数转换后行统计学分析。计数资料用n(%)表示,组间比较用χ2检验。房颤患者全因、心血管死亡率参照2006年人口统计学资料[17],采用直接方法校正年龄和性别进行标化。用Kaplan-Meier法计算房颤患者全因、心血管死亡率,组间比较用Log-rank检验。采用Cox比例风险模型分析房颤患者全因、心脑血管死亡的危险因素。以P<0.05为差异有统计学意义(双侧检验)。
2 结果
2.1 一般情况
2006~2007年度共有101 510例在职和离退职工进行了健康体检,符合房颤诊断标准者438例(包括房扑10例)。排除风湿性心脏病37例、先天性心脏病3例、甲状腺机能亢进性心脏病4例、瓣膜置换术4例,最终以390例房颤患者组成观察队列。随访期间1例服毒自杀,最终纳入统计学分析的房颤患者389例。房颤患者的平均年龄为66.9岁,男性360例(92.5%),持续或永久性房颤369 例(94.9%),阵发性房颤20例(5.1%)。30例(7.7%)患者服用了抗心律失常药物,81例(20.8%)患者服用抗血小板治疗(79例服用阿司匹林、2 例服用氯吡格雷),1例(0.3%)患者服用华法林。53 例(13.6%)患者有脑卒中病史,66例(17.0%)患者有心肌梗死史,44例(11.3%)患者有心衰史。按CHADS2评分分层,低危组83(21.3%)例,中危组162(41.7%)例,高危组144(37.0%)例。除年龄、高血压、糖尿病、心衰、脑卒中等因素外,高危组eGFR、血尿酸、hs-CRP水平、服用血小板治疗人数均高于低危组(P<0.05),其他生化指标组间比较差异无统计学意义,见表1。
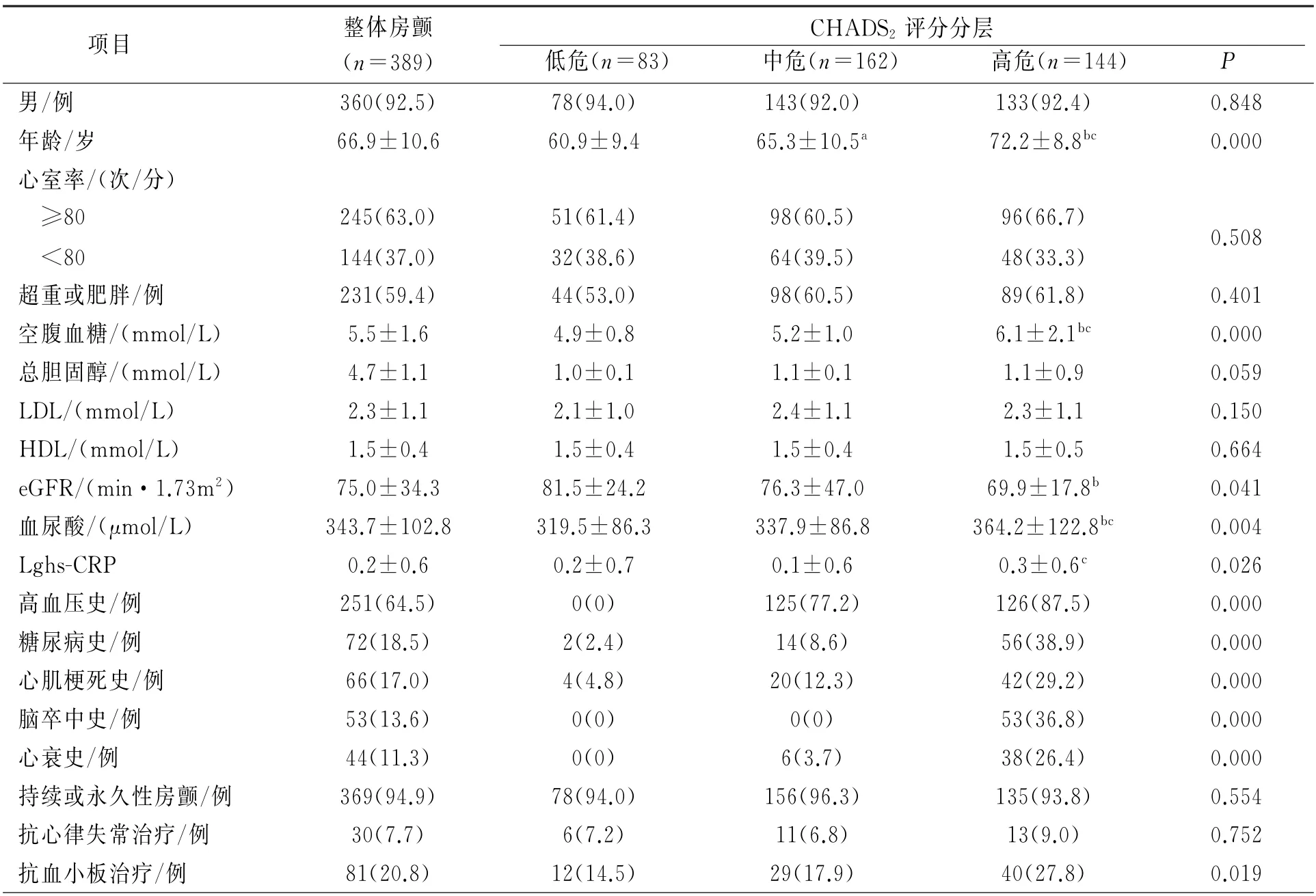
表1 整体、CHADS2 评分分层房颤患者的一般情况
2.2 死亡情况
平均随访[71.5±22.9(0~89)]个月,389例房颤患者中共有136例(35.0%)死亡,其中心脑血管死亡80例(20.6%),脑卒中死亡23例(5.9%)。按2006年中国人口统计资料中年龄、性别分布,采用直接法对全因、心脑血管死亡进行标化,标化年全因死亡率为37.5‰,标化心脑血管年死亡率为18.7‰,标化脑血管年死亡率为2.12‰。按照CHADS2评分分层分析,结果显示随着危险分层增加房颤患者全因、心脑血管死亡率以及心血管、脑血管死亡率逐渐升高,经Log-rank检验差异达到统计学意义(P<0.01、P<0.05),而非心血管死亡未见此趋势,见表2。

表2 房颤患者全因、心脑血管、非心脑血管死亡情况/例
2.3 全因、心脑血管、非心脑血管死亡的Cox风险比例模型分析
以是否全因、心脑血管死亡、非心脑血管死亡为因变量,以性别、年龄、高血压、糖尿病、卒中、心衰、心肌梗死、抗心律失常治疗、抗血小板治疗、超重或肥胖、心室率、总胆固醇、血尿酸、eGFR、hs-CRP 为自变量(其中年龄、血尿酸、总胆固醇、hs-CRP 为连续变量)建立Cox比例风险模型。结果显示年龄、心室率<80次/分、血尿酸为房颤患者全因死亡的独立危险因素(P<0.01)。年龄、心衰史、血尿酸为房颤患者心脑血管死亡的独立危险因素(P<0.05或P<0.01)。年龄为房颤患者非心脑血管死亡的独立危险因素(P<0.01),见表3。
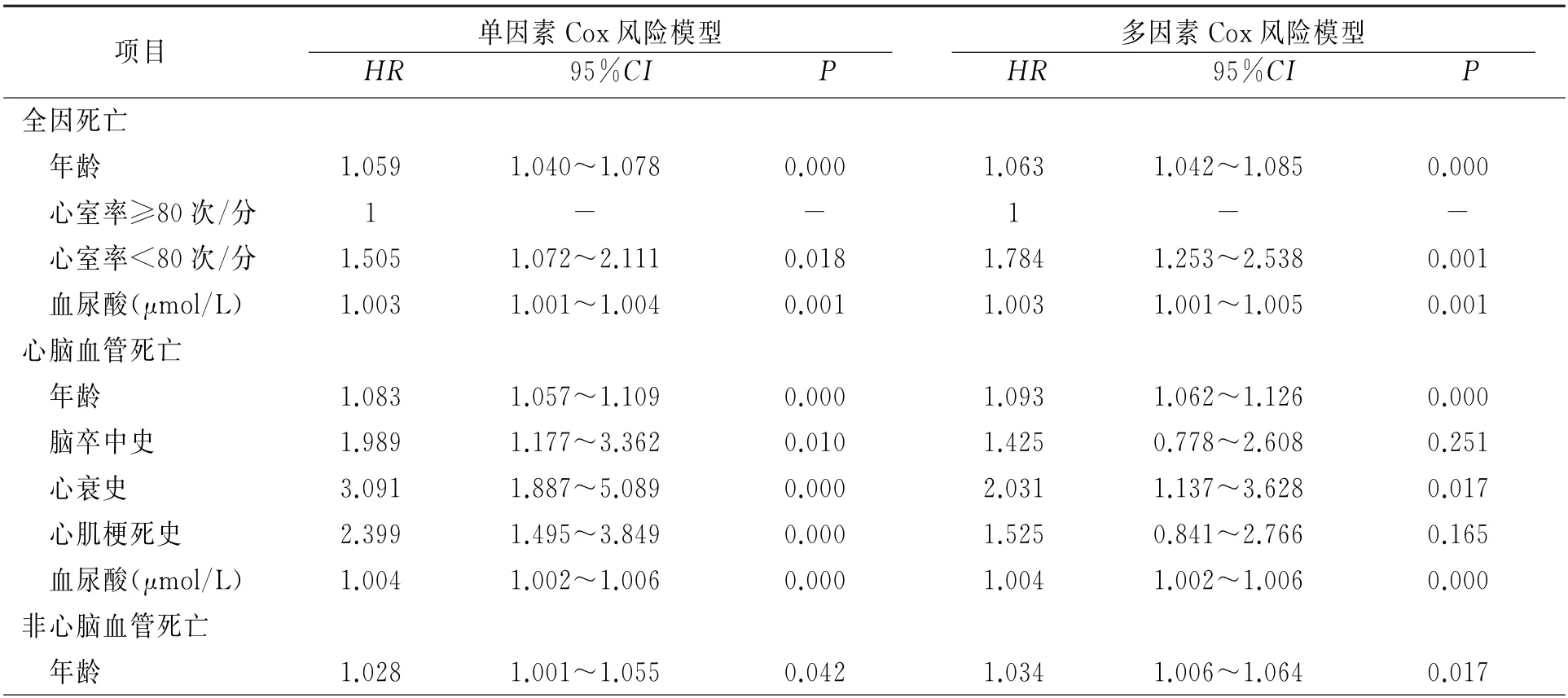
表3 影响房颤患者全因、心脑血管、非心脑血管死亡风险模型
2.4 CHADS2 评分分层对房颤患者全因、心脑血管死亡的影响
以是否全因、心脑血管死亡为因变量,以CHADS2评分分层为自变量建立模型1,校正性别、心肌梗死史、抗血小板治疗史、心室率、超重或肥胖建立模型2,在模型2 基础上校正总胆固醇、eGFR、血尿酸、hs-CRP 建立模型3。结果显示3 种模型中CHADS2评分高危房颤患者全因死亡风险明显增加,以低危组为参照,风险比分别为2.411、2.366、2.495(P=0.001)。3 种模型中CHADS2评分中危、高危房颤患者心脑血管死亡风险增加,以低危组为参照,中危房颤患者心脑血管死亡风险比分别为3.192、3.233、2.976(P<0.05),高危房颤患者心脑血管死亡风险比分别8.502、8.096、7.661(P=0.000),见表4。

表4 CHADS2 评分分层对房颤患者全因、心脑血管死亡的影响
3 讨论
由于受地域、种族和人群特征影响,房颤患者全因、心脑血管死亡率存在较大差异[6,18-19]。美国数据显示房颤患者年全因死亡率约为7‰[20],欧洲数据显示年龄65~74岁房颤患者年全因死亡率63‰~80‰[6]。亚洲数据显示房颤患者年全因死亡率为3‰~11‰[18-19]。本研究对开滦研究队列中389例非瓣膜性房颤患者随访观察了71.5个月,结果显示房颤患者的标化全因年死亡率为37.5‰,标化心脑血管年死亡率为18.7‰。该结果与2011年日本一项研究报道的房颤患者标化全因年死亡率(3.17‰)、标化心脑血管年死亡率(2.38‰)及心脑血管死亡所占比例存在较大差异[19]。分析主要原因如下:①男性房颤患者全因死亡率明显高于女性[6],本研究男性房颤患者所占比例高(92.5%);②持续或永久性房颤是增加房颤患者全因死亡的危险因素[10],本研究入选患者中持续或永久性房颤房颤比例较高(94.9%);③本研究房颤患者服用抗血小板、抗栓治疗率极低(抗血小板治疗率20.8%、抗栓治疗率0.3%)。
本研究显示年龄是房颤患者发生全因、心血管死亡的独立危险因素,风险比分别为1.065(95%CI:1.044~1.087)、1.092(95%CI:1.061~1.123),而高血压、糖尿病、心肌梗死、卒中等疾病并未对房颤患者全因死亡造成影响,该结论与文献报道一致[10]。心衰是房颤患者常伴发疾病[21],是影响房颤患者全因死亡的独立危险因素[6,10]。本研究结果显示11.4%的房颤患者伴发心衰,是房颤患者心脑血管死亡的独立危险因素(HR=1.962,95%CI:1.019~3.525),而并未增加全因死亡风险(HR=1.245,95%CI:0.746~2.078)。分析原因在于本研究对象为社区房颤患者,仅对曾住院房颤患者进行了心功能评价,故可能低估了心衰的发生率。
房颤患者心室率的靶目标值尚未确定。Van Gelder等[22]对614例永久性房颤患者随访2.9年,观察了静息心室率<80次/分和<110次/分的两组房颤患者发生终点事件(心血管事件和死亡)情况,结果发现静息心室率<80次/分患者的累积终点事件率为14.2%,静息心室率<110次/分患者的累积终点事件率为12.1%,尽管两组比较差异无统计学意义,但至少说明将房颤患者心室率控制<80次/分并无明显获益。本研究结果也显示房颤患者心室率<80次/分增加了全因死亡危险(95%CI:1.253~2.538)。将房颤患者按CHADS2评分进行危险分层后建立多因素风险比例模型,心室率<80次/分增加房颤患者全因(95%CI:1.159~2.331)、心脑血管(95%CI:1.066~2.689)死亡危险。该结论为首次发现,待其他研究予以进一步证实。
尿酸是人体内嘌呤代谢的终产物,从肾脏排出体外。近半个世纪以来,人们已不再将其视为仅与痛风相关的一种代谢指标,而是将其与高血压[23]、动脉硬化[24]、冠心病[25]、全因死亡[26]的危险因素给予关注。本研究也发现尿酸是房颤患者全因、心血管死亡的独立危险因素,血尿酸每升高1μmol/L,房颤患者全因、心血管死亡风险增加1.003、1.004倍(全因死亡95%CI:1.001~1.004,心血管死亡95%CI:1.001~1.006),该结论为房颤的防治提供了新思路。但房颤患者常伴发心衰,可能导致肾脏排泄尿酸能力降低,因此该结论不能除外反向因果关系。
CHADS2评分是评估非瓣膜性房颤患者缺血性脑卒中风险的一种常用方法[27],目前也有研究将CHADS2评分用于房颤患者全因死亡预测[10],本研究结果证实CHADS2评分不仅能预测房颤患者全因死亡,而且能够预测心血管死亡。因此认为CHADS2评分可作为评估社区房颤患者发生全因、心血管死亡的预测手段。
本研究存在一定的局限性。第一,本研究的研究对象以男性为主,也并未涵盖农村人口,限制结论的外延;第二,本研究缺乏房颤患者心脏超声资料,因此未能考虑心脏结构对房颤患者全因、心血管死亡的影响;第三,本研究未将房颤患者其他临床治疗资料,如洋地黄、利尿剂、血管紧张素转换酶抑制药或血管紧张素Ⅱ受体拮抗药以及降糖药物、调脂药物等纳入统计学分析。
