基于网络药理学和分子对接分析探讨五苓散治疗肾结石的潜在作用机制
2023-01-03汪翔夏启东寻阳
汪翔,夏启东,寻阳
(华中科技大学同济医学院附属同济医院泌尿外科,湖北 武汉 430030)
肾结石是由于晶体物质(如钙、草酸、尿酸、胱氨酸)在肾脏的异常聚积所致,是泌尿外科最常见的疾病,具高发病率和高复发率的特点。我国肾结石患病率约5.8%,5年复发率高达50%,并呈逐年升高的趋势[1]。疼痛和血尿是肾结石患者最常见的临床症状,疼痛通常表现为腰部酸胀不适或在身体活动增加时有隐痛、钝痛,也可表现为骤然发生的腰腹部刀割样剧烈疼痛,呈阵发性;血尿多发生在疼痛后,有时是唯一的症状。肾结石除诱发肾绞痛外,常引起泌尿系感染和肾功能损害,反复治疗也会给个人和社会带来沉重的经济负担[2]。近年来,肾结石手术发展迅速,但一直缺乏有效的治疗药物和预防手段[3]。有研究结果显示,在常规治疗基础上联合应用五苓散可增强肾结石的排石效果,同时有效预防肾结石复发[4]。但关于五苓散治疗肾结石的具体机制目前尚不清楚。
网络药理学是计算机科学与医学相结合,构建和可视化多基因、多靶点、多途径相互作用网络来评价药物分子机制的一种新方法[5],已被广泛应用于中药研究[6]。运用网络药理学相关技术手段,便于理解中药治疗疾病的作用机制。本研究旨在通过网络药理学和分子对接的方法,探讨五苓散治疗肾结石的潜在分子机制。
1 材料与方法
1.1 获取五苓散活性成分靶点
在中药系统药理学数据库(Traditional Chinese medicines systems pharmacology,TCMSP)(https:∥tcmspw.com/)中搜索五苓散的主要成分,获得其活性化合物及其靶基因。具体根据五苓散的各成分分别选择药名。检索结果显示了五苓散的相关组成化合物及其相应的药动学指标。通过设定口服生物利用度(OB)>30%、类药指数(DL)>0.18的药代动力学指数筛选活性化合物。对于每个活性化合物,通过在TCMSP中寻找相关的靶基因。在Uniprot(https:∥www.uniprot.org/)的帮助下注释基因符号并获得五苓散靶基因集。
1.2 获取肾结石相关基因集
通过Genecards数据库(https:∥www.genecards.org/),OMIM数据库(https:∥omim.org/)、DrugBank数据库(https:∥www.drugbank.ca/)和DisGeNet数据库(https:∥www.disgenet.org/home/)检索肾结石相关基因。将五苓散靶基因集与肾结石相关基因集进行交叉,得到五苓散-肾结石共同靶点。
1.3 构建五苓散活性化合物靶标药理学网络和关键子网络
基于五苓散靶基因集和肾结石相关基因集,利用Cytoscape version 3.8.0构建复合靶网络。利用Cytoscape中的CytoNca plugin鉴定出最有价值的化合物节点,然后构建出排名第1位的化合物节点及其靶基因的关键子网络。
1.4 蛋白质相互作用(PPI)网络和富集分析
利用五苓散-肾结石共同靶基因,采用STRING数据库构建PPI网络。使用R软件4.0.3版本的clusterprofile软件包进行GO和KEGG富集分析,通过生物过程、细胞成分、分子功能和关键信号通路揭示其潜在分子机制。
1.5 分子对接技术
选择化合物-靶标网络中关联最多且最有价值的化合物进行后续分子对接分析。在Uniprot数据库(https:∥www.uniprot.org/)中搜索目标基因编码的受体蛋白。然后从RCSB PDB数据库(https:∥www.rcsb.org/)中下载该蛋白质三维结构。该分子化合物二维结构从PubChem数据库(https:∥pubchem.ncbi.nlm.nih.gov/)下载。利用ChemBio 3D软件计算并输出自由能最小的三维结构。用PyMOL 2.4.0软件对受体蛋白进行脱水,用Autodock软件对蛋白进行氢化和电荷计算。受体蛋白对接位点的参数设置包括小分子配体结合的活性口袋位点。利用Autodock Vina将受体蛋白与五苓散最有价值的分子化合物配体进行对接。
2 结果
2.1 活性化合物和潜在靶点的筛选
利用TCMSP数据库,得到茯苓、泽泻、猪苓、桂枝、白术5种五苓散成分。共获得51个药物靶基因。从Genecards、OMIM、DrugBank和DisGeNet数据库中分别获得720、54、60、262个肾结石相关基因。剔除重复基因并结合搜索结果,共获得729个肾结石相关基因集(图1A)。进一步将药物靶基因与疾病相关基因取交集,最终得到13个五苓散-肾结石共同靶基因(图1B)。
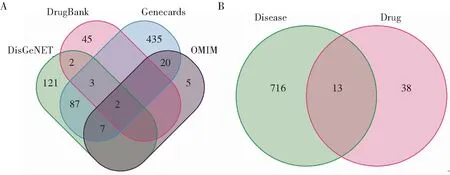
A.肾结石相关基因的鉴定;B.五苓散靶基因和肾结石相关基因的交集
2.2 五苓散活性化合物靶标药理学网络和关键子网络
在明确五苓散活性化合物和五苓散-肾结石共同靶基因后,采用Cytoscape 3.8.0可视化了20个节点和19条关联线路的化合物靶基因相互作用网络(图2A)。一般来说,一个基因可以被多个活性化合物靶向,而一个化合物也可以靶向多个基因。在13个基因中,CHRM3是五苓散成分最具针对性的基因。通过CytoNca plugin确定MOL000358(β-谷甾醇)为最有价值的化合物,随后构建了一个β-谷甾醇及其靶基因的关键子网络(图2B)。
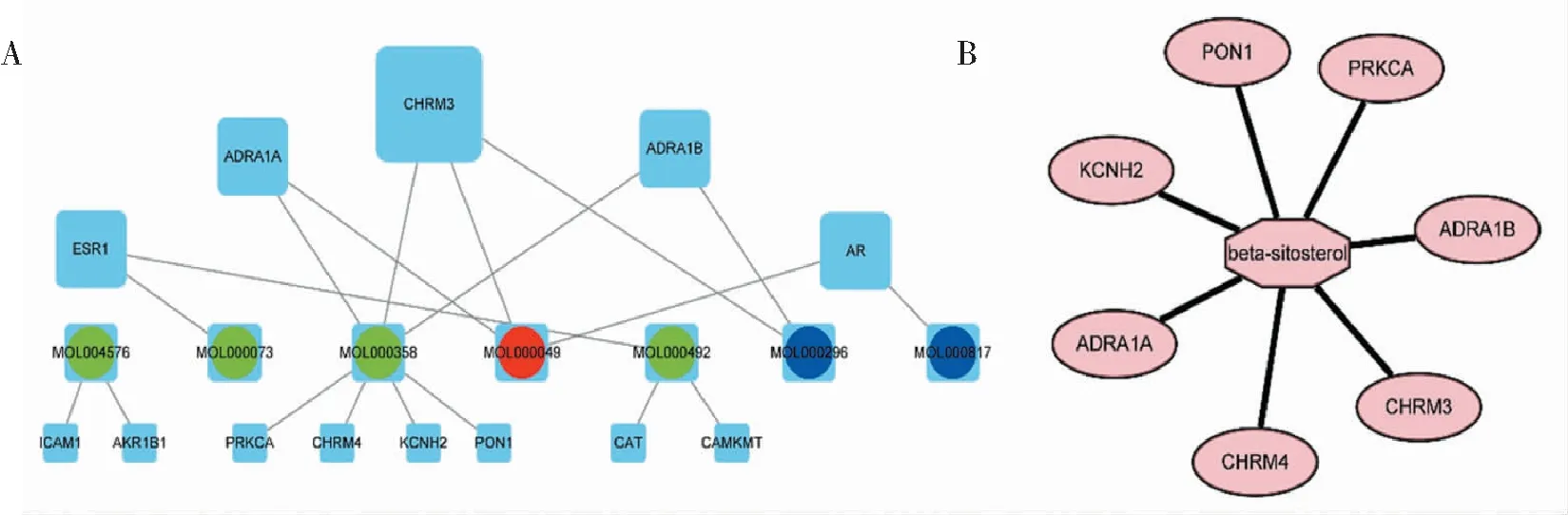
A.药靶相互作用药理学网络,圆形代表五苓散中的小分子化合物,每一种颜色代表一种中药成分;矩形表示肾结石相关的靶基因,边缘表示小分子化合物与靶基因的相互作用;B.基于β-谷甾醇的关键子网络
2.3 PPI网络及靶向基因集富集分析
由STRING数据库衍生的PPI网络显示,五苓散-肾结石共同靶基因编码的蛋白具有复杂的相互作用(图3A,3B)。利用GO富集分析挖掘这13个靶基因的潜在生物学过程、细胞成分和分子功能,共得到326个显著富集的GO项,前10个如图3C所示。GO的富集结果表明,这些靶基因在G蛋白偶联受体信号通路中发挥了重要作用,也在包括血清素、乙酰胆碱、激素、胺等多种激素或神经递质的结合中发挥了重要作用,并在血管收缩的调节中发挥了重要作用。通过KEGG富集分析,靶基因显著富集的8条通路如图3D所示,结果表明这些靶基因主要影响钙信号通路、血管平滑肌收缩、神经活性配体-受体相互作用、心肌细胞肾上腺素能信号通路以及内分泌和其他因素调节的钙重吸收通路。
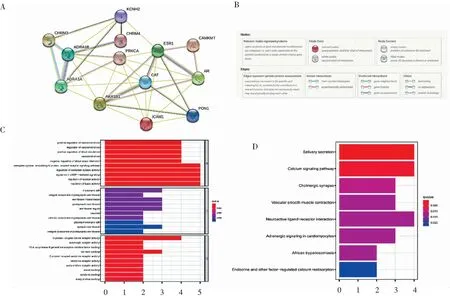
A.从STRING数据库导出的PPI网络;B.对PPI网络中节点和边的标注;C.目的基因GO富集分析;D.目的基因KEGG富集分析
2.4 β-谷甾醇与CHRM3编码蛋白的分子对接
通过软件下载β-谷甾醇的2D结构(图4A)和CHRM3蛋白的3D结构(图4B)。利用ChemBio 3D软件以最小自由能预测β-谷甾醇的三维结构(图4C)。随后,分子对接表明β-谷甾醇可以很容易地进入并结合CHRM3蛋白活性口袋(图4D,4E)。对接评分为-5.9 kcal/moL,进一步表明β-谷甾醇与CHRM3蛋白结合良好。
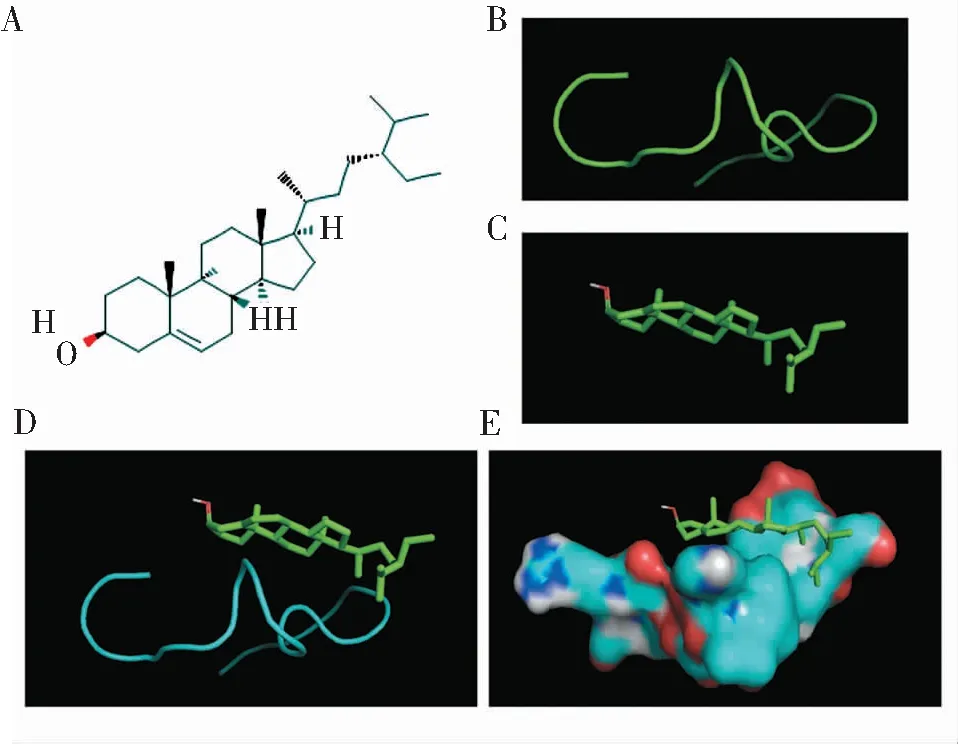
A.β-谷甾醇的二维结构;B.CHRM3蛋白的三维结构;C.β-谷甾醇的三维结构;D,E.β-谷甾醇与CHRM3蛋白的分子对接,其中D为配体和受体的三维结构,E为受体的表面和配体的三维结构
3 讨论
肾结石作为泌尿外科最常见的疾病,发病率逐年上升,但目前仍缺乏有效的药物治疗手段。有研究报道,五苓散加味联合常规西药治疗肾结石效果理想,可降低近期复发率,提高排石率[7],但其具体作用机制仍不得而知。本研究结果显示,五苓散中的13种活性成分在肾结石的治疗中发挥重要作用,并与多种蛋白质和信号通路相关,表明这些活性成分具有潜在的研究价值。β-谷甾醇可能是五苓散发挥治疗肾结石的主要化合物,而M3毒蕈碱受体(CHRM3)是五苓散成分最具针对性的基因。GO和KEGG富集分析结果表明,五苓散-肾结石共同靶基因主要集中在G蛋白偶联受体信号通路、钙信号通路和血管平滑肌收缩信号通路等。毒蕈碱受体属于G蛋白偶联受体家族,包括五个亚型,其中兴奋性毒蕈碱M3受体优先与Gq/11结合[8]。毒蕈碱M3受体通过动员三磷酸肌醇(InsP3)和二酰基甘油(DAG)来增加细胞内的钙[9]。有报道显示,输尿管中存在CHRM3分布[10]。我们通过分子对接证实β-谷甾醇可以很容易地进入并结合CHRM3蛋白活性口袋。对接评分为-5.9 kcal/mol,进一步表明β-谷甾醇与CHRM3蛋白结合良好。由此可见,五苓散可能通过其活性成分β-谷甾醇作用于CHRM3,从而通过调节细胞内的钙离子浓度来介导输尿管蠕动,起到促进结石排出的作用。
Hassan等[11]报道CHRM3可通过影响T84细胞表面SLC26A6表达来调控草酸转运,进而参与肾结石形成。SLC26A6是一种多功能阴离子转运蛋白,主要在小肠绒毛上皮和肾小管上皮细胞顶膜中表达,是体内介导草酸转运最重要的蛋白分子之一。肠道和肾小管上皮中的草酸平衡由SLC26A6维持,其失衡导致高草酸尿和高草酸血症[12]。而高草酸尿是肾结石形成的主要危险因素之一[13]。这提示五苓散中的β-谷甾醇可通过作用CHRM3来调控肠道中SLC26A6蛋白的表达,从而增加肠道草酸的分泌,减少结石复发。然而,这些活性化合物的深层作用机制仍有待进一步实验研究阐明。
综上所述,药理学网络和分子对接分析可揭示五苓散治疗肾结石的潜在机制,这可能为新型肾结石防治药物的设计提供指导。
