山茱萸药材采收加工过程副产物的资源化利用研究现状与展望△
2022-12-26张浩宽郭盛严辉高松李俊科段金廒
张浩宽,郭盛,严辉,高松,李俊科,段金廒*
1.南京中医药大学 江苏省中药资源产业化过程协同创新中心/中药资源产业化与方剂创新药物国家地方联合工程研究中心/国家中医药管理局中药资源循环利用重点研究室,江苏 南京 210023;
2.河南宛西制药股份有限公司,河南 南阳 473000
山茱萸为山茱萸科山茱萸属植物山茱萸Cornus officinalisSieb.et Zucc 的干燥成熟果肉。其味酸、涩,性微温,入肝、肾两经,具有补益肝肾、涩精固脱之功,主要用于治疗眩晕耳鸣、腰膝酸痛、阳痿遗精、内热消渴等[1]。山茱萸属植物全球共4 种,分布于欧洲中部、南部,亚洲东部及北美东部[2]。我国有山茱萸和川鄂山茱萸C.chinensis2 种,其中,山茱萸为临床常用中药,主要分布于秦岭山脉的巴山区、伏牛山区及天目山区等。
随着大健康产业的蓬勃发展,市场对于药食同源的山茱萸需求量剧增。据不完全统计,2019 年全国山茱萸种植面积已超过40万亩(1亩≈666.67 m2),年产量以干货计约6 万t。与此同时,其产地加工过程中产生的叶片、果核等非药用部位产量远高于果肉。初步测算,果核年产量可达25 万t。然而,山茱萸非药用部位的应用基础和资源化利用研究较为薄弱,缺乏有效利用途径,造成资源的巨大浪费和生态环境污染加剧。鉴于此,本文对国内外报道的山茱萸果核及叶片所含的化学成分、生物活性、开发利用等研究现状进行了较为系统的梳理分析,结合中药资源化学研究思路与资源循环利用相关策略[3],提出了山茱萸资源提质增效与产业绿色发展的若干建议,以期为山茱萸传统非药用部位的资源化利用和产业的高质量发展提供参考。
1 资源性化学成分研究进展
目前,对山茱萸药材的研究报道较多,已从中分离鉴定出300 余个化合物,包括环烯醚萜、鞣质、三萜、黄酮等化合物,具有抗肿瘤、降血糖、抗氧化、保护肝脏、调节骨代谢等多种药理作用[4]。也有学者从山茱萸果核及叶中分离鉴定出90 余个化合物(表1),包括3 个黄酮类、20 个鞣质类化合物、10 个有机酸及酚酸类、46 个脂肪酸及其酯类、7个环烯醚萜类、9个三萜类和4个其他类化合物。

表1 山茱萸果核及叶中分离鉴定出的化学成分

续表1

续表1
1.1 山茱萸果核
1.1.1 油脂类成分 山茱萸果核中含有丰富的油脂类成分,有研究表明,其中油脂质量分数为7%~8%,经气相色谱分离鉴定出6 个脂肪酸,分别是月桂酸、硬脂酸、棕榈酸、油酸、亚油酸、亚麻酸。油脂中不饱和脂肪酸(油酸、亚油酸、亚麻酸)的含量较高,占脂肪酸总量的90.58%。其中,亚油酸相对质量分数达70%以上[19]。山茱萸果核由内果皮和种子组成,内果皮质量分数为86.5%,种子质量分数为13.5%。郑玉丽等[20]对山茱萸核不同部位的脂肪油含量进行了测定,结果显示果核脂肪油的平均质量分数为7.89%;内果皮中脂肪油质量分数为2.13%,种子中脂肪油质量分数为48.64%,远高于内果皮。
1.1.2 有机酸和酚酸类成分 杨晖等[12]采用高效液相色谱法(HPLC)测定了山茱萸果核中5 个有机酸(草酸、酒石酸、DL-苹果酸、柠檬酸和没食子酸)的质量分数。结果显示,草酸、酒石酸、DL-苹果酸、柠檬酸和没食子酸的质量分数分别为0.36%、0.78%、1.82%、0.87% 和2.41%。唐凯等[13]采用HPLC测定了不同产地山茱萸果核中的没食子酸、5-羟甲基糠醛、原儿茶酸的质量分数,质量分数由高到低分别为没食子酸、5-羟甲基糠醛、原儿茶酸;其中,汉中镇巴县样品的没食子酸质量分数最高(2.671%),陕西汉中与宝鸡所产山茱萸果核中这3个成分的质量分数较高。有研究采用Folin-Ciocalteu法,以没食子酸为对照品,测得3 批山茱萸果核水溶性提取物中多酚的平均质量分数为39.24%[21]。
1.1.3 鞣质类成分 有研究表明,山茱萸果核中的鞣质为混合型,且以水解型为主,采用络合量法和高锰酸钾法对山茱萸果核不同溶剂提取液中的鞣质进行含量测定,结果显示鞣质质量分数为16.28%~19.53%[22]。安莉等[23]采用干酪素法,以磷钼戊酸为显色剂、没食子酸为对照品,比较了不同产区山茱萸果核中鞣质的含量,结果显示河南>浙江>陕西,其中河南产区山茱萸果核鞣质质量分数达5.05%,且相对稳定。有研究采用干酪素法测定山茱萸果核鞣质含量,并通过响应面法优化了山茱萸果核鞣质的提取工艺,结果表明,料液比1∶22、乙醇体积分数42%、超声温度52 ℃、超声时间71 min为最佳提取工艺,鞣质的质量分数达69.29 mg·g-1[24]。以上报道果核中鞣质的含量差异较大,笔者认为是测定方法不同所致。鞣质为化学性质复杂的多元酚,前者采用的是络合量法及高锰酸钾法,这2 种方法专属性差,易导致测定结果偏高;而后者采用的干酪素法选择性更高,但干酪素只与有生理活性的鞣质产生沉淀,易导致测定结果偏低。综合来看,山茱萸果核含有较为丰富的鞣质资源。
1.1.4 五环三萜类成分 尚遂存等[18]从山茱萸果核中分离鉴定得到白桦脂酸。李军等[25]建立了同时测定山茱萸果壳和果仁中白桦脂酸和熊果酸的方法,并对多个产地的样品进行了含量测定。结果显示,果仁中熊果酸含量显著高于果壳,两者白桦脂酸的含量差异无统计学意义。山茱萸果壳中白桦脂酸质量分数为3.65~5.34 mg·g-1、熊果酸质量分数为0.87~1.72 mg·g-1,果仁中白桦脂酸质量分数为3.61~4.97 mg·g-1、熊果酸质量分数为4.88~7.46 mg·g-1。
1.1.5 环烯醚萜类成分 李军等[9]在山茱萸果核70%丙酮提取物中分离鉴定得到山茱萸新苷。有研究采用HPLC 测定了采自陕西、河北和山西的14 批山茱萸果核中莫诺苷的含量,结果表明14 批样品中莫诺苷的平均质量分数为0.737%,其中汉中宁强县的样品莫诺苷质量分数最高,达1.233%[13]。
除以上化学成分外,山茱萸果核中还含有多糖类、皂苷类、黄酮类、氨基酸类等成分。此外,山茱萸果核中含有丰富的维生素B1、维生素C 和维生素E,富含蛋白质、粗纤维及21个矿物元素等[26-28]。
1.2 山茱萸叶
1.2.1 挥发性成分 山茱萸叶中挥发性成分主要由醇类、萜烯类、酯类、醛酮类、酚酸类、烃类、呋喃类及其他类成分组成。马亚荣等[29]采用静态顶空进样技术(SHS)结合气相色谱串联质谱法(GCMS),对不同温度(65、95、115 ℃)下山茱萸叶中挥发性成分进行定性分析,结果显示,在不同温度条件下挥发性成分的种类和质量分数存在差异,其共有成分为1-戊烯-3-醇、顺式-2-戊烯醇、正己醛、反式-2-己烯醛、3-己烯-1-醇、顺式-2-己烯-1-醇、苯甲醛、邻-异丙基苯、D-柠檬烯、石竹烯和蛇麻烯。其中,反式-2-己烯醛和正己醛在山茱萸叶中质量分数相对较高。山茱萸叶中主要挥发性成分与果肉中所含挥发性成分有所不同。
1.2.2 环烯醚萜类成分 环烯醚萜类是山茱萸中含量较高的成分类群,被认为是山茱萸中的特征性成分。Li等[16]在山茱萸叶的甲醇提取物中分离出4个环烯醚萜,其中包括3 个新的山茱萸醚萜素(山茱萸醚萜素A、山茱萸醚萜素 B、山茱萸醚萜素C)和吕宋荚蒾B。
1.2.3 黄酮类成分 有研究报道,在山茱萸叶中分离鉴定得到芦丁、槲皮素和柚皮素[5-6]。孙建瑞等[30]通过响应面法对豫西山茱萸叶黄酮的提取工艺进行了优化,结果显示,在料液比为1∶31、乙醇体积分数为61%、超声功率为290 W、提取时间为23 min的条件下,山茱萸叶黄酮得率最高,达6.31%。
1.2.4 多糖类成分 以500 g干燥山茱萸叶为原料,通过水提醇沉、过氧化氢除色素等步骤制得山茱萸叶多糖6.797 g,进而采用比色法对山茱萸叶多糖理化性质进行了测定,并采用1-苯基-3-甲基-5-吡唑啉酮(PMP)柱前衍生化HPLC 对山茱萸叶中多糖的单糖组成进行分析,发现山茱萸叶多糖中总糖质量分数为(612.76±1.72)mg·g-1、糖醛酸质量分数为(228.03±0.54)mg·g-1、可溶性蛋白质质量分数为(9.53±0.38)mg·g-1、硫酸根质量分数为(25.21±0.19)mg·g-1;山茱萸叶多糖由甘露糖、鼠李糖、半乳糖醛酸、葡萄糖、半乳糖、阿拉伯糖、岩藻糖7 种单糖构成,采用标准曲线法进行定量,得到其物质的 量比为1.66∶3.20∶6.20∶5.00∶13.00∶14.10∶1.00[31]。
1.2.5 三萜类成分 朱登辉等[32]以齐墩果酸为对照品,采用紫外-可见分光光度法在546 nm 波长下测定了山茱萸叶中总三萜的含量,并通过响应面法对山茱萸叶总三萜的提取工艺进行了优化,结果显示,在料液比1∶38、乙醇体积分数73%、加热回流提取60 min的条件下,山茱萸叶总三萜质量分数最高为6.89%。
1.2.6 鞣质类成分 Lee 等[7]从山茱萸叶中分离得到了第1 个以七糖为核心的没食子酸鞣质1,7-二-O-没食子酰基-D-景天庚酮糖。此外,还分离得到了没食子酰葡萄糖苷2,3-二-O-没食子酰基-D-吡喃葡萄糖、1,2-二-O-没食子酰基-β-D-吡喃葡萄糖、3,4,6-三-O-没食子酰基-D-吡喃葡萄糖、1,2,6-三-O-没食子酰基-β-D-吡喃葡萄糖、1,2,4,6-四-O-没食子酰基-β-D-吡喃葡萄糖、1,2,3,6-四-O-没食子酰基-β-D-吡喃葡萄糖3-O-没食子酰基-4,6-(S)-六羟基联苯酚基-D-葡萄糖、2-O-没食子酰基-4,6-(S)-六羟基联苯酚基-D-葡萄糖、1-O-没食子酰基-4,6-(S)-六羟基联苯酚基-α-D-吡喃葡萄糖、1-O-没食子酰基-4,6-(S)-六羟基联苯酚基-β-D-葡萄糖和日本马桑素F。
2 生物活性研究进展
2.1 果核生物活性
2.1.1 抑菌、抗炎活性 有研究比较了山茱萸果肉及果核对金黄色葡萄球菌和痢疾杆菌的抑制作用,发现果核、果肉具有相似的抑菌活性,并推测没食子酸是其抑菌作用的主要活性成分[33]。张红玉等[34]比较了山茱萸果肉及果核的抗炎作用,分别制备了小鼠棉球植入和大鼠二甲苯致耳肿胀2 种炎症模型,对小鼠肉芽净质量和大鼠耳肿胀度进行测量观察以评价其抗炎活性,结果表明果肉和果核均具有一定的抗炎作用,但同浓度下果肉提取物的作用要强于果核提取物。Jang 等[17]从山茱萸果核乙醇提取物中分离出熊果酸,并对其抗炎活性进行了研究,结果显示,熊果酸可能通过抑制脂多糖和Toll 样受体4(TLR4)在免疫细胞上的结合从而调节核转录因子-κB(NF-κB)和丝裂原活化蛋白激酶(MAPK)信号通路而发挥改善小鼠结肠炎的作用。
2.1.2 抗氧化活性 以维生素C 为对照,从羟自由基、超氧阴离子自由基和1,1-二苯基-2-三硝基苯肼(DPPH)自由基的清除能力这3 个指标评价了山茱萸果核石油醚、乙酸乙酯、无水乙醇、水提取物的体外抗氧化活性,结果表明,山茱萸果核不同提取物的抗氧化活性存在差异,其趋势为水提取物>无水乙醇提取物>乙酸乙酯提取物>石油醚提取物;其中水提取物清除DPPH 自由基的能力要强于阳性药,表明其水提物具有较强的抗氧化活性[35]。李晓明等[36]以维生素C为阳性对照,从DPPH自由基、亚硝酸盐自由基、羟自由基的清除率及总还原力4 个方面来评价山茱萸果核中的多酚类成分抗氧化活性,结果显示,山茱萸果核多酚对羟自由基的清除率要低于维生素C,而在DPPH自由基、亚硝酸盐自由基清除率和总还原力这3 个方面山茱萸果核多酚高于同浓度下维生素C 的效果,且均呈现出良好的量效关系。D-半乳糖在体内代谢可产生过量的自由基,使脑组织抗氧化酶活性下降,脂质过氧化反应增强,这是导致机体衰老、认知功能下降的一个重要机制。有研究表明,山茱萸果核醇提物能明显改善D-半乳糖致衰老小鼠的学习记忆能力,并以超氧化物歧化酶(SOD)、谷胱甘肽过氧化物酶(GSH-Px)活性,总抗氧化能力(T-AOC),丙二醛(MDA)含量作为评价其抗氧化能力的指标,结果表明,与模型组相比,山茱萸果核醇提物各剂量组小鼠脑组织的MDA含量明显下降,SOD、T-AOC活性明显升高,高、中剂量组的GSH-Px也明显升高,表明山茱萸果核醇提物具有提高小鼠脑组织清除自由基的能力[37]。
2.1.3 降血糖活性 张夙夙[38]以阿卡波糖为阳性对照,探究山茱萸核鞣质对α-葡萄糖苷酶的抑制作用与作用类型,结果表明山茱萸核鞣质对α-葡萄糖苷酶具有较好的抑制作用,其半数抑制浓度(IC50)为1076 mg·L-1,与阳性药组相当;进一步研究表明其对α-葡萄糖苷酶的抑制属于可逆性抑制,且属于非竞争性抑制。安莉[24]采用高脂高糖饲料联合低剂量链脲佐菌素(30 mg·kg-1)制备了2 型糖尿病小鼠模型,考察山茱萸果核鞣质对2型糖尿病小鼠空腹血糖、糖耐量(OGTT)、三酰甘油(TG)、总胆固醇(TC)等血脂指标的影响,结果表明,中(200 mg·kg-1)、高(400 mg·kg-1)剂量组、阳性药组与模型组在空腹血糖及各种生化指标方面差异有统计学意义(P<0.05),且呈剂量依赖性,说明山茱萸果核鞣质对2 型糖尿病小鼠有较好的降糖作用。
2.1.4 抗肿瘤活性 余平等[39]比较了山茱萸果肉与果核抗ICR小鼠腹水瘤的作用,结果显示,山茱萸果肉组(2 g·kg-1)和山茱萸果核高剂量组(6 g·kg-1)小鼠的存活时间与0.9%氯化钠溶液组差异有统计学意义(P<0.01),对腹水瘤小鼠的生命延长率分别为69.60%和50.98%。山茱萸果核醇提物具有一定的抗肿瘤活性,以不同浓度果核醇提物处理肝癌细胞HepG2 24 h,使用噻唑蓝(MTT)比色法测定其抑制率,结果表明山茱萸果核醇提物在不同浓度下均能抑制肝癌细胞HepG2 的增殖,且呈浓度依赖性;进一步采用逆转录聚合酶链式反应(RT-PCR)检测胱天蛋白酶-3(Caspase-3)、B 细胞淋巴瘤-2(Bcl-2)mRNA的表达,采用蛋白质印迹法(Western blot)检测Caspase-3、Bcl-2 蛋白的表达,根据实验结果推测山茱萸果核醇提物是通过上调Caspase-3、下调Bcl-2表达,诱导肝癌细胞HepG2的凋亡[40]。
2.1.5 保肝活性 有研究通过观察小鼠肝脏组织切片病理学变化,测定小鼠血清中丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、MDA 水平,肝组织中SOD、GSH-Px 水平,用于评价山茱萸不同部位(果肉、果核、全果)提取物对醋氨酚致小鼠急性肝损伤的保护作用。结果表明,与模型组比较,山茱萸果核、全果、果肉提取物的中、高剂量组小鼠的肝组织病变均有不同程度改善,肝细胞坏死明显减轻,其中山茱萸果核提取物中、高剂量组和山茱萸全果提取物高剂量组小鼠未见肝细胞片状坏死,肝小叶结构基本完整,效果优于果肉中、高剂量组;山茱萸果核提取物和山茱萸全果提取物均能显著降低肝损伤小鼠血清中ALT、AST 水平,且变化较果肉提取物组更明显;此外,中剂量的山茱萸果肉提取物,中、高剂量的山茱萸全果提取物及各剂量山茱萸果核提取物均能显著升高肝损伤小鼠肝组织中GSH-Px、SOD 水平,显著降低肝组织中MDA 水平[41]。提示山茱萸果核具有开发为保肝药物的潜力。
2.1.6 其他作用 此外,山茱萸果核还具有降血压、抗疲劳、治疗佐剂性关节炎、改善心脏功能、舒张血管及抗实验性心律失常等作用[42-45]。
2.2 叶生物活性
2.2.1 抑菌活性 有研究采用滤纸片法测试山茱萸叶黄酮类组分对6种细菌、3种真菌的抑菌活性,结果显示山茱萸叶黄酮类组分对细菌和真菌均有一定的抑菌效果,其中对沙门菌的抑制作用最强,抑菌圈直径达12.04 mm,整体上看,山茱萸叶黄酮类组分对细菌的抑菌效果要强于对真菌的抑菌效果;其对革兰阴性菌的抑菌效果强于革兰阳性菌[30]。
2.2.2 抗氧化活性 有研究以2,6-二叔丁基对甲酚(BHT)作为阳性对照,从DPPH 自由基清除能力和羟自由基清除能力2 个指标来评价豫西山茱萸叶黄酮类组分的抗氧化活性,结果表明,山茱萸叶黄酮类组分能明显清除DPPH 自由基和羟自由基,其中清除羟自由基的能力强于BHT,并且两者的清除率随山茱萸叶黄酮浓度的升高而增强,说明山茱萸叶黄酮类组分的抗氧化能力较强[30]。李玥彤等[31]评价了山茱萸叶多糖对DPPH 自由基和羟自由基清除能力、亚铁离子络合能力及其对H2O2诱导的HepG2细胞活力的影响,发现山茱萸叶多糖对DPPH 自由基的IC50为0.13 mg·mL-1,对羟自由基的IC50为0.56 mg·mL-1,其抗氧化能力与维生素C 相当;不同质量浓度山茱萸叶多糖均可提高氧化损伤HepG2细胞的相对存活率,当其质量浓度为0.4 mg·mL-1时,细胞内MDA 和活性氧(ROS)含量均显著降低。
2.2.3 抗肿瘤活性 Forman 等[46]对5 种山茱萸科植物叶的水提物抗乳腺癌细胞增殖活性进行了比较,其中包括欧洲山茱萸C.mas、红瑞木C.alba、金枝梾木C.flaviramea、日本四照花C.kousa和山茱萸,研究结果显示,所有受试提取物对人乳腺癌MCF-7细胞均具有抗增殖活性,且均呈剂量和时间依赖性。5 种提取物中山茱萸叶的活性最好,其72 h 后细胞存活率为10.3%;此外该研究还将5 种叶中总黄酮(以金丝桃苷表示)、总羟基肉桂酸衍生物(以迷迭香酸表示)、总多酚及鞣质类(以邻苯三酚表示)物质的含量与抗增殖活性做了相关性分析,认为其抑制效果与叶中所含总多酚和鞣质类物质的含量呈正相关。有研究发现,山茱萸叶丙酮提取物能抑制BALB/c 小鼠黑色素瘤移植瘤的生长和糖酵解,降低血清中炎症因子白细胞介素-6(IL-6)、IL-17A、肿瘤坏死因子-α(TNF-α)和γ-干扰素(IFN-γ)的水平,通过抑制信号转导子与转录激活子3(STAT3)信号通路中抗细胞凋亡蛋白Bcl-2、髓细胞白血病因子-1(Mcl-1)等的表达和STAT3 蛋白的磷酸化,促进肿瘤细胞凋亡,并减少肿瘤血管生成,从而发挥抗黑色素瘤作用。此外还发现山茱萸叶50%丙酮提取物中的马钱苷、穿心莛子藨醚萜C 和穿心莛子藨醚萜D、芦丁能显著抑制人黑色素瘤A375 细胞增殖和迁移,并抑制STAT3的磷酸化和核转位。HPLC分析结果表明,提取物中马钱苷、穿心莛子藨醚萜C、穿心莛子藨醚萜D 和芦丁的质量分数分别为0.75%、0.22%、0.48%和0.19%[4]。
3 资源化利用策略及展望
通过对中药资源产业化过程资源价值创新、资源化利用及产业化开发等进行系统研究与实践,从而节约资源、保护环境,推动我国中药资源循环经济和绿色产业发展。本文基于山茱萸果核及叶中含有的活性组分及同属植物资源化利用报道提出其分级利用策略(图1)。
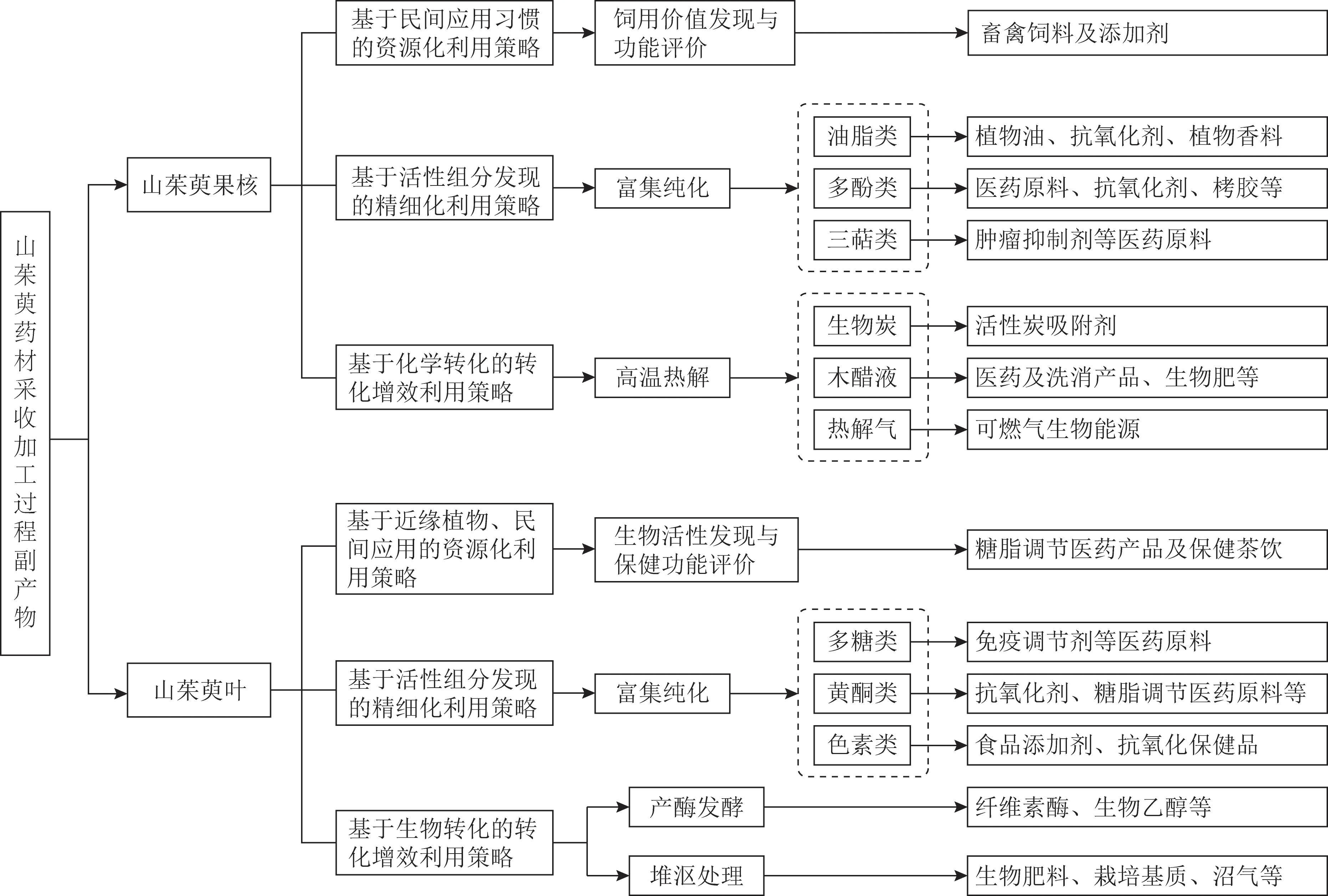
图1 山茱萸采收加工过程副产物资源化利用多元途径
3.1 基于传统记载及近缘植物民间应用习惯的资源化利用策略
据记载,欧洲山茱萸的叶片可用于治疗胃病、高血糖、高血压和伤口愈合,且在土耳其民间也将其用作茶饮[47-49];同属植物毛梾C.walteri的叶片可用于治疗漆毒引起的皮肤炎症或脓肿[50],在韩国医学中也被用作止泻药[51]。这提示可以山茱萸叶为主要原料,在前期相关生物活性研究的基础上,开展具有降血糖、降血压、止泻等功能的医药产品及功能食品开发。此外,民间有利用山茱萸果核饲喂牲畜的习惯。有研究显示,在奶山羊饲粮中添加山茱萸果核,可提高奶山羊的产奶量,且对乳脂率有显著抑制作用;山茱萸果核可通过促进羊奶中短、中链脂肪酸的合成,调控乳腺中乙酰辅酶A 羧化酶(ACC)、硬脂酰辅酶A 去饱和酶(SCD1)和TG水解酶(ATGL)的表达,改善奶山羊乳品质[52],提示山茱萸果核可用于功能性饲料开发,可按照饲料标准对山茱萸叶、果核等非药用部位进行饲用价值分析及饲用功能评价,开发为相关饲用产品或饲料添加剂。
3.2 基于化学组分生物活性发现的精细化利用策略
山茱萸果核中酚类成分具有抗氧化、降压和保肝等功效,可用于制备治疗相关疾病的药物[53-55]。含有山茱萸果核提取物的食品保鲜剂对肉类食品有较好的保鲜效果,可有效减缓肉的腐败变质[56]。山茱萸果核中还含有熊果酸、白桦脂酸、β-谷甾醇等成分,提取富集后可作为医药原料[57-59]。果核中的鞣质类资源可用来提取栲胶用于皮革行业[60]。山茱萸果核中的油脂经提取富集后可用于开发植物油或医药原料等[61]。经蒸馏后得到的山茱萸果核提取物含有60 余种香味物质,精油酸值17.5~18.8,味道独特,且皮肤无不良反应,可用于日化用品及食品添加剂的开发[62]。山茱萸叶中黄酮类和多糖类组分均具有较好的抗氧化活性,提示其在化妆品、保健食品和生物药品领域具有开发前景[30-31,63]。综上所述,基于资源性成分系统分析与资源价值发现等基础研究,构建山茱萸果核及叶片黄酮类、鞣质类、多糖类等资源性物质分离纯化、富集制备技术体系,结合生物活性研究将其开发制备为相关功能产品或医用原料等。
3.3 基于化学/生物转化的转化增效利用策略
基于本课题组前期构建的中药废弃物及副产物转化增效资源化利用模式[64],结合山茱萸果核的理化特性,可在已有报道[65]的基础上,采用热解炭化工艺,将山茱萸果核热解形成生物炭、木醋液、可燃气等资源性产品。其中,生物炭可进一步活化形成活性炭产品;木醋液可依据其活性物质组成开发形成具有抑菌敛疮作用的医药产品或洗消用品、具有促进饲料转化利用的饲用替抗产品,以及叶面肥等资源性产品。此外,采用生物转化的方法对提取后的山茱萸果核及叶片残渣可进行发酵产酶,转化为纤维素酶、木糖醇、生物乙醇等转化产物,最终实现物尽其用、变废为宝,延伸山茱萸资源产业链,提升资源利用效率及效益。
