基于HPLC与NIRS指纹图谱及多元统计分析山茱萸炮制前后差异
2022-12-26方莹洁杜伟锋葛卫红李昌煜张叶峰张光霁
方莹洁,江 姗,杜伟锋,*,葛卫红,李昌煜,张叶峰,张光霁
(1.浙江中医药大学中药饮片有限公司,浙江 杭州 311401;2.浙江中医药大学,浙江 杭州 311402;3.宁波市中药饮片有限公司,浙江 宁波 315336)
山茱萸为山茱萸科植物山茱萸CornusofficinalisSieb.et Zucc.的干燥成熟果肉[1-2],其始载于《神农本草经》,被列为上品,宋代《苏沈》有“酒浸润,蒸透去核取其皮”的记载,元代《活幼心书》记载了酒蒸炮制方法:“酒浸润,蒸透”[3]。目前,临床上常用山萸肉、蒸萸肉以及酒萸肉入药,山萸肉敛阴止汗作用强;蒸萸肉补肾涩精、固精缩尿力胜;酒萸肉借酒力温通,滋补作用强于清蒸品[4]。
现行2020年版《中国药典》[1]从颜色、气味以及含莫诺苷、马钱苷总量上对山萸肉和酒萸肉进行了区分,但不足以体现炮制的特征。山茱萸炮制特征的研究主要集中在炮制前后的指纹图谱及特征性成分的变化。林碧珊等[5]建立了山茱萸炮制前后的UPLC特征图谱,并指认了没食子酸、5-羟甲基糠醛、莫诺苷和马钱苷4个化合物,该方法可以用来区分山茱萸生品和制品;本课题组前期也建立了山茱萸炮制前后的HPLC指纹图谱[6],并指认了6个特征性成分,分别为没食子酸、5-羟甲基糠醛、莫诺苷、獐牙菜苷、马钱苷和山茱萸新苷,并对炮制前后特征性成分的含量变化进行了研究分析[7-8]。近几年,在中药材的定性定量快速分析领域,近红外显示出显著的优越性,涌现出诸多有关山茱萸的近红外研究[9-11]。本实验在前期研究的基础上,优化了HPLC指纹图谱方法,并将HPLC指纹图谱与NIRS指纹图谱相结合,通过多元统计分析建立了更加完善的定性分析方法,从色谱、光谱以及数学分析上为山茱萸生品与制品的综合质量控制提供参考。
1 仪器与试药
1.1 仪器
Agilent-1200高效液相色谱仪(美国安捷伦科技公司);KQ-250B型超声波清洗器(昆山市超声仪器有限公司);ME204E型电子天平(梅特勒-托利多仪器(上海)有限公司);Thermo Antaris II型傅立叶变换近红外光谱仪(美国Thermos公司)。
1.2 试药
对照品没食子酸(批号:110831-201906,纯度≥91.5%)、莫诺苷(批号:111998-201703,纯度≥92.4%)、马钱苷(批号:111640-201808,纯度≥98.6%)均购自中国食品药品鉴定研究院;獐牙菜苷(批号:DST190926-014,纯度≥98%)购自乐美天医药德斯特生物;5-羟甲基糠醛(5-HMF)(批号:Q-042-180112,纯度≥98%)购自成都瑞芬思生物科技有限公司;山茱萸新苷(批号:190104-202103,纯度≥98%)购自上海鸿永生物科技有限公司;乙腈为色谱纯;其余均为分析纯;水为娃哈哈纯净水。
山茱萸来源见表1,S1~S21为山茱萸生品山萸肉,Z1~Z21为山茱萸制品酒萸肉,均按照2020年版《中国药典》加工炮制,并经浙江中医药大学中药饮片有限公司主管中药师钱敏鉴定为山茱萸科植物山茱萸CornusofficinalisSieb.et Zucc.的干燥成熟果肉的炮制加工品。

表1 山茱萸来源
2 方法与结果
2.1 HPLC指纹图谱分析
2.1.1 色谱条件 Agilent Eclipse Plus C18色谱柱(250 mm×4.6 mm,5 μm);流动相为乙腈(A)-0.1%磷酸溶液(B),梯度洗脱:0~50 min,2%~13%A;50~85 min,13%~25%A;流速为1 mL·min-1;检测波长240 nm。柱温35 ℃;进样量10 μL。
2.1.2 供试品溶液制备 精密称取样品粉末(过三号筛)0.5 g,置于具塞锥形瓶中,精密加入80%甲醇25 mL,称重,超声提取(250 W,20 kHz)30 min(加冰袋保持恒温),补重,摇匀,过滤,续滤液用0.45 μm滤膜过滤备用。
2.1.3 对照品溶液制备 取莫诺苷、没食子酸、山茱萸新苷、獐牙菜苷、5-HMF、马钱苷对照品适量,精密称定,加80%甲醇制成混合对照品溶液,对照品浓度分别为5.36 μg/mL、19.37 μg/mL、1.97 μg/mL、16.97 μg/mL、5.11 μg/mL、2.12 μg/mL。
2.1.4 精密度试验 按上述色谱条件连续进样同一批样品溶液(Z1)6次,记录色谱图。以莫诺苷峰为参照峰,计算6个特征峰的相对保留时间及相对峰面积,结果6个特征峰的相对保留时间和相对峰面积RSD<2%(n=6),表明仪器精密度良好。
2.1.5 重现性试验 按上述方法制备6份供试品溶液(Z1),分别进样,记录色谱图。以莫诺苷峰为参照峰,计算6个特征峰的相对保留时间及相对峰面积,结果6个特征峰的相对保留时间和相对峰面积RSD<2%(n=6),表明方法重复性好。
2.1.6 稳定性试验 分别于 0、2、4、6、8、10、12 h按上述色谱条件进样同一批样品溶液(Z1),记录色谱图。以莫诺苷峰为参照峰,计算6个特征峰的相对保留时间及相对峰面积,结果6个特征峰的相对保留时间和相对峰面积RSD<2%(n=7),表明供试品溶液在12 h内稳定性良好。
2.1.7 指纹图谱建立 对本次收集到21批山萸肉样品和21批酒萸肉样品,按“2.1.2”项下方法分别制备供试品溶液,按“2.1.1”项下色谱条件,精密吸取供试品溶液10 μL,分别进样,记录色谱图。根据结果,运用《中药色谱指纹图谱相似度评价系统2012版》进行分析,山萸肉的对照指纹图谱与21批共有模式的指纹图谱见图1、图2,共检测到14个共有色谱峰,与对照品(图5)比对指认其中5个特征峰:2号峰(没食子酸)、7号峰(莫诺苷)、10号峰(獐牙菜苷)、11号峰(马钱苷)和14号峰(山茱萸新苷)。酒萸肉的对照指纹图谱与21批共有模式的指纹图谱见图3和图4,共检测到17个共有色谱峰,与对照品(图5)比对指认其中6个特征峰:4号峰(没食子酸)、5号峰(5-HMF)、10号峰(莫诺苷)、12号峰(獐牙菜苷)、13号峰(马钱苷)、17号峰(山茱萸新苷)。

注:2.没食子酸;7.莫诺苷;10.獐牙菜苷;11.马钱苷;14.山茱萸新苷。

图2 21批山茱萸生品的指纹图谱

注:4.没食子酸;5.5-羟甲基糠醛;10.莫诺苷;12.獐牙菜苷;13.马钱苷;17.山茱萸新苷。
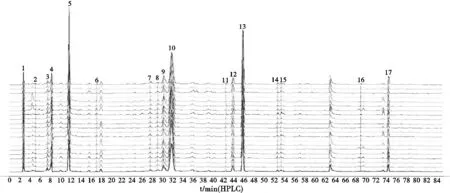
图4 21批山茱萸制品指纹图谱

注:1.没食子酸;2.5-羟甲基糠醛;3.莫诺苷;4.獐牙菜苷;5.马钱苷;6.山茱萸新苷。
2.1.8 指纹图谱数据评价 运用相似度评价系统以对照指纹图谱为参照,分别计算山萸肉和酒萸肉的相似度,见表2和表3。结果显示,山萸肉所有批次相似度均>0.998,相似度好;酒萸肉所有批次相似度均>0.888,相似度较好。酒萸肉相似度值相对较低,可能是由于各饮片公司的炮制条件有所差异,从而导致制品内部存在差异。
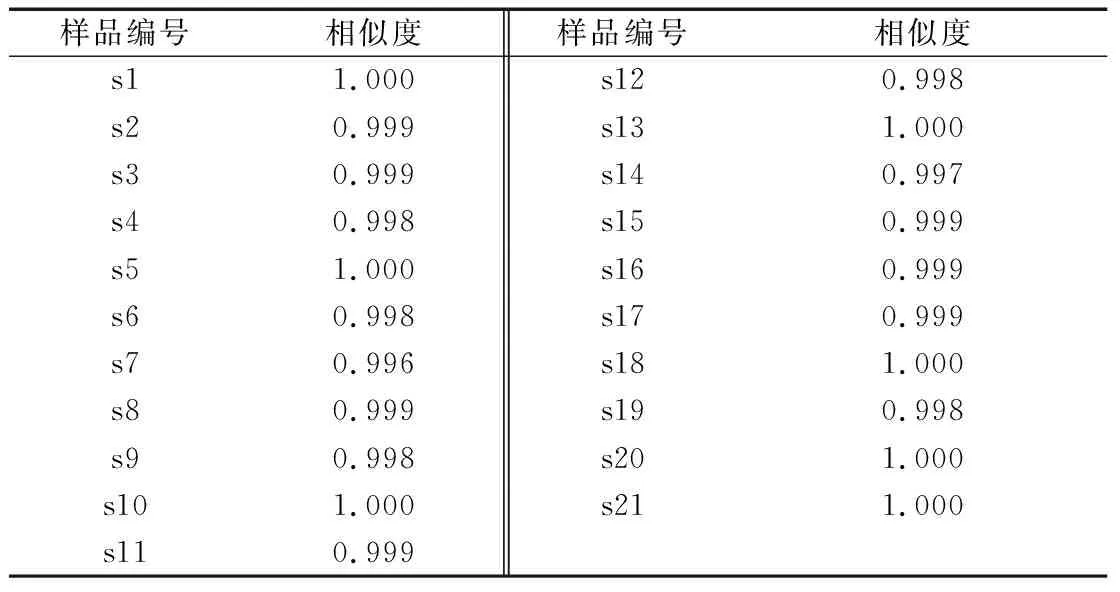
表2 21批山茱萸生品指纹图谱相似度结果
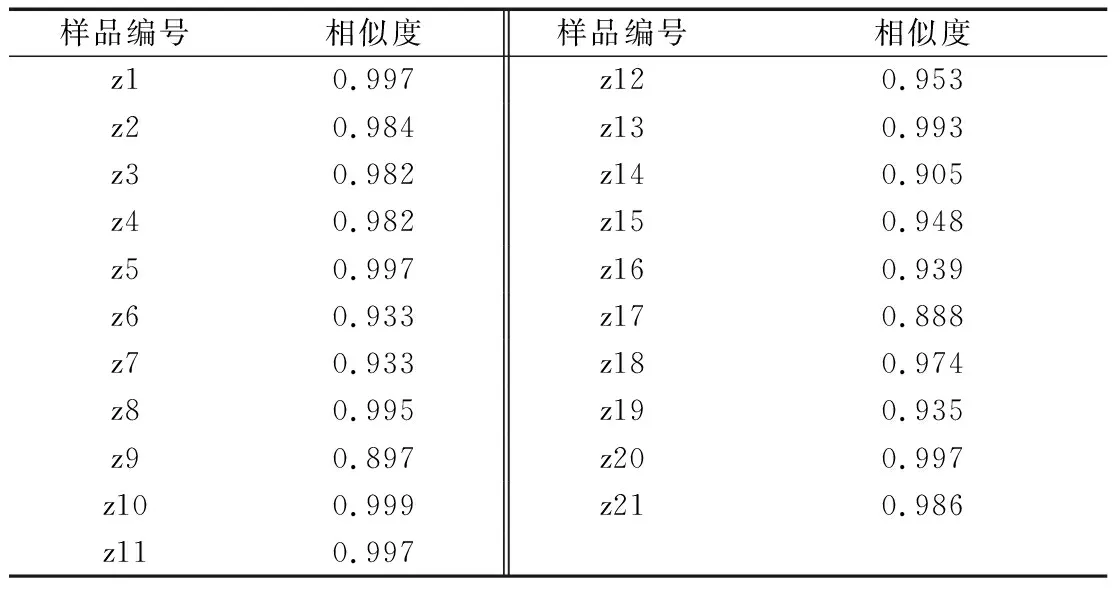
表3 21批山茱萸制品指纹图谱相似度结果
2.2 多元统计分析
2.2.1 聚类分析 以6个特征性成分的相对峰面积为变量,应用SPSS 25.0软件进行聚类分析,采用中位数聚类法,以平方欧式距离作为样品相似度的测度,聚类结果见图6。由图6可知,当距离为15时,分为两大类,1~21样品为1类(均为生品),22~42为1类(均为制品);当距离为10时,分为3类,1~21样品为1类(均为生品),28、35、36、38为1类(均为制品),22~27、29~34、37、39~41为1类(均为制品);而距离为5时,生品1~21仍聚为1类,制品区分为4类。以上可以说明,不同饮品公司的山茱萸生品内部差异性不大,而制品内部差异性较大。

图6 聚类分析树状图
2.2.2 主成分分析 以6个特征峰的峰面积为变量,应用SPSS 25.0软件进行主成分分析,主成分特征值及方差贡献率见表4。当提取到第2个成分时,累计方差贡献率达到87.387%,且两个特征值>1,解释了总方差87.387%的信息。第1主成分的信息主要由色谱峰没食子酸、5-羟甲基糠醛、莫诺苷和山茱萸新苷组成:第2主成分的信息由色谱峰獐牙菜苷和马钱苷组成,见表5。将6个特征成分的峰面积导入SIMCA 14.1软件,选择2个主成分,绘制得到主成分分析得分图,见图7。该结果与聚类分析的结果一致,生品聚为1类,制品聚为1类,其中27和37两个样品分散的较远,结合聚类分析,能够证明制品与生品具有明显差异,生品内部差异不明显,制品内部差异较大。
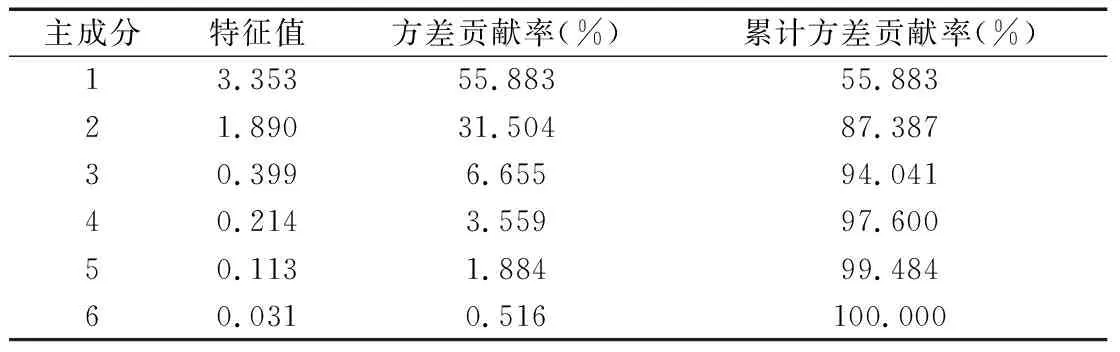
表4 山茱萸样品主成分特征值及方差贡献率

表5 山茱萸样品主成分分析载荷矩阵

图7 主成分分析得分
2.3 近红外定性模型分析
2.3.1 近红外图谱采集 取样品粉末(过三号筛)约10 g,放入石英样品杯中,混合均匀并摊平,扣除参比(内置背景),采集所有样品的光谱图。以积分球漫反射为采样方式,波数区间在4 000~10 000 cm-1之间,分辨率为8.0 cm-1,温度控制在(25±2)℃,相对湿度控制在45%~50%之间。每份样品扫描3次,取其平均光谱作为样品的近红外光谱。得到山茱萸的近红外光谱叠加图,见图8、图9、图10。
2.3.2 判别分析模型建立 采用TQ Analyst软件对山茱萸光谱进行判别分析,以所建模型的性能指数(Performance index,PI)为指标,首先选择多元散射校正(MSC)光程类型,比较原始光谱(Spectrum)图、一阶求导(First derivative,1stD)图、二阶求导(Second derivative,2stD)图,见图8、图9、图10,发现原始光谱图在谱段7 000~10 000 cm-1之间有差异,一阶求导光谱图在谱段5 000~7 500 cm-1之间有差异,二阶求导光谱图在谱段5 000~7 500 cm-1之间有差异,相对来说一阶求导图和二阶求导图较为复杂,选用合适谱段较为困难,因此选用原始光谱图的差异性谱段进行优化。第二步通过比较不同光谱预处理方法(不平滑(No smoothing,NS)、卷积平滑滤波(Savitzky-Golay filter,S-G)、Norris导数平滑滤波(Norris derivative filter,ND))进行筛选,不同光谱预处理方法建模的性能指数见表6,经比较,最终选择谱段为7 000~10 000 cm-1,同时选用“SNV+Spectrum+NS”组合作为预处理方法。
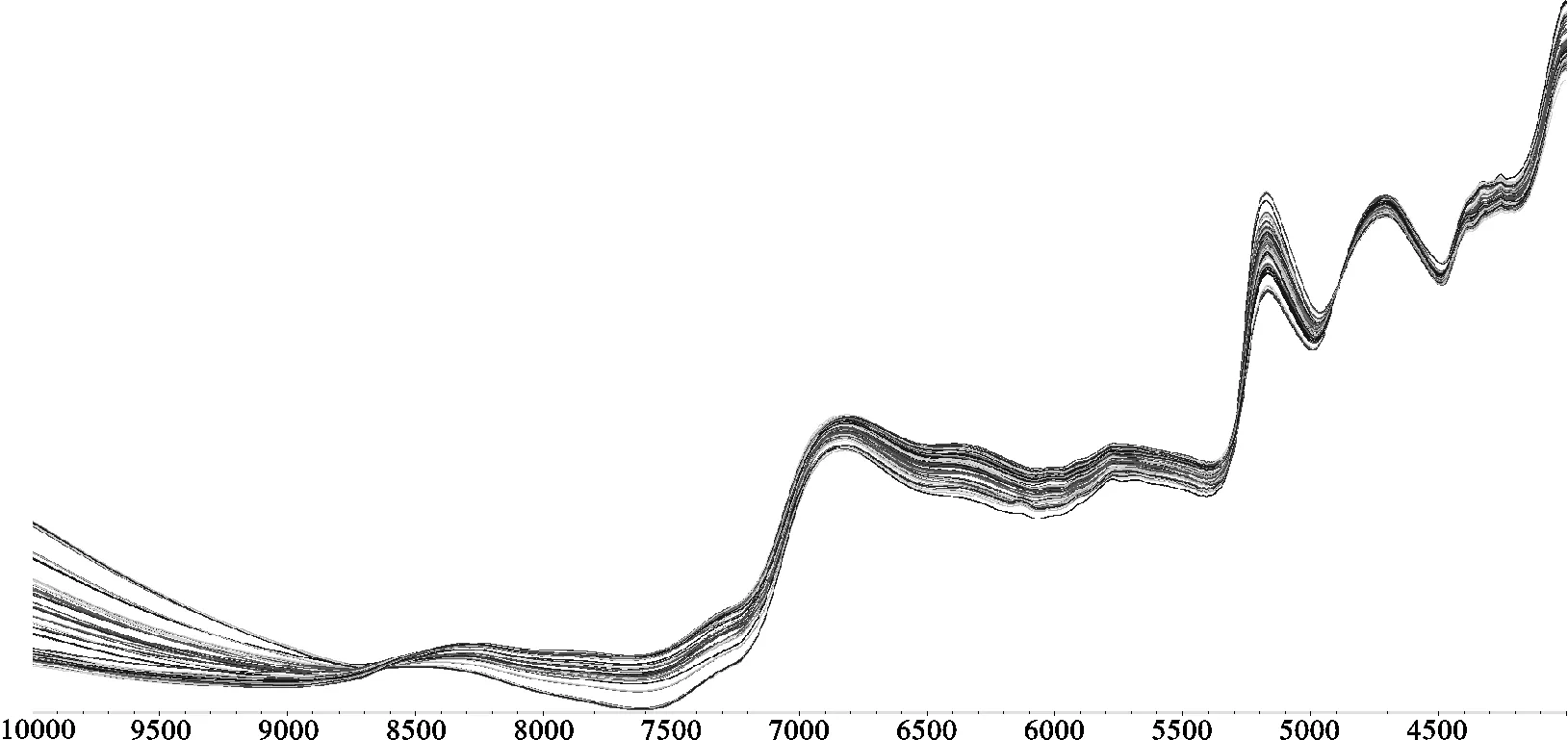
图8 原始光谱
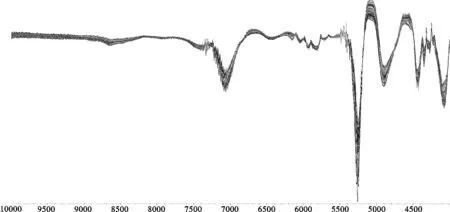
图9 一阶求导光谱

图10 二阶求导光谱

表6 不同光谱预处理方法对性能指数的影响
2.3.3 判别分析结果 山茱萸判别分析结果见图11。由图11可知,山茱萸生品与制品有着明显区分,模型区分度良好。相对来说,生品聚集的范围较小,而制品较为分散,证明了生品与制品存在差异,而生品内部差异不明显,制品内部差异较大。
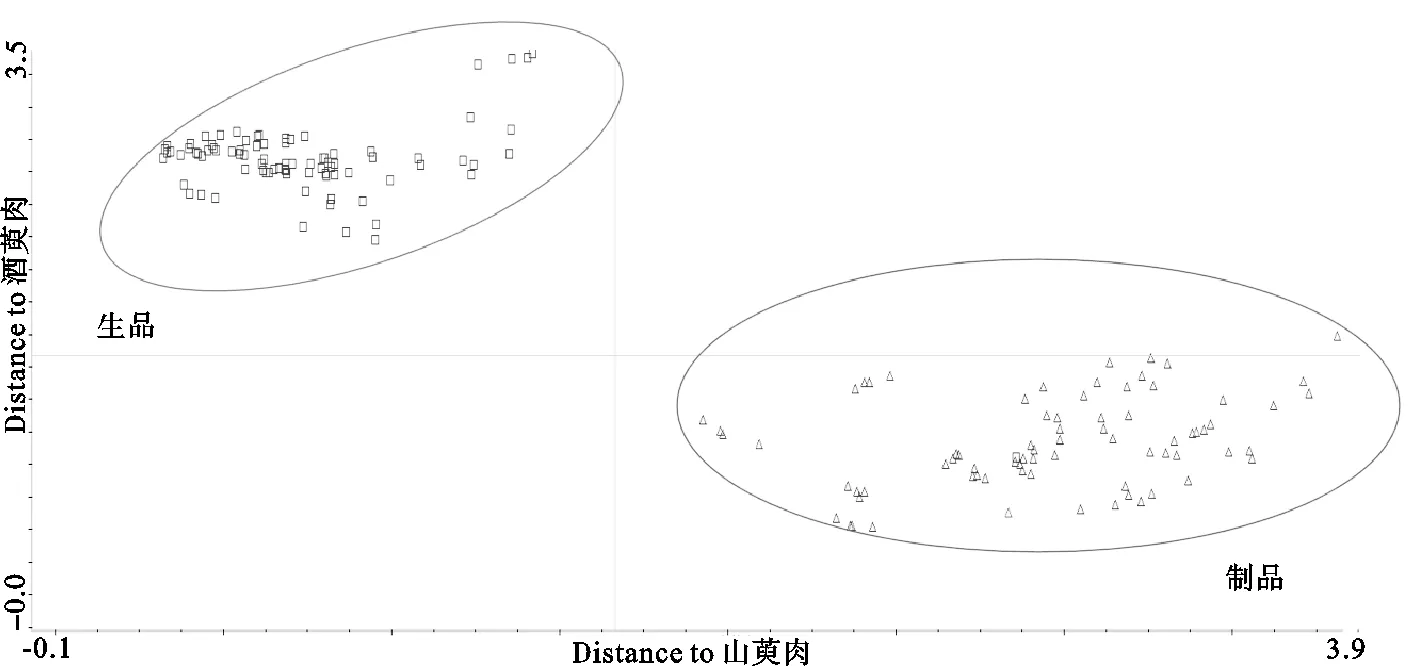
图11 山茱萸近红外判别分析
3 讨论
(1)本研究对HPLC指纹图谱提取时间、柱温和梯度洗脱条件进行了优化。在相同条件下,提取30 min和提取60 min所得到的色谱图无明显差异,因此选择30 min作为最终提取时间;对30 ℃柱温和35 ℃柱温进行考察发现,柱温维持35 ℃时的分离度相对更好,獐牙菜苷和马钱苷更能加以区分;对供试品溶液进行全梯度洗脱时发现,山茱萸色谱峰的出峰时间比较靠前,相对应的流动相极性较大,因此对流动相梯度进行优化,选择极性较大的梯度进行洗脱,节省了乙腈的用量。本研究得到的HPLC指纹图谱方法与前期研究方法相比,缩短了样品提取时间,减少了乙腈使用量,提高了色谱峰的分离度。通过对已知色谱峰峰面积进行聚类分析和主成分分析,即可将样品区分为生品和制品。运用近红外光谱技术,将采集到的近红外光谱图进行判别分析,通过不断优化谱段范围以及预处理方法,最终得到的判别模型区分度良好,性质稳定,能将生品聚为1类,制品聚为1类。
(2)本课题组前期通过HPLC-ESI-MS法分析发现,山茱萸经过炮制后增加了5-羟甲基糠醛这一化学成分[12],通过对比山茱萸生品和制品的HPLC指纹图谱,也可表明经过炮制后的山茱萸新增了5-羟甲基糠醛这一化学成分,基于此,本课题组又对炮制过程的样品进行实验发现,随着炮制时间延长,5-HMF含量从无到有逐渐增加,增加到一定值逐渐趋于平缓。5-HMF是美拉德反应的副产物,是由葡萄糖或果糖脱水生成的化合物,结合前期研究,山茱萸制品的多糖含量相对于生品有所降低[13],由此推测,在炮制过程中,山茱萸多糖水解转化为单糖,单糖进一步脱水生成5-HMF。而5-HMF具有肾毒性[14-15],研究表明,5-HMF对小鼠ICR急性毒性半数致死量(LD50)为871.12 mg·kg-1,按照化学物质毒性分级标准,5-HMF为3级毒性物质[14],因此5-HMF有必要成为山茱萸炮制程度的一个重要指标。对其他成分进行含量比较发现,经过蒸制的山茱萸不论是清蒸还是酒蒸,莫诺苷和马钱苷的含量均显著下降,獐牙菜苷的含量略微增加,而没食子酸的含量显著升高[7-8]。而加酒蒸制和不加酒蒸制对山茱萸的影响还需进一步探究。
(3)本研究建立的HPLC和NIRS指纹图谱联用,并结合多元统计分析山茱萸质量的方法,能从色谱、光谱以及数理统计上较系统地将山茱萸分为生品和制品两类,为整体评价山茱萸质量提供了一种简便方法。基于此,本课题将继续收集样品,并结合已知成分的含量,建立更加客观、便捷的定量分析方法,为山茱萸质量评价及临床用药提供更加科学的参考。
