静态调强放疗与容积调强放疗对宫颈癌术后患者的疗效及剂量学比较
2022-12-23柯瑞全陈崇煌林布雷
柯瑞全 陈崇煌 林布雷
厦门大学附属第一医院肿瘤放疗科,福建省厦门市 361003
宫颈癌是女性生殖系统最常见的恶性肿瘤,其发病率和死亡率较高,且呈现年轻化的趋势[1]。世界卫生组织发布,2018年宫颈癌全球新发和死亡病例分别为56.9万和31.1万[2]。宫颈癌的治疗手段有手术治疗、放射治疗(放疗)、化学治疗(化疗)等,早期宫颈癌患者术后放疗可提高其治疗效果、降低局部复发率和死亡率[3]。静态调强放疗(IMRT)是较成熟的放疗技术,其可根据不同靶区及危及器官(OAR)的不同按一定要求进行剂量调节,在保证靶区照射剂量的同时降低危及器官受量。容积调强放疗(VMAT)是在IMRT基础上发展起来的新型调强技术,其可在360°任何角度对肿瘤进行旋转照射,其照射时间更短,剂量输出效率更高。在以往的报道中,VMAT的剂量学优势得到证实[4],但其在宫颈癌术后的研究较少。基于此,本文主要观察IMRT和VMAT在治疗宫颈癌的剂量学差异,并探讨其疗效。现报道如下。
1 资料与方法
1.1 一般资料 选取2019年8月—2021年7月我院放疗科收治已行手术切除的宫颈癌患者70例作为观察对象。纳入标准:(1)术后病理学确诊为宫颈癌;(2)符合放疗的标准并首次进行放疗;(3)卡氏评分(KPS)[5]>70;(4)无远处转移;(5)年龄>18岁。排除标准:(1)国际妇产科联盟(FIGO)[6]Ⅱb期以上宫颈癌;(2)既往有宫颈手术史;(3)严重的心、肝、肾功能障碍。按照放疗技术的不同分为对照组和观察组,每组35例。对照组年龄33~72岁,平均年龄(56.47±11.23)岁;病理分型:鳞癌30例,腺癌3例,其他2例;FIGO分期:Ⅰa期15例,Ⅰb期12例,Ⅱa期8例。观察组年龄32~74岁,平均年龄(57.13±11.46)岁;病理分型:鳞癌29例,腺癌3例,其他3例;FIGO分期:Ⅰa期14例,Ⅰb期14例,Ⅱa期7例。两组一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经医院伦理委员会审批,所有观察对象均签署知情同意书。
1.2 放疗方法 所有患者均采用Eclipse 15.6设计放疗计划。放疗前采取常规CT扫描,扫描后医生勾画临床靶体积(CTV),在CTV三维方向向上外扩0.6~0.8cm形成计划靶体积(PTV),PTV上下缘外2cm勾画小肠、膀胱、左右股骨头、骨髓等正常组织。对照组实施IMRT,采用Varian Unique直线加速器实施9野固定野动态增强技术。观察组实施VMAT,采用双弧适形技术,于181°~179°及179°~181°方向各拉一个弧。所有患者均采取统一的优化目标和约束条件,采用6MV-X射线,处方剂量为DT 50.0Gy/25fx。5次/周,1次/d,治疗5周。
1.3 观察指标 (1)不良反应:包含白细胞减少、血小板减少、放射性膀胱炎、消化道反应、放射性肠炎。(2)疗效:根据世界卫生组织实体瘤评价标准[7]分为:完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD),总有效率=(CR+PR)/总例数×100%。(3)靶区剂量学比较:利用PTV与OAR的剂量-体积直方图评价两组靶区照射剂量和危及器官照射剂量。指标包含:近似最大剂量D2%、近似最小剂量D98%、平均剂量Dmean、靶区适形性指数CI(越高说明靶区适应性越好,CI=1时表明适应性最好)和均匀性指数HI(HI越大表明PTV内部剂量分布越不均匀)。(4)危及器官照射剂量,指标包含:Dmean、40Gy的受照体积V40、近似最大剂量D2%。
2 结果
2.1 不良反应 观察组总不良反应发生率低于对照组(P<0.05)。见表1 。
2.2 疗效 两组CR、PR、SD、PD及总有效率差异无统计学意义(P<0.05)。见表2。
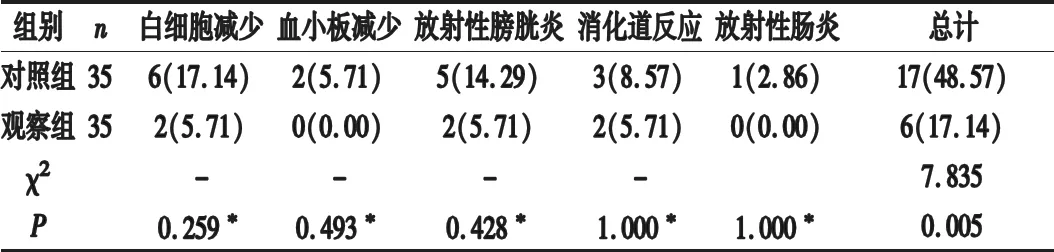
表1 两组不良反应发生率比较[n(%)]
2.3 靶区剂量学比较 观察组D2%、Dmean及CI明显高于对照组(P<0.05),且D98%及HI明显低于对照组。见表3。

表2 两组疗效比较[n(%)]
2.4 危及器官受量比较 观察组膀胱Dmean、左右股骨头Dmean及直肠D2%剂量明显低于对照组(P<0.05),而膀胱D2%、小肠D2%高于对照组(P<0.05)。见表4。
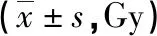
表3 两组靶区剂量学比较
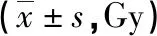
表4 两组危及器官受量比较
3 讨论
放疗是宫颈癌术后重要的治疗手段,其在降低局部复发率的同时还可提高总生存率。有数据表明[8],宫颈癌术后有73.12%的患者采取后续放射治疗。由于宫颈癌靶区不规则,易导致周围正常组织放射性损伤。因此,宫颈癌术后在不影响照射靶区剂量的同时应最大限度地控制周围正常组织的射线受量,降低放射性损伤。随着精准放疗的发展,IMRT成为宫颈癌术后主要放疗手段,其将处方剂量与靶区形状适应,在保证靶区高剂量照射的同时降低了危及器官的受量,降低了不良反应。而VMAT相对于IMRT其照射时间更短,能有效避开在肿瘤中间或凹陷处器官受量,进一步降低周围正常组织损伤率,减少治疗后不良反应[9]。
本文结果显示,观察组总不良反应发生率低于对照组。可见,在宫颈癌放疗中,VMAT相较于IMRT对周围正常组织损伤更小。VMAT本质上是调强放疗的一种,但其在治疗过程中直线加速器机架、多叶光栏MLC在旋转、运动,剂量率也随之变化,大大缩短了照射时间,从而减少了危及器官照射时间,使患者的舒适度提高[10]。同时,VMAT也减少了机器跳数,从而减少了散射线和漏射线对患者的作用。因此,使用VMAT技术其靶区剂量分布更均匀,危及器官受量更小,更好地保护了正常组织,降低了不良反应发生率。本文结果显示,两组总有效率比较差异无统计学意义。可见,两组放疗技术治疗效果相当,均有较好的治疗效果。IMRT和VMAT是在3D适形放疗基础上发展起来的精准放疗,两者均有较好的肿瘤靶区剂量分布,能够保证宫颈癌术后肿瘤靶区足够的放疗剂量,使用不同的放疗技术其处方剂量均为50.0Gy,95%的剂量曲线均覆盖了肿瘤靶区,因此其临床疗效并无统计学意义。
本文结果显示,观察组D2%、Dmean及CI明显高于对照组,且D98%及HI明显低于对照组。可见,VMAT技术较IMRT有更高的靶区照射剂量。VMAT是在常规调强放疗基础上发展起来的新型放疗技术,其可在360°对肿瘤靶区进行旋转照射,其通过高速运动的多叶光栏、直线加速器机架等实现动态、可变的剂量率。通过VMAT不仅大大提高了照射时间,将IMRT的15~30min,缩短至2~6min,而且提高了治疗靶区治疗强度和使用效率[11]。照射时间缩短,相应地危及器官的照射剂量减少。且VMAT适形性更高,靶区外剂量梯度大,明显降低了危及器官照射剂量,从而降低了不良反应发生率[12]。结果还显示,观察组膀胱Dmean、左右股骨头Dmean及直肠D2%剂量明显低于对照组,而膀胱D2%、小肠D2%高于对照组。也有研究指出,VMAT技术剂量分布优于IMRT,不仅其靶区剂量分布更均匀,且对正常组织保护更好,因此其治疗效果会更好,放疗副反应更小。此与本文结果一致。
综上所述,宫颈癌术后IMRT和VMAT均有较好的临床治疗效果,但VMAT剂量分布更优,适形性更好,在保证肿瘤靶区照射剂量强度的同时能更好地减少周围正常组织受量,从而降低不良反应发生率。
