芒果叶碳量子点的制备及其荧光性能研究
2022-12-22覃姣兰王玉椒李秀林林莉瞻
张 超,袁 涛,覃姣兰,王玉椒,李秀林,林莉瞻
(广西高校桂西区域生态环境分析和污染控制重点实验室,广西芒果生物学重点实验室,百色学院化学与环境工程学院,广西 百色 533000)
碳量子点(CQDs)是一种粒子尺寸在10nm以下、单分散、近乎类椭球型的一种碳纳米材料,在金属离子识别与检测、pH值检测、生物成像、光致发光、光电转换等领域的应用广泛,具有较好的应用前景。制备碳量子点的原料来源广泛,成本低,碳水化合物、蜡烛灰、炭黑、生物基质等均能被用作碳源。以草莓为碳源,在180℃下反应12h制备的尺寸为5.2 nm左右的蓝色荧光碳量子点(CQDs),量子产率为6.3%。该碳量子点对Hg2+响应敏感,可以检测痕量Hg2+,检测限为 3nmol・L-1[1]。刘文[2]采用水热反应法,用心里美萝卜合成了一种蓝色荧光碳量子点,直径为1.2~6 nm,量子产率为13.6%,对 Fe3+的检测限是 0.13μmol・L-1。穆海峰课题组[3]以紫甘蓝素为合成原料,硼氢化钠溶液为氧化还原剂,采用水热合成法合成了碳量子点ZGLCQDs。该碳量子点在水溶液中对Cu2+的测定浓度范围约为 0.6×10-6~2.60×10-6mol・L-1,检出限为3.16×10-7mol・L-1。此外,菠菜[4]、香菇[5]、废茶叶[6]、木质素[7]、枫叶[8]、烟灰[9]等也可作为碳源,合成的碳量子点在金属离子检测及成像方面具有突出的应用。
百色是芒果之乡,为此,我们以芒果叶为原料,采用水热法合成了芒果叶荧光碳量子点,研究其荧光性能,并研究其对各种金属离子的响应程度,以寻找一种可用于检测金属离子的高效、灵敏且环保的荧光探针。
1 实验部分
1.1 材料、试剂与设备
芒果叶洗净、烘干至恒重,粉碎,过筛,得到芒果树叶粉末,备用。实验中的无机盐及有机试剂均为分析纯。
YB-600A型高速粉碎机,F-7000型荧光分光光度计,TDZ5-WS型离心机,JA5003B型电子分析天平。
1.2 碳量子点的制备
1.2.1 芒果叶碳量子点(MG/CQDs)的制备
称量0.1 g芒果叶粉末装入聚四氯乙烯内胆中,加10mL超纯水,放入反应釜不锈钢套,置于200℃烘箱中反应5h,取出冷却至室温后,过0.22μm滤膜,得到棕色上清液。将上清液通过透析袋(分子截留量为1000Da),透析2~3d,获得MG/CQDs水溶液,4℃下避光保存,备用。
1.2.2 氮掺杂芒果叶碳量子点(MG/N-CQDs)的制备
称量芒果叶/尿素含量分别为0.1g/0.1g、0.1/0.2g、0.2g/0.1g的3份样品,加入10mL超纯水,按照MG/CQDs的制备方法,制备相应的碳量子点。用荧光分光光度计对3个不同原料的碳量子点进行测定,发现按1∶2比例制备的碳量子点的荧光强度最高,后续实验按此比例进行。该量子点命名为MG/N-CQDs。
1.3 MG-CQDs/MG/N-CQDs的荧光性能实验
1.3.1 激发波长的选择
取MG-CQDs原溶液稀释103倍,分别以290、295、300、305、310nm 为激发波长,测定其发射光谱。取相同体积的MG/N-CQDs原溶液稀释104倍,分别以 300、305、310、320nm 为激发波长,测定其发射光谱。根据发射光谱与激发光谱的强度及对称性,确定碳量子点的最佳激发波长。MG-CQD水溶液的最佳激发波长为300 nm,MG/N-CQDs水溶液的最佳激发波长为305 nm。后续MG-CQD和MG/N-CQDs的荧光性能实验,均在该激发波长下进行。
1.3.2 pH值的影响
分别取5mL稀释后的MG-CQDs溶液至12只10mL的比色管中,参考文献[10],用0.1mol・L-1盐酸溶液、0.01mol・L-1PBS缓冲溶液、0.01mol・L-1Tris-HCI缓冲溶液和0.1mol・L-1NaOH溶液,在1.0~12.0范围内调节pH,定容,用荧光分光光度计测定不同的pH对MG-CQDs/MG/N-CQDs荧光强度的影响。
1.3.3 抗盐性实验
在7只10 mL的比色管中,分别取5 mL稀释104倍的MG-CQDs和MG/N-CQDs溶液,再加NaCl溶液定容至10 mL,使得最终NaCl浓度分别为0、0.25、0.50、0.75、1.25、2.00、2.50mol・L-1,测定各样品的荧光强度。
1.3.4 抗光漂白性实验
将稀释104倍的MG-CQDs和MG/N-CQDs原溶液,置于365nm的紫外光下分别照射0、10、20、30、40、50、60、70 min 后,测定其荧光强度。稀释 104倍的MG-CQDs和MG/N-CQDs原溶液放置0d、7d、14d、25d、32d 后,测定其荧光强度。
1.4 不同金属离子对碳量子点荧光的影响
取5mL稀释104倍的MG-CQDs和MG/N-CQDs原溶液至9支10mL的比色管中,分别加5 mL 浓度为 2.5μM 的 Cr2+、Cd2+、Cu2+、Ni2+、Co2+、Ba2+、Mn2+、Fe2+、Pb2+的水溶液,混合均匀后,测定其荧光强度。
2 结果与讨论
2.1 MG-CQDs/MG/N-CQDs的光学特性
图1为稀释103倍后的MG-CQDs和稀释104倍后的MG/N-CQDs溶液,在不同激发波长下的荧光发射光谱。激发波长为290~310nm时,MGCQDs溶液的荧光强度逐渐降低;激发波长为300nm时,在410nm处有最大荧光发射(I=9466),因此选择300nm为MG-CQDs的激发波长。激发波长在300~320nm变化时,MG/N-CQDs的荧光发射光谱向右移动,且荧光强度下降;激发波长为305nm时,在400nm处的荧光强度最大(I=5328),且用发射波长400nm反扫激发波长,在305nm处有一强激发峰,因此选择305nm为MG/N-CQDs的激发波长。

图1 不同激发波长下MG-CQDs和MG/N-CQDs的荧光发射光谱图
2.2 溶液pH对碳量子点荧光的影响
图2是在pH为1~12的溶液中,MG-CQDs和MG/N-CQDs分别在波长300nm和波长305nm下激发时,在410nm和400nm处的荧光强度。由图可知,MG-CQDs的荧光强度在pH=1~10区间基本不变,在pH=10~12区间,荧光强度稍有增加,但不明显。MG/N-CQDs的荧光强度在一定程度上受到酸碱度的影响。pH<3时,MG/N-CQDs的荧光强度的下降较为明显,从4000a.u下降到3250a.u;pH=6~8时,MG/N-CQDs的荧光强度的变化幅度较小;pH=9~12时,MG/N-CQDs的荧光强度的增幅较大,从3650 a.u升高到4248 a.u。

图2 MG-CQDs和MG/N-CQDs在不同pH值下的荧光强度
可见,在极强酸和强碱性条件下,MG/N-CQDs的荧光强度不稳定,其变化原理可能与MG/N-CQDs表面的基团有关。掺氮量子点表面往往存在大量的羧基和氨基基团,在强酸性和强碱条件下,CQDs表面可能发生质子化和去质子化作用,从而引起该分子中的表面电荷含量发生变化[11]。
2.3 MG-CQDs和MG/N-CQDs的抗盐性
研究表明,离子强度对纳米材料具有较大影响。图3是不同的NaCl浓度对MG-CQDs和MG/N-CQDs荧光强度的影响。随着NaCl的浓度增加,MG-CQDs的荧光强度几乎没有变化,说明离子强度对MG-CQDs的影响较小;而MG-CQDs的荧光强度随着NaCl的浓度增加发生了小幅度的波动,但总体变化不大,说明MG-CQDs和MG/N-CQDs具有良好的抗盐能力,有利于其在生化分析领域的应用,特别是合成的绿色荧光CQDs可作为荧光探针,应用于痕量分析。
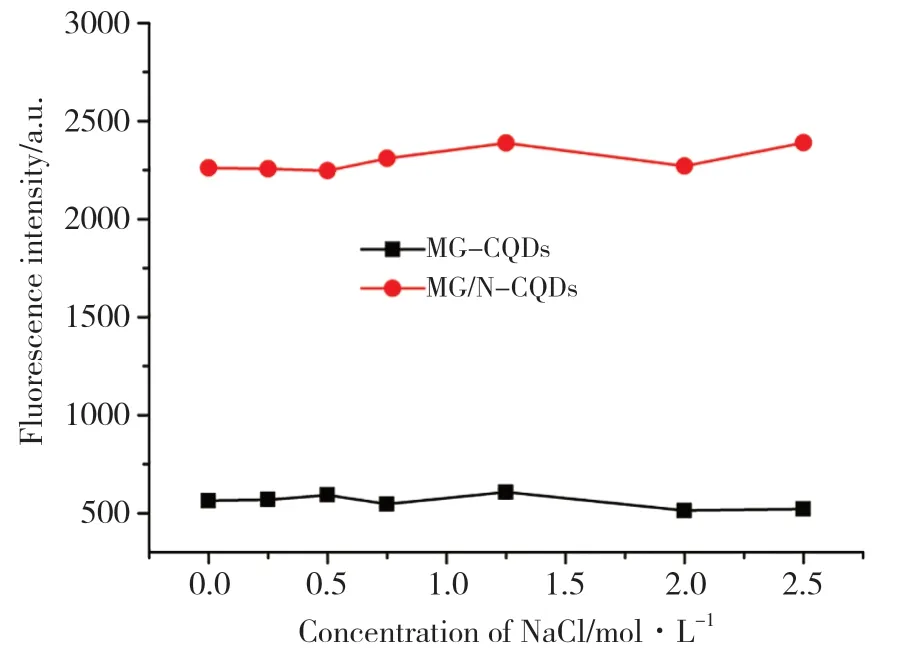
图3 不同浓度的NaCl对MG-CQDs和MG/N-CQDs荧光强度的影响
2.4 MG-CQDs和MG/N-CQDs的抗光漂白性
为了考察MG-CQDs和MG/N-CQDs的光学稳定性,将其水溶液置于365nm紫外灯下照射70min,结果见图4。MG-CQDs的荧光强度不受紫外光的影响,说明MG-CQDs具有良好的抗光漂白性。而MG/N-CQDs的荧光强度随着紫外光照射时间的增加,出现了较明显的下降,光照70min后,荧光强度从3865a.u降到2768a.u,可见光照对MG/N-CQDs的荧光具有猝灭作用。
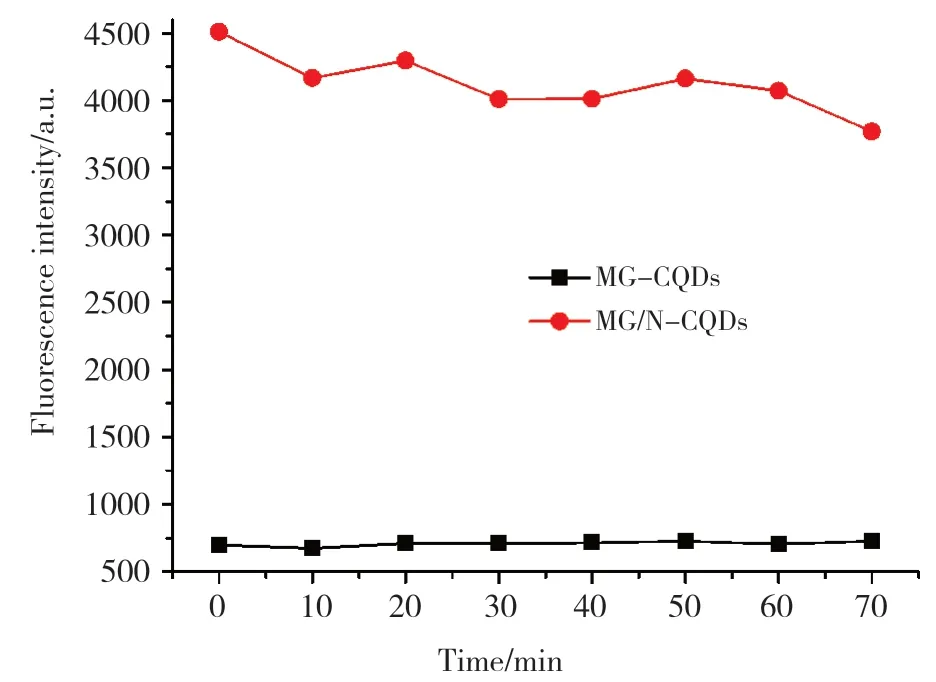
图4 紫外灯照射对MG-CQDs和MG/N-CQDs荧光强度的影响
同时将2份量子点溶液放在5℃的冰箱保存1个月,每隔一段时间测1次荧光强度,结果见图5。与紫外灯照射的结果一样,MG-CQDs的荧光强度几乎没有变化,而MG/N-CQDs的荧光强度随着时间的推移而逐渐下降,从3890a.u降到2669a.u。这一结果进一步说明MG-CQDs具有抗光性,而MG/N-CQDs对光不稳定。

图5 放置时间对MG-CQDs和MG/N-CQDs荧光强度的影响
2.3 MG-CQDs和MG/N-CQDs对不同离子的选择性
碳量子点探针对金属离子具有较好的灵敏性和选择性,近年来关于生物基碳量子点用于检测金属离子的报道层出不穷。图6是浓度为2.5μM的金属离子对MG-CQDs和MG/N-CQDs荧光强度的影响,图中的F0为未加入金属离子时碳量子点的荧光强度,F为加入金属离子后碳量子点的荧光强度。由图6可见,金属离子对MG/N-CQDs的荧光猝灭比 MG-CQDs强,其中 Cu2+对 MG/N-CQDs的猝灭作用最大,加入2.5μM的Cu2+后,MG/N-CQDs的荧光强度从F0= 3760下降到F= 774.7,可见MG/N-CQDs对Cu2+具有较敏感的选择性。

图6 MG-CQDs和MG/N-CQDs对不同金属离子的荧光响应
考察了不同浓度的Cu2+对MG/N-CQDs溶液的荧光强度的影响,结果见图7。加入2μL、2.5μM的Cu2+后,MG/N-CQDs的荧光强度显著下降,从3076a.u降到936.9a.u,荧光猝灭达69.5%,之后随着Cu2+的浓度增加,荧光强度缓慢下降,但总体上不呈线性关系。可见MG/N-CQDs对Cu2+具有较好的选择性,但不具备线性关系,只能进行定性分析。

图7 不同浓度的Cu2+对MG/N-CQDs荧光的响应图谱
3 结论
本文以芒果叶为碳源,尿素为氮源,采用一步水热法制备了具有荧光性能的芒果叶碳量子点(MG/CQDs)和掺氮芒果叶碳量子点(MG/N-CQDs)。相同浓度下,MG/N-CQDs的荧光强度比MG/CQDs高;MG-CQDs和MG/N-CQDs都具有良好的抗盐能力;MG-CQDs的pH耐受性和抗光漂白性强于MG/N-CQDs。在对金属离子的识别分析中,MG/N-CQDs对Cu2+表现出特异选择性,具有开发成检测Cu2+的荧光探针的潜力。
