极早产儿与极低出生体重儿输血治疗的高危因素
2022-12-20邓丽平王彦蕊李海英
邓丽平 王彦蕊 李海英
菏泽市立医院新生儿重症监护室 山东 菏泽 274000
极早产儿与极低出生体重儿因脏器发育不成熟及出生体质量低,容易出现多种并发症,贫血是早产儿常见的疾病之一。输血是早产儿贫血的有效治疗方法,但输血能增加感染、过敏反应、循环负荷过重等不良反应,而且早产儿输血与脑室内出血[1]、支气管肺发育不良[2]、早产儿视网膜病变[3]和坏死性小肠结肠炎[4]有一定关系。本研究回顾性分析我院收治的极早产儿与极低出生体重儿的输血资料,探究输血治疗的高危因素,为临床治疗减少输血从而减少输血相关不良反应提供依据。
1 对象与方法
1.1 研究对象 回顾性分析2019年1月—2020年12月我院新生儿重症监护室收治的极早产儿或极低出生体重儿为研究对象。纳入标准:我院产科分娩或外院转入的早产儿,生后24 h内入院;出生胎龄<32周或出生体质量<1 500 g;治疗好转出院。排除标准:放弃治疗或转院;母亲有胎盘早剥、孕期严重贫血,出生24 h内贫血者;存在急性失血、同族免疫性溶血、非同族免疫性溶血及其他血液系统疾病者。
1.2 研究方法
1.2.1 输血资料收集 2019年1月—2020年12月期间我院新生儿重症监护室共收治1 278例新生儿,极早产儿或极低出生体重儿185例,符合入组标准的患儿117例,根据住院期间是否输注红细胞分为输血组和未输血组。通过院内病历系统回顾性收集患儿一般情况、围产期资料及住院治疗措施、患病情况、输血相关资料,该研究已取得家属知情同意。
1.2.2 输血指征 患儿输血均采用去白悬浮红细胞,输血指征参考《实用新生儿学》的早产儿输血指征和输血方法,每次输血15~20 mL/kg[5]。

2 结果
2.1 一般情况 117例早产儿中,男性患儿60例(51.3%),女性患儿57例(48.7%)。出生时平均胎龄为(31.04±1.57)周,出生时平均体质量为(1 417.99±243.78)g。剖宫产75例(64.1%),自然分娩42例(35.9%),双胎或以上37例(31.6%)。平均住院时间为(35.44±10.22)d,平均住院花费为(4.7±1.8)万元。
117例早产儿中,输血者63例(54.7%),输血时间多在生后2~5周,首次输血日龄平均为(21.56±8.92)d。29例(45.3%)患儿输血1次,18例(28.1%)患儿输血2次,10例(15.6%)患儿输血3次,5例(7.8%)患儿输血4次,2例(3.1%)患儿输血5次。
输血组患儿胎龄、出生体质量、1 min及5 min Apgar评分、入院HCT均低于未输血组P<0.01;输血组入院HGB小于未输血组,P<0.05;失血量多于未输血组,机械通气时间、用氧时间、达全胃肠内营养时间、住院时间、住院花费均大于未输血组,P<0.05。两组患儿性别、分娩方式、是否多胎、产前糖皮质激素应用、母亲妊高症及母亲产前血红蛋白浓度差异无统计学意义。见表1。
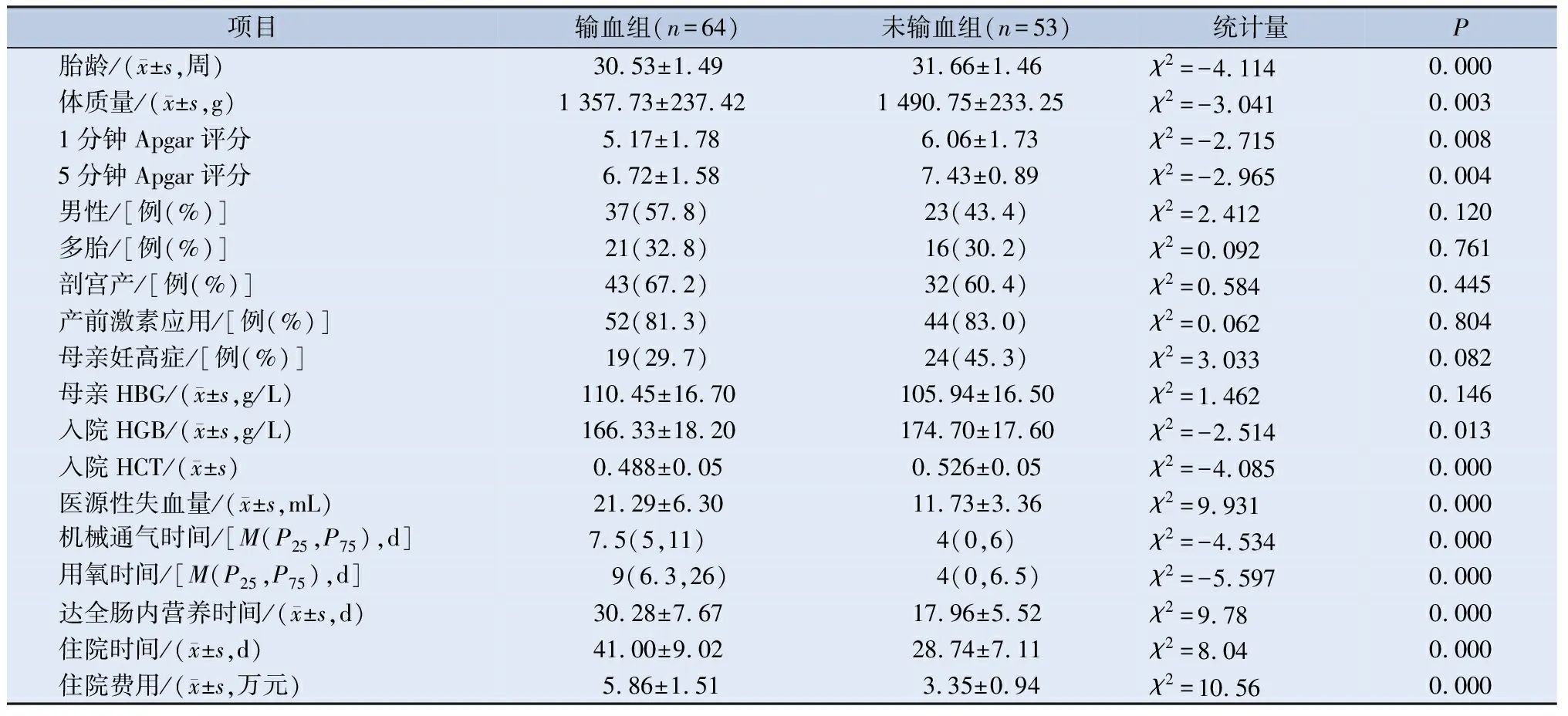
表1 输血组与未输血组基本资料的比较
2.2 临床并发症 输血组新生儿呼吸窘迫综合征、呼吸暂停、支气管肺发育不良、喂养不耐受发生率均高于未输血组,P<0.05。未输血组患儿小于胎龄比例高于输血组,但差异无统计学意义。见表2。
2.3 输血危险因素 以是否输血作为因变量(输血=1,未输血=0),将单因素分析有统计学意义的危险因素及可能的影响因素纳入二元Logistic回归分析,结果显示,失血过多是影响住院期间是否输血治疗的独立危险因素(OR=2.067,P<0.0001);出生体质量高是其保护性因素(OR=0.994,P<0.05)。见表3。

表2 输血组与未输血者并发症的比较/[例(%)]

表3 输血相关因素Logistic回归分析
3 讨论
早产儿红细胞寿命短于足月儿和成人的,仅为35~50 d[6]。新生儿娩出后,由宫内相对缺氧变为宫外相对富氧,以及由胎儿型血红蛋白向成人型血红蛋白转变,期间会有大量红细胞破坏,这是生理性贫血的发生机制。早产儿促红细胞生成素不足,自身营养储备少,全胃肠内营养建立延迟而导致蛋白质、铁、叶酸等营养素缺乏,追赶性生长速度较快,且生后早期呼吸循环不稳定,检验性采血多等不利因素,是导致早产儿贫血不同于足月儿生理性贫血的原因。严重的贫血可引起早产儿组织缺氧、体质量不增、喂养困难,甚至心力衰竭,常需要输注红细胞来提高血红蛋白浓度,从而提升组织携氧能力,改善贫血症状。据报道,高达90%的超低出生体重儿和58%的胎龄小于32周的极早产儿在住院期间接受红细胞输注治疗[7-9]。本项研究发现,输血组患儿胎龄、出生体质量均低于未输血组,多因素Logistic回归分析显示出生体质量高是早产儿输血治疗的保护因素,失血量增多是输血治疗的独立危险因素,同此前Jeon等研究结果相符[10]。本研究发现,输血组患儿失血量为(21.29±6.3)mL,远高于未输血组(11.73±3.36)mL。Widness等[11]研究发现,病情危重的早产儿在生后前6周通常每周丢失11~22 mL/kg血液用于实验室检查,这大约相当于自身15%~30%的循环血容量。Brener等[12]在一项包含了178例极低出生体重儿的研究发现,在采取了减少医源性失血的措施(通过减少血气、血培养、血常规、肝肾功能等检验项目的采血量)后,输血次数和输血量均有明显降低。因此,医源性失血是导致早产儿住院期间输血治疗的主要原因。通过微量采血、床旁检查、减少不必要的实验室检查、采集脐带血进行血型及血培养等实验室检查等措施,可以减少医源性失血,有望减少早产儿输血的几率。
本研究发现,两组患儿性别、分娩方式、是否多胎、是否小于胎龄、母亲妊高症、产前糖皮质激素应用、母亲产前血红蛋白浓度差异无统计学意义。入院时血红蛋白浓度和红细胞压积输血组低于未输血组;生后延迟脐带结扎,新生儿可从胎盘获得额外的血容量,有效提高出生时血红蛋白浓度。Ranjit等[13]研究表明,与生后立即断脐组相比,延迟脐带结扎组早产儿生后1 d的红细胞比容更高,6周时的红细胞比容及血清铁水平也更高。Fogarty等[14]对18项随机对照研究进行了Meta分析,脐带延迟结扎30 s可使红细胞压积增加2.7%,需要输血的早产儿比例减少了10%。因此通过延迟脐带结扎增加胎盘输血,从而提高血红蛋白浓度及压积,减少输血。因考虑到延迟脐带结扎30 s以上可能会导致窒息患儿复苏的延迟,过度胎盘输血增加红细胞数量而引起高胆红素血症加重等风险,截止到此研究结束前我院产科并未常规开展延迟脐带结扎项目。
本研究发现,输血组患儿1 min及5 min Apgar评分均低于未输血组。新生儿产时窒息通常是宫内窘迫的延续,当胎儿宫内缺氧时,胎盘输血减少,窒息抑制骨髓造血功能等因素共同作用,导致患儿贫血加重。输血组患儿住院期间并发症高于未输血组,新生儿呼吸窘迫综合征、呼吸暂停、支气管肺发育不良发生率高于未输血组;呼吸机使用时间、吸氧时间均高于非输血组。胎龄越小,出生体重越低,各脏器系统发育越不成熟,尤其是呼吸系统并发症发生较多。因肺发育不成熟,肺功能低下,为了维持正常的氧合,需要更高的呼吸支持及氧气浓度,同时呼吸支持力度高的患儿也需要相对更高的血红蛋白浓度来提升组织携氧能力。因此,呼吸系统并发症多的患儿输血率较高。有研究发现,输血可能会加重支气管肺发育不良,可能的机制包括氧化损伤的增加或者库存血中的炎症介质导致肺损伤[15]。输血组喂养不耐受发生率高于未输血组,达全胃肠内营养时间比未输血组时间长。因为喂养不耐受及长时间静脉营养,患儿感染等风险增加,发生蛋白质、铁、叶酸、维生素B12、维生素E等营养素缺乏的风险也增高,从而导致贫血程度更重,因而输血的概率也相应增加。因此,如果能减少喂养不耐受,尽早开奶,缩短达全胃肠内营养的时间,可能会减少输血。进而缩短住院时间,减少住院花费,减轻家属和社会的负担。
贫血是早产儿常见的并发症,输血是治疗早产儿贫血的重要方法,但是输血治疗有诸多风险,对早产儿远期神经系统发育的影响亦不明确。巴西一项涉及了16家医院,共纳入4 283例极低出生体重儿的前瞻性研究发现,各家新生儿重症监护室的输血标准并不统一,即使控制了混杂因素后,各中心对输血治疗的影响还在[16]。一项纳入了1 824例超低出生体重儿关于输血阈值对早产儿预后影响的多中心研究发现,在超低出生体重儿这一群体中,采取血红蛋白水平较高的输血阈值,同采取较低的输血阈值相比,并没有改善他们在矫正月龄22~26月时的神经发育结局[17]。
综上所述,在临床工作中,应提高孕产妇保健,减少极早产儿与极低出生体重儿的出生,减少出生后呼吸系统及胃肠道并发症。加强产儿协作,优化窒息复苏流程,减少新生儿产时窒息。
