凝胶材料制备方法及其反应动力学的研究进展*
2022-12-20倪卓莫少妮谢非凡黎智华
倪卓 莫少妮 谢非凡 黎智华
传统的骨修复材料主要有自体骨、异体骨、脱钙骨基质、生物陶瓷和金属材料。自体骨来源有限,异体骨和金属材料等植入材料易发生免疫排斥反应,使伤口愈合时间延长,严重时甚至不愈合。近年来,以天然高分子水凝胶制备生物支架成为研究热点,其模拟人体细胞外基质微环境,负载种子细胞(软骨细胞、骨髓间充质干细胞、成骨细胞)和生长因子,转移至骨组织环境中,诱导干细胞增殖和分化,以促进骨骼生长[1-2]。天然高分子水凝胶是线性高分子通过共价键、氢键、离子键、静电作用或分子间缠绕形成的具有三维网络结构的弹性半固体聚合物,能在水中溶胀而不溶解,具有高吸水性、高保水性和生物稳定性。与合成高分子水凝胶比较,天然高分子水凝胶具有优异的生物相容性、低细胞毒性和生物可降解性等多种优点,适合应用于骨组织工程领域。其中明胶、壳聚糖和海藻酸钠分子链中含有羟基和氨基等活性官能团,具有良好的生物相容性,且可以对其进行改性和功能化,在骨缺损修复和治疗领域具有显著优势。
骨缺损是由于外伤、肿瘤、感染或先天遗传等因素造成骨骼损伤或缺失,针对不同类型的骨缺损,采用不同种类的修复材料治疗不同类型骨缺损尤为重要。本文总结了明胶、壳聚糖和海藻酸钠水凝胶复合材料的制备方法和凝胶反应机理,比较了不同的凝胶反应动力学研究方法,总结其在骨组织修复应用中的研究进展,为凝胶复合材料的分子设计和临床应用提供了思路。
1 凝胶材料制备方法及其凝胶机理
明胶(gelatin)是胶原蛋白的部分水解产物,由18 种不均匀分布的氨基酸组成,分子量为几万至十几万,R1 ~R5 为氨基酸残基(见图1)。明胶分子中含有羟基、羧基和氨基,是两性聚合物。根据制备方法不同,明胶可以分为酸法(A型)明胶、碱法(B型)明胶和酶法明胶,A 型明胶的等电点为7.0 ~9.0,B 型明胶的等电点为4.7 ~5.2。在骨组织修复应用中,明胶没有胶原蛋白出现的蛋白排斥反应,具有低抗原性和生物相容性,是模拟骨组织环境的理想材料。

图1 明胶结构
壳聚糖(chitosan)是甲壳素N-脱乙酰基的产物,壳聚糖的分子结构与甲壳素相似,具有复杂的双螺旋结构(见图2)。壳聚糖分子中含有丰富的氨基与羟基,在分子内和分子间易形成氢键,在酸性介质中溶解,是目前发现的唯一表面带正电荷的天然多糖聚合物,具有生物相容性、可降解性和抗菌性,在骨组织修复工程应用中具有很大的发展潜力。

图2 壳聚糖结构
海藻酸钠(sodium alginate)来源于褐藻类植物,是由β-D-甘露糖醛酸(β-D-mannuronic,M)和α-L-古洛糖醛酸(α-L-guluronic,G)按(1→4)键连接组成的线性阴离子聚合物(见图3)。在海藻酸钠的分子结构中,M单元和G 单元的立体构象不同,以MM、MG、GG 三种配对方式随机交替连接,这两种糖醛酸在分子结构中的比例和排列顺序的变化会导致海藻酸钠性质(粘性、胶凝性和离子选择性)的差异。

图3 海藻酸钠结构
明胶和壳聚糖分子中含有氨基、羟基等活性官能团,海藻酸钠分子中含有羟基、羧基等活性官能团,这些物质来源于动植物,无害无毒,具有良好的生物相容性和可降解性,使用交联剂设计结构制备性能优异的水凝胶材料在骨组织修复工程中具有显著优势。明胶、壳聚糖和海藻酸钠水凝胶复合材料制备方法主要有化学交联法和物理交联法。化学交联法是指线性聚合物在交联剂、热和光等条件作用下形成以共价键连接的三维网络结构聚合物,该过程具有不可逆性。物理交联法主要是通过物理作用(氢键作用、静电作用和范德华力)使线型聚合物形成体型网络结构聚合物,该过程具有热可逆性。
1.1 化学交联法
以化学交联法制备明胶、壳聚糖和海藻酸钠水凝胶复合材料所采用的交联剂可分为共价交联剂和离子交联剂:共价交联剂有戊二醛和生物类化合物(京尼平、茶多酚、阿魏酸和咖啡酸)等;离子交联剂有氯化钙、氯化锌、氯化铜和三聚磷酸钠等。
1.1.1 共价交联
采用戊二醛与含氨基或羟基的明胶和壳聚糖反应制备凝胶材料具有反应速度快和交联程度大的特点。研究发现,戊二醛与含氨基聚合物应受pH和反应物浓度的影响,在较高的pH介质中,交联反应主要由席夫碱反应控制;在较低的pH介质中,戊二醛可能与明胶中羟基脯氨酸和羟基赖氨酸的羟基反应,形成以半缩醛结构为桥联的三维网络结构产物[3]。当反应物浓度较低时,产生分子内交联,醛基与氨基反应形成不稳定的席夫碱结构,进一步反应形成以2, 6-二羟基四氢吡喃聚醚为桥联的三维网络结构聚合物[4](见图4)。虽然戊二醛交联能提高凝胶复合材料的力学性能,但研究发现戊二醛交联剂对负载细胞有一定的毒性,采用浓度超过0.5%的戊二醛与明胶反应制备复合支架时,严重影响支架负载的成骨细胞的生长和增殖[5]。
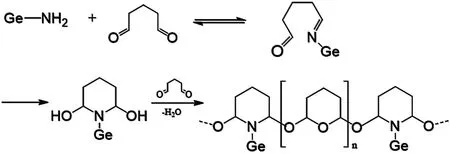
图4 明胶与戊二醛反应
因为醛类交联剂具有细胞毒性,所以采用无毒无害的生物交联剂与明胶、壳聚糖反应制备骨缺损修复凝胶材料成为研究热点,这些天然生物交联剂结构中含有羧基和羟基等官能团,直接或经氧化后与明胶和壳聚糖分子链中的活性基团反应实现交联固化。京尼平是栀子苷经β-葡萄糖苷酶水解后的产物,其细胞毒性低和生物相容性好,与明胶或壳聚糖等含氨基聚合物发生交联反应可以制备组织工程支架[6]。京尼平与含氨基天然高分子反应具有pH 依赖性,在不同pH介质中,京尼平与含氨基天然高分子交联机理不同[7]。在酸性或中性环境中,形成由短链京尼平为交联桥的网状结构聚合物。在碱性介质中,形成以长链京尼平为交联桥的网络结构聚合物。采用京尼平与壳聚糖反应制备骨修复支架,负载人间充质干细胞和成骨细胞进行培养,研究发现京尼平浓度对细胞增殖没有显著影响,材料对细胞的毒性低,促进细胞生长和增殖[8]。
1.1.2 离子交联
海藻酸钠可以与多种二价或三价的金属阳离子反应形成水凝胶,如Ca2+、Zn2+、Cu2+、Cd2+等。海藻酸钠与二价金属离子凝胶化形成“蛋盒模型”(Egg-model),分子中的两个G 段与多个Ca2+离子发生螯合作用,Ca2+离子被海藻酸钠分子夹在中间,由于钙离子诱导链-链缔合作用,形成类似蛋盒的结构[9](见图5)。通过海藻酸钠与金属离子螯合反应制备的水凝胶支架具有多孔结构,是骨修复工程体外细胞培养的良好载体。目前,软骨细胞单层培养去分化是骨组织工程应用中的难题,采用海藻酸盐可以保持软骨细胞形态稳定,使去分化的软骨细胞重新表达,对于软骨组织的构建具有重要意义[10]。

图5 海藻酸钠与氯化钙反应
壳聚糖和明胶分子中含有大量的羟基、氨基和部分酰胺基,可以与二价金属离子(Ca2+、Mg2+、Co2+)发生配位反应形成水凝胶材料。通过制备含铜羧甲基壳聚糖/海藻酸钠复合支架,负载成骨细胞,发现铜离子具有很强的抗菌性,在体内能够有效抑制金黄色葡萄球菌的生长,在修复感染性骨缺损中具有重要意义[11]。
1.2 物理交联法
物理交联法制备水凝胶材料主要是通过物理作用(氢键作用、静电作用和范德华力)使线性聚合物形成体型网络结构的凝胶材料。通过物理方法制备的水凝胶具有热可逆性,加热时凝胶转变为溶液。
1.2.1 氢键作用
氢键交联制备水凝胶通过分子间或分子内的氢键将线性高分子交联形成凝胶材料。明胶凝胶具有溶胶-凝胶转化的可逆性,明胶溶液的温度降低,明胶多肽链被诱导形成反应位点,与相邻的多肽链形成氢键交联,复合为类似胶原的右手超螺旋结构,形成一个交联点,得到具有三维网状结构的明胶凝胶材料,重新加热后,明胶凝胶转化为溶胶。
1.2.2 静电相互作用
通过静电作用制备凝胶材料主要是带有相反电荷聚合物产生静电相互作用使聚合物链发生交联的过程,称为复凝聚或自组装。该过程受反应体系pH、参与复凝聚反应单体的质量比和反应体系温度等因素影响。复凝聚反应以静电相互作用为驱动力,与反应物的带电荷密不可分。因此,影响该过程的关键因素为介质pH。明胶为两性天然高分子,在大于等电点介质中,带负电荷;在小于等电点介质中,带正电荷。在合适pH 介质中,明胶可以与带正电荷聚合物如壳聚糖[12](见图6)制备凝胶复合材料或者与带负电荷聚合物(海藻酸钠、阿拉伯胶)进行复凝聚反应制备凝胶复合支架,其在骨缺损修复中具有重要应用。Gentile等[13]采用明胶与海藻酸钠进行复凝聚反应,以氯化钙为交联剂制备负载生长因子的凝胶材料,结果表明该复合凝胶材料可保持软骨细胞活力,促进细胞增殖,在骨修复中具有显著应用潜力。带正电荷的明胶与带负电荷的海藻酸钠进行复凝聚,制备负载种子细胞的骨修复支架,结果表明与纯壳聚糖支架相比,复合支架具有更高的力学性能和孔隙率,促进细胞黏附、增殖和分化[14]。

图6 明胶与壳聚糖复凝聚反应
2 凝胶反应动力学研究方法
2.1 紫外分光光度法
凝胶材料的反应动力学复杂,可以采用紫外分光光度法研究京尼平交联壳聚糖或明胶反应动力学。京尼平与含氨基聚合物的交联反应为不可逆过程,具有pH依赖性,在紫外吸收光谱中,反应产物在600 nm 波长处存在特征吸收峰,该峰强度随着交联反应时间的增大而增强[15],最终达到平衡。采用紫外分光光度法研究在pH为6.75和10.5条件下乳球蛋白与京尼平的反应动力学[16],建立反应方程=k[β-乳球蛋白]a[Genipin]b,结合Arrhenius方程,得到在pH 为6.75 和10.5 条件下,反应级数分别为0.22 和-0.24,反应活化能为66.2 kJ/mol 和9.40 kJ/mol,表明pH对乳球蛋白与京尼平交联反应具有显著影响。
2.2 流变法
采用“流变动力学”可以表达聚合物反应动力学机理与流变学性能间的关系。根据Flory凝胶化理论,在可逆和不可逆凝胶中,粘度、模量和扭矩等物理量随反应时间增加,对于简单m级不可逆凝胶化过程,凝胶转化率与反应物的初始浓度无关,假设凝胶化过程复合Arrhenius 方程,凝胶时间的倒数与C(m-1)和e(Ea/RT)的乘积成正比,即,tgel为凝胶时间(动力学凝胶化过程中达到凝胶点的时间),C为组分浓度,Ea为反应活化能,m为反应级数。有研究采用流变法研究京尼平与壳聚糖交联反应动力学,结果显示反应活化能为41.26 kJ/mol,反应级数为1.86[17]。京尼平与明胶的交联反应具有温度依赖性,在较高温度下,交联反应符合Arrhenius方程,活化能介于63.2 kJ/mol和67.8 kJ/mol之间[18]。
2.3 其他方法
采用原子吸收光谱可以测定海藻酸钠与氯化钙或氯化锌凝胶过程中钙离子或锌离子浓度变化,以线性模型(LAM)模拟海藻酸钙凝胶与金属离子凝胶反应动力学过程,得到海藻酸钠与氯化钙或氯化锌凝胶反应动力学方程,反应初始速率方程为和LAM 模型假设反应速率或离子交换速率比扩散速率快,建立起反应过程中金属离子浓度与反应时间的关系式通过线型拟合曲线可得到相关动力学参数。原子吸收光谱是以自由金属离子对光的吸收为基础,定量测定化学元素的光谱分析方法,适用于以离子为交联剂的凝胶反应体系。凝胶反应主要是官能团之间的反应,通过红外光谱研究凝胶化过程中特征官能团随时间的变化关系也可以研究凝胶反应动力学过程。
3 凝胶复合生物材料在骨组织修复中的应用
天然高分子水凝胶材料具有三维多孔结构,良好的吸水性、黏弹性和生物相容性,广泛应用于骨组织修复和治疗领域,单一天然高分子凝胶生物支架不能为种子细胞的生长和增殖提供良好的机械性能,常与其他材料复合制备凝胶生物支架用于骨修复和治疗(见表1)。

表1 天然高分子凝胶材料负载细胞用于组织工程
以氯化钙为交联剂制备明胶/海藻酸钠复合水凝胶材料,载入小鼠成软骨前体细胞后,经过培养,细胞存活率仍高达95%[24]。通过低温挤出3D打印法,以辣根过氧化物酶(HRP)为酶交联剂,将丝素蛋白与酪胺改性明胶进行快速交联,制备具有多孔结构的水凝胶支架,植入动物模型12周和16周后进行组织学检查[25]。发现该多孔结构的水凝胶结构稳定,适合软骨组织的再生,与干细胞相结合,在软骨组织修复和再生中具有良好的应用前景。
为了提高负载种子细胞存活率和凝胶复合材料的成骨性能,向负载间充质干细胞的凝胶复合材料中加入生长因子、羟基磷灰石(hydroxyapatite,HA)和骨形态发生蛋白等具有成骨诱导作用的物质,以达到促进骨细胞成骨分化的目的。HA 是骨骼的主要成分,具有良好的生物相容性和骨诱导性,将其与天然高分子复合制备生物支架用于骨修复治疗,结果显示该材料具有良好的机械性能和生物相容性,骨髓间充质干细胞在BG/CS/HA 支架上表现出了明显的增殖[26]。在负载细胞的复合凝胶支架中加入生长因子也显示出促进碱性磷酸酶的表达,增强细胞成骨分化性能,加快骨缺损的修复进程[27-28]。
自愈性水凝胶是一种可实现自我修复的新型智能材料,近年来,采用生物相容性好的天然高分子制备负载种子细胞的自愈性水凝胶成为研究的热点。体内三维环境的变化容易导致凝胶材料中负载的细胞生长状况和形态发生改变,导致细胞存活率低,自愈性水凝胶动态化学键的存在使负载细胞处于动态环境中,促进细胞之间相互接触传递信息和与环境互动,同时注射后的水凝胶在患处实现自愈合将种子细胞固定于患处,有利于抵抗多变的体内环境,使负载种子细胞处于稳定状态,提高种子细胞的存活率,在骨组织修复应用中具有显著优势[29-30]。有研究采用强氧化剂高碘酸钠氧化海藻酸钠制备带醛基的海藻酸,通过氧化海藻酸上的醛基与具有酰肼基的聚乙二醇反应生成可逆共价酰腙键制备水凝胶,研究结果发现该水凝胶不仅具有物理凝胶的凝胶-溶胶性质和pH 敏感性,有望应用于细胞载体[31]。
4 小结与展望
寻找理想的骨修复材料是骨科材料领域的研究热点,理想的骨修复材料应该具有良好的生物相容性、可降解性、良好的力学性能和较高孔隙率、渗透性能等特点。生物类交联剂具有良好的生物相容性和低细胞毒性,有利于种子细胞的黏附、生长和增殖[32]。通过带相反电荷的天然高分子进行自组装或复凝聚,以化学交联法结合物理交联法制备的凝胶复合生物支架为种子细胞的增殖和分化提供了稳定微环境,在颧骨修复和颌骨缺损等骨组织修复和临床治疗具有重要价值。本文总结凝胶反应动力学研究方法和凝胶复合材料在骨修复工程中的应用,对于凝胶生物材料的分子工程设计具有重要意义,为临床应用提供参考。目前,负载种子细胞的天然高分子凝胶载体应用于骨缺损修复治疗仍处于实验室阶段,主要包括有细胞实验、动物实验、力学性能和生物性能评价等,临床研究数据较少。未来研究方向将优化凝胶材料组成和结构,精准模拟骨组织微环境,向临床研究发展,相关技术的发展使天然高分子凝胶材料将在骨组织修复工程领域发挥巨大的作用。
