一种免疫调节肽的小鼠经口急性毒性试验
2022-12-20鲁令华刘晓东杜恒裔王述柏
焉 扬,鲁令华,刘晓东,杜恒裔,邵 坤,王述柏*
(1.青岛农业大学动物医学院,山东青岛 266109;2.青岛农业大学动物科技学院,山东青岛 266109)
生物活性肽是对机体的生命活动有一定生理作用的肽类化合物,相对分子质量小于6 000 D[1-2],其分子结构复杂程度不一[3],是一类介于氨基酸和蛋白质之间的多肽[4]。1902年,英国科学家Bayliss等[5]首次发现了生物活性肽,自此国内外学者对活性肽开展了大量研究[6]。活性肽根据生理功能可分为免疫调节肽、抗菌肽、血压调节肽、神经活性肽、呈味肽等[7-8],其中免疫调节肽因其独特的免疫增强作用备受研究者关注[9-10]。Xu等[11]从中华小公鱼胃蛋白酶产物中筛选出具有免疫调节活性的五肽YVMRF,研究发现这种肽能促进小鼠RAW264.7细胞系分化,增加一氧化氮(NO)、白细胞介素-6、白细胞介素-1和肿瘤坏死因子-α的产量。叶盛旺等[12]从青蛤胃蛋白酶产物中筛选出的活性肽免疫调节活性高,能显著增强小鼠巨噬细胞系RAW264.7的吞噬能力、NO的分泌水平和细胞因子的分泌量。Li等[13]利用木瓜蛋白酶和胰蛋白酶酶解阿拉斯加鳕鱼蛋白得到多肽ACNGR,发现这种肽能提高环磷酰胺诱导小鼠的免疫器官指数,促进脾淋巴细胞的增殖,增加与肠黏膜免疫相关的SIgA、IgA、IL-6、IL-10的分泌,从而增强小鼠肠道黏膜的免疫功能,可见免疫调节肽有望成为动物抗生素类饲用添加剂的替代物。但是,对新型饲用添加剂开展毒理学评价是其推广应用前必不可少的。符大勇等[14]研究了海洋生物表面活性肽(SPR)的急性毒性,试验期间小鼠无任何中毒症状、无死亡,经大体病理学观察发现脏器无异常变化,因此确定SPR对小鼠无毒性。刘泳廷等[15]利用小鼠的急性毒性试验研究野生盔孢伞中鹅膏毒肽的毒性,结果显示小鼠出现不同程度的中毒症状,随鹅膏毒肽剂量的增加肝细胞肿胀、坏死,伴有出血和炎细胞浸润的病变逐渐加重,确定小鼠半数致死量(LD50)为108 mg/kg。笔者以小鼠为实验动物,研究了一种新合成免疫调节肽的急性毒性,旨在为其安全性评价和推广应用提供参考依据。
1 材料与方法
1.1 试验材料免疫调节肽:白色粉末,纯度不低于98.5%,由青岛农业大学预防兽医学研究室制备。小鼠配合饲料及垫料,购自济南朋悦实验动物繁育有限公司。
1.2 实验动物54只体重相近(24~26 g)的清洁级ICR系小鼠,购自济南朋悦实验动物繁育有限公司。
1.3 试验时间和地点试验于2017年5月在青岛农业大学实验动物房和预防兽医学研究室进行。
1.4 试验方法采用急性毒性试验的限量法[16]进行试验设计,将54只小鼠饲养于实验动物房内观察、适应5 d,在此期间自由采食饮水;确认健康无病后,将小鼠随机分为3组(Ⅰ、Ⅱ组为试验组,Ⅲ组为对照组),每组18只(雌雄各半),公母分笼饲养。所有小鼠饲养条件、饮用水、饲料保持一致。实验动物房内室温20~25 ℃,湿度50%~70%,通风良好,并保持卫生清洁。
通过预试期试验获得小鼠适宜灌胃量为0.2 mL/只,根据实测体重计算每只小鼠免疫调节肽的使用量,准确称取待检样品并将其溶于蒸馏水中。试验组Ⅰ和Ⅱ分别灌胃剂量200和400 mg/kg 的免疫调节肽溶液0.2 mL,对照组灌胃等量蒸馏水。灌喂前禁食6 h,只供应饮水,给予受试物后继续禁食2 h。
1.4.1临床观察。试验期间,每天观察小鼠皮肤、被毛、眼、黏膜组织以及呼吸系统、泌尿生殖系统、消化系统和神经系统等组织器官有无异常变化,记录动物发生异常变化的时间、程度以及持续时间,评估可能发生毒性作用的靶器官或组织,精确记录死亡时间和死亡时体重。观察试验期间各组织器官的异常变化,判定依据参见文献[17]。连续观察14 d。
1.4.2生长性能测定。于试验开始当日和试验期末,准确称量试验小鼠体重,每日准确记录加料重、剩料重,计算每日采食量。最后,计算试验期间平均日增重、平均日采食量和料重比。
1.4.3病理学检查。所有小鼠(包括试验过程中死亡小鼠、试验结束时处死小鼠)均进行大体解剖,观察并记录小鼠的肝脏、脾脏、肾脏、心脏、胃、肠、睾丸或卵巢的病理学变化;大体解剖病理改变时,进一步进行病理组织学观察;准确称量各器官重量,计算脏器系数:脏器系数=脏器重量/体重。
1.4.4血液生理学指标检测。
1.4.4.1血样采集。于试验期结束日(第14天),采用摘眼球采血法采集血样,一部分用于检测血常规指标,另一部分离心分离血清,用于检测血清生化指标。
1.4.4.2血常规指标检测。使用全自动流式血细胞计数仪检测,检测指标包括白细胞总数、淋巴细胞比率、中性粒细胞比率、淋巴细胞数目、中性粒细胞数目、红细胞总数、血红蛋白含量、红细胞压积、平均红细胞体积、平均红细胞血红蛋白含量、平均红细胞血红蛋白浓度、红细胞分布宽度变异系数、红细胞分布宽度标准差、血小板总数、平均血小板体积、血小板分布宽度和血小板压积。
1.4.4.3血清生化指标检测。采用全自动生化分析仪和试剂盒检测,检测指标包括血清丙氨酸氨基转移酶活性、天冬氨酸氨基转移酶活性、碱性磷酸酶活性、谷氨酰基转移酶活性以及总蛋白、白蛋白、球蛋白、甘油三酯、胆固醇、尿素、肌酐和葡萄糖含量。试验所用试剂盒均购自北京安普生化科技有限公司。
1.5 数据处理试验数据采用Excel软件初步整理后,使用SPSS 17.0统计软件的单因素方差分析和Duncan法进行组间差异显著性比较。试验结果均以“平均值±标准差”表示。结果分析参考文献[18]的方法。
2 结果与分析
2.1 临床观察结果试验期间各试验组和对照组小鼠的眼部(图1)、鼻孔(图2)、母鼠的乳房(图3)、母鼠的阴部(图4)、公鼠的阴部(图5)以及小鼠的被毛(图6)均未出现异常变化,呈健康状态。

图1 小鼠的眼部变化

图2 小鼠的鼻孔变化

图3 母鼠的乳房变化

图4 母鼠的阴部变化
图5 公鼠的阴部变化

图6 小鼠的被毛变化
2.2 大体解剖病理学检查结果解剖观察各组小鼠的内脏器官(包括胃、肠、肝、脾、肾、心脏、睾丸、卵巢),发现均无临床病理学变化(公鼠见图7,母鼠见图8),呈健康状态。

图7 公鼠的肠、脾、心脏、胃、肾、睾丸和肝
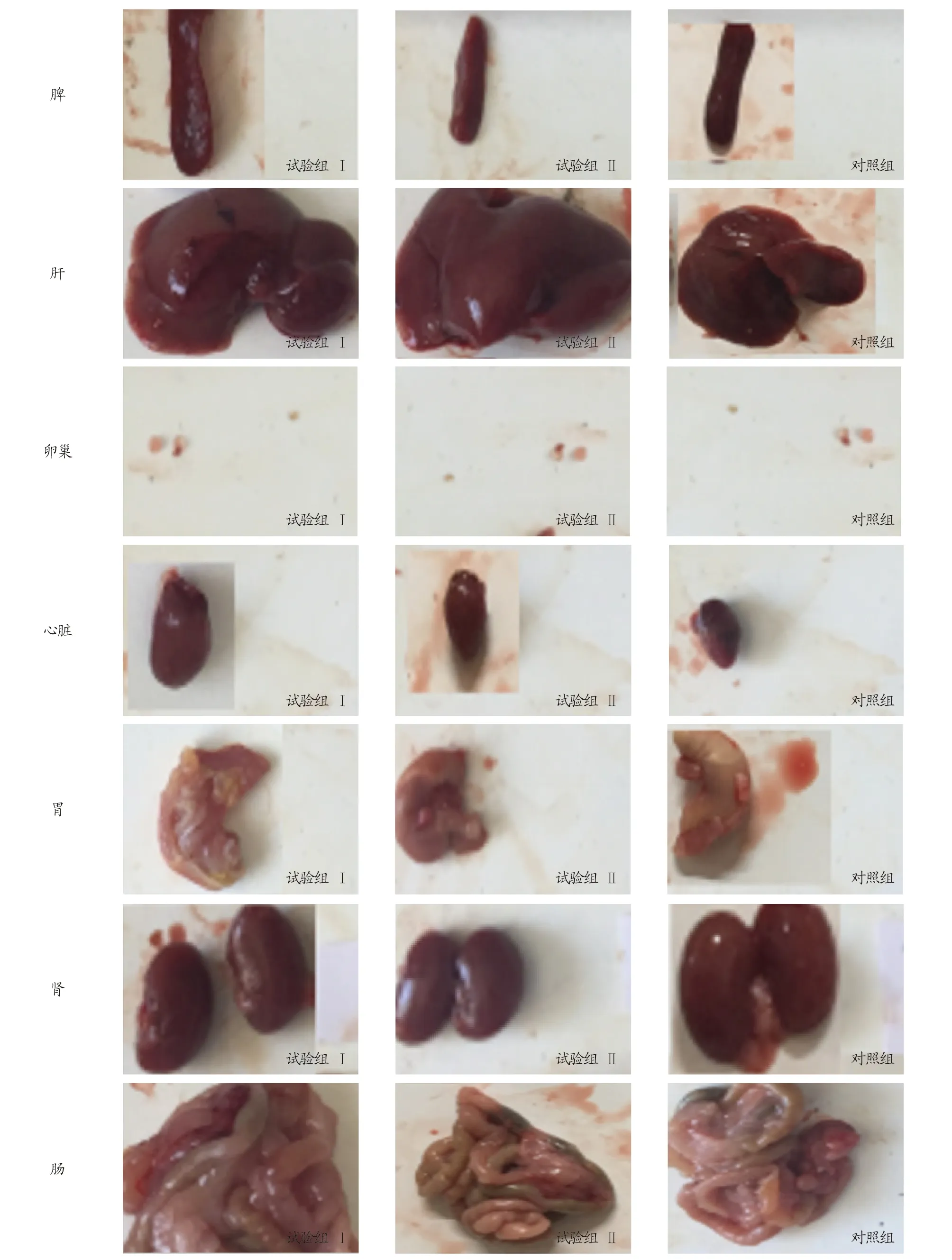
图8 母鼠的脾、肝、卵巢、心脏、胃、肾和肠
2.3 免疫调节肽对小鼠生长性能的影响由表1可知,试验组Ⅱ公鼠末重和平均日增重略高于对照组和试验组 Ⅰ(P>0.05),料重比分别较对照组和试验组 Ⅰ低0.77和0.40,但各组公鼠始重和末重无显著差异(P>0.05),试验期间各组公鼠的平均日采食量和料重比亦无显著差异(P>0.05)。由表2可知,各组母鼠始重无显著差异(P>0.05);试验组Ⅰ、Ⅱ的母鼠末重、平均日增重均显著高于对照组(P<0.05),各组平均日采食量和料重比均无显著差异(P>0.05)。观察期间,各组公鼠和母鼠均无死亡。

表1 各组公鼠生长性能的比较

表2 各组母鼠生长性能的比较
2.4 免疫调节肽对小鼠血常规指标的影响由表3可知,各组小鼠的白细胞总数、淋巴细胞比率、中性粒细胞比率、淋巴细胞数目、中性粒细胞数目、红细胞总数、血红蛋白含量、红细胞压积、平均红细胞体积、平均红细胞血红蛋白含量、平均红细胞血红蛋白浓度、红细胞分布宽度变异系数、红细胞分布宽度标准差、血小板总数、平均血小板体积、血小板分布宽度和血小板压积均无显著差异(P>0.05)。

表3 各组小鼠血常规指标的比较
2.5 免疫调节肽对小鼠血清生化指标的影响由表4可知,各组血清丙氨酸氨基转移酶活性、天冬氨酸氨基转移酶活性、碱性磷酸酶活性和谷氨酰基转移酶活性无显著差异(P>0.05),各组血清总蛋白、白蛋白、球蛋白、甘油三酯、胆固醇、尿素、肌酐和葡萄糖含量均无显著差异(P>0.05)。

表4 各组小鼠血清生化指标的比较

续表4
2.6 免疫调节肽对小鼠脏器系数的影由表5可知,各组公鼠、母鼠的脏器系数(包括肝、脾、肾、心脏、胃、肠)均差异不显著(P>0.05),各组母鼠的卵巢系数及公鼠的睾丸系数亦无显著差异(P>0.05)。

表5 各组小鼠脏器系数的比较
3 讨论
急性毒性试验标准GB 15193—2014规定:无毒或毒性微小的受试物适合采用限量法试验设计[16]。生物活性肽属于此类受试物[18-19],因此该试验采用限量法试验设计检测免疫调节肽的急性毒性作用。周雯等[20]研究了一种生物活性肽粉对小鼠的急性毒性,结果显示经口急性毒性LD50大于10 000 mg/ kg。徐军等[21]通过急性毒性试验研究了芽孢菌肽的毒性,观察动物的中毒表现和死亡时间,并进行毒性判断,雌、雄小鼠的经口急性毒性LD50分别为5 010和7 940 mg/kg。李函频[22]以小鼠为实验动物,研究了融合肽hEGF-AWRK6的急性毒性,结果显示观察期间小鼠无死亡,给药组的脏器系数、精子畸形率、血常规指标与空白对照组相比均无显著差异,因此认为融合肽hEGF-AWRK6无急性毒性。宋淑敏等[23]研究了汉麻籽多肽粉的急性毒性,发现连续14 d的观察期内试验小鼠未见任何中毒症状,亦无死亡发生;对小鼠进行大体病理学观察,未见脏器异常改变,因此确定汉麻籽多肽粉对小鼠的经口急性毒性LD50大于20 000 mg/kg。该试验结果表明,受试小鼠临床观察发现各组织器官无任何异常变化,受试物免疫调节肽对公鼠生长性能无不良影响,可显著提高母鼠体重增长,受试小鼠血常规指标及血清生化指标与对照组均无显著差异;大体解剖观察发现,受试小鼠内脏器官发育正常,无病理变化,与对照组相一致。该试验结果表明免疫调节肽对小鼠未产生急性毒性作用,与上述报道结果相一致。
4 结论
该试验所用免疫调节肽对小鼠无急性毒性作用,最大耐受剂量(MTD)大于5 000 mg/kg。
