替普瑞酮联合西尼必利对慢性萎缩性胃炎的疗效及胃肠激素的影响*
2022-12-20何邦立林亚发符名勇吴毓磊
何邦立,林亚发,符名勇,吴毓磊
(海南省海口市第四人民医院,海南 海口 571100)
慢性萎缩性胃炎是消化系统常见疾病,主要表现为患者胃黏膜上皮和腺体萎缩、数目减少、胃黏膜变薄、黏膜基层增厚,或伴幽门腺化生和肠腺化生,黏膜损伤可出现在胃部的胃角、裂孔疝、胃体、胃窦、贲门等处[1-2]。慢性萎缩性胃炎表现为上腹部隐痛、胀满、嗳气、消瘦、贫血等表观症状,严重影响患者的胃肠道功能和生命健康,随着病情的加重,胃黏膜萎缩、增生、化生等病理过程可能癌变,引发更严重的临床症状[3]。发病后应及时给予积极、有效的治疗,缓解胃部不适症状,治疗原则包括抑制胃酸分泌、保护胃黏膜、中和胃酸、提高胃动力、抗幽门螺杆菌等[4]。西尼必利是新型促胃肠动力药物,为5-羟色胺4受体激动剂,能调节胃肠动力的紊乱状态,是目前临床治疗慢性萎缩性胃炎的常用药物[5]。但其作用机制单一,仅改善胃肠动力,而慢性萎缩性胃炎的发病机制复杂,通常需联用其他药物以提高治疗效果[6]。替普瑞酮是新型广谱抗溃疡药物,在中和胃酸、保护胃黏膜、抑制胃酸分泌、修复胃黏膜损伤、抗氧化应激等方面药理活性良好,既往用于治疗急慢性胃炎、胃溃疡的效果良好[7]。本研究中探讨了替普瑞酮联合西尼必利治疗慢性萎缩性胃炎的临床疗效,以及对患者胃肠激素及炎性因子水平的影响。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:经胃镜检查确诊,符合《慢性萎缩性胃炎中西医结合诊疗共识意见(2017 年)》中诊断标准[8];年龄50~75 岁。本研究方案经我院医学伦理委员会审查通过(伦理批件号为HKSYY201907),患者及其家属对研究内容知情并自愿加入本研究。
排除标准:合并其他消化系统疾病;消化道或胃部手术史;凝血功能障碍;服药治疗过程中出现漏服或误服药物;对本研究中所用药物禁忌;观察指标数据不完整影响疗效判断;自愿退出本研究。
病例选择与分组:选取医院2019年10月至2021年9月收治的慢性萎缩性胃炎患者92例,按随机数字表法分为观察组和对照组,各46例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。详见表1。
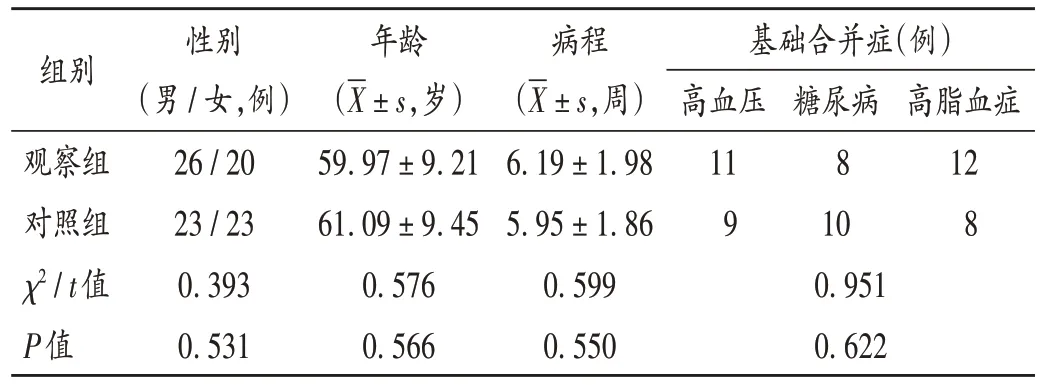
表1 两组患者一般资料比较(n=46)Tab.1 Comparison of the patients′ general data between the two groups(n=46)
1.2 方法
两组患者均予慢性萎缩性胃炎的基础治疗,口服雷贝拉唑钠肠溶片(江苏豪森药业集团有限公司,国药准字H20020330,规格为每片10 mg),每次2片,每日1次,晨服;枸橼酸铋钾胶囊(丽珠集团丽珠制药厂,国药准字H10920098,规格为每粒0.3 g),每次1 粒,每日4 次;口服铝碳酸镁咀嚼片(杭州康恩贝制药股份有限公司,国药准字H20073616,规格为每片0.5 g),每次0.5 g,每日3 次,咀嚼后咽下。对照组患者加用酒石酸西尼必利片(INDUSTRIASFARMACéUTICASALMIRALL,S.A. ,进口药品注册证号H20160477,规格为每片1 mg <按西尼必利计 >),每次 1 片,每日3 次,饭前15 min 口服。观察组患者在对照组治疗基础上加用替普瑞酮胶囊(卫材< 中国> 药业有限公司,国药准字H20093656,规格为每粒50 mg)口服,每次1 粒,每日3 次,饭后口服。两组患者均以2周为1个疗程,共治疗3个疗程。
1.3 观察指标与疗效判定标准
胃镜病理评分:分别于治疗开始前1 d、治疗结束后1 d 采用GVE-2100 型电子胃镜(上海维世康医用电子有限公司,沪械注准20152223077)检查患者的胃黏膜病理状态,对胃黏膜萎缩、上皮化生、异型增生情况进行评分,根据病理结果的严重程度分为无、轻、中、重4个等级,分别计为0,1,2,3分,评分与病理程度呈正比。
胃肠激素水平:分别于开始服药前1 d、服药疗程结束后1 d采集患者空腹静脉血各5 mL,采用Herolab 10A型实验室高速离心机(德国莱比信设备公司)离心(转速为3 000 r/min,离心半径为5 cm,离心温度为20 ℃)15 min。取分离后的血清上清液标本,采用荧光免疫分析法检测胃泌素(GAS)、胃动素(MTL)、胃蛋白酶原Ⅱ(PG Ⅱ)水平,检测仪器为FS-113型全自动免疫荧光分析仪(广州万孚仪器设备公司,粤械注准20172400077),试剂盒由深圳市倍诺博生物科技公司提供。
炎性因子水平:采用酶联免疫吸附法检测血清上清液标本蛋白酶激活受体2 蛋白(PAR2)、淀粉样蛋白A(SAA)、Toll 样受体4(TLR - 4)水平,检测仪器为HM -SY96S 型酶联免疫分析仪(山东恒美电子科技公司,鲁械注准201512140100),试剂盒由武汉赛培生物技术公司提供。
疗效判定[9]:显效,腹痛、腹胀、嗳气症状完全消退,胃镜检查病理评分下降高于80%;有效,上述表观症状均显著改善,胃镜检查示胃黏膜溃疡出血停止,胃镜检查病理评分下降30%~80%;无效,上述表观症状及胃镜检查示溃疡出血情况均未改善,胃镜检查病理评分下降低于30%。总有效=显效+有效。
安全性:记录患者治疗期间的药品不良反应发生情况,包括口干、便秘、皮疹、转氨酶升高。
1.4 统计学处理
采用SPSS 25.0 统计学软件分析。计量资料符合正态分布和方差齐性的以表示,组间比较采用独立样本t检验,组内比较采用配对样本t检验;计数资料以率(%)表示,行χ2检验。P<0.05为差异有统计学意义。
2 结果
结果见表2至表6。

表2 两组患者临床疗效比较[例(%),n=46]Tab.2 Comparison of clinical efficacy between the two groups[case(%),n=46]
表3 两组患者胃镜病理评分比较(,分,n=46)Tab.3 Comparison of gastroscopic pathology scores between the two groups(,point,n=46)

表3 两组患者胃镜病理评分比较(,分,n=46)Tab.3 Comparison of gastroscopic pathology scores between the two groups(,point,n=46)
注:与本组治疗前比较,*P < 0.05。表4和表5同。Note:Compared with those before treatment,*P < 0.05(for Tab. 3-5).
组别胃黏膜萎缩治疗前2.49±0.50 2.44±0.52 0.470 0.639治疗后0.65±0.19*0.91±0.26*5.476 0.000治疗后0.56±0.16*0.79±0.24*5.408 0.000治疗后0.61±0.18*0.83±0.25*4.844 0.000上皮化生治疗前2.38±0.59 2.43±0.54 0.423 0.673观察组对照组t值P值异型增生治疗前2.43±0.50 2.36±0.54 0.645 0.520
表4 两组患者胃肠激素水平比较(,n=46)Tab.4 Comparison of gastrointestinal hormone levels between the two groups(,n=46)
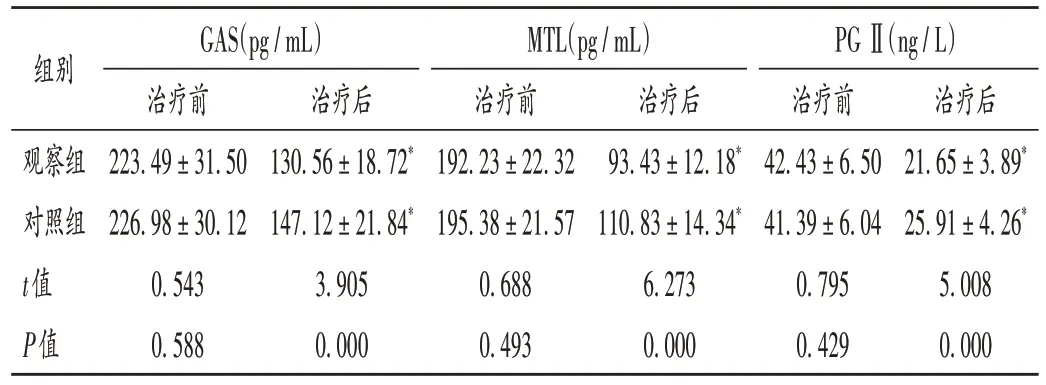
表4 两组患者胃肠激素水平比较(,n=46)Tab.4 Comparison of gastrointestinal hormone levels between the two groups(,n=46)
组别PG Ⅱ(ng/L)治疗前42.43±6.50 41.39±6.04 0.795 0.429 GAS(pg/mL)治疗前223.49±31.50 226.98±30.12 0.543 0.588治疗后130.56±18.72*147.12±21.84*3.905 0.000 MTL(pg/mL)治疗前192.23±22.32 195.38±21.57 0.688 0.493治疗后93.43±12.18*110.83±14.34*6.273 0.000观察组对照组t值P值治疗后21.65±3.89*25.91±4.26*5.008 0.000
表5 两组患者炎性因子水平比较(,n=46)Tab.5 Comparison of inflammatory factor levels between the two groups(,n=46)
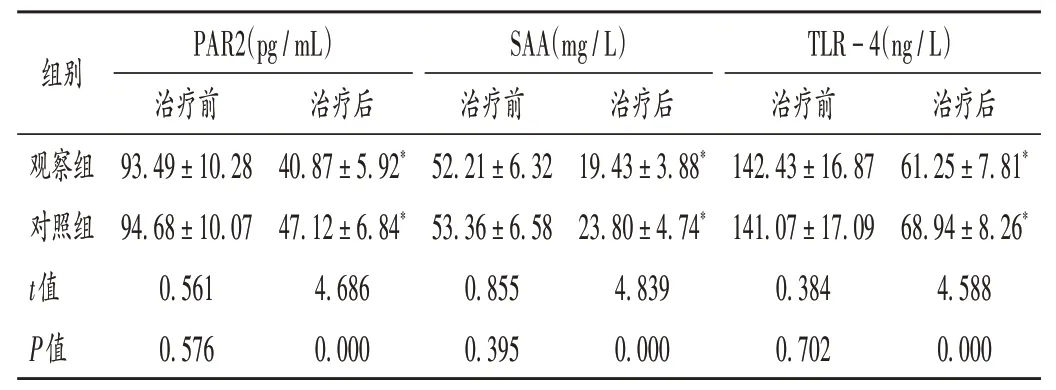
表5 两组患者炎性因子水平比较(,n=46)Tab.5 Comparison of inflammatory factor levels between the two groups(,n=46)
组别PAR2(pg/mL)治疗前治疗后治疗后SAA(mg/L)治疗前治疗后TLR-4(ng/L)治疗前93.49±10.28 94.68±10.07 0.561 0.576 61.25±7.81*68.94±8.26*4.588 0.000 40.87±5.92*47.12±6.84*4.686 0.000 52.21±6.32 53.36±6.58 0.855 0.395观察组对照组t值P值19.43±3.88*23.80±4.74*4.839 0.000 142.43±16.87 141.07±17.09 0.384 0.702

表6 两组患者药品不良反应发生情况比较[例(%),n=46]Tab.6 Comparison of the incidence of adverse drug reactions between the two groups[case(%),n=46]
3 讨论
慢性萎缩性胃炎临床发病率较高,发病原因和发生机制复杂,不良饮食习惯、幽门螺杆菌感染、长期服用非甾体抗炎药等损伤胃黏膜的药物、遗传因素、精神心理因素、免疫因素等均是慢性萎缩性胃炎发病的重要诱因[10]。发病机制在于患者的胃黏膜防御修复和胃黏膜受损间的不平衡,胃酸大量分泌并超出胃黏膜自身的修复能力,且多种因素导致胃黏膜表面的反复损伤,最初出现胃黏膜固有腺体萎缩,并伴有上皮化生、异型增生等病理改变,进而出现胃肠道功能症状,影响患者的消化功能。西尼必利为5-羟色胺4受体激动剂,通过拮抗胆碱能神经末梢的多巴胺受体,能调节患者的胃肠动力紊乱,改善慢性萎缩性胃炎患者的胃肠道症状,恢复正常的胃肠道功能[11]。本研究中对照组患者以西尼必利治疗,总有效率超过70%,表明西尼必利对慢性萎缩性胃炎有一定的治疗效果,但疗效仍有可提升空间。
替普瑞酮为新型广谱胃黏膜保护剂,可从多个作用机制对慢性萎缩性胃炎发挥治疗作用。本研究中观察组患者增加替普瑞酮胶囊口服治疗,患者的总有效率显著提升,表明替普瑞酮对慢性萎缩性胃炎有良好的治疗效果。相关动物实验表明,替普瑞酮可抑制胃黏膜损伤及溃疡产生过程中活性氧有关的48/80 复合物及血小板激活因子,直接发挥抗萎缩性胃炎作用[12]。替普瑞酮可增加胃黏膜上皮细胞分泌胃黏膜黏液,含有一定量的碳酸氢盐,能中和胃酸,有效抵御胃酸的侵蚀[13]。另外,替普瑞酮能提高对胃黏膜的保护作用,通过增加前列腺素E2、热休克蛋白、高分子糖蛋白等细胞因子的合成与分泌,发挥良好的胃黏膜保护作用[14]。替普瑞酮通过增加和改善胃黏膜血流循环状态,使损伤处胃黏膜的血供充足,加速损伤黏膜上皮的修复和再生,对萎缩性胃炎损伤黏膜有良好的修复作用。因此,观察组患者治疗后的胃镜病理包括胃黏膜萎缩、上皮化生、异型增生均显著改善。
慢性萎缩性胃炎的发生导致患者胃肠道功能异常,胃肠激素包括GAS,MTL,PGⅡ水平均呈异常表达。其中,GAS 是由胃肠道分泌的一种胃肠激素;MTL 是一种重要的胃肠激素,可提高胃肠道黏液的分泌功能,促进胃窦和胃体收缩。体内胃肠激素水平升高会导致肠道蠕动加速,出现腹痛及胃肠道功能不适等症。PGⅡ是一种反映胃黏膜损伤的炎性蛋白,由胃底黏液颈细胞分泌,胃黏膜受到损伤时会刺激PGⅡ合成并释放入血,其表达水平能反映胃黏膜损伤程度[15]。本研究中,观察组患者治疗后的GAS,MTL,PGⅡ水平均显著低于对照组,表明替普瑞酮能改善患者的胃肠道功能。
慢性萎缩性胃炎发病过程是一个炎性反应参与的过程,伴随着多种炎性因子水平的上升。PAR2属G蛋白偶联受体家族的一员,具有多重生理活性,在炎性反应、胃肠道平滑肌收缩功能中发挥调控作用。SAA 是一种急性时相反应蛋白,在胃溃疡患者中由于胃黏膜急性损伤引起的炎性反应能刺激巨噬细胞释放SAA 入血而出现高表达。TLR-4 是机体产生的一种内源性细胞因子,与机体免疫和炎性反应密切相关,但炎性反应发生时炎性损伤能刺激TLR - 4 介导的信号通路的开放引起TLR-4的表达上调[16]。本研究中观察组患者治疗后的PAR2,SAA,TLR-4水平均显著低于对照组,表明替普瑞酮的抗炎作用良好。观察组患者未出现新的严重不良反应,提示安全性较好。
综上所述,替普瑞酮联合西尼必利治疗慢性萎缩性胃炎的临床疗效显著,能改善患者的胃镜病理状况,降低胃肠激素水平,抑制炎性因子表达,且安全性良好。
