Soleris微生物快速检测系统在巴氏杀菌乳中的应用验证
2022-12-14邢益俊林木娣赖书莹曹学思杨爱君纪坤发
邢益俊,何 瑛,林木娣,赖书莹,曹学思,杨爱君,纪坤发
广东燕塘乳业股份有限公司,广东广州 510507
0 引言
牛奶富含多种营养成分,是理想的营养补充品。随着生活水平的不断提高,人们对牛奶的营养成分及安全性要求越来越高,食品安全问题日益受到广大消费者的关注。微生物污染作为影响牛奶卫生安全的主要原因,一直以来都是乳品企业和监管机构预防和监控的主要指标之一。大肠菌群是微生物污染监控最重要的一项[1],乳品中大肠菌群含量超标可能危害消费者肠道健康,引发食物中毒或其他食源性疾病[2]。大肠菌群是指需氧及兼性厌氧、在35~37 ℃培养条件下,48 h内能分解乳糖产酸产气的革兰氏阴性无芽孢杆菌。目前,大肠菌群的检测方法主要有平板计数法[3]、乳糖胆盐多管发酵法[4]、LST多管发酵法[5]、纸片法[6]、PCR试剂盒法[7]、酶底物法[8]等。其中平板计数法、乳糖胆盐多管发酵法和LST多管发酵法是常用的检测方法。而传统的微生物检验方法涉及的试验过程较长,需要有大量人员参与,严重影响检验效率及工厂对产品的快速放行。巴氏杀菌乳杀菌强度低,对牛奶中天然活性成分的保留较多,但保质期较短,大肠菌群快速检测技术对于防止食源性疾病的危害及企业产品的快速放行具有重要意义。
本文应用Soleris微生物快速检测系统对巴氏杀菌乳中大肠菌群进行快速检测,通过与传统国标平板计数法《GB 4789.3—2016 食品安全国家标准 食品微生物学检验 大肠菌群计数》第二法进行对比,验证该方法对牛奶大肠菌群检测的可行性与准确性。
1 仪器与材料
1.1 仪器
SolerisTM128微生物快速检测系统,美国Neogen公司;培养箱,上海一恒科学仪器有限公司;移液枪,德国Brand公司;漩涡振荡器,广州海太光电生物科技有限公司;电子天平,常州市衡正电子仪器有限公司。
1.2 试剂
结晶紫中性红胆盐琼脂VRBA,北京陆桥技术股份有限公司;煌绿乳糖胆盐肉汤BGLB,北京陆桥技术股份有限公司;NaOH(AR级别),广州化学试剂厂;Soleris大肠菌群试剂瓶,美国Neogen公司;二级水(符合GB/T 6682—2008 分析试验室用水)。
1 moL/L NaOH溶液:用小烧杯称取NaOH4 g,加入40 mL二级水,搅拌溶解后转入100 mL容量瓶中,再用水反复冲洗小烧杯一并转入到容量瓶中,最后定容到刻度。
1.3 材料
生牛乳,本公司本土自营牧场;评估大肠菌群为阴性的巴氏杀菌乳,本公司产品。
2 方法与分析
2.1 工作原理
Soleris大肠菌群检测试剂瓶是基于传统的微生物培养理论与染色技术研发而成,在预制的试剂瓶中放置特异性的培养基和专用指示剂,在适宜的温度条件下,当微生物在培养瓶中繁殖时,会发生代谢产物改变培养基pH值或释放CO2等生化反应,从而引起试剂瓶底部的琼脂栓颜色的变化。Soleris微生物快速检测系统利用光电检测仪器,每隔6 min监测试剂瓶底部琼脂栓的颜色变化,将信号转换成光度值,反映微生物的生长情况,通过实时监测吸光值的变化,可快速实现对样品中微生物的定性、半定量及定量的检测(图1)。

图1 Soleris微生物快速检测系统检测原理
2.2 试验方法
2.2.1 阳性样品制备
用VRBA培养基对生牛乳进行大肠菌群分离培养,36 ℃培养18~24 h,挑取典型菌落接种到BGLB管中36 ℃培养48 h,进行确认。把经过确认的大肠菌群菌落接种到巴氏杀菌乳中,36 ℃培养过夜进行增菌,制备成大肠菌群阳性样品,编号为样品Y,放入冰箱冷藏备用。
2.2.2 Soleris微生物快速检测系统方法和平板计数法检测结果的一致性验证
为了更好地模拟巴氏杀菌乳在Soleris微生物快速检测系统中检测,选择经检验确认大肠菌群为阴性的巴氏杀菌乳代替生理盐水作为稀释液。取5 mL阳性样品Y加入到含有45 mL确认过大肠菌群为阴性的巴氏杀菌乳的带盖灭菌瓶中,用旋涡振荡器将其充分混匀,用1 moL/L NaOH溶液调整其pH至6.7±0.3,编号为A1,依次稀释样品至10-2、10-3、10-4、10-5、10-6、10-7、10-8,对应编号分别为A2、A3、A4、A5、A6、A7、A8,再对A8进行1:1稀释,编号为A8-2x。选择进行梯度稀释的样品,移取1 mL,分别加入到Soleris大肠菌群试剂瓶中,上下颠倒2~3 次,混匀后将试剂瓶盖回旋1/4,保持气流交换,上机检测,同时按照平板计数法进行对照试验,每个样品重复2次,以上稀释过程全程不超过15 min。具体检测结果见表1。
《GB 19645—2010 食品安全国家标准 巴氏杀菌乳》对巴氏杀菌乳中大肠菌群的限量要求为:5 个样品中不得有超过2 个样品检测结果大于5 CFU/mL。从表1可以看出,当平板计数法检测结果>1 CFU/mL时,仪器均能检出,而且含菌量越多,仪器检出时间越短,两种方法的检测结果具有良好的一致性。此外,同稀释梯度2 个平行样品检出时间的RSD值在0%~2.70%之间,重复性良好。
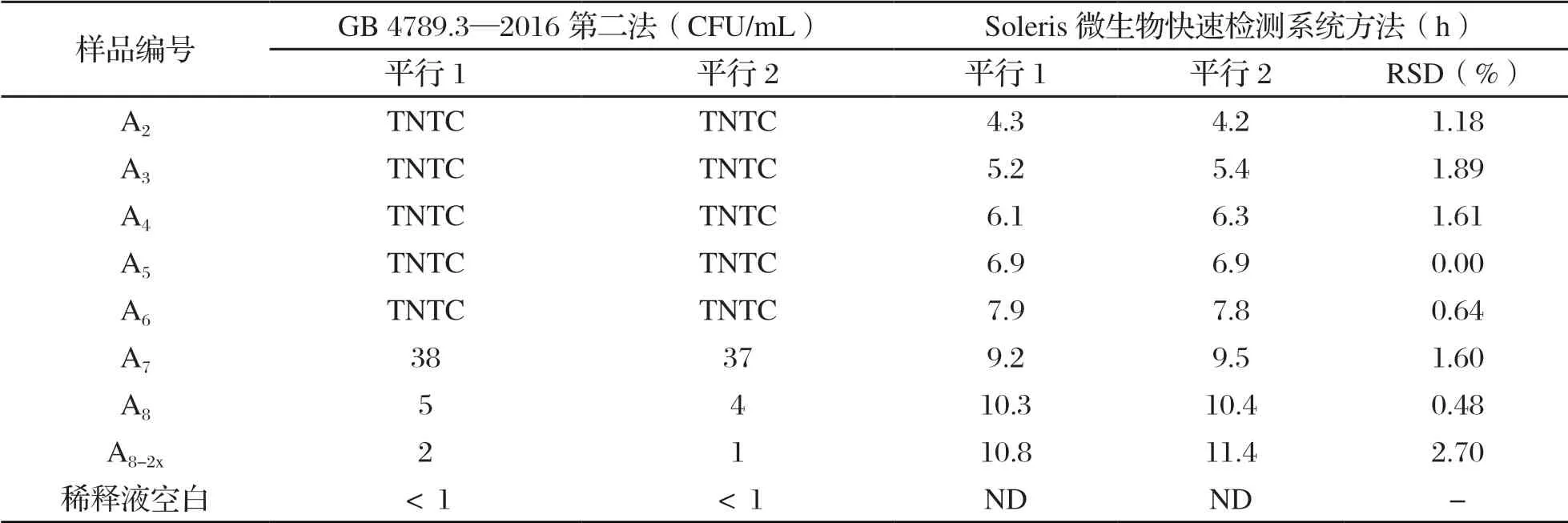
表1 Soleris微生物快速检测系统方法和平板计数法检测结果
2.2.3 Soleris微生物快速检测系统方法的灵敏度验证
基于风险监控的需求,企业对巴氏杀菌乳中大肠菌群的限量要求设定为<1 CFU/mL。试验选择A8-2x稀释梯度按照GB 4789.3-2016和Soleris微生物快速检测系统方法同步进行20 次重复试验。由于稀释倍数大,菌落可能无法被捕捉到,所以从中挑取10 个平板计数法菌落数检出在1~2 CFU/mL之间的样品对应的仪器检出时间,结果详见表2。

表2 临界样品的重复性试验结果
从表1、2可以看出,当平板计数法检出样品中大肠菌群含量≥1 CFU/mL的监控限值时,Soleris微生物快速检测系统方法均有检出,没有出现假阴性的情况。当平板计数法检出样品中大肠菌群含量为1 CFU/mL时,Soleris微生物快速检测系统方法检出时间为10.8~11.4 h,RSD值为1.62%。比起平板计数法培养需要18~24 h,该方法检测时间显著缩短,且灵敏度高,重复性良好。随着样品中大肠菌群污染越严重,Soleris微生物快速检测系统能越早地进行风险预警。
2.2.4 Soleris微生物快速检测系统方法的特异性验证
选择10 个评估大肠菌群为阴性的巴氏杀菌乳样品,同时进行Soleris微生物快速检测系统方法和平板计数法对照检测,每个样品重复2 次,得到的结果如表3。从表3可知,当巴氏杀菌乳样品平板计数法检测结果为<1 CFU/mL时,Soleris微生物快速检测系统方法结果均为“ND”(未检出),该方法未出现假阳性的结果,样品基质本身亦未对检测结果产生干扰。因此,Soleris微生物快速检测系统方法对巴氏杀菌乳大肠菌群的检测具有良好的特异性[9]。
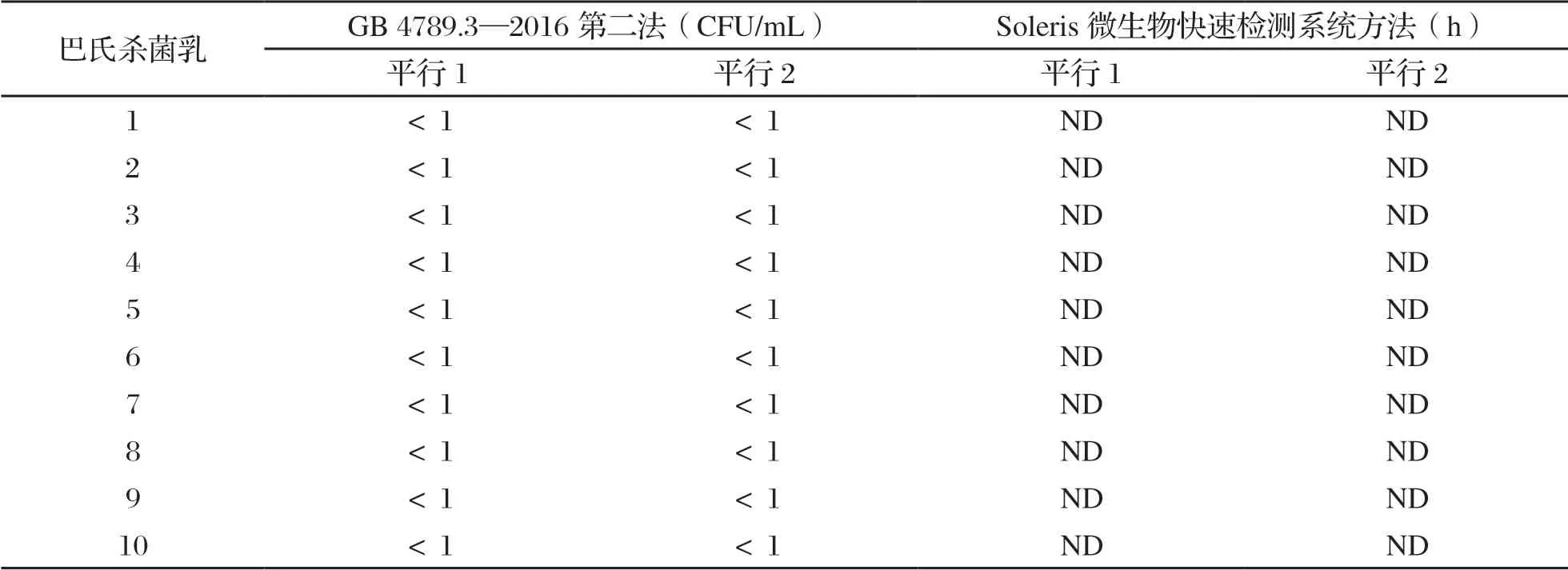
表3 阴性样品的重复性试验结果
3 讨论
结合表1、表2的结果,当平板计数法检出样品中大肠菌群含量为1 CFU/mL时,Soleris微生物快速检测系统方法检出时间为10.8~11.4 h,在企业实际生产放行过程中,为了更好地进行风险控制,可以将仪器检测的截止时间延长2 h,设置为13.5 h,确保风险被有效控制。
4 结论
本文建立Soleris微生物快速检测系统方法对巴氏杀菌乳中大肠菌群进行快速检测,该方法操作简便、实时快速,与国标平板计数法具有良好的一致性,重复性良好,能有效减少人为误差。Soleris微生物快速检测系统方法从检测到出结果只需要12 h左右,比传统的国标方法所需时间大大缩短,为企业巴氏杀菌乳快速放行提供决策依据。
