孤立性血管环胎儿气管受压及预后情况分析
2022-12-10吴娟胡圆榘王铭尚红磊林杉刘云姜竹栗河舟
吴娟,胡圆榘,王铭,尚红磊,林杉,刘云,姜竹,栗河舟
(郑州大学第三附属医院,河南 郑州 450052)
血管环是由于主动脉弓及其分支的发育异常所导致的一种先天性畸形,大血管异常环绕气管、食管可对其造成不同程度的压迫[1]。血管环可造成部分患儿出现呼吸窘迫、喘鸣、反复呼吸道感染以及吞咽困难等[2]。回顾以往的研究多集中在通过超声多切面扫查诊断及鉴别诊断胎儿血管环,对于产前气管受压及预后情况的报道较少。本研究通过孕期胎儿超声心动图检查测量气管参数,结合磁共振(Magnetic resonance imaging,MRI)和染色体检查结果,对血管环胎儿的预后进行综合评估分析,并随访出生后情况。
1 资料与方法
1.1 研究对象
选取2017 年12 月—2021 年2 月在我院经超声心动图检查诊断为孤立性血管环的82 例胎儿作为病例组,包括双主动脉弓(Double aortic arch,DAA)16 例、右位主动脉弓伴左锁骨下动脉迷走(Right aortic arch with aberrant left subclavian artery,RAA+ALSA)63 例、肺动脉吊带(Pulmonary artery sling,PAS)3例,入组胎儿均符合孤立性血管环的诊断标准:主动脉弓及分支血管异常,环绕气管和(或)食管形成血管环,不伴发其他心内和心外畸形。另选取同孕周的正常胎儿90 例作为正常组。DAA 组孕妇年龄22~35岁,平均(29.1±2.1)岁,孕周22~33周,平均(28.24±2.86)周;RAA+ALSA 组孕妇年龄20~41岁,平均(31.4±2.8)岁,孕周21~34周,平均(29.13±3.27)周;正常组孕妇年龄19~39岁,平均(28.8±3.1)岁,孕周20~36周,平均(28.56±4.34)周。正常组与DAA 组、RAA+ALSA 组之间孕周的差异无统计学意义(P>0.05)。受检孕妇检查前均知情同意。
1.2 仪器与方法
胎儿超声心动图检查采用GE Voluson E8 和开立P60 彩色多普勒超声诊断仪,RAB4-8-D 探头及VC2-9 探头,频率4~8 MHz 及2~9 MHz;MRI 检查使用GE Crator 1.5T MR 扫描仪,选择Fiesta、SSFSE 序列进行扫查。胎儿超声心动图检查及测量:参照胎儿超声心动图规范进行检查,观察主动脉弓及其分支、肺动脉分支及动脉导管的位置与连接关系,以及与气管的相互关系。采用两线垂直的测量方法,在三血管-气管切面测量正常组、RAA+ALSA组、DAA 组胎儿气管前后径、左右径(图1a~1c),用手动描迹法测量各组气管面积及周长,在三血管切面测量PAS 组气管前后径、左右径(图1d),应用手动描迹法测量PAS 组气管面积及周长。所有数据均测量3 次取平均值。
1.3 随访
随访时间为出生后1 月~3岁,随访病例组产前染色体及MRI 检查结果、妊娠结局及生长发育情况,重点观察出生后患儿是否出现呼吸道症状,包括喘鸣、窒息、反复呼吸道感染及呼吸骤停等。
1.4 统计学方法
采用SPSS 26.0 软件对数据进行统计学分析,符合正态分布且方差齐的计量资料以均数±标准差()表示,组间比较采用单因素方差分析,若各组组别间的差异有统计学意义,则运用LSD-t 检验对各组间行两两比较,以P<0.05 为差异有统计学意义。
2 结果
2.1 血管环胎儿产前气管参数比较
正常组、DAA 组、RAA+ALSA 组产前气管参数见表1。RAA+ALSA 组气管左右径、周长、面积均较正常组小(P<0.05)。DAA 组气管前后径、左右径、面积、周长均较正常组小(P<0.05)。DAA 组气管前后径、左右径、面积、周长均较RAA+ALSA 组小(P<0.05)。3 例PAS 胎儿气管前后径为(2.03±0.43)mm,左右径为(1.59±0.38)mm,面积为(2.13±0.32)mm2,周长为(4.20±0.56)mm,气管形态发生显著改变,气管左右径小于前后径。其中1 例PAS 胎儿产前超声及MRI 检查均显示气管受压,气管隆嵴位置下移,支气管夹角增大,提示合并支气管桥(图2)。
表1 正常组、DAA 组、RAA+ALSA 组产前气管参数()
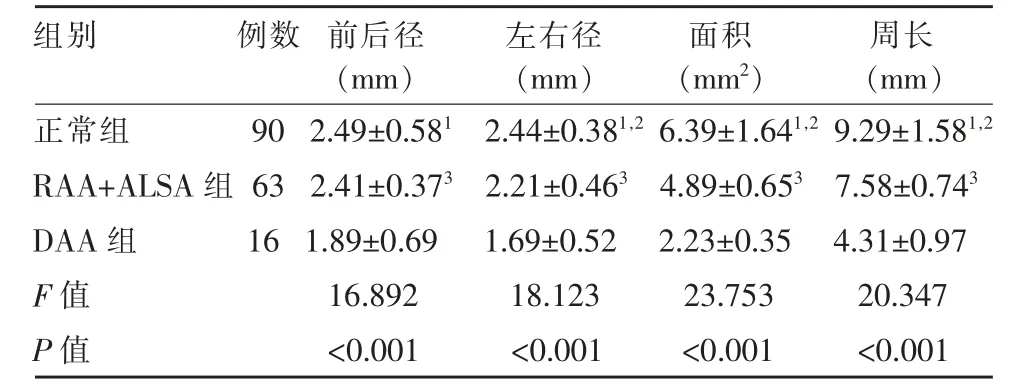
表1 正常组、DAA 组、RAA+ALSA 组产前气管参数()
注:1:与DAA 组比较,P<0.05;2:与RAA+ALSA 比较,P<0.05;3:与DAA 组比较,P<0.05。
2.2 血管环胎儿产前染色体检查结果及产后随访 情况
82 例血管环胎儿中54 例产前接受染色体检查,结果提示染色体异常3 例(5.56%,3/54),2 例为22q11.2 微缺失综合征,1 例为16p11.2 微缺失综合征,均经引产后病理证实为RAA+ALSA,其余血管环胎儿均经出生后心脏超声检查、增强CT 检查或手术确诊。DAA 组出生后出现呼吸道症状10 例(62.50%,10/16),均进行手术治疗,术后患儿的呼吸道症状有不同程度的缓解或消失,其中1 例产前超声及MRI 检查均提示气管受压严重,出生后CT 血管造影显示气管受压程度有所减轻。6 例DAA 组患儿年龄小且无相关气管受压症状,未行手术治疗。随访期间所有患儿生长发育、活动量较健康儿童无明显差异。RAA+ALSA 组出生后出现呼吸道症状1 例(1.67%,1/60),并进行手术治疗,59 例随访期间未出现相应气管受压的临床症状,随访期间所有患儿生长发育正常。PAS 组出生后均出现呼吸道症状,均行手术治疗,术后随访患儿生长发育、活动量较健康儿童无明显差异。
3 讨论
血管环因其解剖结构围绕气管,可导致气管受压,压迫较重者可出现呼吸困难等[3-4],甚至需要手术治疗[5-6]。通过测量血管环胎儿气管的变化,可反应血管环对气管的压迫程度,进一步反应出生后是否会出现呼吸系统症状。
本研究RAA+ALSA 组胎儿气管参数中气管左右径、周长、面积均小于正常组(P<0.05),随访结果显示产后仅1 例出现呼吸道症状,这可能是因为气管受压程度较轻或随访时间短。DAA 组气管前后径、左右径、面积、周长均较正常组、RAA+ALSA 组小(P<0.05),产后随访10 例患儿出现呼吸道症状。RAA+ALSA 组出生后1.67%的患儿出现呼吸道症状,DAA 组出生后62.50%的患儿出现呼吸道症状,可以看到DAA 组血管环胎儿产前气管参数较RAA+ALSA 组小,出生后出现呼吸道症状的比例较RAA+ALSA 组高,分析原因考虑为DAA 的“O”型血管环之间包绕的空间小,RAA+ALSA 的“U”型血管环包绕的空间较大,“O”型血管环对气管压迫明显。本研究中6 例DAA 胎儿在随访期间未出现呼吸道症状,可延长随访时间做进一步研究。本研究PAS组有1 例合并支气管桥。支气管桥是指异常支气管分支由左主支气管发出,供应右肺组织氧气,同时伴或不伴右主支气管缺失[7]。文献报道,PAS 合并支气管桥的发生率可达78%[8]。血管环可合并21-三体综合征和22q11 微缺失综合征,这些患儿神经发育迟缓、语言障碍等风险偏高[9]。
本研究82 例血管环胎儿中54 例接受染色体检查,结果提示染色体异常者3 例(5.56%,3/54),均为RAA+ALSA 病例。因此,出现血管环畸形,尤其是RAA+ALSA 的胎儿应建议其进一步行染色体检查,以排除染色体异常。
胎儿时期气管内充满羊水,肺部无气体干扰,动脉导管正常开放,产前超声检查可清晰完整地显示血管环结构以及和气管的包绕关系[10-12]。本研究显示正常胎儿产前超声检查气管呈无回声管状结构,血管环胎儿气管受压时三血管气管或三血管切面气管明显变小,管腔狭窄,冠状面可见大血管跨过气管处,气管明显受压,受压处向内凹陷。由此可见,产前超声心动图检查可清晰显示胎儿气管形态及受压情况。MRI 检查不受胎儿孕周及体位因素的影响,可完整清楚的显示气管及与周围血管的关系,因此对于血管环超声检查及评估气管通畅性有很好的补充作用[13]。
综上所述,产前超声心动图检查可清晰显示胎儿气管的形态及受压情况,结合胎儿心脏MRI 及染色体检查可为产前咨询和预后评估提供帮助。
