某儿童医院145例抗肿瘤药物药品不良反应分析
2022-12-08陈婷婷
李 悦,张 宝,杨 红,陈婷婷,马 晓
(贵州省贵阳市妇幼保健院·贵州省贵阳市儿童医院药学部,贵州 贵阳 550003)
儿童恶性肿瘤的患病率、病死率逐年上升,已成为儿童第二常见死因[1]。目前,全球各国批准上市的抗肿瘤药物约150种,该类药具有细胞毒性,对机体内肿瘤细胞及正常细胞均有杀伤作用[2-3]。2018年,我国发布《国家药品不良反应监测年度报告》,在国家基本药物化学药品和生物制品不良反应/事件报告中,抗肿瘤药占26.1%,位居第二;抗肿瘤药物的严重药品不良反应(ADR)构成比居首[4]。儿童的各个组织、器官等功能尚未发育成熟,用药风险较成人更大,故应持续关注儿童使用抗肿瘤药物的安全性[5]。本研究中统计分析了某妇女儿童专科医院2017年至2019年上报至中国医院药物警戒系统的儿童使用抗肿瘤药物引发的ADR报告145例,旨在了解该类ADR的一般规律及特点,为儿童临床安全使用抗肿瘤药提供参考。现报道如下。
1 资料与方法
选 取 某 院2017年1月1日 至2019年12月31日 上报至中国医院药物警戒系统的儿童抗肿瘤药物ADR报告145例。纳入患儿年龄<18岁,原患疾病为肿瘤类疾病,使用抗肿瘤类药物治疗,资料内容清晰完整,ADR均经关联性评价并复核;排除重复报告,资料不完整病例。采用Excel软件统计患儿的性别、年龄、原患疾病、ADR涉及的药品种类、给药途径、ADR发生时间、累及系统/器官、临床表现、ADR类别及转归情况等并分析。
2 结果
2.1 性别和年龄分布
结果见表1。其中男女比例为1∶0.61;根据联合国“儿童权利公约”定义设置年龄段(≤3岁为婴幼儿,>3~6岁为学龄前期,>6~12岁为学龄初期,>12~18岁为青春期),可见,学龄前期患儿ADR发生率最高,其次为学龄初期。
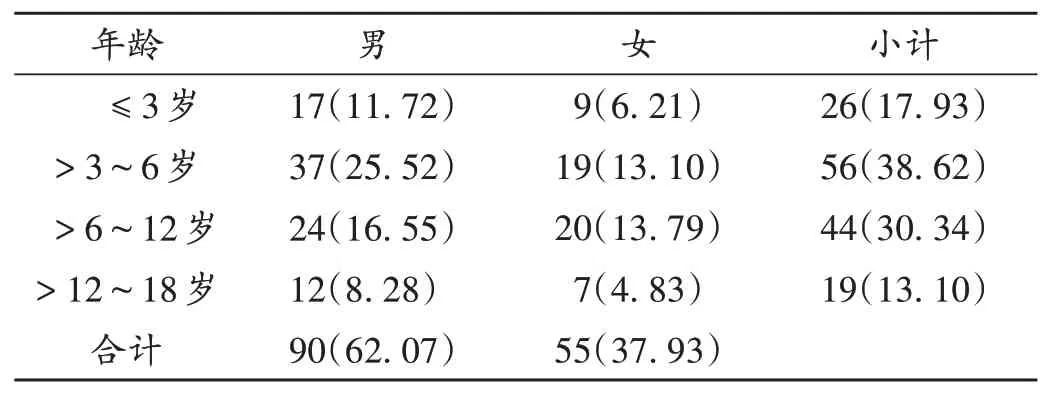
表1 患儿性别与年龄分布[例(%),n=145]Tab.1 Distribution of children's sex and age[case(%),n=145]
2.2 原患疾病
145例ADR报告中,白血病占比最大(140例,96.55%),其中尤以急性淋巴细胞白血病(ALL)居多(126例,86.90%),其他肿瘤占比较少(5例,3.45%)。
2.3 ADR涉及药物种类
引发ADR的抗肿瘤药物类别以抗代谢类居首,具体药物以注射用阿糖胞苷最多。详见表2(因部分患儿联用多种抗肿瘤药物,故总数超过145例。表3同)。
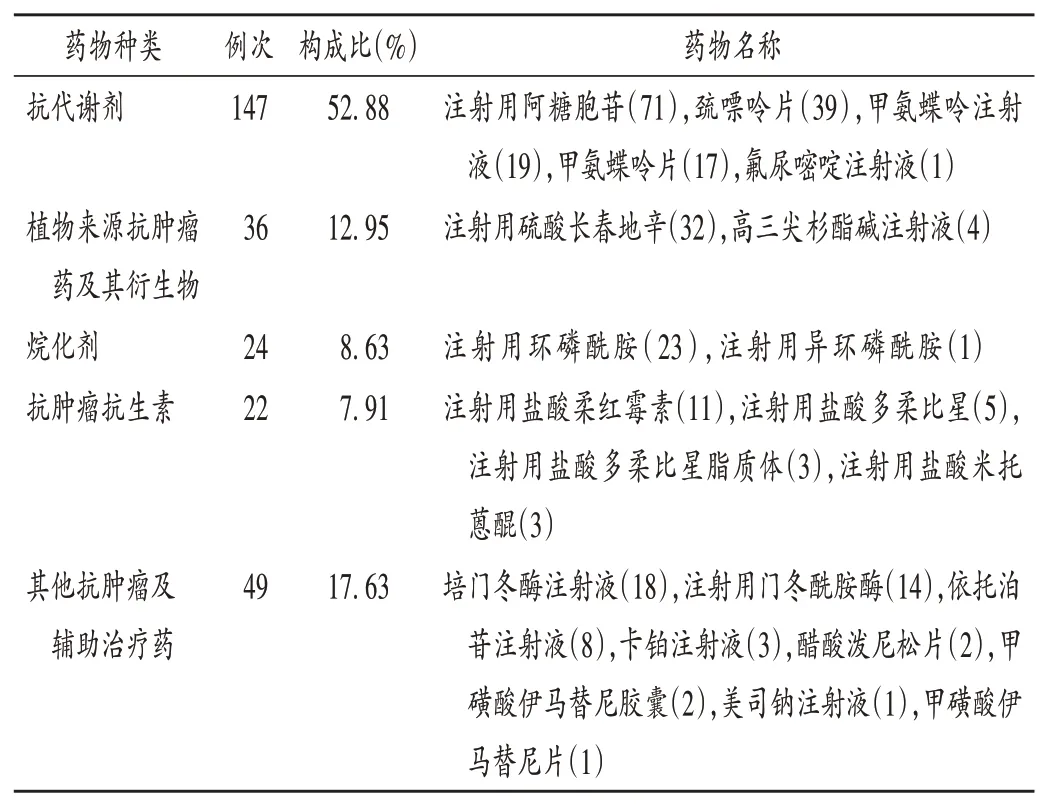
表2 ADR涉及的药品种类分布(n=278)Tab.2 Distribution of categories of anti-tumor drugs involved in ADR(n=278)
2.4 给药途径
145例ADR报告中共涉及5种给药途径,详见表3。以注射给药为主(217例次,78.06%),其中尤以静脉滴注最多(145例次,52.16%)。
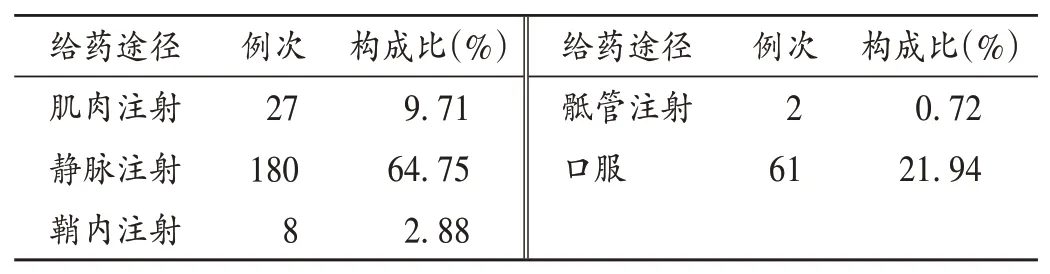
表3 ADR给药途径分布(n=278)Tab.3 Distribution of administration routes inducing ADR(n=278)
2.5 ADR发生时间
145例ADR报 告中,ADR发生 于 用药3 d内 最多(59例,40.69%),其中用药过程中30例(20.69%);用药4~7 d 38例(26.21%);用药8~14 d 30例(20.69%),>14 d 18例(12.41%)。
2.6 累及系统/器官及临床表现
ADR累及系统/器官以血液系统最常见,主要临床表现为骨髓抑制(包括粒细胞缺乏、红细胞减少、白细胞减少、血小板减少);其次为消化系统(49例次,26.63%),主要临床表现为肝功能异常。详见表4(因部分患者ADR报告中临床表现多,故总数超过145例)。

表4 ADR累及系统/器官及其临床表现(n=184)Tab.4 Organs/systems involved in ADR and their main clinical manifestations(n=184)
2.7 ADR类别及转归
145例ADR报告中,一般ADR 24例(16.55%),其中新的一般ADR 1例;严重ADR 121例(83.45%),其中新的严重ADR 1例。经对症治疗,痊愈42例(28.97%),好转89例(61.38%),不详14例(9.66%)。
3 讨论
3.1 抗肿瘤药物与个体化给药
本研究结果显示,儿童抗肿瘤药物ADR报告中,男多于女,可能原因为前者基数大、就诊率高;加之男女之间生理差异导致对抗肿瘤药物敏感性不同[6],故急性淋巴细胞白血病的发生率男大于女[7]。ADR可发生于儿童生长的各个阶段,>3~12岁患儿ADR发生率较高,其原因可能同样为该年龄段患儿就诊率高、基数大。由于儿童的组织、器官等功能尚未发育成熟,肾脏排泄功能不完善,排泄缓慢,半衰期延长,血药浓度高,导致患儿机体对药物的代谢及清除能力、耐受力不足。且不同患儿之间表现出较大的个体差异,易引发ADR[8]。因此,临床医师和药师在给患儿使用抗肿瘤药物时应严密监测患儿的生理状况和血药浓度,根据患儿的年龄、体质量、肝肾功能等指标个体化给药。
3.2 ADR与原患疾病
儿童白血病约占全部儿童肿瘤的1/3,是儿童最常见的恶性肿瘤,其中以ALL和急性髓细胞性白血病(AML)为主[9]。本次纳入的145例ADR报告中以白血病最常见,其中ALL居多。儿童易患白血病可能是由于儿童体内的DNA尚未完整及机体免疫功能差,遗传、染色体变异及接触电离辐射等也是儿童白血病的诱因[10]。提示应关注儿童生存环境,对于有家族遗传史的儿童还需提高警惕,尽早干预,预防并减少白血病发生。
3.3 ADR与给药途径
药物通过静脉给药可直接入血,无吸收过程,不存在首过效应,起效快,已成为住院患儿抗肿瘤药物主要的给药方式。本研究中,抗肿瘤药物致儿童ADR以注射给药途径为主,其中静脉注射(含静脉滴注)居多。静脉给药药品配制液的稳定性,输液、滴注的浓度与速率等因素均可能影响ADR的产生,因此临床静脉注射抗肿瘤药物时,应严格按药品说明书操作。
3.4 引发ADR的药品种类与构成比
本研究中,抗代谢类抗肿瘤药ADR发生率最高,其中以注射用阿糖胞苷最多,其次为巯嘌呤片。阿糖胞苷为嘧啶类抗代谢药,临床主要用于治疗儿童急性白血病,其通过抑制细胞DNA合成、干扰细胞增殖而发挥疗效,与其他类型的抗代谢药无交叉耐药性[11];巯嘌呤是ALL维持治疗的重要药物,其能持续杀伤残留的肿瘤细胞而使患儿始终处于完全缓解状态。近年来应用抗代谢类抗肿瘤药治疗儿童急性白血病提高了患儿的完全缓解率及长期生存率,但随着剂量增大,毒副作用也逐渐增多[12],这与儿童各组织器官发育不完全,免疫力低下息息相关。因此,在使用抗代谢类抗肿瘤药时应严密监测血药浓度。此外,应对其药理作用及耐药机制进行深入研究,为临床合理用药、确定最佳治疗方案和个体化用药提供科学依据。
3.5 ADR累及系统/器官及临床表现
累及系统/器官包括血液系统、消化系统、全身反应、皮肤及其附件等,血液系统损害居首位,临床主要表现为骨髓抑制。骨髓是人体的主要造血器官,包括造血细胞和造血微环境两大部分,多数抗肿瘤药物为细胞毒性药物,不仅抑制或杀伤肿瘤细胞,对体内正常造血细胞也有毒害作用,因此,大多数化疗药物的共同ADR为骨髓抑制[13]。ADR发生时间多为用药后3 d内,其次为4~7 d和8~14 d,提示临床医师和药师应加强患者用药后2周内的不良反应监测。
