HPLC-MS/MS法测定罗非鱼中4种四环素类抗生素残留量及不确定度评定
2022-12-07高云慨陈小妹陈春泉郑金明尹青春
高云慨,陈小妹,陈春泉,肖 璇,郑金明,尹青春
(海南省食品检验检测中心,国家市场监管重点实验室(热带果蔬质量与安全),海南海口 570100)
四环素类抗生素是由放线菌属产生或半合成具有并四苯衍生物结构特征的广谱抑菌剂,对多数病原细菌具有较强抑制作用。在水产品养殖中,四环素、土霉素、金霉素和多西环素作为饲料添加剂和治疗药品被广泛用于防治肠道感染和促生长[1]。随着该类药物的频繁使用,由食物链富集导致的水产品药物残留越来越严重,超量的药物残留会对人体产生一定毒副作用,危害人类健康。因此,许多国家对水产品养殖中使用的抗生素进行严格监控。我国食品安全国家标准规定,水产品肌肉组织中四环素类抗生素单个或组合残留限量为200 μg·kg-1[2]。
不确定度分析是国际上推荐的用于定量评估测量的有效手段[3],其大小决定了定量分析结果的准确性[4-5]。当检测结果在限值附近时,该评估对测量结果准确性及可靠性具有重要作用[6]。目前国内对水产品抗生素残留的测定方法主要有HPLC和LC-MS/MS法[7-11],但存在前处理复杂、用时长等问题。目前关于水产品中四环素、土霉素、金霉素和多西霉素残留测定不确定度评定的相关信息鲜有报道。本研究参照《测量不确定度评定与表示》(JJF 1059.1—2012)[12]、《化学分析中不确定度的评估指南》(CNAS—GL006:2019)有关规定[13],对国标《食品安全国家标准 水产品中土霉素、四环素、金霉素、多西环素残留量的测定》(GB 31656.11—2021)[14]前处理过程进行改进,以罗非鱼为基质对4种四环素类抗生素残留量的测量不确定度进行分析评定,考察该检测结果的准确性,同时掌握该方法关键检测环节,为其他水产品的测定及不确定度评定提供参考依据。
1 材料与方法
1.1 材料与仪器
1.1.1 材料
土霉素标准品:纯度93.8%,CAS号64-75-5;金霉素标准品:纯度81.5%,CAS号64-72-2;四环素标准品:纯度96.3%,CAS号2058-46-0;多西环素标准品:纯度92.4%,CAS号24390-14-5,以上标准品为混标,购自天津阿尔塔科技有限公司。乙酸乙酯(CH3COOC2H5)、乙腈(CH3CN)、甲醇(CH3OH)、正己烷(C6H6)、甲酸(HCOOH),以上试剂均为色谱纯,购自上海安谱公司。
1.1.2 仪器
AB Sciex Triple Quad™ 4500质谱仪(AB 4500,美国SCTEX);电子分析天平(XS204S,瑞士梅特勒);超声波清洗机(SK 7200,上海科导超声仪器);氮吹仪(XcelVap-XCV 5400,美国Horizon);固相萃取仪(W-SPE 24,美国LabTech);PRime HLB固相萃取柱(6 CC/200 mg,美国Waters);低温冷冻离心机(5804R,德国Eppendorf);手动移液器(德国Brand)。
1.2 实验方法
1.2.1 样品前处理
称取2.0 g罗非鱼均质样品至50 mL干净离心管中,加入10 mL乙腈(含1%甲酸),漩涡混匀后超声10 min,于10 000 r·min-1下离心5 min;精确移取全部上清液至PRime HLB固相萃取柱,收集全部滤液于氮吹仪中40 ℃下吹至近干,最后用甲酸(0.1%)-乙腈定容至1 mL,摇匀后0.22 μm过膜,供质谱分析。
1.2.2 标准系列溶液配制
标准储备液的制备:按要求向标准品瓶中准确加入1 mL甲醇溶液,旋涡混匀,制成含土霉素、四环素、金霉素、多西环素的混标储备液,其浓度分别为 100.1 μg·mL-1、100.5 μg·mL-1、100.0 μg·mL-1和 100.3 μg·mL-1。
标准工作液的制备:向10 mL容量瓶中准确加入100 μL制备好的混标储备液,甲醇定容后超声混匀,配制成混合标准工作液,其浓度分别为1.001 μg·mL-1、1.005 μg·mL-1、1.000 μg·mL-1和 1.003 μg·mL-1。
标准曲线的制备:选择6份阴性空白基质,经提取和净化后依次加入 5 μL、10 μL、20 μL、50 μL、100 μL、250 μL 制备好的混标工作液,余下操作同1.2.2,得标准曲线工作溶液。
1.2.3 仪器条件
(1)色谱条件。Eclipse Plus-C18反相色谱柱(100 mm×2.1 mm,1.7 μm,Agilent);柱温设置为40 ℃;流动相A为0.2%甲酸水溶液、B为纯甲醇;流速为0.2 mL·min-1,洗脱程序见表 1。
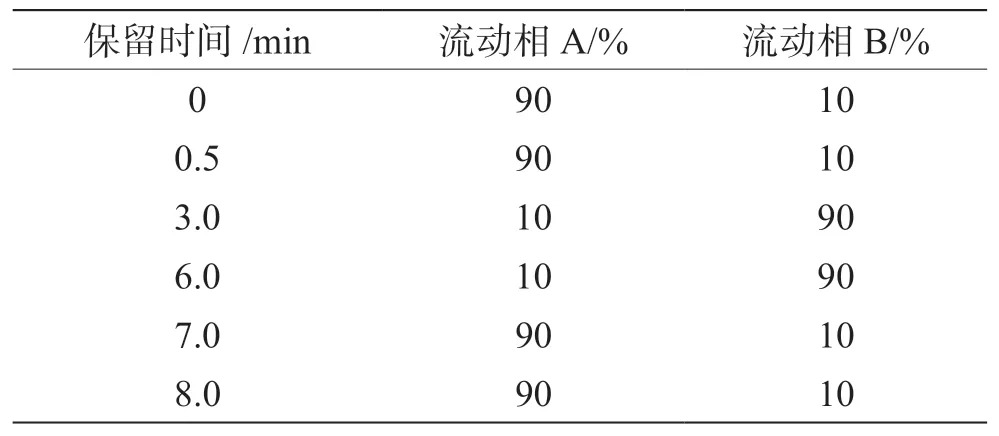
表1 色谱梯度洗脱程序
(2)质谱条件。电喷雾电离源(ESI);扫描模式为正离子模式;采集选用多反应监测(MRM)模式;喷雾电压4 500 V,关键质谱条件参数见表2。
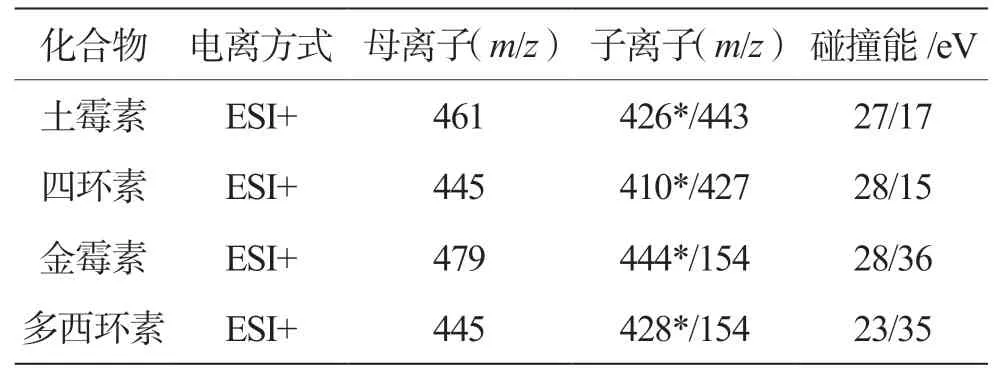
表2 4种抗生素化合物离子对和碰撞能量参数
1.2.4 不确定度数学模型的建立
罗非鱼样品抗生素含量计算公式:

式中:X为罗非鱼样品各组分残留量,μg·kg-1;C为标准曲线读取得到抗生素的浓度,ng·mL-1;V为罗非鱼样品提取液定容体积,mL;F为罗非鱼样品提取液稀释倍数;m为罗非鱼样品取样量,g。
2 结果与分析
2.1 罗非鱼样品前处理过程引入的相对标准不确定度urel(q)
2.1.1 样品称量过程引入的相对标准不确定度urel(m)
样品使用Mettler Toledo XS 204 万分之一电子天平进行称量,经检定得该最大允许误差为±0.05 mg,结合《数字指示秤检定规程》(JJG 539—2016)[15]规定,按均匀分布,取则不确定度为称量样为2.0 g,计算得样品称量引入的相对标准不确定度为urel(m)=u(m)/m=1.44×10-5。
2.1.2 罗非鱼样品提取液定容引入的相对标准不确定度urel(t)
样品按1.2.1法处理后用定容至1 mL,根据《常用玻璃量器检定规程》(JJG 196—2006)[16]规定,20 ℃时,1 mL容量瓶容量允差为±0.01 mL,按均匀分布,取则容量允差的标准不确定度操作过程温度为25 ℃,经查甲醇膨胀系数为1.1×10-3℃-1,得出体积变化产生的不确定度为1 mL×1.1×10-3℃-1×5 ℃=0.005 5 mL,按均匀分布计算,则计算得该容量瓶定容引入的相对标准不确定度为
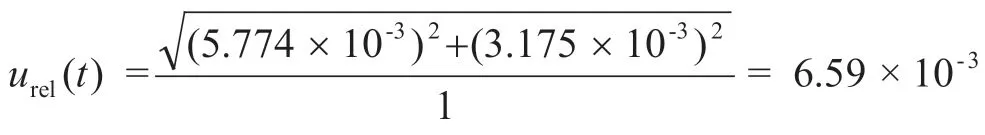
则罗非鱼样品前处理过程引入的相对标准不确定度为
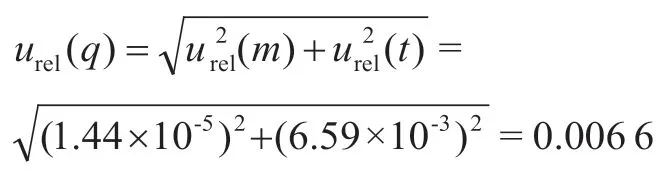
2.2 标准储备液配制引入的相对标准不确定度urel(p)
2.2.1 标准品纯度不确定度urel(pc)
以土霉素为例,土霉素标准品纯度93.8%,其纯度标准偏差为6.2%。按均匀分布计算,取则
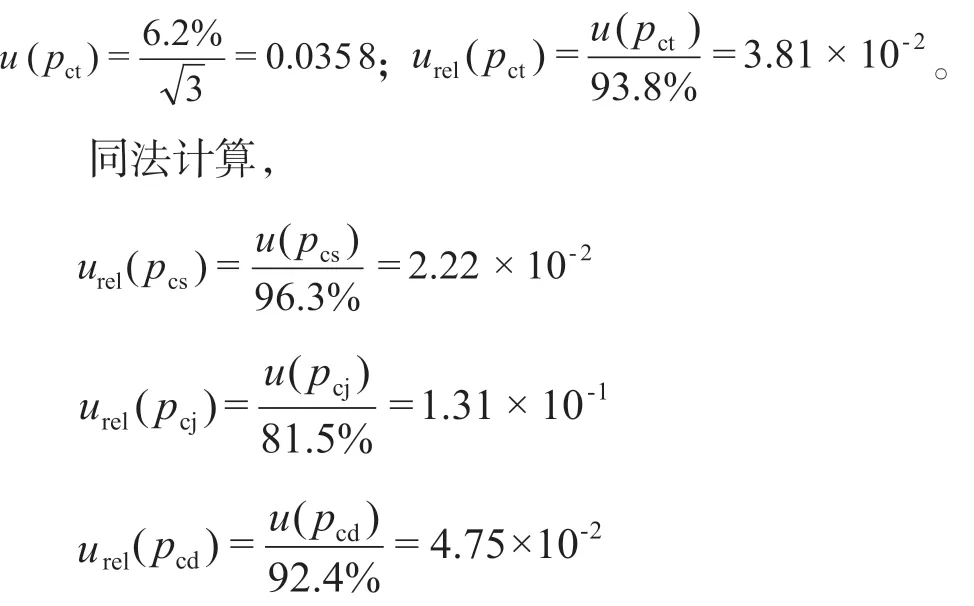
2.2.2 标准品稀释引入的相对标准不确定度urel(pr)
(1)1 mL容量瓶引入的相对标准不确定度urel(pr1)。容量瓶和移液器的使用是标准品稀释过程引入不确定度的主要因素,根据《常用玻璃量器检定规程》(JJG 196—2006)规定,20 ℃时,1 mL容量瓶容量允许误差为±0.01 mL,按均匀分布计算,取则经查乙腈膨胀系数为1.37×10-3℃-1,操作过程温度为25 ℃,则体积变化产生的不确定度为 1×1.37×10-3×5=0.006 9 mL,按均匀分布计算,
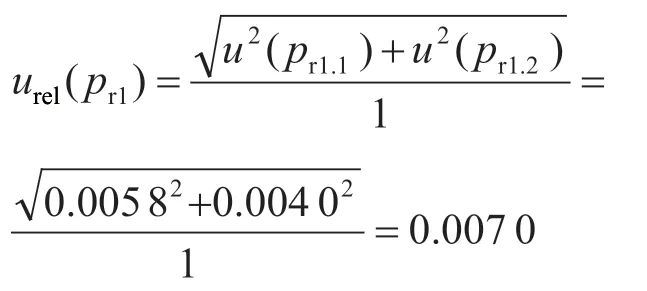
(2)10 mL容量瓶引入的相对标准不确定度urel(pr2)。20 ℃时,10 mL的容量瓶容量允许误差为±0.02 mL,按均匀分布计算,取则

经查甲醇的膨胀系数为1.1×10-3℃-1,操作过程温度为25 ℃,则体积变化产生的不确定度为10×1.1×10-3×5=0.055 mL,按均匀分布,则
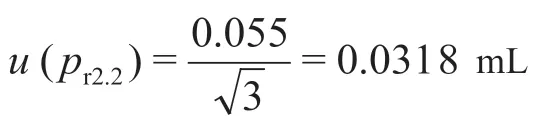
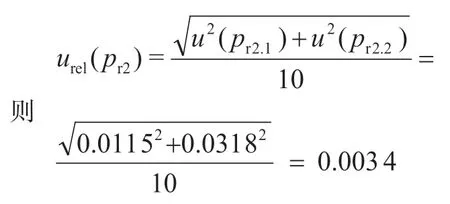
(3)移液器引入的相对标准不确定度urel(pr3)。根据《移液器检定规程》(JJG 646—2006)[17]及检定证书,20 ℃时,100~1 000 μL移液器在吸取1 mL溶液时最大容量允差为1 000×1.0%,按均匀分布,取则经查甲醇膨胀系数为1.1×10-3℃-1,操作过程温度为25 ℃,则体积变化产生的不确定度为 1 000×1.1×10-3×5=3.175 μL,按均匀分布计算,则
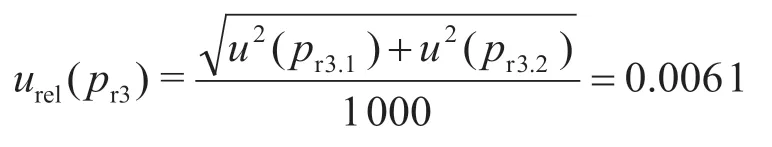
同理,计算其他量程移液器的相对标准不确定度。移液器移取不同体积溶液产生的相对标准不确定度见表3。
综上所述,计算不同药品的标准溶液配制引入的相对标准不确定度。以土霉素为例,根据实际稀释过程来选择移液器,由表3计算可得标准系列溶液配制引入的相对标准不确定度,则
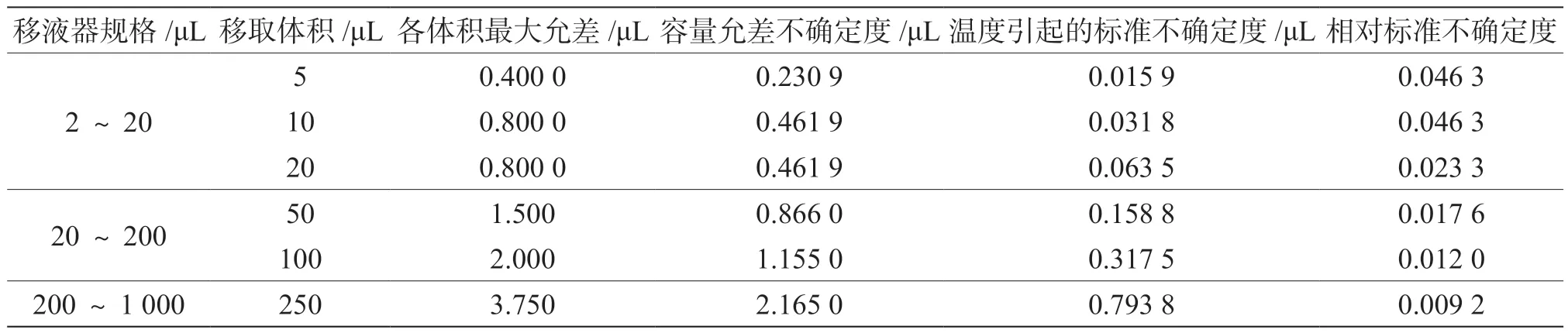
表3 移液器使用引入的不确定度
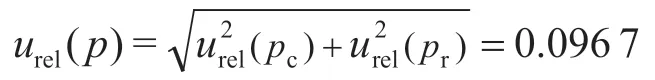
4种化合物配制过程中容量瓶及移液器使用情况均相同,同法计算,各相对标准不确定度结果见表4。

表4 不同药品的标准溶液配制引入的相对标准不确定度urel(p)
2.3 标准曲线拟合引入的相对标准不确定度urel(n)
标准工作曲线按照方法要求对6个点进行测定,经最小二乘法线性拟合得到各化合物浓度与对应峰面积及相应线性方程,结果见表5。
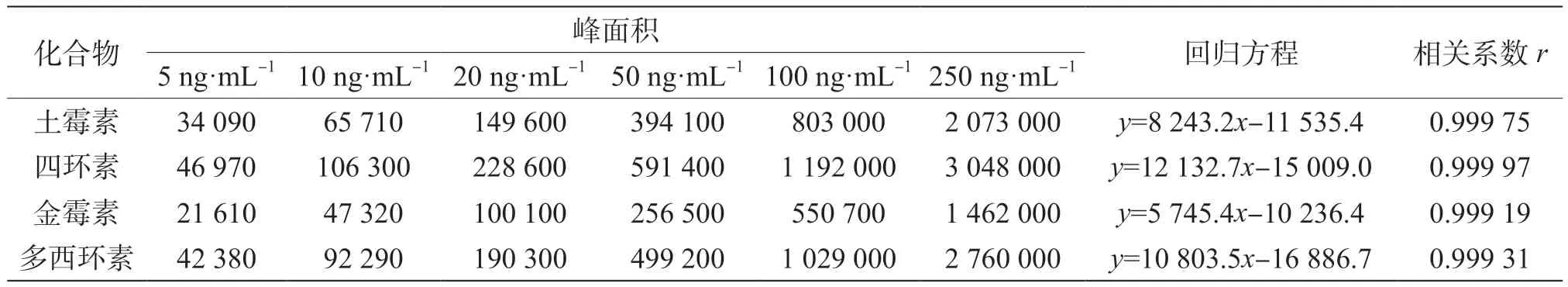
表5 4种抗生素化合物标准系列溶液的标准曲线回归方程及相关系数
标准曲线拟合相对标准不确定度计算公式为
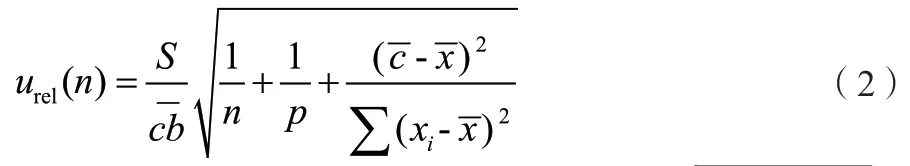
式中:S为拟合曲线标准偏差,b为线性回归方程斜率;c为提取液各次测定得到的浓度;n为标准曲线系列溶液测定总数(n=6);p为提取液重复测定次数(p=6);x为化合物各标曲点浓度。
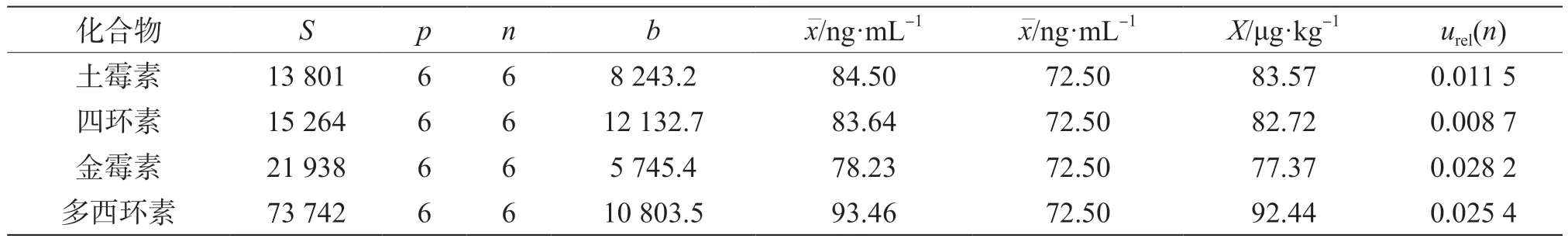
表6 标准曲线拟合引入的不确定度相关值
2.4 合成相对不确定度评定
各化合物不确定度分量互不相关,综合上述,罗非鱼中土霉素、四环素、金霉素、多西环素含量测定结果的合成相对不确定度结果见表7。

表7 4种抗生素化合物的合成相对不确定度
2.5 测量不确定度报告
罗非鱼样品中土霉素、四环素、金霉素、多西环素含量检测结果分别为 83.57 μg·kg-1、82.72 μg·kg-1、77.37 μg·kg-1、92.44 μg·kg-1,参照《测量不确定度评定与表示》(JJF 1059.1—2012)和《化学分析测量不确定度评定》(JJF 1135—2005)[18],在P=95%置信概率下,选择包含因子k=2,以土霉素为例,则扩展不确定度测定结果最终结果表示为Xt=(83.57±16.31)μg·kg-1(k=2)。同法计算,四环素、金霉素、多西环素的最终结果分别表示为Xs=(82.72±15.24)μg·kg-1(k=2)、Xj=(77.37±24.90)μg·kg-1(k=2)和Xd=(92.44±19.25)μg·kg-1(k=2)。
3 结论与讨论
本研究相较于最新国标方法,对前处理过程进行两方面的改进,分别为采用乙腈(含1%甲酸)作为提取溶液代替乙二胺四乙酸二钠、醋酸铅的3次重复提取过程;采用PRime HLB固相萃取柱代替Oasis HLB萃取柱,净化过程不需要活化、淋洗及洗脱。该方法的测量不确定度报告显示的扩展不确定度为15.24~24.90,许莺婷等[19]测定鱼粉中诺氟沙星、环丙沙星和恩诺沙星残留量,扩展不确定度为3.42~38.84。结果表明,改进后的方法操作简单、分析时间短、准确性高。
根据该方法的数学模型,对实验过程中样品前处理、标准溶液配制过程、标准曲线拟合3个方面进行数据分析,结果显示,标准溶液配制过程和标准曲线拟合引入的不确定度最大,其次是样品前处理过程。为减少标准溶液配制过程中产生的误差,建议使用较高纯度标准品、定期校准容量瓶及移液器。另外,通过增加平行样及平行测定次数,从而提高测定结果的准确性。
