纳米零价铁改性生物炭对污染土壤中Cd稳定化效果及作用机制研究
2022-12-02许亚琼王雪佳李荣华肖然张增强
许亚琼,王雪佳,李荣华,肖然,张增强*
(1.西北农林科技大学资源环境学院,陕西 杨凌 712100;2.西南大学长江经济带农业绿色发展研究中心,重庆 400715;3.西南大学资源环境学院,重庆市土肥资源高效利用重点实验室,重庆 400715)

当前农田土壤重金属污染已经成为了亟待解决的环境问题[1]。在众多重金属污染物中,镉(Cd)由于其较强的生物毒性、易迁移和易生物累积的特点而备受关注[2]。作为耕地土壤中的首要污染物,Cd 的点位超标率超过7.0%[3]。近年来,随着我国北方地区土壤以及主要粮食作物Cd 超标事件的曝出,中碱性农田土壤的Cd 污染已经引起社会的广泛关注[4-5]。王婷等[6]在调研天津污灌区农田土壤重金属污染时发现土壤中 Cd 的超标率为 43%(0.09~3.5 mg·kg-1),且60%的油麦菜受到Cd的污染。前期在陕西省潼关县土壤重金属污染调查中,课题组也发现农田土壤Cd的超标率高达78.4%,12.0%的小麦样品中Cd 含量超过了食品中污染物限量标准中的限值(GB 2762—2005)。因此,开展中碱性Cd污染农田土壤的修复对于保障区域农产品安全具有重要意义。
纳米零价铁(nano zero-valent iron,nZVI)作为一种环境友好材料,具有丰富的活性表面位点、较高的反应活性和比表面积,在有毒重金属(特别是Cd)的去除/稳定化方面受到了广泛的关注[7-8]。但是材料易氧化和易团聚的特性限制了其实际应用的效果,而以生物炭作为载体,进行纳米零价铁改性可以有效解决以上问题[9]。当前,国内外学者在利用纳米零价铁改性生物炭(nZVI-BC)对液相中Cd(Ⅱ)的去除方面开展了大量的研究工作[10-11]。但是,有关nZVI-BC 对土壤中Cd 的稳定化,特别是对中碱性土壤中Cd 的稳定化效果和长效稳定化作用机制的研究还比较缺乏,有关材料老化过程中Cd与nZVI-BC 界面相互作用的机制和环境因素对土壤的Cd稳定化过程的影响还缺乏系统的研究[12]。基于此,本研究以玉米秸秆制备的生物炭为载体负载nZVI,选择Cd为目标污染物,采用批试验与养护试验相结合的方法,并利用现代光谱分析技术,研究了nZVI-BC 对中碱性土壤中Cd 的稳定化作用过程和反应机制,以期为中碱性Cd 污染土壤的稳定化修复提供技术与产品支撑。
1 材料与方法
1.1 生物炭的制备与改性
玉米秸秆采集自西北农林科技大学实验农场。样品采集后,切成5~8 cm 的小段,用去离子水清洗去除表面浮土后置于烘箱内于105 ℃烘干。烘干后的玉米秸秆粉碎过筛(60 目)后备用。实验中所用试剂:NaOH、MgSO4、FeCl3·6H2O、C2H5OH、KBH4、HNO3、Cd(NO3)2·4H2O 等均购自国药集团化学试剂有限公司,纯度为分析纯。实验中所需的化学溶液均以去离子水配制。
原始生物炭(BC)的制备:以粉碎好的玉米秸秆为原料,采用限氧控温裂解法制备原始生物炭,即用马弗炉以5 ℃·min-1的升温速率升温至550 ℃,在峰值温度下保持1 h 后停止加热,冷却至室温。将制备的生物炭研磨过60目筛后备用。
纳米零价铁改性生物炭(nZVI-BC)的制备:nZ⁃VI-BC 采用常规液相还原法制备[13],在三颈烧杯中将9.625 g的FeCl3·6H2O 溶于200 mL乙醇和水的混合物(3/1,V/V),加入10 g 制备好的原始生物炭,于40 kHz超声30 min 后形成生物炭和铁的混合溶液,在通N2的条件下持续搅拌30 min,随后向混合溶液中滴入50 mL 硼氢化钾溶液(28.78 mg·L-1),混合搅拌30 min后结束反应;样品通过离心分离,用乙醇洗涤3 次后置于冷冻干燥机(Lab-1A-50,北京)中真空干燥得到nZVI-BC。样品存放于真空干燥器中备用。
1.2 吸附试验
1.2.1 吸附动力学试验
称取(0.400 0±0.000 5)g生物炭样品(BC或nZVIBC)置于250 mL 锥形瓶中,加入200 mL 浓度为250 mg·L-1的 Cd(Ⅱ)溶液(pH=6±0.2),在 25 ℃、180 r·min-1条件下恒温振荡24 h,每隔一段时间(0、2、5、10、20、30、45、60 、90、120、180、240、360、480、600、720、1 440 min)吸取上清液 2 mL,溶液过 0.45 µm 滤膜后用火焰原子吸收光谱仪(FAAS ICE 3500,Thermo Fisher,美国)测定其中Cd的含量。
1.2.2 等温吸附试验
称取(0.020 0±0.000 5)g 生物炭样品置于一系列50 mL离心管中,加入10 mL初始浓度分别为0、5、10、25、50、100、200、250、500、1 000 mg·L-1的Cd(Ⅱ)溶液(pH=6±0.2),在 25 ℃、180 r·min-1条件下恒温振荡吸附24 h后用火焰原子吸收光谱仪测定其中Cd的含量。
1.3 养护试验
1.3.1 供试土壤
采集学校实验田表层土壤(0~20 cm)样品,自然风干后去除碎石和植物残茬,过2 mm 筛备用。土壤理化性质:pH 为(8.36±0.10),EC 为(134±1.2)µS·cm-1,有机质含量为2.46%,土壤Cd 含量为0.054 mg·kg-1。通过外源喷施含Cd 溶液的方式制备人工Cd 污染土壤(Cd含量为2.976 mg·kg-1)[14]。
1.3.2 土培试验
根据生物炭添加类型、土壤含水率和污染程度(清洁和污染)共设置8个处理(T1~T8,表1)。在塑料盒(19.5 cm×14.2 cm×5 cm)中装入Cd污染土壤(1 kg),然后埋入含生物炭(0.25 g)的尼龙网袋(600目、5 cm×5 cm),将塑料盒转移至人工气候箱内进行为期90 d的静态养护试验。养护温度为20 ℃,光照周期为16 h∶8 h(光∶暗),每隔3 d将旱地条件处理翻搅一次,每日按质量法补充去离子水至表1 要求的含水量,分别模拟水田和旱地两种环境条件进行养护试验。分别于养护后第0、3、7、14、31、62、90 天取样,每次取出3个炭包,用去离子水冲洗干净,真空冷干后将3 个炭包中的样品混合均匀并转移至塑封袋中于真空干燥器中保存备用。利用电感耦合等离子体原子发射光谱仪(ICP,Agilent 720)、傅里叶红外光谱仪(FTIR,Nicolet 670,美国)和 X 射线光电子能谱仪(XPS,Thermo Scientific Escalab 250Xi,美国)对材料进行分析,测定材料中Cd 的含量和分布情况以及材料的结构特性。

表1 土壤养护试验设计Table 1 Simulation trials designed in this study
1.4 材料表征与理化性质分析
将生物炭与高纯水以 1∶20(m∶V)的固液比,在180 r·min-1、25 ℃条件下恒温振荡 1 h 后,利用 pH 计和电导率仪测定上清液的pH 和EC;使用元素分析仪测定了生物炭上C、N、S、H 的含量(EA,UNICUBE,艾利蒙塔,德国);采用马尔文Malvern Zetasizer Nano ZS90 zeta电位分析仪测定了生物炭的Zeta电位;利用多孔物理吸附仪(BET,EVO,康塔,美国)分析了生物炭的比表面积和孔径分布,用场发射扫描电子显微镜(SEM,Zeiss Sigma 300,英国)以及布鲁克电制冷X 射线能谱仪(EDS,XFlash6I30,布鲁克,美国)对生物炭的形貌及表面元素分布进行了表征,用傅里叶红外光谱仪(FTIR,Nicolet 670,美国)对生物炭的表面官能团进行了测定。使用X 射线衍射研究了生物炭的表面晶体组成(XRD,Smartlab 9,日本),用X 射线光电子能谱仪(XPS,Thermo Scientific Escalab 250Xi,美国)分析了生物炭表面元素(Fe、C、O)的价态,用电感耦合等离子体原子发射光谱(ICP,Agilent 720,美国)测定养护后生物炭中的Cd含量。
1.5 数据处理
材料对溶液中Cd(Ⅱ)吸附量的计算公式如下:

式中:qe是在平衡浓度Ce时吸附剂的平衡吸附容量,mg·g-1;C0是溶液中吸附质的初始浓度,mg·L-1;Ce是达到吸附平衡时溶液中吸附质的浓度,mg·L-1;V是吸附溶液的体积,L;m是吸附剂质量,g。
采用伪一级动力学方程(Pseudo-first-order)和伪二级动力学方程(Pseudo-second-order)对数据进行非线性拟合:
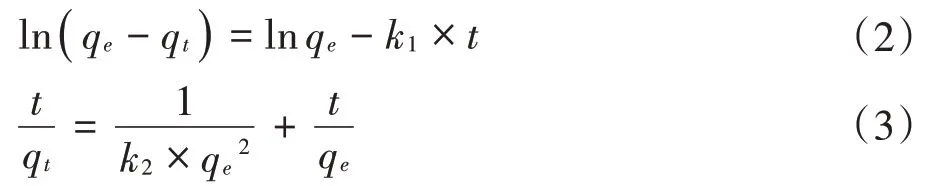
式中:qt是在t时刻吸附剂对吸附质的吸附量,mg·g-1;k1(min-1)和k2(mg·g-1·min-1)分别为伪一级动力学常数和伪二级动力学常数。
分别采用Langmuir 和Freundlich 方程对等温吸附数据进行拟合:

式中:Qmax是吸附剂的理论最大吸附量,mg·g-1;KL是结合常数,L·mg-1;KF是与吸附容量和吸附强度有关的常数,(mg·g-1)(L·mg-1)1/n;n是Freundlich常数。
采用Excel 2010 软件对数据进行初步处理;使用SPSS 22.0 软件进行单因素方差分析,在0.05 的概率水平下观察不同处理之间是否存在差异;采用Origin 9.0软件制图。
2 结果与讨论
2.1 生物炭的理化性质及形貌结构
如表2所示,BC和nZVI-BC均呈碱性且BC的pH值略高于nZVI-BC,这可能与改性过程中盐基离子的损 失 有 关[15]。 BC 和 nZVI-BC 的 pHpzc分 别 为 6.14 和5.95,表明两种材料均可以通过静电吸附的方式吸附溶液中的Cd(Ⅱ)。由于nZVI的负载,nZVI-BC中C、N、S的含量均有不同程度的下降,这与本课题组之前的研究结果类似[16]。同时,nZVI的负载使得nZVI-BC的比表面积与孔体积也有所下降,但平均孔径略微增加。

表2 BC和nZVI-BC的理化性质比较Table 2 Comparison of physicochemical properties of BC and nZVI-BC
图1a 为BC 和nZVI-BC 吸附前的红外光谱。两种材料表面均含有丰富的官能团:在3 050~3 600 cm-1处的谱带与纤维素或氧化铁引起的伸缩振动有关[17],在 1 595 cm-1和 1 619 cm-1附近的 峰归因于的 伸 缩 振 动 ,在 880 cm-1/800 cm-1和460 cm-1处的峰分别对应芳香族而在波数1 090 cm-1处的峰则是纤维素/半纤维素主链上的nZVI 负载进一步增加了生物炭表面官能团的丰富度,表现为:1 439 cm-1处对应的COOH,1 349 cm-1处对应的,1 210 cm-1处对应的键,1 005 cm-1处对应的键,930 cm-1处对应的NH3键。红外图谱中,717 cm-1处对应的以及在576 cm-1处观察到的键[19-20],表明nZVI 已被成功负载到生物炭表面。而且,X 射线衍射图谱中Fe0特征峰(2θ=44.67°)的出现(图1b),也说明了nZVI 的成功负载[21]。此外,从扫描电镜-能谱图谱中可以发现富含铁元素的球形颗粒随机分布在生物炭表面(图1c~图1f);nZVI-BC 材料表面Fe 的含量约为17.49%,这与理论负载量十分接近,说明nZVI主要负载在生物炭的表面,这也与本课题组以往的结果类似[22]。

图1 BC和nZIV-BC的FTIR图谱(a);BC和nZIV-BC的XRD图谱(b);BC(c)和nZIV-BC(d)SEM显微照片;nZIV-BC的Mapping图谱(e);nZIV-BC的EDS图谱(f)Figure 1 Images of FTIR spectra(a)and XRD spectra(b)of BC and nZIV-BC;SEM micrographs of BC(c)and nZIV-BC(d);Mapping spectra of nZIV-BC(e)and EDS spectra of nZIV-BC(f)
2.2 (改性)生物炭对溶液中Cd(Ⅱ)的吸附特性
2.2.1 吸附动力学
如图 2 所示,BC 和 nZVI-BC 对 Cd 的吸附量均随着时间的增加而增加进而趋于平稳,这与材料表面吸附位点逐步被占据有关[23]。BC对溶液中Cd(Ⅱ)的吸附速率较慢,反应在12 h之后才能达到动态平衡。相比而言,nZVI 的负载显著提高了材料对Cd 的吸附速率,超95%的Cd 吸附发生在反应开始的前0.5 h,材料对Cd(Ⅱ)的吸附在3 h 之后达到了动态平衡。为了进一步掌握材料对Cd 的吸附动力学特性,对吸附结果进行了动力学模型拟合,具体参数如表3 所示。相较于伪一级动力学模型,BC 和nZVI-BC 在吸附过程中都更符合伪二级动力学模型,表现为较高的回归系数,说明BC和nZVI-BC 对溶液中Cd的吸附以化学吸附为主[24]。

表3 BC与nZVI-BC关于Cd(Ⅱ)吸附的伪一阶和伪二阶动力学模型参数Table 3 Pseudo-first order and Pseudo-second order fitting parameters for Cd(Ⅱ)adsorption by BC and nZVI-BC
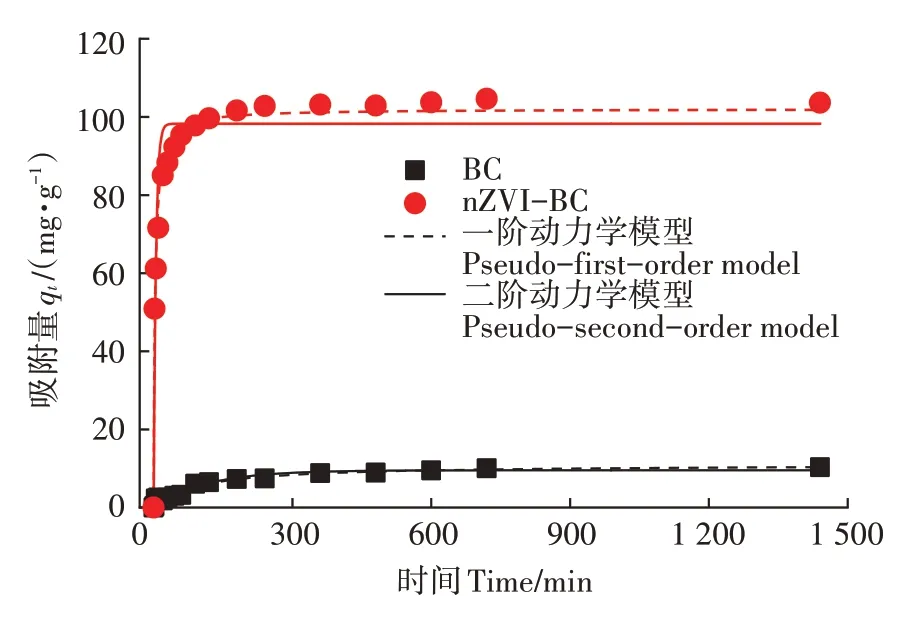
图2 BC与nZVI-BC关于Cd(Ⅱ)吸附的吸附动力学及拟合模型Figure 2 Adsorption kinetics and fitted models of Cd(Ⅱ)adsorption on BC and nZVI-BC
2.2.2 吸附等温线
图3为BC和nZVI-BC对溶液中Cd(Ⅱ)吸附的等温曲线。两个材料对于Cd(Ⅱ)的吸附均呈非线性且材料对Cd 的吸附量均随初始Cd 浓度的增加而增加。通过Langmuir 和Freundlich 模型对数据进行拟合发现:Langmuir 模型能够更好地拟合吸附数据,表现为较高的回归系数(0.99 vs 0.96)(表4),表明材料对Cd的吸附为单分子层吸附[25]。nZVI-BC 对Cd(Ⅱ)的饱和吸附量为 125.5 mg·g-1,是 BC 的 5.3 倍,这与负载的nZVI为Cd(Ⅱ)的吸附提供额外的吸附位点有关。相比而言,YANG 等[26]的研究发现负载nZVI的生物炭对溶液中Cd(Ⅱ)的饱和吸附量仅为33.81 mg·g-1。本研究中生物炭上更高的nZVI 负载是造成Cd 吸附量差异的主要原因[27]。

表4 BC和nZVI-BC关于Cd(Ⅱ)吸附的Langmuir和Freundlich模型拟合参数Table 4 Langmuir and Freundlich model fitting parameters for Cd(Ⅱ)adsorption by BC and nZVI-BC

图3 BC和nZVI-BC关于Cd(Ⅱ)吸附的Freundlich和Langmuir等温线Figure 3 Freundlich and Langmuir isotherms of Cd(Ⅱ)adsorption on BC and nZVI-BC
2.3 (改性)生物炭对Cd污染土壤的稳定化机制研究
表5 为养护试验各个阶段BC 和nZVI-BC 上Cd含量的动态变化。随着养护时间的增加,BC 上负载的Cd 含量呈上升趋势。养护90 d 后,在模拟旱地环境条件下,BC 中 Cd 的含量为 1.53 mg·kg-1,略高于模拟水田土壤条件下的1.10 mg·kg-1。类似地,陈昱等[28]将玉米秸秆生物炭老化2个月后,发现其对于Cd的固定量在原来的基础上提升了12.9%。在旱地和水田模拟条件下,nZVI-BC 对Cd 的负载量分别在第14 天(852.16 mg·kg-1)和第 3 天(1 511.20 mg·kg-1)达到峰值。此后,随着反应时间的增加,nZVI-BC 对Cd的负载能力呈现下降的趋势。尽管如此,养护90 d后nZVI-BC 上Cd 的负载含量[111.20 mg·kg-(1水田)和192.33 mg·kg-(1旱地)]也远高于BC的。
不同处理条件下BC表面官能团的动态变化如图4a所示。相比于未经老化的BC样品,在1 439 cm-1左右处出现了峰,并且在 3 376~3 429、1 595~1 619、1 090、800 cm-1和461 cm-1处的峰的强度增加,说明经过老化之后生物炭表面的含氧官能团的强度和种类有所增加。类似地,黄兆琴等[29]发现经过化学老化后,生物炭表面羟基、羧基、酮羰基、脂肪醚、酯基等含氧官能团的含量均有不同程度的变化。研究发现生物炭老化过程中在其表面形成的含氧官能团对材料Cd(Ⅱ)吸附具有重要的意义[30-31]。相比于初始生物炭,老化生物炭对土壤Cd 具有更强的吸附能力[32],且这些被固定的Cd 具有更强的稳定性[33]。这主要是因为表面含氧官能团提供的孤对电子可以进入金属离子的空轨道,从而产生强配位配合物[34-35]。因此,老化后BC 上含氧官能团的增加是导致其Cd 负载量增加的主要原因。尽管如此,也有研究发现老化处理降低了生物炭对Cd 的吸附,这可能与材料中无机组分在老化过程中的损失有关[12,31]。养护前后,nZVI-BC 上表面官能团的变化与BC 类似(图4b)。值得注意的是,nZVI-BC 上存在的峰(576 cm-1)在养护过程中逐渐削弱直至消失,结合nZVI-BC 上Fe 元素含量的变化(表5)以及材料上Cd负载量的变化,表明Fe 的形态和含量的变化是导致nZVI-BC对Cd负载量变化的关键。

图4 BC(a)and nZVI-BC(b)在养护试验中的FTIR光谱Figure 4 FTIR spectra of BC(a)and nZVI-BC(b)in simulation trials

表5 养护试验各个阶段BC和nZVI-BC上Cd的负载量Table 5 Load capacity of Cd on BC and nZVI-BC in each stage of simulation trials
XPS 的结果分析发现(图5):对于nZVI-BC,养护前后其C 元素大多以C(Ⅰ)284.8 eV的形式存在[36-37]。随着养护的进行,nZVI-BC 中C(Ⅱ)和C(Ⅲ)峰的相对分布占比增加,说明吸附过程出现了含氧官能团与Cd(Ⅱ)发生沉淀和络合作用,与表面官能团形成键,主要是以Cd(OH)2和CdO以及CdCO3的形式存在[38],同时还包括键的形成[39]。因此,在nZVI-BC 表面土壤中的Cd 以金属氧化物、碳酸盐沉淀形式被固定或以有机功能基团形式被络合,这也与FTIR的结果相一致。

图5 nZVI-BC在养护实验中反应前后的XPS谱图:(a)宽扫描谱图;(b)C1s扫描谱图;(c)O1s扫描谱图;(d)Fe2p扫描谱图Figure 5 XPS spectra of nZVI-BC before and after the reaction in the simulation trials:(a)wide-scan spectra,(b)C1s narrow scan spectra,(c)O1s narrow scan spectra,and(d)Fe2p narrow scan spectra

随着nZVI-BC的不断氧化,nZVI-BC表面会形成厚的铁氧矿物,使得被包裹其中的Fe0核难以再起到还原作用,进而使得其对Cd固定效果减弱;而水田模拟条件下,nZVI-BC在刚开始的有氧土壤环境中,可以通过电化学腐蚀(式6和式7)释放出Fe(Ⅱ),并快速生成铁的氧化矿物来固定Cd,此外,nZVI电化学腐蚀过程会产生OH−,这将使得Cd主要通过形成氢氧化物沉淀被固定(式8),但随着溶解氧被消耗,产生的Fe(Ⅱ)将会以游离态存在于土壤溶液中,nZVI-BC上的Fe含量相应减少,这就使得Cd的固定量总体下降更为明显。
3 结论
(1)nZVI 改性显著提高了生物炭对于Cd(Ⅱ)的吸附。相比于原生生物炭,nZVI 改性生物炭(nZVIBC)对 Cd 的饱和吸附量达 125.5 mg·g-1,为原始生物炭的5.3倍。
(2)nZVI-BC 对于Cd 污染土壤中Cd(Ⅱ)的稳定化机制包括沉淀、共沉淀及与生物炭表面含氧官能团络合。
(3)nZVI-BC 对Cd 污染土壤中Cd(Ⅱ)的稳定效果受反应时间的影响较大,旱地和水田模拟条件下材料对Cd 的稳定化效果也存在明显的差异,随着养护时间的增加,材料对Cd 的稳定化效果逐渐减弱但仍保持在较高水平且远高于生物炭。
