开放性零缺血结合同步切缝技术在复杂性孤立肾肾癌治疗中的应用
2022-11-30滕立臣王文涛李浩潘宏鑫李长福
滕立臣 王文涛 李浩 潘宏鑫 李长福
因先天性或后天性获得因素导致一侧肾脏切除或失去功能,仅留存对侧肾被称为孤立肾,发病率极低,据统计仅为0.5‰~2.0‰[1-2]。孤立肾罹患肾癌更为罕见,肾部分切除术是主要的治疗方式。与单侧散发性肾癌不同,因必须兼顾保证有良好的肿瘤学和肾功能结果,对于大多数泌尿外科医生来说其治疗仍然具有较大的挑战性。近年来,腹腔镜及机器人辅助腹腔镜技术在肾部分切除术方面发展迅速,但对于肿瘤体积较大(T1b 及以上)、位置接近肾门部或内生性等复杂性孤立肾肾癌,在肾部分切除术时,为保证手术顺利进行需阻断肾动脉,而随着肾脏缺血时间的延长,会不可避免损害肾功能,因而导致肌酐升高和少尿,甚至无尿。虽然腹腔镜(包括机器人辅助腹腔镜)手术已广泛应用,但也需要阻断动脉,否则可能引起出血,造成操作困难或其他严重术中及术后并发症。为了避免这种不利因素、最大限度保留肾单位和减少肾脏缺血再灌注损伤,零缺血肾部分切除术可全程保持肾脏正常的血液灌注无疑是最佳选择。本研究旨在通过对开放性零缺血结合同步切缝的肾部分切除术进行探讨,为复杂性孤立肾肾癌的治疗提供借鉴。
1 材料与方法
1.1 临床资料
回顾性分析2017 年10 月至2021 年10 月5 例于哈尔滨医科大学附属肿瘤医院诊治的复杂性孤立肾肾癌患者的临床资料,包括年龄、性别、体质指数(BMI)、侧别、临床TNM 分期、肿瘤直径、手术时间、术中出血量、术前及术后的肌酐、尿素氮及胱抑素变化、术后并发症及肿瘤学结果等,其中因一侧行肾癌根治术后对侧的肾脏继发肾癌3 例、先天性功能性孤立肾肾癌1 例、先天性解剖性孤立肾肾癌1 例。病理结果均为肾透明细胞癌,肿瘤直径≥7 cm 为 2 例,4 例肾癌Fuhrman 分级为2 级、1 例为3 级,由单一术者完成开放性零缺血结合同步切缝的肾部分切除术。适应证:1) 临床分期T1b 及以上;2)肾窦部肿瘤,包括肾门前唇或后唇肿瘤;3)内生性肿瘤;4)需行半肾切除术患者。
1.2 方法
1.2.1 手术方法 患者麻醉后,取健侧卧位,后取患侧第11 肋间切口,进入腹膜后间隙,切开侧椎筋膜后显露肾动脉,根据影像学的结果在肿瘤边缘处切开肾周脂肪,但保留肿瘤表面的脂肪,显露输尿管。对于肾门部肿瘤,沿输尿管向上显露肾门部肾肿瘤,明确肿瘤与肾盂壁及肾动脉和静脉之间的解剖关系,避免切除过程中损伤上述结构。紧邻肾盂,距离肿瘤边缘约0.5 cm 处使用组织剪切开肾实质,沿着肿瘤的轮廓始终在肿瘤周围正常肾组织内保持切除,小的静脉出血点使用电刀或双极电凝钳止血,对于叶间动脉断端的搏动性出血或较大的静脉出血则使用可吸收3-0 倒刺线垂直于血管方向连续缝合或“8”字缝合,对于肾段动脉出血也可以采用2-0 倒刺线于尾端夹一枚Hemlock夹,经出血点邻近的肾被膜入针,跨过出血点出针,轻轻牵拉,必要时再贯穿出血点缝扎,均能确切止血,保持术野清晰继续切除剩余部分的肿瘤,以利于精准切除肿瘤,避免切破肿瘤包膜造成癌细胞播散种植,保持肾脏的血供。为了保证无瘤操作,避免针尖刺破包膜,缝合方向多是背向肿瘤,即由内向外反针缝合,如果肾集合系统切开也一并缝合,直至肿瘤完整切除,再完整缝合肾组织创面的基底部,根据出血情况必要时加缝一层。再根据肿瘤的位置使用2-0 可吸收倒刺线行连续锁边缝合(肾窦部肿瘤)或肾脏切缘连续缝合(肾上下极肿瘤)。最后检查肾缝合创面无出血后再使用可吸收线连续缝合肾周脂肪囊,覆盖肾脏切缘。
1.2.2 随访 术后采用定期门诊复查或电话随访。每3~6 个月随访1 次,包括病史、体格检查、血常规、血生化检查、胸部及腹部超声或CT 检查。随访时间为3~48 个月,平均随访30.4 个月,最近1 次随访5例患者肾功能均在正常范围。
1.3 统计学分析
采用SPSS19.0 软件进行统计学分析。采用配对样本t检验分析术前及术后肾功能肌酐、尿素氮及胱抑素水平。以P<0.05 为差异具有统计学意义。
2 结果
2.1 手术情况
5 例患者均采用零缺血结合同步切缝技术顺利完成手术(表1)。手术过程见图1A~C,同步切缝技术的要点见图1D,全部患者无中转肾动脉阻断,亦无中转根治性肾切除术。手术时间为135~180 min,平均手术时间165 min,术中失血量分别为300~700 mL,平均失血量450 mL,患者均在术后第1 天下床活动,术后住院时间为6~8 天。

图1 开放性零缺血结合同步切缝技术的术中操作视野及关键步骤示意图
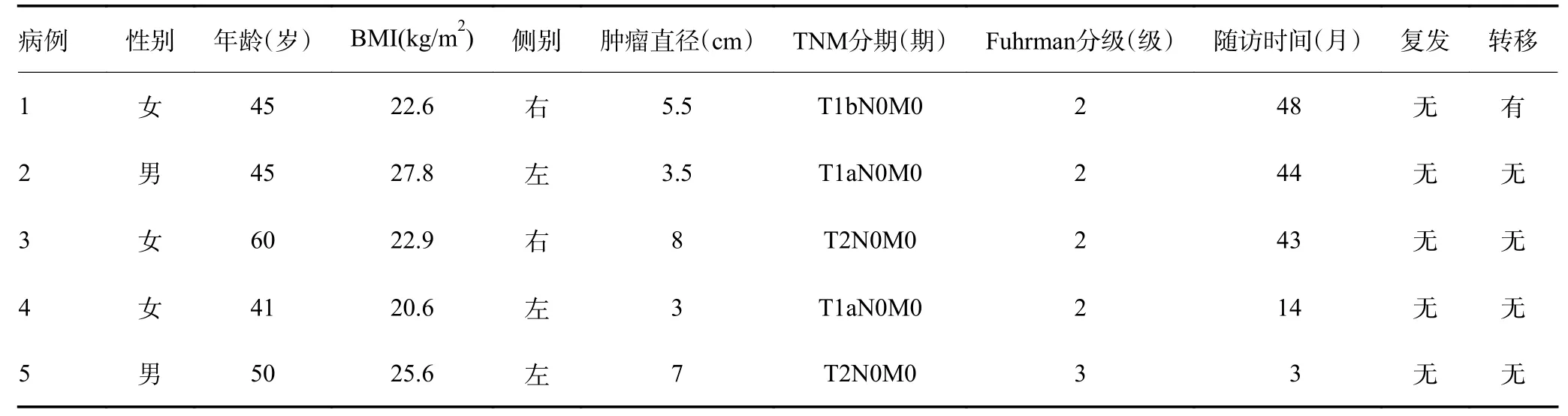
表1 患者的临床资料
2.2 术后肾功能的变化
与术前肾功能相比,除1 例患者术后第1 天肌酐升高明显外,由术前126 μmol/L 升高到174 μmol/L,其余4 例均无明显升高。术前与术后第1 天、第3 个月、第1 年和第2 年的血肌酐、血尿素氮和胱抑素水平进行比较发现,除术后第1 年的胱抑素和第2 年的尿素氮外,其余时间的肌酐、尿素氮及胱抑素水平差异均无统计学意义(均P>0.05,表2)。
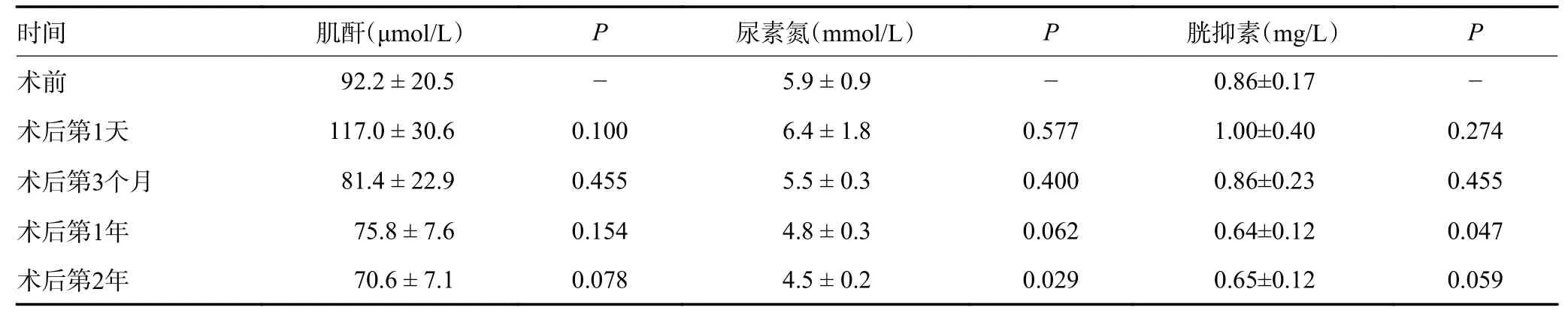
表2 患者的术前与术后肾功能变化
2.3 术后并发症
5 例患者中1 例术后第1 天出现尿漏,经行膀胱镜留置F6 双“J”管后,术后第2 天尿漏消失,其余4 例均未出现早期及晚期并发症。5 例患者中仅1 例于术后第2 年随诊检查胸部CT 发现右侧第8 肋骨转移,其余4 例随访中均无复发及转移。
3 讨论
目前,因孤立肾肾癌的保留肾单位术的风险高、难度大、并发症多及保肾要求高,仍是泌尿外科的难点之一。尽管设备与技术在不断进步,但国内外专家对于在诸多治疗方法中如何选择最佳的治疗策略尚缺乏共识。零缺血肾部分切除术在双肾的单发肿瘤中已有实施[3-4],但在复杂性孤立肾肾癌中鲜有报道。近年来,腹腔镜或机器人辅助的腹腔镜手术逐渐成为肾部分切除术的主流技术,但对于T1b 期及以上和复杂性孤立肾肾癌采用零缺血肾部分切除术仍存在着较大的风险。本研究采用开放性零缺血肾部分切除术结合同步切缝技术治疗复杂性孤立肾肾癌,在保护肾功能和减少术中失血并保持术野清晰方面有着独特的优点,并且经随访也证明了其良好的有效性和安全性。本研究的患者均未行过中转肾动脉阻断的肾部分切除术或根治性肾切除术,随访期内长期生存,并且保持良好的肾功能,取得了良好的结果。
开放性零缺血结合同步切缝技术较已开展的孤立肾肾癌的治疗方式有着明显的优势:1)常规阻断肾动脉后肾部分切除术除了出现肾缺血再灌注损伤外,部分患者可能出现肾动脉栓塞,由于长时间冷热缺血可发生不可逆性损伤,肾功能难以恢复,引起急性肾功能衰竭或慢性肾功能不全。尽管超选择性肾段动脉阻断被认为在保留功能方面有一定优势,但对于复杂性孤立肾肾门部较大肿瘤和多发肿瘤在技术上仍存在较大难度,而开放性零缺血结合同步切缝技术则有效避免了这一缺陷。2)肿瘤射频或微波消融术的优点是创伤较小,缺点是如果肿瘤体积较大或与肾动静脉及肾盂等结构距离近,将会增加血管和肾盂热损伤的风险,与标准的肾部分切除术相比,由于不切除肿瘤,复发的风险明显升高[5-7]。3)工作台手术及自体肾移植与开放性零缺血结合同步切缝技术有相似的适应证,但缺点是手术复杂,总手术时间长,需7~10 h,创伤大,并且需一定基础的肾移植技术作为保障[8-9],与之相比,开放性零缺血结合同步切缝技术则有无需吻合血管、无肾脏冷缺血并保持肾脏于原位等优点,使手术更加简化。
孤立肾肾癌的肾部分切除术具有更高的挑战性,并且术后早期和晚期并发症的风险高[10],常见的有尿漏、出血、急性肾功能衰竭等。本研究采用开放性零缺血及同步切缝技术被证明是安全有效的,在切除肿瘤、保护肾功能及降低并发症风险方面发挥了非常重要作用。常规的开放性零缺血肾部分切除术可能增加切缘阳性率,增加复发及发生并发症的风险[11],而同步切缝技术可始终保持清晰的手术视野,保证切除层面在正常的肾组织内,对肿瘤体积较大(T1b 期及以上)和复杂的肿瘤更有优势,弥补了腹腔镜或机器人辅助腹腔镜下零缺血肾部分切除术仅适用于小体积(T1a)肿瘤的缺点。研究显示,腹腔镜和机器人辅助腹腔镜肾部分切除术所切除的肿瘤直径多为3 cm 左右,并且为非孤立肾肾癌患者[12-13]。本研究显示,开放性零缺血结合同步切缝技术对于肿瘤体积较大和复杂性孤立肾肾癌可优先选择。开放性零缺血结合同步切缝技术的另一优点是最大限度保护孤立肾肾癌患者的术后肾功能。研究显示,近20%孤立肾肾癌患者术后肌酐升高超过50 μmol/L[14],但本研究患者的术后不同时间各项肾功能指标与术前相比均无明显升高,可能与术中保持肾脏零缺血密切相关。本研究中仅1 例患者出现术后肌酐水平约50 μmol/L 升高,可能与其BMI较高(27.8 kg/m2)及术前肌酐水平偏高(126 μmol/L)有关,增加了肾脏代偿负荷。
综上所述,开放性零缺血结合同步切缝技术在孤立肾肾癌的肾部分切除术中安全有效,在肿瘤治疗和保护肾功能方面有着诸多优势,特别是对于肿瘤体积较大或复杂性孤立肾肾癌患者。虽本研究患者的例数较少且为回顾性研究,且目前无法开展前瞻性对照研究,但由于能为孤立肾肾癌患者带来诸多获益,仍然值得推广应用。
