间歇性θ短阵脉冲经颅磁刺激联合动作观察疗法对轻、中度阿尔茨海默病患者认知功能的影响
2022-11-25蒋孝翠苏清伦赵秦刘臻贾旭武
蒋孝翠,苏清伦,赵秦,刘臻,贾旭武
阿尔茨海默病(Alzheimer’s disease,AD)是世界范围内最常见的退行性病变,是痴呆的最常见原因[1]。研究显示,中国大于65岁的老年人AD的患病率高达4.8%[2],随着人口老龄化的加剧,其发病率在全球范围内呈上升趋势,给社会、家庭、公共卫生、医疗护理带来了重大负担。AD最常见的最初症状是记忆新信息的能力逐渐下降,这是因为最先被损伤、破坏的神经元通常位于大脑中与形成新记忆有关的区域[3]。AD的治疗包括药物治疗和非药物治疗,药物治疗的目的是逆转神经递质缺陷和改善AD的症状,但疗效有限,且不能逆转AD的进展[1]。近年来非药物治疗措施逐渐引起重视,非药物治疗的策略侧重于维持患者的认知、日常生活活动能力、运动功能。θ短阵脉冲刺激(theta burst stimulation,TBS)是一种高效的模式化重复经颅磁刺激,于2005年由HUANG等[4]首次提出,该刺激模式可以模拟海马神经元放电,具有耗时短、强度低、效应强等特点。根据刺激与间歇时间的不同,以及对大脑皮层兴奋性的不同影响,可分为引起兴奋效应的间歇性TBS(intermittent TBS, iTBS)及产生抑制作用的连续性TBS(continuous TBS,cTBS)。已有文献证实,iTBS可以改善脑卒中患者的认知功能及运动功能[5-6],关于其在阿尔茨海默病的应用研究较少。镜像神经元系统(Mirror Neuron System,MNS)是一组特殊的视觉运动神经元系统,有研究显示,MNS可通过观察他人的动作而被激活[7]。MNS与多种人类脑高级功能有关,比如动作模仿、语言、情感、认知等。动作观察疗法(action observation therapy,AOT)是旨在激活MNS促进脑高级功能恢复的一种新的治疗方法。目前已有研究表明,镜像神经元系统可改善脑卒中后患者的言语、认知、运动功能[8-9],但将MNS应用于改善AD患者认知功能的研究较少。基于此,将iTBS、AOT延伸应用于阿尔茨海默病患者,研究iTBS联合动作观察疗法对轻、中度阿尔茨海默病患者认知功能的影响。
1 资料与方法
1.1 一般资料 选取2021年6月~2021年12月连云港市第一人民医院康复医学科在院的轻、中度AD患者52例。疾病的诊断依据美国国家衰老研究所(National Institute of Aging,NIA)和阿尔茨海默病学会 (Alzheimer’s Association,AA)2011发布的诊断标准[10](NIA-AA,2011)。纳入标准:年龄60~80岁;AD患者病情稳定,临床痴呆评价量表(Clinical De-mentia Rating,CDR)评价得分为1分(轻度痴呆)或2分(中度痴呆);受试者或家属签署知情同意书。排除标准:其他因素所致的痴呆患者;合并视、听觉障碍,不能进行镜像神经元系统训练;存在精神疾病者;合并其他严重的躯体疾病:如严重心、肺、肝、肾功能不全等;体内有金属异物或其他植入体内电子装置。按照随机数字表法将52名轻、中度AD患者随机分为对照组26例、观察组26例。本研究已通过连云港市第一人民医院伦理委员会批准,伦理号为:KY-20210630002-01。2组患者的年龄、性别构成、病程、受教育年限一般资料比较,差异无统计学意义。见表1。
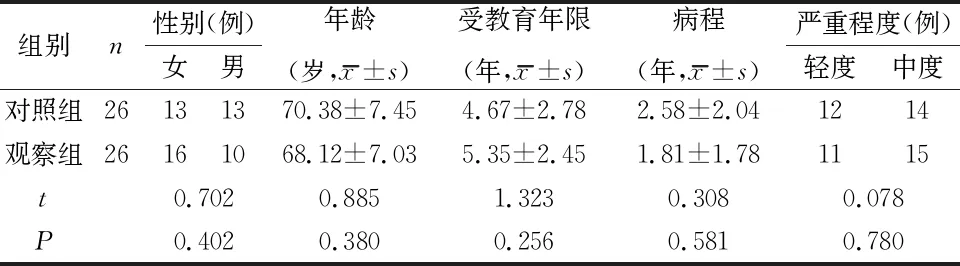
表1 2组患者一般资料比较
1.2 方法 2组AD患者均接受常规药物治疗、认知功能训练、运动训练。对照组在此基础上采用AOT,
观察组在对照组基础上联用iTBS。认知功能训练包括:记忆训练、计算训练、注意力训练、理解训练、地点时间定向训练等。运动训练包括:MOTOMED踩踏车训练、下肢减重机器人步行训练。iTBS:采用武汉依瑞德医疗设备新技术有限公司生产的CCY-Ⅱ型经颅磁刺激仪,选择8字形磁刺激线圈,磁刺激线圈与头皮相切。电刺激部位为双侧额叶背外侧(dorsolateral prefrontal cortex,DLPFC),磁刺激强度为80%静息运动阈值,丛内频率50Hz,丛内脉冲3,丛间频率5Hz,丛内个数10,重复次数20,间歇8s,脉冲总数为600,一侧刺激时间为20s,双侧刺激时间为40s。6d为1个疗程,每个疗程间隔1d,总共进行4个疗程的治疗。AOT:患者在言语治疗室进行治疗。选用镜像神经元康复训练系统(mirror neuron system therapy,mnst1.0),选择系统中的认知治疗部分。患者在治疗室取坐位,佩戴镜像神经元的视频输出系统,通过视频输出系统VR眼镜及耳机患者可以观看到视频以及相应的语音。治疗内容包含有认知训练部分的手部动作观察视频180个,比如:拖地、写信、打字、翻书等,每个视频时长1min左右,每个词汇的视频包含3个部分。第1个部分为观察该词汇表达者的口型并配有语音;第2个部分为观察词汇的手部动作视频,视频配有语音;第3个部分为同时观察口型及手部动作视频,视频配有语音,嘱患者集中注意力听语音、观看口型及手势动作,根据语音及口型进行复述,根据动作视频进行模型。将180个视频分成6组,每天播放1组视频,治疗时间30min,1次/d,每周治疗6d,连续治疗4周。
1.3 评定标准 ①认知功能评定:采用蒙特利尔认知评估(Montreal Cognitive Assessment, MoCA)、简易智能精神状态检查量表(Minimum Mental State Examination,MMSE)进行认知功能评估。MoCA量表内容包括:视空间与执行能力(连线测试、临摹立方体、画钟测试)、命名、记忆(即刻记忆)、注意力、计算、语言、抽象能力、延迟回忆、定向力,总分为30分正常。MMSE总分为30分,MoCA、MMSE均得分越高患者认知功能越好。MoCA量表较MMSE量表强调执行能力、注意力等的评估,敏感度更高[11]。②日常生活活动能力评估:基本日常生活能力评定采用改良Barthel指数进行评估,包括10项内容:进食、洗澡、修饰、穿脱衣服、大便控制、小便控制、使用厕所、床-椅转移、平地走50m、上下楼梯。改良Barthel指数总分为100分,得分越高,表示日常生活自理能力越好。工具性日常生活活动采用功能活动问卷(Frequently Asked Questions,FAQ)进行评估,评分越高,功能障碍越重。

2 结果
2.1 2组治疗后认知功能比较 2组治疗前MMSE评分与MoCA评分差异无统计学意义。2组治疗后MMSE评分、MoCA评分均高于治疗前,观察组MMSE评分、MoCA评分改善幅度均高于对照组(P<0.05)。见表2。

表2 2组治疗前后MMSE和MoCA评分比较 分,
2.2 2组治疗后日常生活活动能力比较 治疗前,2组Barthel指数评分及与FAQ评分差异无统计学意义;治疗后,2组Barthel指数评分与FAQ评分均明显高于治疗前(P<0.05),且观察组改善程度高于对照组(P<0.05)。见表3。

表3 2组治疗前后改良Barthel指数和FAQ评分比较 分,
3 讨论
TBS是经颅磁刺激的一种特殊模式,能在更短时间内诱发皮层的可塑性反应,影响大脑功能重组[12]。目前研究发现TBS的作用机制主要为:①TBS影响基因与蛋白的表达,促进了突触的可塑性[13];②钙离子依赖的双向调控,iTBS对皮质兴奋性产生易化作用。在本研究中选择了DLPFC作为刺激靶点,因为DLPFC对认知处理过程起着重要作用,包括工作记忆、语言、注意力、计划、决策、执行功能以及认知调控等[14]。且AD患者双侧大脑均有受累,因而选用双侧刺激的方式。在本研究中选择双侧DLPFC作为刺激靶点,但Hall等[15]研究发现,左侧DLPFC在促进社会认知方面有着更有力的作用,在今后研究中将进一步做疗效的对比研究。已有研究发现,将DLPFC处连续10d的iTBS刺激治疗能够改善脑卒中患者的认知功能[16],仪文斌的研究也证实了iTBS联合常规的康复训练有望进一步改善脑卒中患者的认知功能[6]。
猴子大脑皮层中镜像神经元被激活的发现是研究人类大脑中镜像神经元的第一步,这一研究推动了镜像疗法在许多神经系统疾病中的应用[17]。Hari等[18]在1998年利用脑磁图研究了动作观察中镜像神经元系统的参与,镜像神经元系统在人类的模仿中发挥着重要作用,当一个人观察另一个人的行为时,镜像神经元系统就会被激活。研究发现,大脑不同区域的MNS系统可能有不同的功能,其中与认知、语言、理解动作有关的主要为顶额镜像系统[19]。主要存在于中央前回下部、额下回下部、顶下小叶头部、颞中回等区域[20]。动作的模仿需要复杂的认知功能,这种认知功能是在包括观察在内的几个阶段逐步构建起来的[21]。AD患者脑组织的神经生物学改变与其认知功能衰退密切相关[22],包括额顶区、颞区的脑血流量下降、皮质弥散性萎缩、脑室扩大等。基于以上这几点,我们推测iTBS产生的皮层兴奋易化作用可以加强镜像神经元的激活,因此在本研究采用iTBS以及AOT联合治疗,激活镜像神经元进而改善AD患者认知功能。
在本研究中,观察组通过常规的认知功能训练辅以iTBS以及AOT治疗发现,MMSE评分改善幅度为5.46±0.99分,MoCA评分的改善幅度为3.88±1.45分,认知功能的改善显著优于对照组,推测在iTBS使得皮层产生兴奋性易化作用后,立即进行动作观察疗法,可以使得镜像神经元的激活产生一定的叠加效应,因而观察组的治疗效果优于单纯的对照组。而且朱玉莲等[5]研究发现,iTBS兴奋皮质的后效应时间至少可以持续20~30min。因此在本研究中,采用了先进行iTBS后立即进行动作观察疗法的训练。观察组AD患者的日常生活活动能力改善10.23±1.97分,工具性日常生活活动能力改善6.65±1.81分,推测可能为动作观察疗法中的模仿行为促进了AD患者的学习功能,进而促进了行为的改良,提高了患者的日常生活活动能力。镜像神经元为建立模仿技能提供了基本的神经基础。功能磁共振成像(functional magnetic resonance imaging,fMRI)研究显示,进行模仿任务的患者皮层激活显著高于非模仿任务的患者[23-24]。Burns[25]的研究表明,在脑卒中患者的康复中使用运动观察疗法,可能会加速功能活动的恢复,通过fMRI检查后显示,患者的皮层区域在观察后被激活。Hamzei等[26]研究初级感觉运动皮层的神经可塑性,使用镜像疗法进行对照实验,受试者在4天内每天进行20min的手部运动观察任务。研究发现,与对照组相比,使用镜像疗法的实验组手部运动功能明显改善。因此推测,镜像疗法会影响神经回路,神经回路会对运动行为重新编程[26],而iTBS对皮层兴奋的易化作用加深了AD患者的学习和模仿过程。
综上所述,镜像神经元通过与人类神经运动区相互作用参与模仿学习,iTBS皮层兴奋的易化作用可能优化学习过程,可提高阿尔茨海默病患者的认知功能以及日常生活活动能力,有望在临床中推广使用。本研究中选用的评估认知功能采用的是MMSE、MoCA,从认知评估角度指标略显不足,后续将增加神经电生理和功能影像指标完善观察指标。在本研究中,干预机制的研究涉及较少,研究时间较短,无法确定iTBS联合动作观察疗法对AD患者认知功能的长期影响。
