氮族元素常见问题的突破
2022-11-17赵多刚
赵多刚
(山东省邹平市第一中学)
氮族元素是高中化学的重要内容,与氮族元素相关的习题灵活多变.学生应做好常见问题的归纳,并结合例题掌握具体突破思路.
1 基础题的突破
为了能更好地突破基础题,学生应牢固记忆氮族元素在元素周期表中的具体位置,明确氮族元素构成的常见化合物以及对应元素的化合价.要养成良好的学习习惯,认真阅读课本中的内容,构建系统的基础知识网络,为顺利解题奠定坚实的基础.
例1如图1所示为大气中氮的循环示意图,则( ).
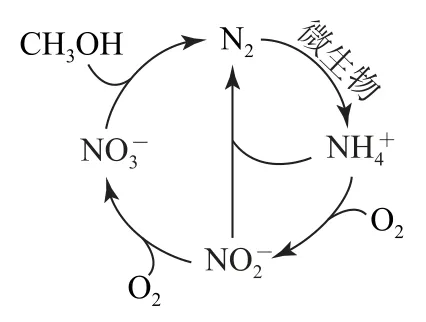
图1
A.图中所有含氮微粒中N 元素的化合价只有0、+3、+5
B.氮循环过程中NO3-被甲醇氧化为N2
C.温度越高,N2转化为NH4+的速率越快
D.NH4+和NO2-反应的离子方程式为
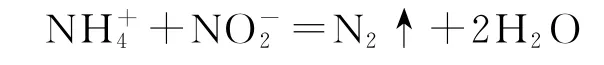
分析该题较为基础,解题时认真观察图示给出的内容,联系所学知识,不难得出正确答案.中N 元素的化合价为-3,中N 元素的化合价为+5,而N2中N 元素的化合价为0.因此,转化为N2的过程中,是被还原的,N2转化为是在微生物的作用下进行的,并不是温度越高速率越快.综上分析只有选项D 正确.
2 推断题的突破
为更好地解答与氮族元素相关的推断题,学生一方面要记忆有关氮族元素化合物的特征反应、反应条件、反应产物等.另一方面,要掌握解答推断题的相关技巧.认真阅读题干,积极联系所学,充分挖掘题干中的隐含条件.
例2图2为NH3发生转化的关系图,则以下说法正确的是( ).
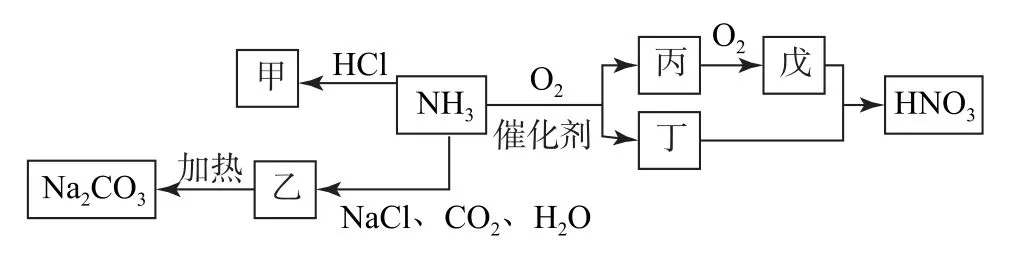
图2
A.甲中含有极性共价键、配位键及离子键
B.戊和丁反应时氧化剂和还原剂物质的量之比为2∶1
C.浓硝酸见光易分解且易挥发,应用棕色试剂瓶盛放且用胶塞密封
D.将CO2和NH3依次通入饱和氯化钠溶液中,过滤可制得乙
分析该题难度中等,解答时要从氨的催化氧化反应切入,再推断出其他物质.其中氨气发生催化氧化可得NO 和H2O,即丙为NO,丁为H2O,则戊为NO2.甲为NH4Cl.NH3和NaCl、CO2、H2O 反应生成NaHCO3,则乙为NaHCO3.由此,对给出的4个选项进行分析可得答案为A.
3 计算题的突破
解题时要先确定反应产物,而后分析相关元素在反应前后化合价的变化,再结合得失电子守恒列出相关方程进行计算.
例3向含有amolCu和bmolCuO的混合物中加入10mL6mol·L-1的稀硝酸时,固体刚好完全溶解,得到标准状况下224mL气体(纯净物),则( ).
A.a∶b=3∶2
B.反应中转移电子0.1mol
C.被还原的硝酸为0.06mol
D.将少量铁粉投入该稀硝酸中生成Fe(NO3)2
分析Cu和稀硝酸反应生成NO 气体,Cu元素从0价上升到+2价,硝酸中N 元素从+5价降低至+2价,被还原的硝酸的物质的量和生成NO 的物质的量相等,由题意得

转移的电子数为0.01 mol×3=0.03 mol,选项B、C均错误.由得失电子守恒可得a=0.015mol.由Cu元素守恒可得

则a∶b=3∶2,选项A 正确.稀硝酸和少量铁粉反应的产物为Fe(NO3)3,选项D 错误.答案为A.
4 图像题的突破
图像题往往隐含很多条件,解题的关键在于通过审题,正确理解题意.同时,要认真读图,搞清楚图像中横纵坐标的含义,挖掘隐含知识.
例4铁和不同浓度的硝酸反应时各种还原产物的相对含量与硝酸溶液浓度的关系如图3所示,以下说法不正确的是( ).
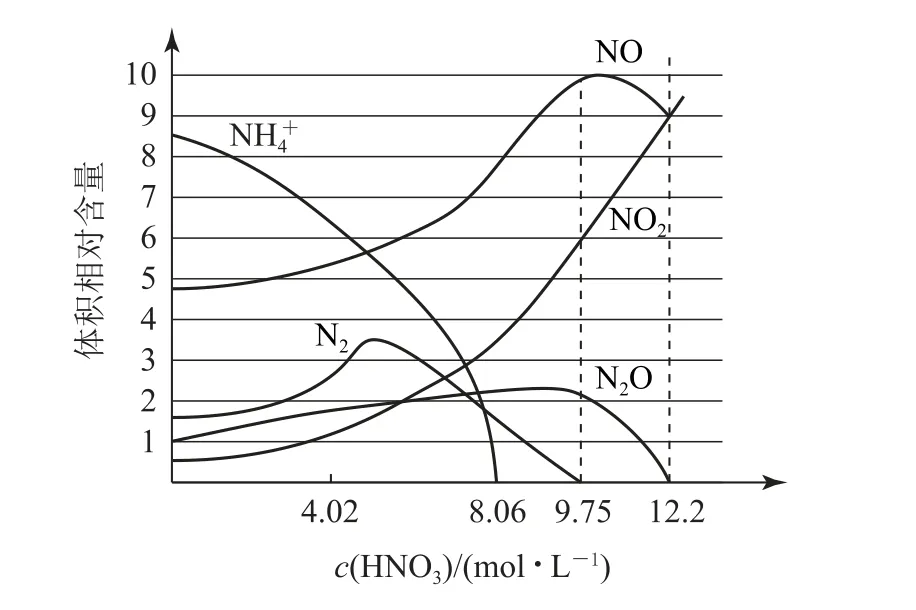
图3
A.硝酸的浓度越小,其还原产物价态越低的成分越多
B.硝酸与铁反应往往会同时生成多种还原产物
C.当硝酸浓度为9.75 mol·L-1时,氧化剂和还原剂的物质的量之比为15∶13
D.铁可以和大于12.2mol·L-1的硝酸溶液反应说明不存在钝化现象
分析NH4+中N元素的化合价为-3 价,HNO3浓度越小,其相对含量越高,选项A 正确.由图3易得,不同浓度硝酸对应不同还原产物,选项B 正确.当硝酸浓度为9.75mol·L-1时,还原产物分别为NO、NO2、N2O,相对含量之比为5∶3∶1,设物质的量分别为5mol、3mol、1mol,消耗HNO3物质的量为10mol,转移电子总数为5 mol×3+3 mol×1+1mol×4×2=26 mol,则对应还原剂铁的物质的量为,即,氧化剂和还原剂的物质的量之比为,选项C正确.常温下,Fe遇浓硝酸发生钝化,铁可以和大于12.2 mol·L-1的硝酸溶液反应,并不能说明无钝化现象,选项D 错误.
5 实验题的突破
例5采用图4装置探究NO 和铜粉的反应,并收集生成的气体.反应前向装置中先通入一段时间的氮气.已知FeSO4+NO=[Fe(NO)]SO4.
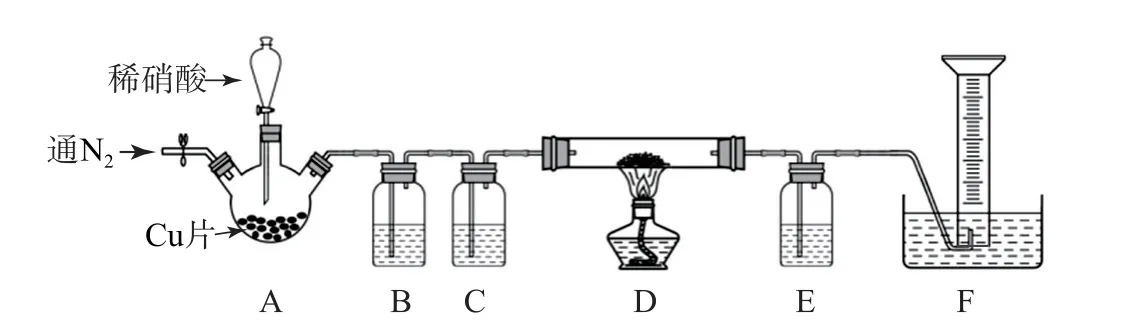
图4
(1)C 中的药品为________,E 的作用为________.
(2)D 中固体逐渐变黑,并生成一种无毒气体,对应的反应方程式为_________.
(3)反应前装置D 硬质玻璃管和铜粉的质量为m1g,反应后质量为m2g,则反应生成气体在标准状况下的体积为_________L(用m1,m2表示,下同),反应开始加入Cu的质量至少为________g.
分析装置A 用于制备NO,其中装置C是为了干燥生成的NO,应使用浓硫酸.E 中为FeSO4,用于除去未反应的NO.因生成一种无毒气体,由元素守恒可知该气体为N2,结合氧化还原反应原理可得对应的反应方程式为.结合化学反应方程式以及反应前后的质量差,可得生成N2的质量为,对应标准状况下的体积V=同理可求得NO 的质量为,由2Cu~2NO,可计算得到Cu的质量为4(m2-m1)g.
氮族元素在高中化学中占有重要地位,学生要夯实基础知识,提高解题效率.
(完)
