肿瘤免疫治疗所致细胞因子释放综合征的研究进展
2022-11-12刘燕贾煜娴李婷婷
刘燕 贾煜娴 李婷婷
作者单位:530021 南宁 广西医科大学附属肿瘤医院乳腺及骨软组织肿瘤内科
近年来,随着全球癌症发病率和死亡率的不断升高,传统癌症治疗方法,如手术、放疗和化疗难以获得满意的临床疗效。20世纪90年代中期,免疫学家发现了免疫检查点治疗并开启了肿瘤免疫治疗新时代[1]。免疫检查点抑制剂(immune checkpoint inhibitions,ICIs),主要通过恢复T细胞活性发挥抗肿瘤作用,是目前最常见的肿瘤免疫治疗方式之一[2]。如靶向特定信号通路的小分子药物,已经加入了基于T细胞工程的细胞免疫疗法,新型抗CD19嵌合抗原受体T细胞(chimeric antigen receptor T cell,CAR-T cell)治疗对CD19高表达的恶性肿瘤产生了安全有效的临床疗效[3]。然而,在多达三分之一的癌症患者中出现了直接和强大的免疫效应反应显著相关毒性,最典型的毒性为细胞因子释放综合征(cytokine release syndrome,CRS)。CRS的特征是循环细胞因子水平升高、急性全身炎症反应以及继发性器官功能障碍。本文综述CRS的定义、潜在的免疫学机制、诊断与鉴别诊断、临床表现和临床治疗等方面的研究进展,为获得良好的临床疗效以及更好地开展肿瘤免疫治疗提供有益借鉴。
1 CRS的定义及评估
CRS是指一类由于免疫细胞被激活而释放出大量细胞因子所导致的急性全身性炎症反应综合征。目前,CRS尚缺乏统一和被广泛认可的定义。FAJGENBAUM等[4]提出了以下3项评估标准:⑴循环细胞因子水平升高;⑵急性全身性炎症反应综合征;⑶继发性器官(一般是肾、肝或肺)功能损害。2018年美国ASBMT共识将CRS界定为经免疫治疗后引起内源性或输注性T细胞或其他免疫学效应细胞的激活或参与的超生理反应[5]。从目前来看,尽管有关CRS的定义都强调了疾病快速发展并产生严重的不良后果,但是定义的指标不尽相同。此外,CRS疾病特征因癌症类型、定义方式的不同而不同。因此,目前亟需对CRS达成相对统一的评估标准,这对CRS的发病机制和临床治疗研究具有重要意义。
CRS最初在异基因造血干细胞移植后的急性移植物抗宿主病中被报道[6],此后与之相关的临床试验和基础研究陆续开展,对CRS的认识也不断增加。然而,CRS真正引起广泛关注是在新型冠状病毒(SARS-CoV-2)及其引发的肺炎(COVID-19)大流行以后。CHRISTIE等[7]通过研究蝙蝠的抗病毒机制,以减轻COVID-19引起的人体细胞因子“风暴”。到目前为止,笔者根据clinicaltrials网站(https://clinicaltrials.gov/)总结了39项已完成(图1A)和34项正在进行的(图1B)临床试验,发现除了病毒感染之外,CAR-T细胞、脓血症和器官移植等也会诱发CRS。近年来,随着免疫治疗的发展,相继发现使用CAR-T细胞治疗后会发生全身性炎症反应,使用免疫效应细胞疗法也出现了类似现象[8]。
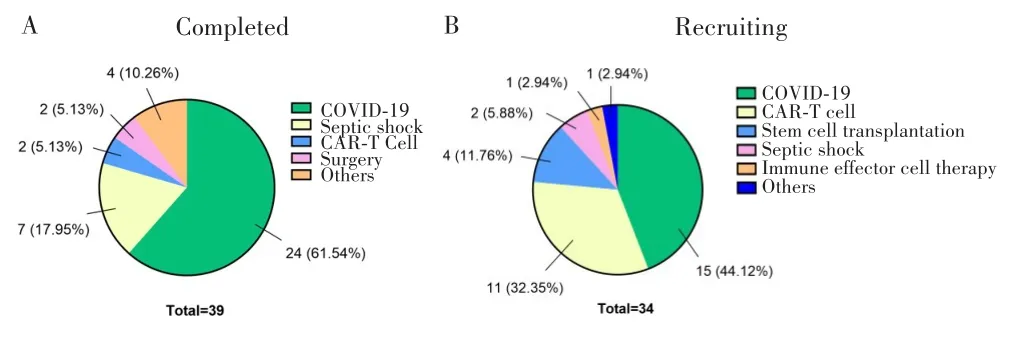
图1 按引起CRS主要病因分类的已完成(A)和正在进行(B)的临床试验的数量和百分比Fig.1 The number and percentage of CRS based completed(A)and recruiting(B)clinical trials classified by major etiological factors
此外,越来越多的回顾性研究证实CRS是与免疫治疗相关,以及由免疫治疗导致的一种新的进展模式。CRS主要见于免疫治疗后,且CRS与免疫微环境息息相关。PD-1/PD-L1被阻断后导致肿瘤微环境的改变,如部分肿瘤浸润免疫细胞IL-10释放增多、Th17细胞活化引起促炎因子IL-17表达增多等[9]。也有研究认为CRS是肿瘤晚期的自然过程,是缺乏有效的治疗手段导致的,而非肿瘤免疫治疗所特有,化疗或靶向治疗过程中也有CRS现象的发生[10],但尚缺乏大样本随机对照试验的探索。
2 CRS发生的免疫学机制
CRS严重阻碍了肿瘤免疫治疗的临床疗效,但CRS的潜在免疫学机制尚未阐明。CAR-T细胞和肿瘤细胞之间的相互作用会激活与宿主相邻的细胞,尤其是巨噬细胞,从而引发大量细胞因子释放,导致与CRS相关的全身症状。LIU等[11]研究表明CAR-T细胞通过分泌颗粒酶B激活孔形成家族蛋白E(gasdermin E,GSDME),触发靶细胞焦亡,随后释放的因子可激活巨噬细胞中GSDME裂解的caspase 1,最终导致CRS的发生;而敲除GSDME、消除巨噬细胞或抑制caspase 1可抑制小鼠模型中CRS的发生;且CRS的严重程度与GSDME水平呈正相关。巨噬细胞还能募集CAR-T细胞所释放的细胞因子并活化,如TNF-α、IL-2、GM-CSF和IFN-γ等[12]。单核细胞也可能是 CRS 中IL-6和IL-1的关键介质和主要来源,在CAR-T细胞治疗前去除单核细胞可以保护小鼠免受致命的CRS攻击[13]。此外,树突状细胞、内皮细胞也被认为参与了IL-6的产生。IL-6主要通过结合膜结合mIL-6R或sIL-6R而激活其下游JAK和STAT3信号[4]。活化的内皮细胞分泌大量的IL-6和其他促炎因子,导致细胞因子释放的正循环。值得注意的是,除了最常见的全身性CRS外,也有研究发现局部CRS(local cytokine release syndrome,L-CRS)是非霍奇金淋巴瘤(non-Hodgkin lymphoma,NHL)最早出现的毒性反应,主要表现为局部肿胀和发红[14]。CAR-T细胞起初局限分布在肿瘤组织中,触发L-CRS,但随着CAR-T细胞和细胞因子的逐渐积累,其最终进入循环系统并产生全身性CRS。然而,L-CRS的机制可能是独特的,因为抑制IL-6可能会加重L-CRS[15]。因此,有必要进行更深入的研究探讨其特定机制。
3 CRS的诊断和鉴别诊断
早期诊断是CRS有效治疗的关键,但是目前由于CRS缺乏特异性的临床表现且病情进展迅速,患者死亡前常误诊或延误诊断。实验室检查包括转氨酶、乳酸脱氢酶和三酰甘油等指标,其水平升高可能是CRS的诊断特征[16-17]。明显的炎症标志物,如血清铁蛋白升高也是CRS的典型特征[18]。
鉴别CRS与其他临床表现相似的疾病也非常关键。严重的CRS与嗜血细胞性淋巴组织增生综合征和肿瘤溶解综合征等具有许多共同点。嗜血细胞性淋巴组织增生综合征具有独特的外周血T细胞激活状态,CD38high/HLA-DR+CD8+T细胞增多是活动性嗜血细胞性淋巴组织增生综合征与CRS区别的可靠标志[19]。肿瘤溶解综合征一般表现为发热、急性肾衰竭、心律失常和癫痫等症状,通常可根据特征性实验室指标异常如高尿酸血症、高钾血症、高磷血症和低钙血症等与CRS鉴别。系统性过敏反应往往同时也发生皮疹、高热、通气障碍、低血压以及胃肠道表现[20]。但是,上述综合征在停止治疗或给予抗组胺药、糖皮质激素等处理后一般预后良好。值得注意的是,大多数肿瘤患者往往处于免疫抑制期,致使CRS在临床上无法与脓毒症区分,所以一旦感染无法消除,应积极启动经验性的抗生素疗法。
4 CRS的临床表现
CRS是一种由快速免疫激活引起的抗原非特异性毒性反应。在临床上,CRS患者通常表现出非特异性综合征,也可出现从流感样轻度症状到严重的威胁生命健康的过度炎症等多种症状。CRS轻度症状包括发烧、疲劳、头痛、皮疹、关节痛和肌痛。较严重的CRS患者以低血压和高烧为特征,可发展为不受控制的全身性炎症反应,出现需要升压药循环的休克、血管渗漏、弥散性血管内凝血和多器官系统衰竭。
CRS的发病时间是输液后2~3 d,通常症状轻微,在数小时至数天内逐渐发展。大多数CRS患者在输液后14 d内开始,持续7~8 d[21]。CRS最初症状为发热,有时体温>40.5℃;其他症状类似流感样疾病,包括肌痛、头痛、乏力和厌食等表现。在CRS患者中已经观察到主要器官功能障碍包括心脏、肺部、肝脏、肾脏等。大多数CRS患者是自限性的,但是部分患者发展为更严重的症状,如低血压、心动过速、胸腔积液、肺水肿和缺氧等,可导致多器官衰竭,其中器官功能障碍可能继发于低血压或缺氧,但也可能是细胞因子大量释放而直接影响所致。此外,CRS也可能出现低纤维蛋白原血症和弥散性血管内凝血,特别是在非常严重的CRS中[22]。肌钙蛋白升高和射血分数下降在严重CRS中也很常见[23]。全身炎症标志物,包括超敏C反应蛋白和铁蛋白在严重CRS中可能异常升高[24]。器官特异性标志物如肝脏转氨酶、胆红素、血尿素氮、肌酸和肌酐等也普遍升高[25]。感染和延迟性细胞减少症也很常见,特别是在急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)和严重CRS患者中,且与死亡率有关[26]。若CRS症状和体征得到及时识别和处理,这种器官功能障碍是可以预防或逆转的,因此临床上应该高度警惕。
5 CRS的临床治疗
肿瘤免疫疗法中CRS的临床治疗方案已经从简单的对症治疗演变为基于生命支持的综合治疗(图2,根据网站https://clinicaltrials.gov/总结归纳)。总体控制目标是防止危及生命的CRS发生,同时最大程度保持有益的抗肿瘤作用。
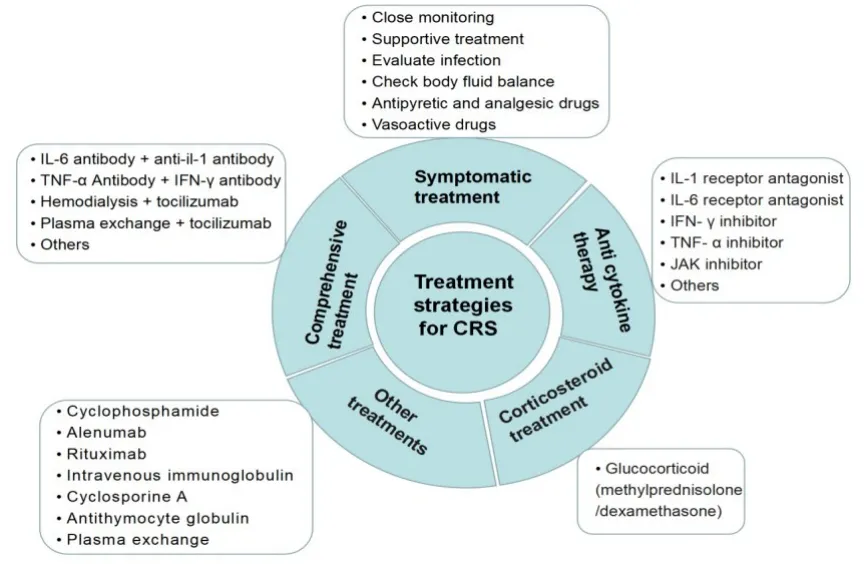
图2 CRS的临床治疗Fig.2 Clinical treatment of CRS
5.1 对症支持治疗
对于肿瘤免疫治疗的患者,结合其临床表现和检验指标可对CRS进行分级进而选择合适的治疗方案。轻度CRS只需要进行对症处理且可在门诊治疗,但当出现进展性CRS时需要及时住院治疗。当CRS患者出现发热时可用冰浴、降温毯和对乙酰氨基酚处理,但不能使用非甾体抗炎药;CRS和败血症的症状是重叠的,患者往往也会出现免疫抑制和/或中性粒细胞减少等表现,因此当患者出现发热时,需要进行全面的与感染相关的检查并使用广谱抗生素,此外还需要强化其他支持性护理,包括血管活性药治疗低血压,并按需给予吸氧[27-28]。
5.2 抗细胞因子治疗
由于细胞因子在驱动CRS病理中起着关键的作用,因此可通过使用IL-6、IL-1、IFN-γ或TNF-α等细胞因子抑制剂来抑制细胞因子信号的转归[29]。根据网站https://clinicaltrials.gov/统计发现,目前临床试验中常用的干预药物包括Anakinra、Itacitinib、Fludarabine等(图3)。尽管这些药物毒副作用令人担心,但迄今为止,在正确有效的医疗处理条件下都显示出了很有前景的效果[30]。

图3 按干预措施分类的基于CRS的临床试验数量和百分比Fig.3 The number and percentage of CRS based clinical trials classified by interventions
5.2.1 抗IL-6受体拮抗剂 IL-6与其受体结合可诱导强烈的促炎信号通路。其中,Tocilizumab是一种人源化的IL-6受体单克隆抗体,中度至重度进行性低血压或缺氧的CRS患者,主要使用IL-6受体拮抗剂Tocilizumab治疗。FITZGERALD等[31]发现在复发/难治性急性淋巴母细胞白血病患者中接受T细胞治疗后,46%的患者可出现3~4级CRS,但是在使用Tocilizumab治疗后,CRS发病率明显降低,且可在4 h内降低氧气和血管收缩剂的需求量,快速降温和改善临床症状。目前美国FDA已经批准Tocilizumab用于治疗严重的或威胁生命的CRS[32]。
5.2.2 抗IL-1受体拮抗剂和抗IL-18抗体 促炎因子IL-1也能促进CRS的进展,研究表明,IL-1受体拮抗剂Anakinra能显著减少免疫治疗过程中产生的CRS和神经毒性[33],提示IL-1在CRS发病机制中占据重要作用。由于细胞焦亡可释放IL-1β,因此抗IL-1β的单克隆抗体(Canakinumab)也能减轻CRS患者感染的严重程度[34]。此外,促炎因子IL-18可诱导细胞产生炎性细胞因子,但是IL-18的促炎作用可被高亲和力的内源性拮抗剂IL-18结合蛋白所中和。当使用IL-18受体的单抗时,可防止巨噬细胞活化综合征时伴随的全血细胞减少和血细胞吞噬等病情进展的症状[35]。类似地,用重组的IL-18结合蛋白也能降低耐药突发性脊柱炎和复发的巨噬细胞活化综合征患者的发作频率和严重程度[36]。
5.2.3 抗TNF-α抗体及其他促炎细胞因子抑制剂 TNF-α可通过促进其他细胞因子或炎症因子释放,参与机体的免疫炎性反应。在甲型流感病毒感染的小鼠中,给予抗肿瘤坏死因子中和抗体治疗后,小鼠肺免疫细胞渗透明显减少并提高了总体生存率[37]。在脓毒症小鼠中,注射抗TNF-α抗体后总体存活率也明显升高[38]。类似地,在一项单臂开放标签Ⅱ/Ⅲ期试验中,抗IFN-γ抗体Emapalab对免疫失调和过度炎症为特征的原发性嗜血细胞淋巴组织细胞病具有治疗作用且临床不良现象发生率较低[39]。此外,Janus相关激酶1/2抑制剂芦可替尼治疗后,CRS患者的炎症标志物、T细胞和单核细胞活化水平明显改善,提示芦可替尼对嗜血细胞性淋巴组织细胞增多(hemophagocyticlymphohistiocytosis,HLH)患者安全有效,且耐受性较好,这对HLH和其他细胞因子释放综合征患者也具有指导治疗意义[40]。但是目前大部分细胞因子抑制剂并没有推广到人类身上,仍需要进一步研究。
5.3 类固醇药物
类固醇药物是抑制过度炎症反应和CRS的有效治疗方法。然而皮质类固醇可能会影响CAR-T细胞的扩增和持久性抑制抗肿瘤功效,因此接受CAR-T治疗的患者应避免使用皮质类固醇作为CRS一线治疗。但是在非常严重的CRS病例中也需要皮质类固醇管理。由于多种细胞因子可能在CRS的后期阶段发挥作用,皮质类固醇可以诱导全身发生免疫抑制,而且可以抑制相关免疫细胞的增殖和产生细胞的因子。然而,使用皮质类固醇与CAR-T疗效降低有关[41]。GARDNER等[42]研究发现Tocilizumab和/或皮质类固醇在早期干预B系急性淋巴细胞白血病后能达到早期并及时阻止CRS进展的效果,且不减弱抗白血病疗效,这种干预有助于提高复发/难治性患者的治疗指数[43]。这可能与早期使用类固醇激素可以防止进展为严重的CRS相关。但由于可能不利于CAR-T持续存在的皮质类固醇剂量和持续时间尚未明确,建议使用最低的有效剂量和最短的有效持续时间的类固醇药物。
5.4 综合治疗
在CRS治疗上,单一细胞因子的疗效是有限的。在脓毒症小鼠模型中,联合应用TNF-α和IFN-γ的抗体比单一使用细胞因子阻断TNF-α或IFN-γ更能提高存活率[44]。TNF-α和IFN-γ的联合应用也保护了小鼠在感染SARS-CoV-2期间免于死亡[38]。CRS与细胞因子IL-6水平升高有关,Tocilizumab因可阻断IL-6受体而成为治疗CRS的主要手段[45]。然而,Tocilizumab未能保护小鼠免受CAR-T细胞介导的CRS和神经毒性,但Anakinra可挽救致命的神经毒性[46],表明抗IL-6和抗IL-1抗体联合疗法或可对抗CAR-T细胞诱导的细胞因子风暴或神经毒性。此外,张亦琳等[47]使用Tocilizumab治疗2级以上CRS患者后,相应的临床症状明显缓解,异常实验室指标均降至正常,说明Tocilizumab在治疗肿瘤免疫治疗引起的CRS中具有重要作用。对于Tocilizumab治疗无效的3~4级CRS,临床上推荐辅助血液透析滤过及血浆置换等方式以提高临床效益[48]。随着多学科综合治疗的出现,在CRS治疗策略上的联合方案诊治疗效得到提升,但仍需探索更好的治疗方案。
5.5 其他疗法
除了以上治疗方法,目前CRS的其他治疗方式还包括依那西普、环磷酰胺、Alemtuzumab、抗血清球蛋白和造血干细胞生成等。总体上在肿瘤免疫治疗中,CRS的发生机制及其解决策略仍需不断验证和创新,才能使肿瘤免疫治疗更有效和更安全。
6 小结
肿瘤免疫治疗是一把双刃剑,有助于根除肿瘤的同时也会出现严重威胁生命的不良反应。目前对于肿瘤免疫疗法中发生的CRS仍缺乏统一可行的准确定义,有关CRS的文献多为回顾性研究,不利于进行大规模前瞻性CRS相关研究。CRS发生的机制正在逐步揭开,有望为新的干预策略提供更多见解。此外,化疗、手术等其他抗癌治疗方式同样也有引起肿瘤CRS的现象,CRS并非肿瘤免疫治疗所特有,如何与肿瘤免疫治疗所致的CRS区别有待深入研究。对于肿瘤免疫疗法中CRS的临床治疗方案,倡导“以生命支持为基础的综合治疗”,一旦高度怀疑CRS,应立即暂停肿瘤免疫治疗,并尽早重新评估,优化给药方案。总之,未来建立统一有效的诊断标准,开发针对细胞因子升高的药物或抗体,实现对细胞因子升高的精确治疗,防止肿瘤免疫治疗所致危及生命的CRS,让患者最大程度从免疫治疗中获益。
