添加剂对汽车电池用Mg2 Ni 合金性能的影响
2022-11-09李琦峰
宋 捷 ,李琦峰
(1.山西机电职业技术学院汽车工程系,山西 长治 046000;2.宁夏大学机械工程学院,宁夏 银川 750021)
相较于液态氢/固态氢,储氢材料可在一定温度/压力下存储和释放更大密度的氢,且存储条件相对温和。在各类储氢材料中,Mg2Ni 合金由于成本低、储氢容量高(质量分数为3.67%)等特点[1],有望成为下一代金属氢化物-镍电池的负极材料,受到人们的广泛关注。Mg2Ni 系储氢合金作为电池负极材料应用于碱性电解液时,会因较差的室温吸氢/放氢动力学性能受到一些限制[2]。较好的解决办法是在Mg2Ni合金中加入金属化合物添加剂,改善微观结构,提升储氢合金的储氢性能。目前的研究主要集中在过渡族金属氟化物(NbF5、TiF3等)、低温型储氢合金(LaNi5、Ti-V 等)对Mg 基储氢材料储氢性能的影响上[3],有关氢化物(LaH3、TiH2等)对Mg2Ni 基储氢合金储氢性能影响的报道较少[4]。
本文作者拟通过在Mg2Ni 合金中添加LaH3、TiH2和LaH3-TiH2复合添加剂的方法,考察添加剂种类对复合材料物相组成、微观形貌和储氢性能的影响,为具有良好储氢动力学性能的Mg2Ni 基储氢合金的开发与应用提供一定的指导。
1 实验
1.1 实验原料
实验原料包括:LaH3(北京产,AR)、TiH2(北京产,AR)和LaH3-TiH2添加剂(LaH3和TiH2的质量比为1 ∶1),以及感应熔炼法制备的Mg2Ni 合金(株洲产)。
1.2 试样制备
Mg2Ni 合金预处理:先将Mg2Ni 合金进行机械破碎,过100 目筛后,在H-Sorb 2600 型高温高压气体吸附仪(北京产)上,于350 ℃下以2.00 MPa 的压力氢化处理120 min,再在350 ℃下充分放氢,并在高纯氩气氛围下保存,待用。
将添加剂(LaH3、TiH2和LaH3-TiH2)与预处理后的Mg2Ni合金在FRITSCH P6 型高能球磨机(德国产)上以350 r/min的转速球磨120 min(球料比10 ∶1,磨球直径为8 mm),制得M(M=LaH3、TiH2和LaH3-TiH2)质量分数为10%的Mg2Ni+10%M 储氢合金,并在真空(10-5Pa)下密封保存,待用。
1.3 测试方法
用Empyrean X 射线衍射仪(荷兰产)分析储氢合金的物相组成,CuKα,λ=0.154 0 nm,管压40 kV、管流35 mA,扫描速率为2(°)/min,步长0.02°;采用Jade-6.5 软件分析晶胞参数[5];用VEGA3 型扫描电子显微镜(捷克产)观察微观形貌,并采用附带的能谱仪测试微区成分;用H-Sorb 2600 型PCT 测试仪绘制压力(P)-组成(C)-温度(T)曲线和储氢合金的等温吸氢/放氢曲线,P-C-T 曲线绘制时使用高纯氢气(99.999%),测试温度为250 ℃;等温吸氢/放氢曲线绘制时,吸氢、放氢的初始压力分别为3.00 MPa 和0.01 MPa。
2 结果与讨论
2.1 物相结构
图1 为LaH3-TiH2复合添加剂充分吸/放氢后的XRD 图。

图1 LaH3-TiH2 复合添加剂充分吸/放氢后的XRD 图Fig.1 XRD patterns of LaH3-TiH2 composite additive after full hydrogen absorption/desorption
从图1 可知,LaH3-TiH2复合添加剂充分吸氢后,主要物相为LaH3和TiH2;而充分放氢后的主要物相为LaH2和TiH2。即LaH3-TiH2复合添加剂充分吸氢后,LaH3相在充分放氢后转变为LaH2相,TiH2相由于稳定性较好而保持不变。
图2 为Mg2Ni+10%M 储氢合金充分吸/放氢后的XRD图,相应的储氢合金的晶胞参数列于表1。

图2 Mg2Ni+10%M 储氢合金充分吸/放氢后的XRD 图Fig.2 XRD patterns of Mg2Ni+10%M hydrogen storage alloys after full hydrogen absorption/desorption

表1 Mg2Ni+10%M 储氢合金的晶胞参数Table 1 Cell parameters of Mg2Ni+10%M hydrogen storage alloys
从图2 和表1 可知,充分吸氢后的Mg2Ni+10%M 储氢合金组成为:M=LaH3时,主要有Mg2NiH4和LaH3相;M=TiH2时,主要有Mg2NiH4、TiH2和TiNiH 相;M=LaH3-TiH2时,主要有Mg2NiH4、LaH3和TiH2相。这表明LaH3-TiH2复合添加时,储氢合金充分吸氢后,不会出现仅添加TiH2时出现的TiNiH 相,主要是因为LaH3-TiH2复合添加剂在球磨制备过程中结合得更紧密,不会进一步与基体Mg2Ni 发生反应,形成TiNiH 相[6]。充分放氢后的Mg2Ni+10%M 储氢合金组成为:M=LaH3时,主要有Mg2Ni 和LaH3相;M=TiH2时,主要有Mg2Ni、TiH2和TiNi 相;M=LaH3-TiH2时,主要有Mg2Ni、LaH2、LaH3和TiH2相。这表明LaH3-TiH2复合添加时,储氢合金充分放氢后,LaH3相出现分解并形成LaH2相,而仅添加LaH3时不会形成LaH2相,说明LaH3-TiH2复合添加时,LaH2相的形成与TiH2的添加有关[7]。在球磨过程中,氢化物(LaH3-TiH2、LaH3和TiH2)会嵌入基体中,发生晶胞形变,晶胞体积比纯Mg2Ni/Mg2NiH4小,造成H/Mg 和H/Ni 原子间相互作用的改变[8],并改善储氢合金的热力学性能。
图3 为Mg2Ni+10%M 储氢合金的SEM 图。

图3 Mg2Ni+10%M 储氢合金的SEM 图Fig.3 SEM photographs of Mg2Ni+10%M hydrogen storage alloys
从图3 可知,M=LaH3时,储氢合金中存在较多的亮白色颗粒状物质。能谱分析表明,该区域La 的质量分数约为92.34%,而灰色基体区域La 的质量分数仅为3.19%,说明LaH3的添加会在储氢合金中形成局部富集;M=TiH2时,储氢合金中未见明显亮白色区域,选区位置的能谱分析表明,Ti 元素的质量分数约为8.96%,此时TiH2主要以弥散分布形态存在于储氢合金中;M=LaH3-TiH2时,储氢合金中仅可见极少量亮白色区域,能谱分析表明,La 和Ti 的质量分数在亮白色选区分别为21.59%和23.05%,而在灰色基体区域分别为4.29%和5.01%。由此可见,复合添加LaH3-TiH2,可以改善LaH3在储氢合金中的分布状态,避免局部富集现象的出现。
2.2 储氢性能
Mg2Ni+10%M 储氢合金的P-C-T 曲线见图4。

图4 Mg2Ni+10%M 储氢合金的P-C-T 曲线Fig.4 Pressure(P)-composition(C)-temperature(T) curves of Mg2Ni+10%M hydrogen storage alloys
从图4 可知,纯Mg2Ni 合金的吸氢和放氢平台分别位于0.140 MPa 和0.036 MPa;添加不同氢化物后,Mg2Ni+10%M储氢合金的吸氢和放氢平台都有所提升;相较于纯Mg2Ni 合金,M=LaH3、TiH2和LaH3-TiH2时,吸氢平台分别提升了0.060 MPa、0.040 MPa 和0.090 MPa;放氢平台分别提升了0.010 MPa、0.018 MPa 和0.020 MPa。与仅添加LaH3或TiH2的储氢合金相比,复合添加LaH3-TiH2时,储氢合金的吸氢和放氢量都有所提高。这主要与TiH2的加入可以改善LaH3在储氢合金中的分布状态,以及热力学性能有关[9]。
Mg2Ni+10%M 储氢合金的等温吸氢曲线见图5。

图5 Mg2Ni+10%M 储氢合金的等温吸氢曲线Fig.5 Isothermal hydrogen absorption curves of Mg2Ni+10%M hydrogen storage alloys
从图5 可知,相较于纯Mg2Ni 合金,Mg2Ni+10%M 储氢合金的等温吸氢性能有不同程度的改善;在时间为7 000 s时,储氢合金的最大吸氢容量按M 的不同,从大至小依次为TiH2、LaH3-TiH2和LaH3;且在相同时间内,Mg2Ni+10%M 储氢合金的吸氢容量都高于纯Mg2Ni 合金。此外,在等温吸氢开始阶段,Mg2Ni+10%M 储氢合金的吸氢容量增加速度比纯Mg2Ni 合金快,主要是由于球磨过程中Mg2Ni+10%M 储氢合金表面具有更多的活性点,使H 原子的扩散速率加快[10]。M=LaH3时,储氢合金中LaH3的局部聚集会减少H 原子的扩散通道,导致相同时间内的吸氢容量相对较小。
Mg2Ni+10%M 储氢合金的等温放氢曲线见图6。

图6 Mg2Ni+10%M 储氢合金的等温放氢曲线Fig.6 Isothermal hydrogen desorption curves of Mg2Ni+10%M hydrogen storage alloys
从图6 可知,在相同时间下,添加氢化物的储氢合金的放氢容量要高于纯Mg2Ni 合金,放氢容量按M 的不同,从大至小依次为TiH2、LaH3-TiH2和LaH3。由此可见,M=LaH3、TiH2和LaH3-TiH2时,Mg2Ni+10%M 储氢合金的等温放氢性能较纯Mg2Ni 合金都有不同程度改善,主要与氢化物的添加有助于增加储氢合金中的氢扩散通道有关[11]。此外,相较于图4 的储氢容量,图5 和图6 的最大吸/放氢量都有很大差别,主要与压力不同有关。
Mg2Ni+10%M 储氢合金的范特霍夫曲线见图7。对图7中曲线拟合[12],得到的放氢热力学参数见表2。
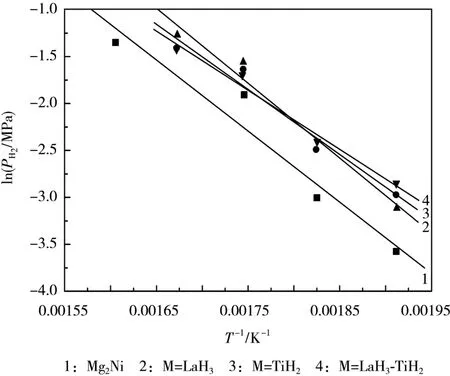
图7 Mg2Ni+10%M 储氢合金的范特霍夫曲线Fig.7 Van’t Hoff curves of Mg2Ni+10%M hydrogen storage alloys
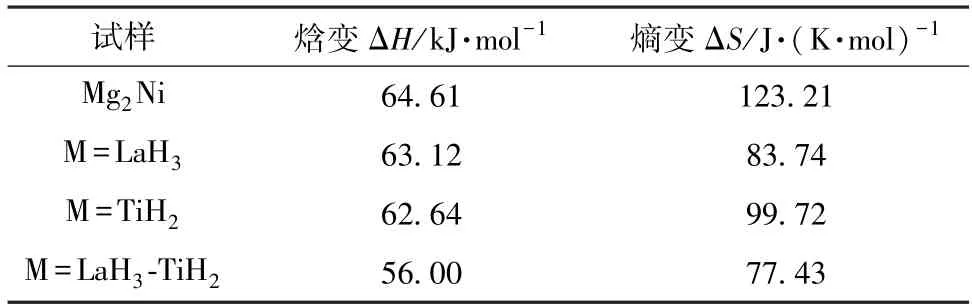
表2 Mg2Ni+10%M 储氢合金的放氢热力学参数Table 2 Thermodynamics parameters of hydrogen desorption of Mg2Ni+10%M hydrogen storage alloys
从表2 可知,对于纯Mg2Ni 合金,焓变ΔH和熵变ΔS分别为64.61 kJ/mol 和123.21 J/(K·mol);在储氢合金中加入氢化物添加剂后,Mg2Ni+10%M 储氢合金的ΔH和ΔS都有不同程度的降低,且M=LaH3-TiH2时,储氢合金的ΔH和ΔS最小,分别为56.00 kJ/mol 和77.43 J/(K·mol)。这说明,添加氢化物有利于Mg2Ni+10%M 储氢合金的放氢,且M=LaH3-TiH2时,相较纯Mg2Ni 合金最容易放氢,主要是因为氢化物的添加可提升Mg2NiH4放氢反应的催化性能[13];且复合添加LaH3-TiH2时,储氢合金中Mg2NiH4相晶胞体积最小,对储氢合金的放氢热力学性能的改善效果最好。
为了研究氢化物对储氢合金等温放氢性能的影响,采用Jander 方程[14]对等温温度为250 ℃时储氢合金的放氢曲线进行拟合,如图8 所示,计算如式(1)所示:
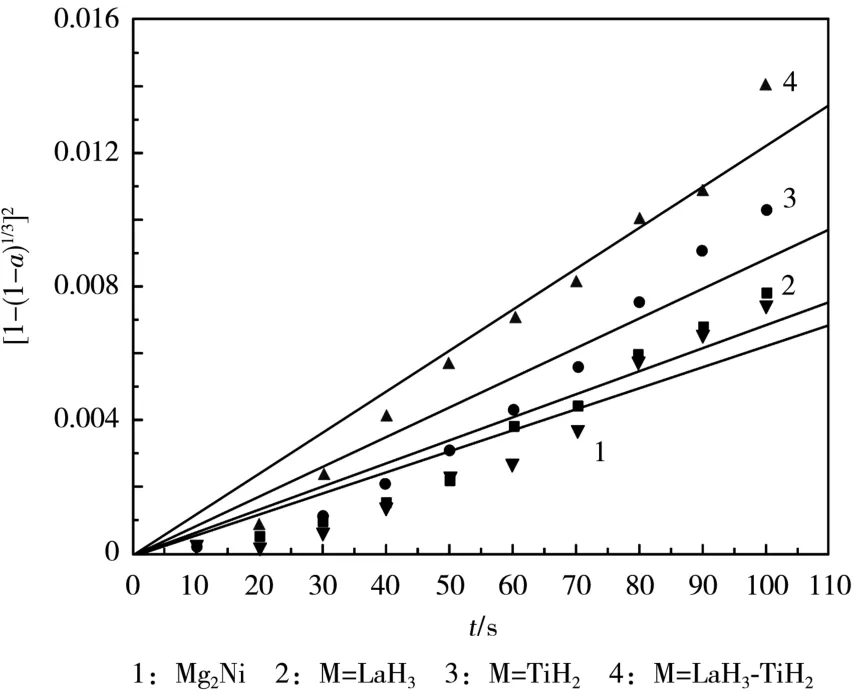
图8 Mg2Ni+10%M 储氢合金的放氢Jander 拟合曲线Fig.8 Jander fitting curves of hydrogen desorption of Mg2Ni+10%M hydrogen storage alloys

式(1)中:t为时间;a为反应百分数。
从图8 可知,M=LaH3、TiH2和LaH3-TiH2时,储氢合金的氢扩散速率k分别为6.83×10-5、8.79×10-5和12.22×10-5,大于纯Mg2Ni 合金的6.22×10-5。
氢扩散速率k越大,表明氢扩散性能越好,说明氢化物的添加可以提升储氢合金的氢扩散性能。M=LaH3-TiH2时,储氢合金的k最大、氢扩散性能最好,主要是因为LaH3-TiH2的添加可增加储氢合金中氢的扩散通道,且LaH3与TiH2的相互作用会减小Mg2NiH4的晶胞体积、促进Mg2NiH4的放氢反应[15],更有助于氢从储氢合金中溢出,提高氢扩散性能。
3 结论
本文作者在Mg2Ni 合金中添加LaH3、TiH2和LaH3-TiH2复合添加剂,研究了不同种类添加剂对Mg2Ni 合金物相组成、微观形貌和储氢性能的影响,主要结论如下:
储氢合金充分吸氢后的组成为:M=LaH3时,主要有Mg2NiH4和LaH3相;M=TiH2时,主要有Mg2NiH4、TiH2和TiNiH 相;M=LaH3-TiH2时,主要有Mg2NiH4、LaH3和TiH2相。储氢合金充分放氢后的组成为:M=LaH3时,主要有Mg2Ni 和LaH3相;M=TiH2时,主要有Mg2Ni、TiH2和TiNi相;M=LaH3-TiH2时,主要有Mg2Ni、LaH2、LaH3和TiH2相。
LaH3的添加会在储氢合金中形成局部富集:M=TiH2时,储氢合金中未见明显亮白色区域;M=LaH3-TiH2时,储氢合金中仅可见极少量亮白色区域。复合添加LaH3-TiH2,可以改善LaH3在储氢合金中的分布状态。
相较于纯Mg2Ni 合金,M=LaH3、TiH2和LaH3-TiH2时,吸氢平台分别提升0.06 MPa、0.04 MPa 和0.09 MPa;放氢平台分别提升0.010 MPa、0.018 MPa 和0.020 MPa;储氢合金的吸氢/放氢容量从大至小顺序为:M=TiH2、M=LaH3-TiH2、M=LaH3和纯Mg2Ni 合金;在储氢合金中加入氢化物后,Mg2Ni+10%M 储氢合金的焓变ΔH和熵变ΔS都有一定的降低,且M=LaH3-TiH2时,ΔH和ΔS最小;M=LaH3、TiH2和LaH3-TiH2时,储氢合金的氢扩散速率k大于纯Mg2Ni 合金的6.22×10-5,分别为6.83×10-5、8.79×10-5和12.22×10-5。
复合添加LaH3-TiH2可改善LaH3在储氢合金中的分布状态,吸氢和放氢量都有所提高,且M=LaH3-TiH2时,ΔH和ΔS最小、k最大,对储氢合金储氢性能的改善效果最好。
